2. 福建三明森林生态系统国家野外科学观测研究站, 350007, 福州;
3. 福建省林业调查规划院, 350003, 福州
中国水土保持科学  2024, Vol. 22 2024, Vol. 22  Issue (1): 12-20. DOI: 10.16843/j.sswc.2023055 Issue (1): 12-20. DOI: 10.16843/j.sswc.2023055 |
退化土壤固碳潜力巨大。联合国粮农组织报道[1]称目前全球已有约1/3的土壤退化,土壤有机质的损失可达20~80 t/hm2[2],预计全球恢复退化土壤的碳吸存潜力可达0.3~0.8 Pg/a[3]。土壤侵蚀是导致土壤退化的主要原因之一。截至2021年底,我国土壤侵蚀总面积达267.42万km2,占国土面积27.96%[4]。在此背景下,大面积人工林应运而生,但与当地天然林土壤相比,单一树种人工林土壤有机碳(soil organic carbon,SOC)质量分数仍处于较低水平。尤其是在热带亚热带地区,高温多雨的气候限制高度风化土壤SOC的长期储存,恢复和提升土壤的碳积累面临巨大挑战。研究表明,南方红壤侵蚀区恢复30多年的马尾松人工林表层(0~10 cm)SOC质量分数仅约12 g/kg[5],提升马尾松人工林SOC水平和持续碳固持能力成为该区生态治理过程的重要环节。
植被类型影响SOC的周转和稳定[6],不同植被类型凋落物质量的高低影响养分的释放与归还[7],而土壤微生物介导陆地生态系统的碳循环过程,特别是微生物群落组成和功能在其中发挥重要作用。相关研究[8]表明,与单一凋落物输入相比,树种混交后不同碳氮比(C/N)的凋落物输入与混合分解更能为土壤微生物提供多元化和高质量的养分来源,形成土壤微生物群落结构和活性特征[8],影响微生物残体等次生微生物源有机质的形成进而影响SOC的形成与动态[9]。因此,厘清树种混交过程中土壤微生物对凋落物特征变化的响应情况及其对SOC固存的调控机理至关重要。
鉴于此,笔者采用成对实验设计,选择福建省龙岩市长汀县河田镇红壤侵蚀退化地上恢复19 a和39 a的马尾松(Pinus massoniana)纯林与马尾松+木荷(Schima superba)混交林为研究对象,通过测定不同恢复年限和林分的表层SOC质量分数、凋落物数量和质量、土壤微生物生物量及其群落结构,验证以下2个假设:1)随着松阔混交年限的延长,混交林凋落物C/N会相对降低,提高土壤氮有效性;2)由于凋落物质量的提高,土壤中偏向利用高质量凋落物的微生物(如细菌)逐渐增加,可能降低真菌和细菌比值,改变土壤微生物群落结构,提高表层SOC质量分数。笔者探求高质量凋落物的阔叶树种与马尾松混交能否有效促进侵蚀退化地SOC的积累,旨在为科学评价中国南方红壤严重侵蚀区退化马尾松林改造提供理论依据,助力我国实现双碳目标。
1 研究区概况研究区位于福建省龙岩市长汀县河田镇(E 116.18°~116.32°,N 25.33°~25.48°),为全国极强度水土流失区之一,属中亚热带季风气候,雨量充沛,雨热同期,年均降水量1 685.6 mm。地形为河谷盆地,四面环山,海拔300~400 m。地带性土壤为燕山运动早期形成的中粗粒花岗岩发育的红壤,风化壳深厚,抗侵蚀能力较差。地带性植被遭大面积破坏严重,现有植被主要为马尾松次生林和人工林,林下植被多为芒萁(Dicranopteris dichotoma)。
采用成对实验设计,于2020年8月,选取土壤母岩条件相同,地形条件相似,位于晨光村恢复19 a的马尾松纯林(Y19-C)和马尾松+木荷混交林(Y19-H),以及位于八十里河恢复39 a的马尾松纯林(Y39-C)和马尾松+木荷混交林(Y39-H)4个样地(表 1),每个样地4个重复,构成不同恢复年限和松阔混交的交互实验处理。
| 表 1 样地基本概况 Tab. 1 Basic background characteristics of sample plots |
于2020年8月在恢复19 a的纯林和混交林、恢复39 a纯林和混交林的每个样地中随机布设20 m×20 m的样方,开展样地调查。利用直径为5 cm土钻,按照S型取土原则对表层0~10 cm土样进行采集,每个样方采集10钻,每个样地共采集40钻,将其充分混合并密封后置于保温箱内,带回实验室去除石砾、根系以及>2 mm的碎屑并过2 mm土壤筛,用于测定微生物生物量碳(microbial biomass carbon, MBC)、微生物生物量氮microbial biomass nitrogen,MBN)、磷脂脂肪酸(phospholipids fatty acid, PLFA)和矿质氮等指标。取部分过2 mm的湿土风干后过0.149 mm筛,用于测定SOC质量分数。
同时,分别在每个样方中随机选择4个40 cm×40 cm小样方收取地面全部枯枝落叶,称其鲜质量,带回实验室,烘干称量,并计算凋落物现存量。
2.2 样品测定与计算1) 凋落叶C、N质量分数:通过植物C、N元素分析仪(Elementar Vario EL Ⅲ)测定样品的C、N质量分数,计算凋落物的C、N归还量。
| $ A=BC。$ | (1) |
式中:A为凋落物C或N储量,kg/hm2;B为凋落物现存量,t/hm2;C为凋落物C或N质量分数,g/kg。
2) 土壤MBC、MBN:采用氯仿熏蒸法浸提[10],并分别采用总有机碳分析仪(TOC-VCPH, Shimadzu, Kyoto, Japan)、连续流动分析仪(Skalar San++, Holland)测定。
3) SOC质量分数的测定:称取800~100 mg过100目筛的干土,采用土壤C、N元素分析仪(Elementar Vario EL Ⅲ, Germany)测定。
4) 土壤微生物群落组成:采用PLFA法[11-12]测定。利用PLFA技术,选取其中18种土壤微生物类群的磷脂脂肪酸作为标志物。这些标志物可分为饱和直链脂肪酸(i14:0,i15: 0,al5: 0,il6: 0,i17: 0,a17: 0,10Me16: 0,10Me17:0,10Me18:0)、单不饱和脂肪酸(16: 1 o5c,16: 1 o 9c,16: 1 o7c,18: 1 o7c,18: 1 o 5c,18: 1 o 9c)、以及双不饱和脂肪酸(18:2o6,9c)、环丙基脂肪酸(cy17: 0),其中有12种细菌PLFA标志物,2种真菌PLFA标志物,1种丛枝菌根真菌PLFA标志物,3种放线菌PLFA标志物(表 2)。
| 表 2 检验土壤微生物种群的脂肪酸标志物 Tab. 2 PLFAs used in the analysis of microbial communities |
采用Excel 2013中进行数据初步处理,统计分析采用软件SPSS 20.0进行,相关图表采用Origin 2021软件完成,采用AMOS 20.0绘制环境因素与土壤有机碳之间的结构方程模型。采用双因素方差分析对不同恢复年限、马尾松纯林以及混交林的实验数据进行显著性检验。环境因子与土壤微生物以及土壤有机碳之间的相关关系采用Pearson相关系数进行评价,显著性水平设为P<0.05。
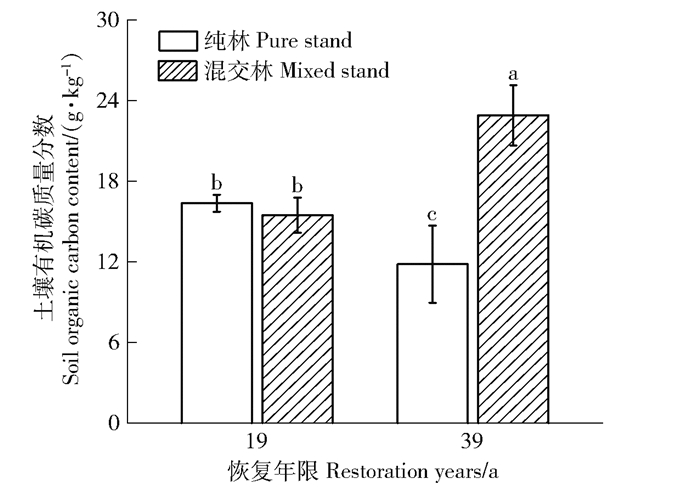
3 结果与分析 3.1 有机碳质量分数的变化恢复19 a样地表层SOC在马尾松纯林与马尾松和木荷混交林中无显著差异,恢复39 a混交林表层SOC质量分数比恢复19 a马尾松纯林高39.8%,比恢复39 a马尾松纯林高93.6%(P<0.01,图 1)。相同林分类型中,恢复39 a马尾松纯林表层SOC质量分数比恢复19 a马尾松纯林低27.8%(P<0.05),而恢复39 a混交林表层SOC质量分数比恢复19 a混交林高48.0%(P<0.05)。
|
小写字母表示不同恢复年限和林分4个处理间的显著差异,显著性水平为0.05,下同。 The lowercase letters indicate significant differences between the four treatments of different years and stands at the significance level of 0.05, the same below. 图 1 不同恢复年限样地土壤SOC质量分数的变化 Fig. 1 Changes of soil SOC content in different restoration years |
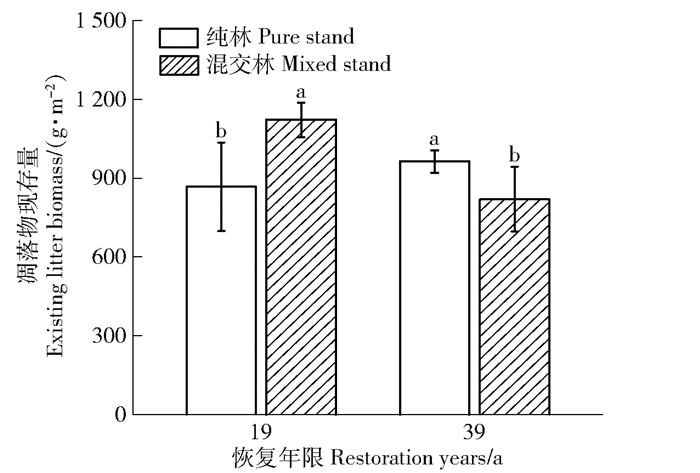
恢复19 a样地混交林凋落物现存量比纯林高29.4%(P<0.05,图 2),而恢复39 a混交林与纯林凋落物现存量减少14.9%(P<0.05)。相同林分类型中,恢复19 a和恢复39 a的马尾松纯林凋落物现存量无显著变化,而恢复39 a混交林凋落物现存量比恢复19 a纯林高低26.9%(P<0.05)。
|
图 2 凋落物现存量 Fig. 2 Existing litter biomass |
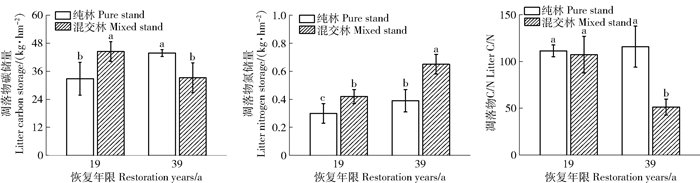
恢复19 a样地中,混交林凋落物C、N储量均显著高于相应的马尾松纯林(P<0.05,图 3),分别高35.5%和41.3%,而2种林分凋落物C/N无显著差异;恢复39 a样地中,混交林凋落物C储量比纯林低24.1%(P<0.05),N储量比纯林高67.3%(P<0.05),而C/N则比纯林显著下降55.8%(P<0.05)。相同林分类型中,恢复39 a纯林凋落物C储量比恢复19 a纯林高33.6%(P<0.05),而凋落物N储量和C/N无显著变化;恢复39 a混交林凋落物C储量和C/N均显著低于恢复19 a马尾松混交林(P<0.05),分别低25.2%和52.3%,而凋落物N储量则高55.0%(P<0.05)。
|
图 3 地表凋落物C、N储量及C/N Fig. 3 C, N storage and C/N ratio in litter |
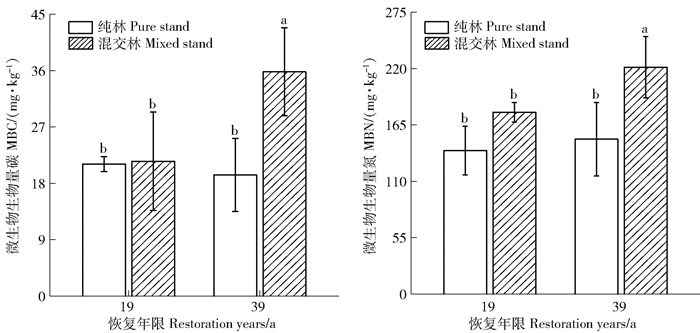
恢复19 a与39 a混交林土壤MBC均显著高于相应的马尾松纯林(P<0.05,图 4),分别高26.7%和46.5%;恢复19 a样地土壤MBN在2种林分中差异不显著,而恢复39 a样地混交林土壤MBN比纯林提高84.9%(P<0.05)。相同林分类型中,恢复19 a和39 a马尾松纯林土壤MBC和MBN变化均不显著,而恢复39 a混交林土壤MBC与MBN比恢复19 a混交林分别高24.7%和66.4%(P<0.05)。
|
图 4 不同恢复年限样地土壤微生物生物量碳和微生物生物量氮的变化 Fig. 4 Changes of MBC and MBN in different restoration years |
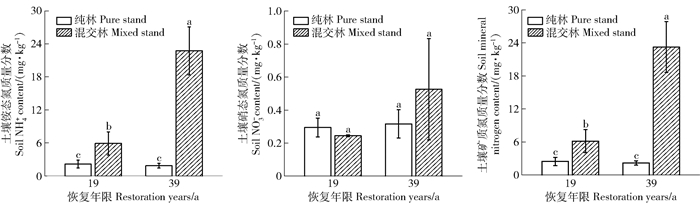
恢复19 a与39 a混交林土壤NH4+质量分数均显著高于相应的马尾松纯林,分别高173.7%和1 127.5%(P<0.05,图 5);恢复19 a与39 a混交林土壤NO3-质量分数与相应的马尾松纯林无显著差异;恢复19 a与39 a混交林土壤矿质氮质量分数均显著高于相应的马尾松纯林,分别高150.7%和972.6%(P<0.05)。在相同的林分类型中,恢复19 a与39 a的马尾松纯林土壤NH4+、NO3-和矿质氮质量分数变化均不显著,而恢复39 a的混交林土壤NH4+质量分数和矿质氮质量分数比恢复19 a的混交林分别高285.8%和279.0%(P<0.05),NO3-质量分数则无显著变化。
|
图 5 不同恢复年限样地土壤矿质氮质量分数的变化 Fig. 5 Changes of soil mineral nitrogen contents in different restoration years |
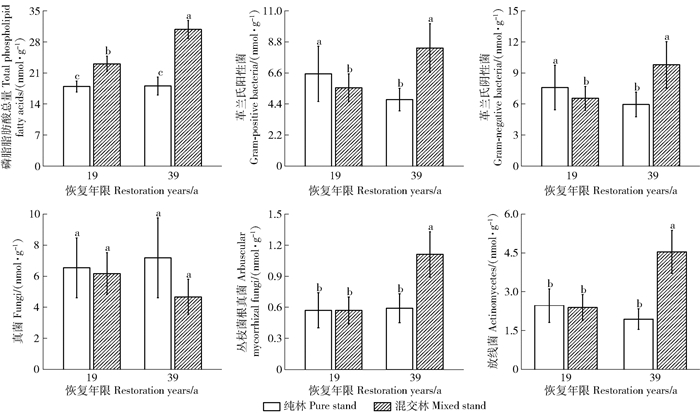
恢复19 a混交林与纯林土壤PLFAs、GP、GN、VAM和ACT均无显著差异,而恢复39 a马尾松+木荷混交林的PLFAs、GP、GN、VAM和ACT比纯林分别高36.0%、77.5%、64.6%、86.6%和133.8%(P<0.05)。相同林分类型中,恢复39 a混交林GP、GN、VAM和ACT比恢复19 a分别高50.8%、49.4%、93.3%和90.2%(P<0.05),而2个恢复年限纯林间PLFAs、GP、GN、VAM和ACT均无显著变化。另外,真菌在2个恢复年限和2种林分间差异均不显著,说明混交与林龄对真菌影响均不显著。
恢复19 a马尾松纯林与马尾松+木荷混交林革兰氏阳性菌与革兰氏阴性菌的比值(GP/GN)、真菌与细菌的比值(F/B)、饱和脂肪酸与单不饱和脂肪酸的比值(monounsaturated fatty acid/saturated fatty acid, mono/sat)和环丙基脂肪酸与前体结构的比值(cyclopropyl fatty acids/precursor structure, cy/pre)均无显著差异;恢复39 a混交林F/B比纯林低60.6%(P<0.05),而cy/pre、mono/sat均比纯林高27.1%(P<0.05),其他无显著差异(表 3)。相同林分类型中,恢复39 a纯林F/B比恢复19 a高43.5%(P<0.05),恢复39 a混交林的cy/pre和mono/sat分别比恢复19 a高(P<0.05),而F/B则低61.0%(P<0.05),其他均无显著差异。
| 表 3 土壤微生物磷脂脂肪酸标志物比值 Tab. 3 Soil microbial phospholipid fatty acid marker ratio |
相关分析可知,研究区内表层SOC质量分数皆与土壤MBN(0.734**)、矿物质氮(0.869**)、PLFAs(0.789**)、VAM(0.812**)、细菌(0.675**)呈现极显著正相关,与凋落物C/N(-0.836**)呈极显著负相关,与F/B(-0.806*)呈显著负相关,与MBC(0.563*)呈显著正相关。
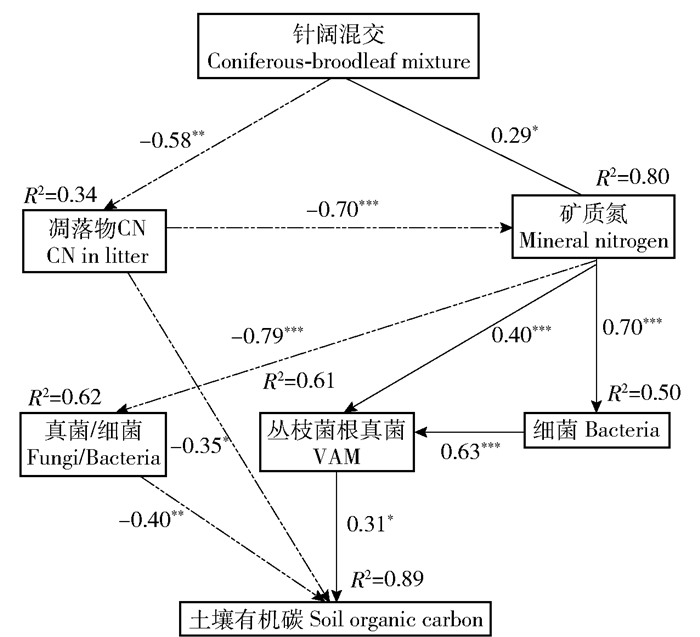
应用结构方程模型进一步揭示林分改造过程中影响表层SOC的关键过程。结果表明,松阔混交过程中凋落物C/N、氮有效性、F/B、VAM和细菌数量是驱动SOC变化的关键因子,其中凋落物C/N、VAM和F/B为直接影响因子,效应值分别为-0.348、0.311和-0.402,该模型解释了松阔混交对SOC作用的86.8%(图 7)。松阔混交提高凋落物质量,并直接影响着土壤碳氮水平,影响丛枝菌根真菌和细菌数量,改变微生物群落结构,最终影响SOC的积累。
4 讨论 4.1 松阔混交凋落物对土壤有机碳的影响近年来,关于针叶林改造为针阔混交林对SOC的影响大致呈现出不显著和正向显著2种结论[13],本研究中,恢复19 a样地马尾松+木荷混交林的表层SOC质量分数略低于马尾松纯林,差异不显著,这可能是在混交效应尚未触发的背景下,土壤异质性引起的微小差别;而恢复39 a样地中,混交林表层SOC质量分数显著高于马尾松纯林土壤(图 3),说明较长期混交对侵蚀退化地表层SOC产生显著的促进效应。混交效应产生的这种时间限制,主要与混交年限对凋落物质量的影响有关。
凋落物作为连接森林植物与土壤的关键媒介,是土壤碳库输入的重要来源。LÜ等[14]采用生物大分子和同位素示踪技术定量了林下植被芒萁对SOC的相对贡献,发现凋落物质量较高(C/N较低)的芒萁对侵蚀退化红壤马尾松人工林SOC的贡献高达54%~61%,凋落物质量可能是我国南方退化红壤区马尾松人工林土壤碳固存能力的关键影响因子。本研究以凋落叶C/N低的木荷为混交树种,使其在自然生长的过程中产生高质量凋落物,持续不断中和原有针叶树种马尾松所产生的低质量凋落物,即改变凋落物中难分解与易分解组分的比例以提高整体凋落物的质量。结果显示,短期(19 a)混交能够提高凋落物C储量,但并未提高凋落物质量;较长期(39 a)混交显著提高凋落物N储量,并降低凋落物C/N,说明通过马尾松与木荷混交提升凋落物质量是一个较长期的过程。其可能的原因为:混交前期,由于土壤肥力低,木荷生长不良,生产的凋落叶较少,对马尾松松针的高C/N中和作用不明显。随着恢复年限的增加,木荷凋落叶输入量引起其生长增大,加之木荷的枝叶和树根生物量积累及占全树的比率均比马尾松高,因此,低C/N的木荷叶在全部凋落物中所占比例增大,稀释效应不断加强,凋落物C/N下降,整体的凋落物质量随之明显提升。
4.2 松阔混交土壤微生物群落结构的响应及其对土壤有机碳的影响特定的气候和土壤条件下,微生物活动受凋落物的数量和质量的影响。植被类型改变凋落物中难、易分解组分的比例,调整其C、N等元素的质量分数[15],使凋落物的分解速率和周转速度随之变化,并改变土壤微生物基质利用的难易程度以及所能提供给微生物的碳源和氮源[16-17]。植物凋落物的C/N是其归还土壤后土壤MBC、MBN质量分数差异的主要原因,刘满强等[18]研究发现人工林土壤中MBC与MBN质量分数表现为小叶栎>混交林>木荷>马尾松,王春阳等[19]的室内凋落物添加实验表明加入低C/N凋落物的土壤MBC和MBN均高于加入高C/N凋落物的土壤。在本研究中,马尾松与木荷混交林的土壤MBC显著高于纯林且随时间增加,土壤MBN在恢复19 a时与马尾松纯林差异不显著,恢复39 a时显著高于纯林(图 4),表明凋落物质量提高有利于促进土壤MBC、MBN的增加,提高土壤有效养分,促进微生物生长与活跃。与此同时,结构方程模型表明,凋落物C/N的降低通过增加矿质氮的供应,诱导松阔混交林土壤微生物结构改变(图 7)。恢复39 a样地马尾松+木荷混交林表层土壤的微生物数量尤其是细菌和丛枝菌根真菌生物量显著高于纯林(图 6),且F/B在恢复39 a混交林中最小(表 3),说明松阔混交可在维持真菌生物量的同时,可提高细菌生物量进而调节微生物的群落组成。这可能是由于研究所采用的阔叶树种——木荷为内生菌根树种,可为细菌提供更多更丰富的易分解、小分子有机物,而细菌和其他腐生微生物分解有机质、促进氮的矿化,为丛枝菌根真菌提供养分,供植物生长,因此细菌与丛枝菌根真菌互利共生,丛枝菌根真菌和细菌数量不断增多。这类微生物周转速率相对较快,其数量增加将产生更多微生物残体,加之真菌周转速率也可能随土壤环境的改善而加快,由此导致更多的微生物残体不断在土壤中积累,增加微生物来源碳的贡献进而促进SOC的增加。
|
图 6 不同恢复年限样地土壤微生物群落组成的变化 Fig. 6 Changes of soil microbial community composition in different restoration years |
|
(x2=4.929, P=0.896, GFI=0.920, RMSEA=0)。其中,实线表示正效应,虚线表示负效应,箭头粗细表示影响强弱;箭头旁指数为权重系数;R2表示解释变量大小;RMSEA近似误差均方根;*, P<0.05;**, P<0.01; ***, P<0.001。 (x2=4.929, P=0.896, GFI=0.920, RMSEA=0). Solid or dashed line indicates positive or negative effects, respectively. Width of the arrow indicates strength of the effect. The digits besides the arrows are weight coefficients; R2 indicates for size of the variable and RMSEA is approximate error root mean square; *, P < 0.05; **, P < 0.01; ***, P < 0.001。 图 7 凋落物质量对土壤有机碳积累的调控机制 Fig. 7 Regulation mechanism of litter mass on soil carbon and nitrogen |
1) 较长期的松阔树种混交能显著提升侵蚀退化地马尾松人工林表层SOC质量分数,其有效性随恢复年限增加而增强。恢复19 a样地中,表层SOC在马尾松纯林与混交林中无显著差异;而恢复39 a样地中,混交林表层SOC质量分数较纯林高93.6%(P<0.05)。另外,恢复39 a混交林SOC质量分数较恢复19 a纯林和恢复19 a混交林分别高39.8%和48.0%(P<0.05)。
2) 侵蚀退化地马尾松人工林土壤表层SOC的积累主要受到凋落物质量和土壤氮素水平的限制,与MBC、MBN、PLFAs、矿质氮和细菌呈现显著或极显著正相关,与凋落物C/N和F/B呈显著或极显著负相关。
3) 在混交效应促发过程中,凋落物质量成为SOC质量分数变化的触发因子,微生物也发挥至关重要的作用,成为联接凋落物质量、土壤氮素水平与SOC的桥梁。马尾松与木荷混交后,随着恢复年限的延长,木荷凋落物持续输入引起的稀释效应,显著降低混交林凋落物的C/N,增加微生物养分来源和土壤N有效性,促进土壤微生物细菌类群和丛枝菌根真菌生物量,改变微生物群落结构,最终影响SOC的积累。未来退化马尾松林SOC水平提升的关键是进行林分改造,引入一定数量的凋落物质量较高的树种,适当的施肥可进一步促进土壤碳汇效应,助力实现碳中和战略目标。
| [1] |
联合国粮食及农业组织. 2022年粮食及农业状况[EB/OL]. [2022-12-02]. https://www.fao.org/publications/home/fao-flagship-publications/the-state-of-food-and-agriculture/2022/zh. Food and Agriculture Organization of the United Nations. The State of Food and Agriculture 2022[EB/OL]. [2022-12-02]. https://www.fao.org/publications/home/fao-flagship-publications/the-state-of-food-and-agriculture/2022/zh. |
| [2] |
LAL R. Soil carbon sequestration impacts on global climate change and food security[J]. Science, 2004, 304(5677): 1623. DOI:10.1126/science.1097396 |
| [3] |
LAL R. Soil management and restoration for C sequestration to mitigate the accelerated greenhouse effect[J]. Progress in Environmental Science, 1999, 1(4): 307. |
| [4] |
中华人民共和国水利部. 2021年中国水土保持公报[EB/OL]. [2022-07-16]. http://www.mwr.gov.cn/sj/tjgb/zgstbcgb/202207/t20220713_1585301.html. Ministry of Water Resources of the People's Republic of China. China soil and water conservation bulletin 2021[EB/OL]. [2022-07-16]. http://www.mwr.gov.cn/sj/tjgb/zgstbcgb/202207/t20220713_1585301.html. |
| [5] |
邓翠, 吕茂奎, 曾敏, 等. 红壤侵蚀区植被恢复过程中有机碳组分变化[J]. 水土保持学报, 2017, 31(4): 178. DENG Cui, LÜ Maokui, ZENG Min, et al. Changes of SOC components during vegetation restoration in eroded red soil region[J]. Journal of Soil and Water Conservation, 2017, 31(4): 178. |
| [6] |
DOU Xiaolin, XU Xia, SHU Xiao, et al. Shifts in soil organic carbon and nitrogen dynamics for afforestation in central China[J]. Ecological engineering, 2016, 87: 263. DOI:10.1016/j.ecoleng.2015.11.052 |
| [7] |
ZENG X, ZHANG W, CAO J, et al. Changes in soil organic carbon, nitrogen, phosphorus, and bulk density after afforestation of the "Beijing-Tianjin Sandstorm Source Control" program in China[J]. Catena, 2014, 118: 186. DOI:10.1016/j.catena.2014.01.005 |
| [8] |
XUE Liang, REN Huadong, LI Sheng, et al. Soil bacterial community structure and co-occurrence pattern during vegetation restoratio in karst rocky desertification area[J]. Frontiers in Microbiology, 2017, 8: 2377. DOI:10.3389/fmicb.2017.02377 |
| [9] |
LINAG Chao, SCHIMEL J P, JASTROW J D. The importance of anabolism in microbial control over soil carbon storage[J]. Nature Microbiology, 2017, 2(8): 1. |
| [10] |
VANCE E D, BROOKES P C, JEMKINSON D S. Microbial biomass measurements in forest soils: The use of the chloroform fumigation-incubation method in strongly acid soils[J]. Soil Biology & Biochemistry, 1987, 19(6): 697. |
| [11] |
FROSTEGÅRD Å, TUNLID A, BÅÅTH E. Use and misuse of PLFA measurements in soils[J]. Soil Biology and Biochemistry, 2011, 43(8): 1621. DOI:10.1016/j.soilbio.2010.11.021 |
| [12] |
LANDESMAN W J, DIGHTON J. Response of soil microbial communities and the production of plant-available nitrogen to a two-year rainfall manipulation in the New Jersey Pinelands[J]. Soil Biology & Biochemistry, 2010, 42(10): 1751. |
| [13] |
徐芷君, 刘苑秋, 方向民, 等. 亚热带2种针叶林土壤碳氮磷储量及化学计量比对混交的响应[J]. 水土保持学报, 2019, 33(1): 165. XU Zhijun, LIU Yuanqiu, FANG Xiangmin, et al. The responses of soil carbon, nitrogen and phosphorus storage andtheir stoichiometry in two coniferous forests to mixed effect in subtropical area[J]. Journal of Soil and Water Conserva-tion, 2019, 33(1): 165. |
| [14] |
LÜ Maokui, XIE Jinsheng, GIARDINA C P, et al. Understory ferns alter soil carbon chemistry and increase carbon storage during reforestation with native pine on previously degraded sites[J]. Soil Biology & Biochemistry, 2019, 132: 80. |
| [15] |
VEEN G F, FRESCHAT G T, ORDONEZ A, et al. Litter quality and environmental controls of home-field advantage effects on litter decomposition[J]. Oikos, 2015, 124(2): 187. DOI:10.1111/oik.01374 |
| [16] |
GILLESPIE L M, HTTENSCHWILER S, MILCU A, et al. Tree species mixing affects soil microbial functioning indirectly via root and litter traits and soil parameters in European forests[J]. Functional Ecology, 2021, 35(10): 2190. DOI:10.1111/1365-2435.13877 |
| [17] |
郭婧, 喻林华, 方晰, 等. 中亚热带4种森林凋落物量、组成、动态及其周转期[J]. 生态学报, 2015, 35(14): 4668. GUO Jing, YU Linhua, FANG Xi, et al. Litter production and turnover in four types of subtropical forests in China[J]. Acta Ecologica Sinica, 2015, 35(14): 4668. |
| [18] |
刘满强, 胡锋, 何园球, 等. 退化红壤不同植被恢复下土壤微生物量季节动态及其指示意义[J]. 土壤学报, 2003, 40(6): 937. LIU Manqiang, HU Feng, HE Yuanqiu, et al. Seasonal dynamics of soil microbial biomass and its significance to in dicate soil quality under different vegetations restored on degraded red soils[J]. Acta Pedologica Sinica, 2003, 40(6): 937. |
| [19] |
王春阳, 周建斌, 董燕婕, 等. 黄土区六种植物凋落物与不同形态N素对土壤微生物量碳N含量的影响[J]. 生态学报, 2010, 30(24): 7092. WANG Chunyang, ZHOU Jianbin, DONG Yanjie, et al. Effects of plant residues and nitrogen forms on microbial biomass and mineral nitrogen of soil in the Loess Plateau[J]. Acta Ecologica Sinica, 2010, 30(24): 7092. |