2. 中国科学院大学 北京 100049
2. University of Chinese Academy of Sciences, Beijing 100049, China
金红石是生产高档钛白粉、电焊条、金属钛及钛合金的主要原料[1-2]。我国天然金红石资源绝大多数为低品位原生矿,其储量占全国金红石资源总量的86%,而仅有14%的金红石砂矿适用于重选分离。在处理复杂的多金属低品位且细粒嵌布的原生金红石矿时,重力分离效率急剧下降[3]。随着浮选技术的发展,许多有效的捕收剂已成功应用于原生金红石矿的浮选,使泡沫浮选成为分离原生金红石和脉石矿物的最有效方法[4]。
Wang等[5]使用壬基异羟肟酸(Nonyl Hydroxamic Acid, NHA)作为捕收剂研究金红石的浮选行为及其表面化学性质。试验结果表明:在pH为6.2~8.3时,NHA对金红石有良好的捕收性能,它们以物理和化学的组合方式吸附在金红石表面。Li等[4]研究了在水杨羟肟酸存在时,Pb2+离子对金红石浮选的活化机制。结果表明:Pb2+离子活化后,水杨羟肟酸与羟基化的金红石表面形成TiO-Pb-SHA的化合物并吸附在金红石表面。Liu等[6]发现苯乙烯膦酸和正辛醇(Octanol, OCT)对金红石浮选有协同作用,认为苯乙烯膦酸化学吸附在金红石表面上,而正辛醇与苯乙烯膦酸相连,长链烃指向溶液内部。
尽管众多金红石的浮选捕收剂在实验室浮选中表现出了良好的性能,但目前SPA在金红石浮选工业中仍被广泛使用。然而,SPA在工业应用中的用量每吨矿石通常超过0.8 kg,几乎占整个浮选总成本的一半以上。近几十年来,含有机膦的化合物对水资源的污染已经引起了广泛的注意[7-9]。阴离子和非离子表面活性剂之间的相互作用一直是胶体化学的热点[10-13]。很多人在混合表面活性剂体系中发现了协同行为,其中临界胶束浓度远低于单独的体系,并且溶液的表面张力急剧下降[14-16]。阴离子与非离子表面活性剂之间的协同作用会对矿物浮选产生影响,导致阴离子表面活性剂吸附后非离子表面活性剂的吸附能力显著提高。阴离子和非离子表面活性剂以高度致密的混合单分子层的形式协同吸附在矿物表面[17-19]。
由于正壬醇(N-nonyl Alcohol, NNA)的碳链较长,NNA比OCT具有更好的效果。NNA的泡沫性质和疏水性强于OCT。在此研究中,通过浮选试验来研究NNA对金红石浮选的影响。通过泡沫性质测试、表面张力、Zeta电位测量和红外光谱分析来研究SPA和NNA在金红石表面的协同吸附机理。从固-液界面和气-液界面等几个方面分析了NNA对金红石浮选行为的影响,以及NNA和SPA的相互作用机制。这些结果希望对原生金红石矿的高效低毒的新型捕收剂的开发有所帮助。
1 样品和研究方法 1.1 样品制备实际矿石取自湖北枣阳金红石矿。矿样经过颚式破碎机和对辊破碎至3 mm以下,然后通过磨矿机研磨至74 μm以下占95%。样品的主要化学成分为3.08%的TiO2、0.013%的S、0.074%的P、13.55%的Fe2O3、7.32%的CaO、6.95%的MgO、16.72%的Al2O3、43.28%的SiO2、2.38%的Na2O和0.22%的K2O。因此,TiO2的品位仅为3.08%,主要杂质为SiO2、Al2O3、Fe2O3、CaO和MgO。有害元素是S和P,含量较低。样品的物相分析结果显示:其包含2.43%的金红石、0.63%的钛铁矿、0.04%的榍石、67.33%的角闪石、11.76%的钙铁榴石、7.74%的钠云母、3.10%的绿帘石、1.55%的绿泥石、0.89%的石英、2.29%的长石、1.25%的粘土和0.99%的其他杂质,其表明主要钛矿物是金红石。
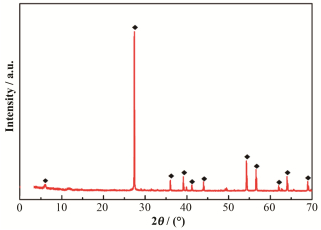
用于机理分析的单矿物金红石样品取自湖北枣阳金红石矿。首先手选挑出部分脉石矿物和杂质,将金红石样品用陶瓷球磨机粉碎并研磨。然后将38~74 μm的金红石颗粒储存在广口瓶中,并通过多次磁选分离,重选除杂和湿筛进行纯化。最后,反复用去离子水清洗矿物颗粒,并进行低温干燥。X射线衍射光谱分析(X-ray diffraction, XRD)的结果如图 1所示。详细的XRD操作参数参考Han等的研究[20]。XRD结果表明:单矿物金红石样品符合浮选的要求。
|
图 1 金红石单矿物的XRD图谱 Figure 1 The XRD pattern of rutile |
浮选试验在1.5L-XFD型浮选机中进行,矿浆浓度为30%(质量分数)。将500 g实际矿石样品磨矿至0.074 mm(占95%)后置于浮选槽中。然后依次加入pH调整剂、抑制剂和捕收剂。其中矿浆的搅拌时间分别为3 min、3 min和5 min。最后浮选5min,过滤和干燥浮选精矿和尾矿产品并称重,通过XRF测量精矿和尾矿产品中金红石的品位并计算回收率。
1.2.2 表面张力测量在室温条件下,使用具有铂板的BZY-1自动张力计测量溶液的表面张力。微束火焰除去Pt板上任何可能的有机污染物,直至Pt变亮。使用室温下的去离子水来校准每组测量的表面张力值。在测量之前,每个样品稳定10 min直至达到平衡。每个点取三个连续的测量值并取平均值。
1.2.3 Zeta电位测量用JS94H微电泳仪测定金红石表面的Zeta电位。将样品研磨至小于5 μm。在该测试中,将20mg单矿物金红石样品加入到含有10-3 mol∙L-1 KCl作为支持电解质的50 mL去离子水的100 mL烧杯中。加入相应的浮选试剂,然后将悬浮液在磁力搅拌器中搅拌15 min,使用NaOH或H2SO4溶液测量悬浮液pH。在各条件下重复测定三次,结果取平均值。
1.2.4 傅里叶变换红外光谱分析红外光谱由NEXUS-470光谱仪记录。取单矿物金红石样品(2.0 g)与40 mL溶液混合,然后在玛瑙研钵中研磨30 min,过滤并用相应的pH缓冲溶液冲洗三次。随后将样品在室温下真空干燥,然后进行傅里叶变换红外光谱(Fourier Transform Infrared Spectrometer, FT-IR)测量。
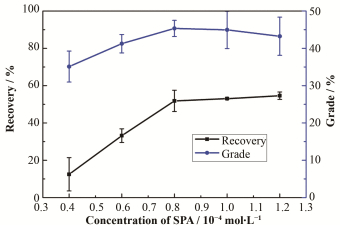
2 结果和讨论 2.1 浮选测试浮选精矿中金红石的品位和回收率随SPA浓度的变化关系如图 2所示。由图 2,随着SPA浓度的增加,精矿中金红石的品位和回收率都增加。特别是当SPA浓度为0.8×10-4 mol∙L-1时,精矿中金红石品位达最大值(约45%),此时回收率为52.26%。当SPA浓度继续增加时,品位明显下降,回收率略有增加。因此选择SPA浓度为0.8×10-4 mol∙L-1作为最佳用量。
|
图 2 精矿中金红石的品位和回收率与SPA浓度的变化关系 Figure 2 The grade and recovery of concentrate as a function of the concentration of SPA |
当混合捕收剂(SPA和NNA)的总用量为0.8×10-4 mol∙L-1时,精矿中金红石的浮选回收率和品位随NNA的比例变化关系如图 3所示。随着NNA比例的增加,金红石的浮选回收率先增加后降低,当NNA与SPA比例为1:1,金红石的浮选回收率达到最大值(79.16%),此时精矿中金红石的品位为49%。特别是当它们的比例超过80%时,回收率低于20%。结果表明:当NNA被单独作为浮选捕收剂时,几乎没有捕收能力。这与Sun等[21]发现脂肪醇对氧化矿物几乎没有捕收能力的现象相同。

|
图 3 固定混合捕收剂总用量为0.8×10-4 mol∙L-1时,精矿中金红石的回收率和品位随NNA的比例变化关系 Figure 3 The grade and recovery of rutile as a function of the proportion of NNA: fixed the total dosage of collectors (0.8×10-4 mol∙L-1) |
溶液中表面活性剂分子被固体表面吸附的现象与溶液的表面张力有关[22]。低的表面张力有利于吸附表面活性剂分子。表面活性剂浓度的增加,相当于表面张力的下降[23]。单层吸附具有有限容纳表面活性剂分子的能力,并且当表面活性剂达到一定浓度时,溶液的表面张力达到临界值,这一点在传统上被认为是临界胶束浓度(Critical Micelle Concentration, CMC)。其中表面被认为是接近饱和,形成的胶束与本体阻碍了表面活性剂的进一步吸附。
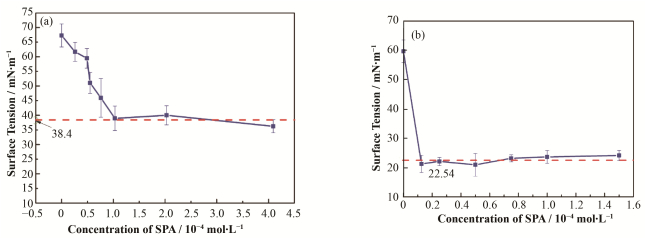
图 4显示溶液的表面张力随捕收剂浓度的变化关系。在图 4(a)中,虚线表示表面张力的平衡值,当表面张力达到平衡值时,表面活性剂浓度在CMC值附近。可以明显发现,SPA溶液的CMC值约为1.0×10-4 mol∙L-1。高的CMC值直接导致浮选捕收剂高的消耗,这也是金红石浮选过程中捕收剂SPA用量大的原因。在图 4(b)中,固定SPA浓度为0.4×10-4 mol∙L-1,溶液的表面张力约为60 mN∙m-1。加入NNA后,表面张力急剧下降。当NNA浓度为0.1×10-4 mol∙L-1时,表面张力达到平衡值。另外,图 4(b)中的平衡值(22.54 mN∙m-1)低于图 4(a)中的平衡值(38.40 mN∙m-1)。
|
图 4 溶液的表面张力随SPA (a)和NNA (b)浓度的变化关系 Figure 4 The surface tension of the solutions as a function of the concentration of SPA (a) and NNA (b) |
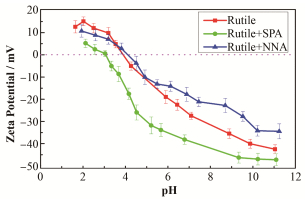
阴离子表面活性剂在矿物表面的吸附不可避免地导致其表面电势的变化。图 5显示了捕收剂吸附前后,金红石表面Zeta电位与矿浆pH的变化关系。在没有捕收剂存在时,金红石表面等电点出现在pH为4.0±0.1,这与以前的结果极为一致[24]。当0.4×10-4mol∙L-1的NNA存在时,金红石表面的Zeta电位在pH为2~5内没有明显变化,这表明NNA在pH为2~5内几乎不吸附在金红石表面上。然而,当0.4×10-4 mol∙L-1的SPA存在时,金红石表面的Zeta电位明显向负方向移动,这表明在研究的pH范围内,SPA以带负电荷的物质形式吸附在金红石表面。
|
图 5 金红石表面的Zeta电位随捕收剂浓度的变化关系 Figure 5 Zeta potential on the rutile surface as a function of pH without and with a single collector |
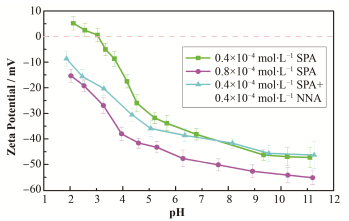
为了研究NNA和SPA的协同吸附效果,测量了SPA的不同浓度以及SPA和NNA的混合捕收剂对金红石表面Zeta电位的影响。图 6显示,随着SPA浓度的增加,金红石表面的Zeta电位显著降低(曲线1与曲线3比较),说明SPA的吸附量随着SPA浓度而明显增加。由曲线2和曲线3可知:由于两种情况下的SPA浓度相同,混合捕收剂存在时金红石表面Zeta电位明显低于单独SPA存在时。在图 5中,发现单独NNA几乎对金红石表面Zeta电位没有任何影响。很明显,NNA可以显著改善SPA在金红石表面的吸附行为。
|
图 6 不同的SPA浓度以及SPA和NNA的混合捕收剂对金红石表面Zeta电位的影响 Figure 6 Zeta potential on the rutile surface as a function of pH with different concentration of SPA and mixed SPA and NNA |
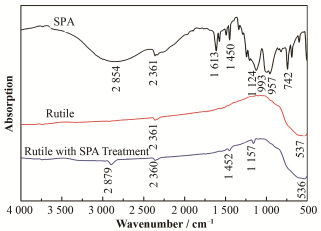
图 7显示SPA吸附前后金红石表面的红外光谱。SPA吸附后,在金红石表面出现了新的红外吸收峰。这些新的红外吸收峰分别位于1157 cm-1、1452 cm-1和2879 cm-1处,它们是SPA官能团的特征吸收峰[25-26]。结果表明:SPA与金红石表面羟基发生化学反应,并以化学吸附的形式吸附在金红石表面[6]。
|
图 7 SPA、金红石和用SPA处理的金红石红外光谱 Figure 7 The infrared spectrum of SPA, rutile and rutile treated with SPA |
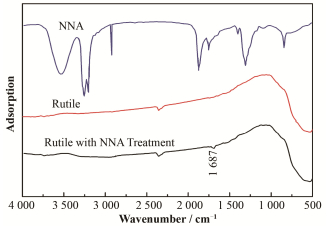
图 8显示了NNA吸附前后,金红石表面红外光谱的变化。然而,NNA吸附处理后的金红石表面并没有出现明显的红外吸收峰。在1687 cm-1处出现的红外吸收峰,并不是NNA的特征吸收峰。这表明单独的NNA几乎不吸附在金红石表面上,这与Zeta电位测量的结果极为一致。
|
图 8 NNA、金红石和NNA处理后金红石的红外光谱 Figure 8 The infrared spectrum of NNA, rutile and rutile treated with NNA |
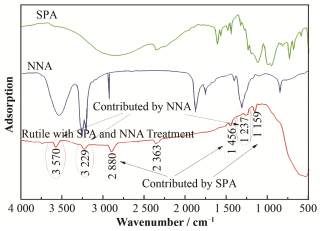
图 9显示了用SPA、NNA和SPA与NNA协同吸附处理后金红石表面的红外光谱。SPA和NNA协同吸附处理后的金红石表面出现了新的红外吸收峰。这些新出现的红外吸收峰包含了SPA(出现在1159 cm-1、1456 cm-1和2880 cm-1)和NNA(出现在1237 cm-1、3329 cm-1和3570 cm-1)的特征吸收峰特征[21]。这表明NNA可以在混合捕收剂处理后,吸附在金红石表面。结合前面的结果可以发现,NNA在金红石表面上的化学吸附是间接的,必须以SPA作为中间介质。
|
图 9 SPA、NNA和混合捕收剂SPA和NNA处理后金红石红外光谱 Figure 9 The infrared spectrum of SPA, NNA and rutile treated with mixed collector of SPA and NNA |
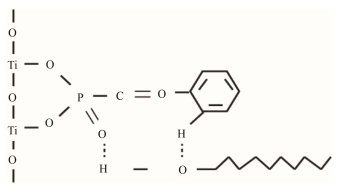
图 10是SPA与NNA的协同吸附模型。在前面试验研究的基础上,我们推断SPA和NNA在金红石表面的协同吸附机制应该是:SPA以化学吸附的形式优先吸附在金红石表面,然后NNA和SPA发生氢键作用,以SPA为桥梁,间接吸附在金红石表面。
|
图 10 SPA和NNA在金红石表面协同吸附模型 Figure 10 The model of the synergistic adsorption of SPA and NNA on the rutile surface |
1) 混合捕收剂的浮选指标明显优于单一捕收剂,并且混合捕收剂中SPA的用量仅为单独使用时的一半。
2) 当SPA与NNA的比例为1:1时,浮选指标达到最佳值,泡沫量和稳定性也处于最佳值。
3) 少量的NNA可以快速降低溶液的表面张力,溶液中的CMC可以从1×10-4 mol∙L-1降低到0.4×10-4 mol∙L-1。另外,平衡值处的表面张力从38.40 mN∙m-1显著降低至22.54 mN∙m-1。
4) 单一的NNA不能吸附在金红石表面,当NNA和SPA用作混合捕收剂时,SPA首先吸附在金红石表面上,然后NNA与SPA以氢键的形式连接,间接吸附在金红石表面。
| [1] |
Li T, Wu Y L, Wang Q F, et al. TiO2 crystalline structure and electrochemical performance in two-ply yarn CNT/TiO2 asymmetric supercapacitors[J]. Journal of Materials Science, 2017, 52(13): 7733-7743. DOI:10.1007/s10853-017-1033-6 |
| [2] |
Nam I, Park J, Park S, et al. Observation of crystalline changes of titanium dioxide during lithium insertion by visible spectrum analysis[J]. Physical Chemistry Chemical Physics, 2017, 19: 13140-13146. DOI:10.1039/C7CP01613A |
| [3] |
Terzi M, Kursun I. Investigation of recovery possibilities of rutile minerals from the feldspar tailings with gravity separation methods[J]. Russian Journal of Non-Ferrous Metals, 2015, 56(3): 235-245. DOI:10.3103/S106782121503013X |
| [4] |
Li H Q, Mu S X, Weng X Q, et al. Rutile flotation with Pb2+ ions as activator:adsorption of Pb2+ at rutile/water interface[J]. Colloids & Surfaces A Physicochemical & Engineering Aspects, 2016, 506: 431-437. DOI:10.1016/j.colsurfa.2016.06.046 |
| [5] |
Wang J, Cheng H W, Zhao H B, et al. Flotation behavior and mechanism of rutile with nonyl hydroxamic acid[J]. Rare Metals, 2016, 35(5): 419-424. DOI:10.1007/s12598-014-0386-0 |
| [6] |
彭勇军, 李晔, 许时. 苯乙烯膦酸与脂肪醇对金红石浮选的影响[J]. 中国有色金属学报, 1999, 9(2): 358-362. PENG Yongjun, LI Ye, XU Shi. Effect of interactions between styryl phosphoric acid and aliphatic alcohol on rutile flotation[J]. The Chinese Journal of Nonferrous Metals, 1999, 9(2): 358-362. DOI:10.19476/j.ysxb.1004.0609.1999.02.028 |
| [7] |
Xu R, Zhang M, Mortimer R J, et al. Enhanced phosphorus locking by novel lanthanum/aluminum-hydroxide composite:implications for eutrophication control[J]. Environmental Science & Technology, 2017, 51(6): 3418-3425. DOI:10.1021/acs.est.6b05623 |
| [8] |
Conley D J, Paerl H W, Howarth R W, et al. Ecology controlling eutrophication:nitrogen and phosphorus[J]. Science, 2009, 323(5917): 1014-1015. DOI:10.1126/science.1167755 |
| [9] |
Wang L J, Pan G, Shi W Q, et al. Manipulating nutrient limitation using modified local soils:a case study at Lake Taihu (China)[J]. Water Research, 2016, 101: 25-35. DOI:10.1016/j.watres.2016.05.055 |
| [10] |
Danov K, Kralchevsky P, Ananthapadmanabhan K. Micelle-monomer equilibria in solutions of ionic surfactants and in ionic-nonionic mixtures:a generalized phase separation model[J]. Advances in Colloid and Interface Science, 2014, 206: 17-45. DOI:10.1016/j.cis.2013.02.001 |
| [11] |
Milanovic M, Krstonosic V, Dokic L, et al. Insight into the interaction between Carbopol(A (R)) 940 and ionic/nonionic surfactant[J]. Journal of Surfactants and Detergents, 2015, 18(3): 505-516. DOI:10.1007/s11743-015-1677-7 |
| [12] |
Shi Z T, Chen J J, Liu J F, et al. Anionic-nonionic mixed-surfactant-enhanced remediation of PAH-contaminated soil[J]. Environmental Science and Pollution Research, 2015, 22(16): 12769-12774. DOI:10.1007/s11356-015-4568-6 |
| [13] |
Al-Faraji S, Al-Maamari R, Aoudia M. Sodium alkyl ether sulfonates (SAES):dual anionic-nonionic behavior in synthetic brine having high salinity and hardness[J]. Journal of Surfactants and Detergents, 2015, 18(1): 113-121. DOI:10.1007/s11743-014-1593-2 |
| [14] |
Wang L, Sun W, Hu Y H, et al. Adsorption mechanism of mixed anionic/cationic collectors in Muscovite-Quartz flotation system[J]. Minerals Engineering, 2014, 64: 44-50. DOI:10.1016/j.mineng.2014.03.021 |
| [15] |
Chen C, Zhu H L, Sun W, et al. Synergetic effect of the mixed anionic/non-ionic collectors in low temperature flotation of scheelite[J]. Minerals, 2017, 7(6): 87. DOI:10.3390/min7060087 |
| [16] |
Jiang H, Ji W, Yang Q, et al. Synergistic adsorption and flotation of new mixed cationic/nonionic collectors on muscovite[J]. Minerals, 2017, 7(5): 74. DOI:10.3390/min7050074 |
| [17] |
Zhang L, Kang W, Xu D, et al. The rheological characteristics for the mixtures of cationic surfactant and anionic-nonionic surfactants:the role of ethylene oxide moieties[J]. Rsc Advances, 2017, 7(22): 13032-13040. DOI:10.1039/c6ra28071d |
| [18] |
Zhao T H, Gu J Y, Pu W F, et al. Study on the synthesis and properties of an eco-friendly sugar-based anionic-nonionic surfactant[J]. Rsc Advances, 2016, 6(74): 70165-70173. DOI:10.1039/c6ra11596a |
| [19] |
Zhu P, Zhu Y, Xu Z C, et al. Effect of polymer on dynamic interfacial tensions of anionic-nonionic surfactant solutions[J]. Journal of Dispersion Science and Technology, 2016, 37(6): 820-829. DOI:10.1080/01932691.2015.1065502 |
| [20] |
Han J W, Jiao F, Liu W, et al. Innovative methodology for comprehensive utilization of spent MgO-Cr2O3 bricks:copper flotation[J]. Acs Sustainable Chemistry & Engineering, 2016, 4(10): 5503-5510. DOI:10.1021/acssuschemeng.6b01163 |
| [21] |
Sun L, Hu Y H, Sun W. Effect and mechanism of octanol in cassiterite flotation using benzohydroxamic acid as collector[J]. Transactions of Nonferrous Metals Society of China, 2016, 26(12): 3253-3257. DOI:10.1016/S1003-6326(16)64458-8 |
| [22] |
Langmuir I. The constitution and fundamental properties of solids and liquids[J]. Journal of the American Chemical Society, 1916, 38(11): 1221-2295. DOI:10.1021/ja02268a002 |
| [23] |
Shahir A, Arabadzhieva D, Petkova H, et al. Effect of under-monolayer adsorption on foamability, rheological characteristics, and dynamic behavior of fluid interfaces:experimental evidence for the guggenheim extended interface model[J]. Journal of Physical Chemistry C, 2017, 121(21): 11472-11487. DOI:10.1021/acs.jpcc.7b02483 |
| [24] |
Xiao W, Cao P, Liang Q N, et al. The activation mechanism of Bi3+ ions to rutile flotation in a strong acidic environment[J]. Minerals, 2017, 7(7): 113. DOI:10.3390/min7070113 |
| [25] |
Olu-Owolabi B, Unuabonah E. Kinetic and thermodynamics of the removal of Zn2+ and Cu2+ from aqueous solution by sulphate and phosphate-modified bentonite clay[J]. Journal of Hazardous Materials, 2010, 184(1): 731-738. DOI:10.1016/j.jhazmat.2010.08.100 |
| [26] |
Deval V, Kumar A, Gupta V, et al. Molecular structure (monomeric and dimeric) and hydrogen bonds in 5-benzyl 2-thiohydantoin studied by FT-IR and FT-Raman spectroscopy and DFT calculations[J]. Spectrochimica Acta Part A Molecular & Biomolecular Spectroscopy, 2014, 132(21): 15-26. DOI:10.1016/j.saa.2014.04.101 |


