2. 四川理工学院 化学与环境工程学院 自贡 643000
2. College of Chemistry and Environmental Engineering, Sichuan University of Science & Engineering, Zigong 643000, China
随着核工业的发展,必将产生大量放射性废物,铀作为主要放射性元素之一,其半衰期很长(T1/2 (235U)=7.04×108 a、T1/2 (238U)=4.47×109 a),且兼具重金属化学毒性和辐射危害[1]。在自然界中,铀常以+4和+6价化合物稳定存在[2]。其中以铀酰根离子(UO22+)形式存在的+6价铀易溶于水,且在地下水/岩土体系中具有很强的迁移性,容易对周边环境造成严重危害。
为了防止核素的泄露,当今国际上普遍采用“深地质处置法”来确保处置安全[3]。粘土岩因具有非渗透性、吸附性和自封闭性等性质[4],被广泛应用于放射性核素的处置,现已将内蒙古阿拉善粘土岩作为处置库围岩预选场址。高岭土作为粘土成分中的主要组分,具有物理化学性质相对稳定、渗透性差等特点,因此探究放射性核素在高岭土的吸附行为特征对深入了解粘土岩的吸附作用机理尤为重要。
现国内外大量学者对其他粘土矿物进行了研究,如Li等[5]探究了U(Ⅵ)在高庙子膨润土上的吸附特征,发现pH和离子强度对吸附影响较大;Du等[6]从pH、离子强度、腐殖酸和温度等影响因素出发,研究了伊利石对U(Ⅵ)的吸附特征;Troyer等[7]探究磷酸盐对U(Ⅵ)在蒙脱石上的吸附影响,发现磷酸盐不能增加蒙脱石对U(Ⅵ)的吸附。但针对放射性废物在粘土岩处置环境中的物理化学行为研究仍相对较少,同时由于地质构造的不同,不同深度和地质环境会造成较大的温度差异[8],而温度对核素在地质环境中物理化学行为特征具有重要的影响。因此本实验工作采用粘土矿物高岭土为吸附剂进行U(Ⅵ)的吸附行为研究,探讨了不同温度对U(Ⅵ)在高岭土上的吸附影响规律,为放射性废物处置安全评价提供一定的基础理论依据。
1 实验部分 1.1 仪器与试剂UV-1100型紫外可见分光光度计,上海美析仪器有限公司;Nicolet-5700红外吸收光谱仪,美国尼高力公司。
高岭土,上海市奉贤奉城试剂厂;八氧化三铀、氯化钠、氯化镁、氯化钾、无水氯化钙、碳酸氢钠、无水碳酸钠、硝酸钠、无水硫酸钠、偶氮胂(Ш)等均为分析纯试剂。
1.2 实验方法实验用液的配置:将八氧化三铀配置成质量浓度为1 g·L-1的U(Ⅵ)标液后进行实验。
实验部分:实验在298.15 K、308.15 K、318.15K和328.15 K下采用静态吸附法测定吸附后溶液中所剩U(Ⅵ)的浓度。在10 mL离心管中加入0.03 g高岭土和一定体积的去离子水,静置1 d后,加入一定量的U(Ⅵ)标液,振荡至吸附平衡后取出,离心(4000 r·min-1) 1 h,取1 mL上清液用紫外分光光度法[9]测定其中U(Ⅵ)的浓度。
1.2.1 U(Ⅵ)的初始浓度的影响探究U(Ⅵ)的初始浓度对不同温度下吸附实验的影响,以0.03 g高岭土为吸附剂,以6.00 mL、5.94mL、5.88 mL、5.76 mL、5.52 mL、5.04 mL去离子水为液相环境,分别加入6 μL、60 μL、120 μL、240 μL、480 μL、960 μL U(Ⅵ)标液作吸附质,吸附平衡后,测定溶液中U(Ⅵ)的含量。
1.2.2 pH的影响探究pH对不同温度下吸附实验的影响,以0.03g高岭土为吸附剂,以6 mL pH分别为3、5、7、9和11的HCl、NaOH溶液为液相环境,加入30 μL U(Ⅵ)标液作吸附质,吸附平衡后,测定溶液中U(Ⅵ)的含量。
1.2.3 共存离子的影响探究共存离子对不同温度下吸附实验的影响,以0.03 g高岭土为吸附剂,以6 mL浓度为0.01mol·L-1的Na+、Mg2+、K+、Ca2+、NO3-、Cl-、HCO3-、CO32-和SO42-溶液为液相环境,加入30 μL U(Ⅵ)标液作吸附质,吸附平衡后,测定溶液中U(Ⅵ)的含量。
1.3 分析方法分别在恒温298.15 K、308.15 K、318.15 K和328.15 K条件下考察高岭土对U(Ⅵ)的吸附性能,吸附性能可用吸附量表示,其关系表达式[10]为:
| $ q = \frac{{\left( {{C_0} - {C_{\rm{e}}}} \right)V}}{m} $ | (1) |
式中:q为单位质量高岭土对U(Ⅵ)的吸附量,μg·g-1;C0、Ce分别是吸附前后溶液中U(Ⅵ)的浓度,μg·L-1;V为溶液总体积,mL;m为吸附剂高岭土的质量,g。
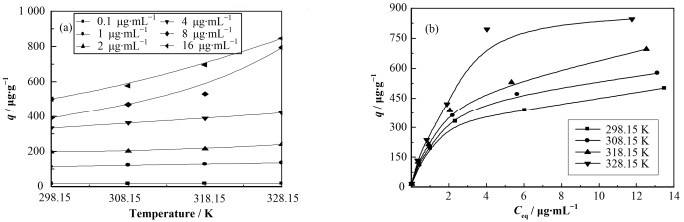
2 结果与讨论 2.1 高岭土对U(Ⅵ)的吸附等温线U(Ⅵ)浓度影响实验中,由式(1)得到298.15 K、308.15 K、318.15 K和328.15 K下高岭土对U(Ⅵ)的吸附效果图,如图 1所示。由图 1(a)可知,同一温度下U(Ⅵ)初始浓度越高,吸附量越大;由图 1(b)可知,随着温度的升高,高岭土对U(Ⅵ)的吸附效果越好。当U(Ⅵ)浓度较低时,高岭土对U(Ⅵ)的吸附较弱,此时温度的促进作用也较弱。当浓度增加时,升温对U(Ⅵ)在高岭土上吸附作用有明显的促进效果。实验说明,U(Ⅵ)浓度越高吸附效果越好;温度升高能够促进高岭土对U(Ⅵ)的吸附。
|
图 1 不同U(Ⅵ)的初始浓度下温度对吸附的影响(a)和高岭土对U(Ⅵ)的吸附等温线(b) Figure 1 Effect of temperature on the adsorption of U(Ⅵ) on kaolin under the different initial concentration of U(Ⅵ) (a), the adsorption isotherm of U(Ⅵ) on kaolin (b) |
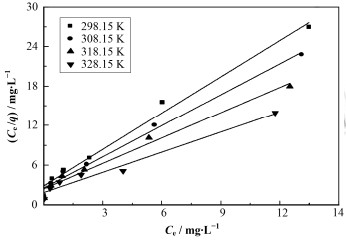
固-液体系的吸附过程可采用Langmuir吸附等温式[11]描述,并用其吸附模型对数据进行拟合,拟合结果如图 2所示。
| $ \frac{{{C_{\rm{e}}}}}{q} = \frac{1}{{b{q_{\max }}}} + \frac{{{C_{\rm{e}}}}}{{{q_{\max }}}} $ | (2) |
|
图 2 不同温度下高岭土对U(Ⅵ)的Langmuir吸附等温线 Figure 2 Langmuir adsorption isotherm of the adsorption of U(Ⅵ) on kaolin at different temperatures |
式中:b为Langmuir吸附常数;qmax为单位质量高岭土对U(Ⅵ)的最大吸附量,μg·g-1。
Langmuir等温吸附拟合数据如表 1所示,结合图 2和表 1可知,298.15 K、308.15 K、318.15 K和328.15 K下高岭土对U(Ⅵ)的最大吸附量分别为544.2 μg·g-1、637.0 μg·g-1、829.7 μg·g-1和986.5μg·g-1与实验值501 μg·g-1、576 μg·g-1、696μg·g-1和846 μg·g-1趋势相同,且随着温度的升高最大吸附量也增大。同时,Langmuir等温吸附模型的相关系数R2均大于0.96,说明Langmuir吸附模型能很好描述高岭土对U(Ⅵ)的吸附过程。
| 表 1 U(Ⅵ)在高岭土上吸附的Langmuir和Freundlich方程参数 Table 1 Langmuir and Freundlich equation parameter on the adsorption of U(Ⅵ) on kaolin |
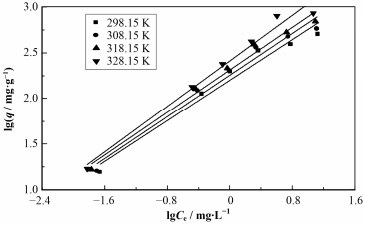
Freundlich等温吸附模型(图 3)也可用于高岭土对U(Ⅵ)的吸附过程,其线性关系式[12]为:
| $ \lg q = \lg {K_{\rm{F}}}{\rm{ + }}n\lg {C_{\rm{e}}} $ | (3) |
|
图 3 不同温度下高岭土对U(Ⅵ)的Freundlich吸附等温线 Figure 3 Freundlich adsorption isotherm of the adsorption of U(Ⅵ) on kaolin at different temperatures |
式中:KF、n为Freundlich吸附常数。
Freundlich等温吸附拟合数据如表 1所示。由表 1可知,0 < n < 1,说明高岭土对U(Ⅵ)的吸附属于优势吸附[13],且n均小于0.7,说明高岭土对U(Ⅵ)具有一定的亲和力,可以通过吸附去除溶液中的U(Ⅵ)。同时,lgKF可描述吸附量大小,lgKF越大,吸附量也越大。由表 1可知,lgKF又随着温度的升高而增大,说明温度越高吸附效果越好。
2.1.3 高岭土对U(Ⅵ)吸附热力学吸附热力学可用来判断高岭土对U(Ⅵ)的吸附过程的自发性以及吸附属于吸热过程还是放热过程,通过热力学研究可以了解吸附过程的趋势。高岭土对U(Ⅵ)吸附过程的热力学参数可由以下关系式得到[14]:
| $ \Delta G = - RT\ln K $ | (4) |
| $ {\left( {\frac{{\partial \Delta G}}{{\partial T}}} \right)_P} = - \Delta S $ | (5) |
| $ \Delta H = \Delta G + T\Delta S $ | (6) |
式中:R为理想气体常数,8.314 J·mol-1·K-1;T为温度,K;通过Kd (q/Ce)对Ce作图,其截距即为K值;P为压强,kPa;ΔG为吉布斯自由能,kJ·mol-1;ΔS为熵,kJ·K-1·mol-1;ΔH为吸附热,kJ·mol-1。
由式(4)、(5)、(6)得到U(Ⅵ)在高岭土上的吸附热力学函数值ΔG、ΔS、ΔH,如表 2所示。
| 表 2 U(Ⅵ)在高岭土上的吸附热力学参数 Table 2 Thermodynamic parameter on the adsorption of U(Ⅵ) on kaolin |
由表 2可知,熵ΔS为正值,说明高岭土对U(Ⅵ)的吸附使得吸附质分子自由度增加,吸附过程中熵是增加的;ΔG均为负值,说明高岭土对U(Ⅵ)的吸附是自发过程,且随着温度升高,吉布斯自由能逐渐减小,说明升温有利于吸附的自发进行;ΔH为正值,说明高岭土对U(Ⅵ)的吸附过程属于吸热过程,温度越高吸附效果越好,与Freundlich吸附模型拟合的分析结果一致。
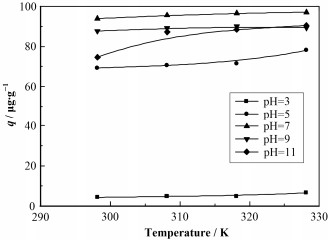
2.2 pH对吸附的影响在pH影响实验中,随着温度升高,高岭土对U(Ⅵ)的吸附能力增强;在水相pH改变条件下,pH对吸附的影响远大于温度的影响。其具体变化趋势如图 4所示。由图 4可知,升高温度对U(Ⅵ)在高岭土中的吸附有微弱的促进作用。在同一温度下,pH对吸附影响较大。当pH从3上升到7时,298.15K、308.15 K、318.15 K和328.15 K下的q分别快速从4.3 μg·g-1、4.9 μg·g-1、4.9 μg·g-1和6.6μg·g-1上升到93.9 μg·g-1、95.6 μg·g-1、96.6μg·g-1和97.1 μg·g-1,高岭土对U(Ⅵ)的吸附能力显著上升,当pH在7~11之间变化,q缓慢下降,分别降至74.6 μg·g-1、87.2 μg·g-1、88.4 μg·g-1和90.5 μg·g-1。可见pH为7时,高岭土对U(Ⅵ)的吸附效果最佳。
|
图 4 不同pH条件下温度对吸附的影响 Figure 4 Effect of temperature on the adsorption of U(Ⅵ) on kaolin at different pH |
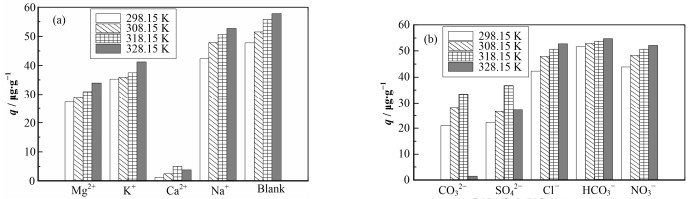
离子影响实验中,阳离子共存条件下,高岭土对U(Ⅵ)的吸附影响如图 5(a)所示。由图 5(a)可知,Na+、Mg2+、K+和Ca2+金属阳离子的存在均对吸附有抑制作用,其中抑制吸附效果最为明显的是Ca2+,这可能是因为Ca2+能够与高岭土中CO32-、HCO3-、OH-等阴离子反应,生成物覆盖在高岭土颗粒的表面,使其表面活性位点不能与UO22+结合,抑制吸附作用。其次是Mg2+、K+和Na+,Mg2+为二价阳离子,在竞争吸附时需要进攻两个负活性位点,导致Mg2+的抑制作用强于K+和Na+;同时K+的水合离子半径大于Na+的水合离子半径,根据竞争吸附规律:水合离子半径越小竞争能力越强[15],因此K+的抑制作用要强于Na+。在同一阳离子条件下,温度升高会促进高岭土对U(Ⅵ)的吸附作用。
|
图 5 共存阳离子(a)和阴离子(b)对吸附的影响 Figure 5 Effect of coexisting cations (a) and anions (b) on the adsorption of U(Ⅵ) on kaolin at different temperature |
阴离子共存条件下,高岭土对U(Ⅵ)的吸附影响如图 5(b)所示。由图 5(b)可知,Cl-、HCO3-和NO3-对实验影响较小,而CO32-和SO42-对吸附有抑制作用。推测其原理是CO32-和SO42-能与溶液中的UO22+结合生成UO2CO3、UO2(CO3)22-、UO2(CO3)34-和UO2SO4、UO2(SO4)22-、UO2(SO4)34-等配合物[16-17],抑制了高岭土对U(Ⅵ)的吸附。同时,温度对同一阴离子的影响整体呈促进作用,说明在不同温度下同一阴离子的吸附效果不同,温度越高,吸附效果越好。
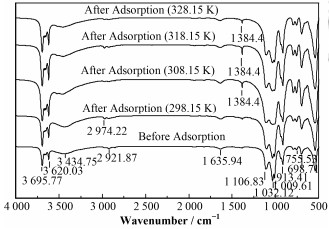
2.4 吸附前后高岭土的FT-IR光谱分析不同温度条件下吸附前后高岭土的红外光谱分析结果如图 6所示。由图 6可见,吸附前高岭土的波数在3695.77 cm-1和3620.03 cm-1处有较尖锐的吸收峰,是高岭土的O-H吸收峰,在两峰之间还有两处弱吸收峰,也是O-H振动引起的;1106.83cm-1、1032.12 cm-1和1009.61 cm-1处的吸收峰是Si-O伸缩振动引起的;913.41 cm-1、755.53cm-1和698.71 cm-1处的三个峰分别是由Si-O、Si-Si和Si-Al伸缩振动引起的。同时发现298.15 K、308.15 K、318.15 K和328.15 K下吸附U(Ⅵ)后的红外光谱图有所差异,当温度升高,峰值发生微小移动和强度变化,说明高岭土表面吸附了U(Ⅵ);当温度升至308.15 K时,在1384.4 cm-1处出现新峰,说明此时存在化学吸附。
|
图 6 吸附前后高岭土的FT-IR图谱 Figure 6 FT-IR spectra of kaolin before and after adsorption |
通过开展粘土矿物高岭土对U(Ⅵ)的吸附实验研究,探讨了不同温度对U(Ⅵ)在高岭土上的吸附影响规律,获得了以下结论:
1) 随着U(Ⅵ)初始浓度增加,高岭土对U(Ⅵ)的吸附量增加,由Langmuir等温吸附模型得到298.15 K、308.15 K、318.15 K和328.15 K高岭土对U(Ⅵ)的最大饱和吸附量分别为544.2 μg·g-1、637.0 μg·g-1、829.7 μg·g-1和986.5 μg·g-1;由Freundlich等温吸附模型可知,高岭土对U(Ⅵ)的吸附属于优势吸附,温度越高吸附效果越好;热力学研究表明:高岭土对U(Ⅵ)的吸附过程是自发的吸热过程。
2) 在水相pH改变条件下,pH对吸附的影响远大于温度的影响。当pH较低时,U(Ⅵ)在高岭土中的吸附有强烈抑制作用,pH升高至弱酸性、中性和碱性时可以促进吸附,在pH为7时,高岭土对U(Ⅵ)的吸附效果最佳,同时升高温度对U(Ⅵ)在高岭土中的吸附有促进作用。
3) 相同离子条件下温度对高岭土吸附U(Ⅵ)产生促进作用。共存离子中Ca2+、CO32-和SO42-对吸附有较大的抑制作用,其中Ca2+能够与高岭土中CO32-、HCO3-、OH-等阴离子反应,生成物会抑制吸附;CO32-和SO42-能与溶液中的UO22+结合生成配合物,减少了UO22+含量,使吸附量减少。
4) 通过对不同温度条件下高岭土吸附前后红外吸收光谱对比发现,298.15 K、308.15 K、318.15K和328.15 K下高岭土的红外吸收峰相对于吸附前的吸收峰发生了移动和强度变化,且温度升至308.15K时有新峰出现,说明温度达到一定值后,高岭土对U(Ⅵ)的吸附不仅是物理吸附,还存在化学吸附。
| [1] |
张晓菲, 赵长琦, 刘丽宏. 贫铀的危害及铀促排剂的研究进展[J]. 北京师范大学学报(自然科学版), 2010, 46(4): 517-521. ZHANG Xiaofei, ZHAO Changqi, LIU Lihong. Hazards of depleted uranium advance in uranium chelating agents research[J]. Journal of Beijing Normal University (Natural Science), 2010, 46(4): 517-521. |
| [2] |
郭建. 天然金属铀的首次发现[J]. 铀矿地质, 2016, 32(2): 128. GUO Jian. The first discovery of natural uranium[J]. Uranium Geology, 2016, 32(2): 128. DOI:10.3969/j.issn.1000-0658.2016.02.011 |
| [3] |
Wang P, Zhao Y A, Gao M, et al. Integrated geo-information database for geological disposal of high-level radioactive waste in China[M]. Springer Singapore, 2017. DOI:10.1007/978-981-10-4424-3_2
|
| [4] |
赖捷, 刘畅, 冷阳春, 等. 粘土岩对铀(Ⅵ)的吸附特征研究[J]. 四川大学学报(自然科学版), 2017, 54(4): 815-821. LAI Jie, LIU Chang, LENG Yangchun, et al. Study of adsorption characteristic uranium(Ⅵ) on clay rock[J]. Journal of Sichuan University (Natural Science), 2017, 54(4): 815-821. DOI:10.3969/j.issn.0490-6756.2017.04.025 |
| [5] |
Li S C, Wang X L, Huang Z Y, et al. Sorption and desorption of uranium(Ⅵ) on GMZ bentonite:effect of pH, ionic strength, foreign ions and humic substances[J]. Journal of Radioanalytical and Nuclear Chemistry, 2016, 308(3): 877-886. DOI:10.1007/s10967-015-4513-7 |
| [6] |
Du Y F, Yin Z X, Wu H Y, et al. Sorption of U(Ⅵ) on magnetic illite:effects of pH, ions, humic substances and temperature[J]. Journal of Radioanalytical and Nuclear Chemistry, 2015, 304(2): 793-804. DOI:10.1007/s10967-014-3893-4 |
| [7] |
Troyer L D, Maillot F, Wang Z, et al. Effect of phosphate on U(Ⅵ) sorption to montmorillonite:ternary complexation and precipitation barriers[J]. Geochimica Et Cosmochimica Acta, 2016, 175: 86-99. DOI:10.1016/j.gca.2015.11.029 |
| [8] |
吴海东. 高温条件下金刚石钻头钻进实验研究[D]. 吉林: 吉林大学, 2017. WU Haidong. Experimental research on diamond bit drilling under high temperature[D]. Jilin: Jilin University, 2017. http://cdmd.cnki.com.cn/Article/CDMD-10183-1017160704.htm |
| [9] |
杜浪, 李玉香, 马雪, 等. 偶氮胂Ⅲ分光光度法测定微量铀[J]. 冶金分析, 2015(1): 68-71. DU Lang, LI Yuxiang, MA Xue, et al. Determination of micro uranium by arsenazo Ⅲ spectrophotometry[J]. Metallurgical Analysis, 2015(1): 68-71. DOI:10.13228/j.b0yuan.issn1000-7571.009388 |
| [10] |
卢嘉炜, 苏伟, 谢华. 地质特种水泥对模拟含铀废液的静态吸附动力学研究[J]. 核技术, 2017, 40(9): 090501. LU Jiawei, SU Wei, XIE Hua. Study on static adsorption kinetics of simulated uranium-bearing wastewater by geological specialty cement[J]. Nuclear Techniques, 2017, 40(9): 090501. DOI:10.11889/j.0253-3219.2017.hjs.40.090501 |
| [11] |
李胜英, 钟光波, 陈伟芳, 等. Fe/SiO2复合材料的制备及其对Cd2+的吸附[J]. 化工环保, 2016(1): 73-77. LI Shengying, ZHONG Guangbo, CHEN Weifang, et al. Preparation of Fe/SiO2composite material and its adsorption capability to Cd2+[J]. Environmental Protection of Chemical Industry, 2016(1): 73-77. DOI:10.3969/j.issn.1006-1878.2016.01.015 |
| [12] |
吴婉滢, 姚广超, 张晓文, 等. 改性稻草对钍的吸附行为[J]. 核技术, 2015, 38(4): 040301. WU Wanying, YAO Guangchao, ZHANG Xiaowen, et al. Adsorption behavior of modified rice straw to thorium[J]. Nuclear Techniques, 2015, 38(4): 040301. DOI:10.11889/j.0253-3219.2015.hjs.38.040301 |
| [13] |
欧阳平, 范洪勇, 张贤明, 等. 粉煤灰对废润滑油中水的吸附热力学[J]. 功能材料, 2017, 48(3): 3063-3067. OUYANG Ping, FAN Hongyong, ZHANG Xianming, et al. Adsorption thermodynanmics of water in waste oil by flyash[J]. Journal of Functional Materials, 2017, 48(3): 3063-3067. DOI:10.3969/j.issn.1001-9731.2017.03.011 |
| [14] |
Gao Y, Chen C, Chen H, et al. Synthesis of a novel organic-inorganic hybrid of polyaniline/titanium phosphate for Re(Ⅶ) removal[J]. Dalton Transactions, 2015, 44(19): 8917-8925. DOI:10.1039/C5DT01093D |
| [15] |
张真瑞. 湖泊沉积物中不同级分富里酸对重金属吸附行为研究[D]. 内蒙古自治区: 内蒙古大学, 2017. ZHANG Zhenrui. Binding characteristics of heavy metals to natural fulvic acid fractions sequentially extracted from the lake sediments[D]. Inner Mongolia Autonomous Region: Inner Mongolia University, 2017. http://cdmd.cnki.com.cn/Article/CDMD-10126-1017104811.htm |
| [16] |
Jiang S B, Wang H Y, Zhong Z J, et al. Simulation of U(Ⅵ) speciation in human interstitial fluid[J]. Journal of Isotopes, 2011, 24(1): 52-57. |
| [17] |
Vercouter T, Vitorge P, Amekraz B, et al. Stoichiometries and thermodynamic stabilities for aqueous sulfate complexes of U(Ⅵ)[J]. Inorganic Chemistry, 2008, 47(6): 2180. DOI:10.1021/ic701379q |


