2. 中国科学院大学 北京 100049
2. University of Chinese Academy of Sciences, Beijing 100049, China
钍用于核燃料时存在一些有利特征[1],使得钍基混合氧化物作为潜在的先进核燃料受到了广泛的关注[2-5]。虽然232Th本身不是易裂变核素,但是其可以通过捕获中子而最终转变成易裂变的233U。钍铀混合氧化物存在于钍基核燃料循环的各个阶段。例如,使用ThO2作为增殖材料时,在中子辐照下会逐渐生成Th1-xUxO2混合氧化物。此外,也可以将ThO2与235U氧化物混合来使堆芯维持临界直到生成足够多的233U;另一方面,在钍基乏燃料后处理过程中Th1-xUxO2混合氧化物成分遭遇氧化后会变成Th1-xUxO2+y混合氧化物。钍铀混合氧化物的熔点、溶解性和氧化还原等物理化学性能与其微观结构存在密切联系。因此,深入研究钍铀混合氧化物的微观结构对钍基核燃料循环具有重要意义。
ThO2与UO2具有相近的几何结构,它们的晶体结构都是萤石结构,其Th和U被8个氧包围,分别形成U-O8和Th-O8立方体,只是Th-O和U-O键长存在差异。但是,ThO2和UO2拥有非常不一样的电子结构,ThO2是电荷转移绝缘体,而UO2是Mott绝缘体[6-7]。此外,与UO2的5f轨道能量低于6d轨道情况不同的是,ThO2的5f轨道能量高于6d轨道,且5f与6d轨道的能量差异更小[8]。UO2与ThO2之间的差异还体现在化学活性上,ThO2是化学惰性的,不与氧发生反应且难溶于水[9]。相反,UO2的化学活性较强,在温和的含氧环境下也会发生氧化反应,生成五价和六价化合物,其中最常见的UO22+铀酰结构非常容易溶解在水中。有研究发现,当U进入ThO2晶格后会形成钍铀氧化物固溶体,其晶胞参数随U含量的变化满足Vegard定律[10]。此外,有研究还发现钍铀混合氧化物中Th的存在会对U的氧化等行为产生影响[11]。要深入认识钍铀混合氧化物中Th对U的氧化还原行为的影响关键在于对Th1-xUxO2+y的局域结构进行研究。
基于同步辐射的X射线吸收精细结构(X-ray Absorption Fine Structure, XAFS)谱,包括X射线吸收近边谱(X-ray Adsorption Near Edge Structure, XANES)区域和扩展X射线吸收谱(Extended X-ray Adsorption Fine Structure, EXAFS)区域,能够提供与其它技术互补的结构信息,包括中心吸收原子的局域电子和几何结构[12-14]。由于同步辐射XAFS技术还具备元素选择性,可以分别对钍铀混合氧化物中钍和铀的局域结构进行研究。例如,Hubert等[15]利用EXAFS技术对Th1-xUxO2混合氧化物的局域结构进行了研究,结果发现其Th-O和U-O键长分别与纯ThO2和UO2相比变化很小,暗示着Th1-xUxO2存在局域晶格扭曲。众所周知,UO2的独特属性之一是它有能力适应多变的化学计量比,且在有氧环境例如空气中会逐步氧化成U3O7和U3O8。然而,二氧化铀氧化过程的许多重要方面仍然没有得到充分理解,对U被添加进入ThO2后形成的Th1-xUxO2+y混合氧化物的微观结构还缺乏深入认识。
本文采用共沉淀法合成了具有不同U含量的钍铀混合氧化物样品(Th1-xUxO2+y),结合粉末X射线衍射(X-ray Diffraction, XRD)表征,利用同步辐射XAFS技术研究了Th1-xUxO2+y样品中Th和U的局域结构,进一步对Th0.8U0.2O2+y样品的EXAFS实验数据进行了拟合,得到了键长和配位数等局域几何结构信息,深入分析了Th-U相互作用对Th0.8U0.2O2+y的微观结构影响。
1 实验部分利用共沉淀法制备了不同U含量的钍铀混合氧化物样品。首先将适量前驱物Th(NO3)4·6H2O与UO2(NO3)2·6H2O溶解在去离子水中,配置成具有不同Th/U摩尔比例的混合溶液,然后在磁力搅拌条件下滴加过量的氨水溶液,溶液中有浅黄色沉淀物生成,利用离心机将生成的浅黄色凝胶沉淀物离心下来,弃上清液后加去离子水对沉淀物进行清洗后再离心,把得到的浅黄色凝胶转移至烘箱中,于60℃温度下干燥48 h,得到干凝胶,然后将干凝胶放入马弗炉中800 ℃煅烧8 h得到灰黑色固体,最后将固体研磨制得钍铀混合氧化物粉末样品。通过改变前驱物混合溶液中Th/U摩尔比例,我们制备了U摩尔含量分别为5%、10%和20%的钍铀混合氧化物粉末样品,形式上写为Th1-xUxO2+y样品(x=0.05、0.1、0.2;0 < y < 0.2)。在相似的实验条件下制备了ThO2和U3O8标样,将部分U3O8标样置于管式炉中,然后在5% H2+95% Ar气氛中1300℃还原处理16 h制得UO2标样。
实验室制得的Th1-xUxO2+y样品和UO2标样的粉末XRD数据是在Bruker D8先进X射线衍射仪上测量得到,X射线源采用Cu靶的Kα发射线,使用Ni作为滤光片,电子管电流和电压分别为40 mA和40 kV,扫描的2θ角范围是10°~90°,扫描步长0.02°,数据点积分时间0.15 s。
Th1-xUxO2+y样品的Th和U L3边XAFS实验数据是在上海同步辐射光源(Shanghai Synchrotron Radiation Facility, SSRF)的BL14W1线站上[16]采集得到。上海光源的电子储存环能量是3.5GeV,采用恒流模式(Top-up operation)运行,将电子束流维持在约250 mA。线站使用双晶Si(111)单色器将X光单色化,利用气体电离室测量入射和透射X光强度,在透射模式下采集样品的Th L3边XAFS,利用32元Ge固体探测器在荧光模式下收集样品的U L3边XAFS信号。使用Zr金属箔进行单色器的能量校正。每个样品的XAFS数据都是在室温下测量两遍之后作平均处理。实验过程中没有发现X射线导致的样品氧化。使用Demeter软件包对样品的Th和U L3边XAFS谱进行规范化的数据处理和分析[17]。利用Athena软件获得归一化的吸收系数,然后使用Artemis软件对EXAFS数据进行理论拟合。通过FEFF 9.0程序计算获得理论相移和散射振幅。对3.0~120 nm-1范围的k3加权EXAFS振荡进行傅里叶变换,拟合相关实验数据时R空间窗口选择0.12~0.45 nm。通过拟合ThO2和UO2标样来确定Th和U的振幅衰减因子S02分别为0.75和0.76。根据Nyquist公式:Nind=2ΔRΔk/π,设定拟合所使用的独立参数个数。最终通过拟合得到局域结构参数,例如配位数(N)、键长(R)、Debye-Waller因子(σ2)和内势能移动(ΔE0)。
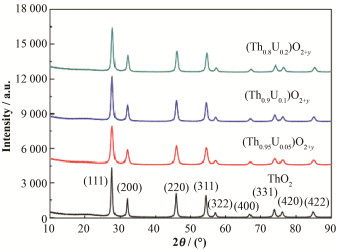
2 结果与讨论我们对实验上制备好的Th1-xUxO2+y和ThO2样品进行了粉末XRD表征,以确定其晶型(图 1),XRD实验数据显示:Th1-xUxO2+y样品只存在与ThO2类似的萤石晶格结构衍射峰,其中27.7°、32°、45.9°、54.5°和57°衍射峰分别对应于ThO2的(111)、(200)、(220)、(311)和(222)晶面,说明制备的钍铀混合氧化物不存在显著的相分离。对XRD谱图进行仔细观察发现,随着U含量增加,Th1-xUxO2+y样品的衍射峰逐渐向高衍射角方向轻微移动,说明Th1-xUxO2+y样品的晶胞长度随U含量增加出现了一定程度的收缩,这主要是因为掺杂的U具有比Th更小的半径而导致Th1-xUxO2+y样品的晶格参数略小于ThO2。由于U和Th原子半径存在差异,掺杂可能导致晶格出现局域扭曲,同时Th和U可能出现局部的相分离。为了进一步研究Th1-xUxO2+y样品的Th和U局域结构及Th-U相互作用,我们对Th1-xUxO2+y样品进行了同步辐射XAFS技术表征。
|
图 1 合成的Th1-xUxO2+y与ThO2样品的粉末XRD数据 Figure 1 Powder XRD patterns of as-synthesized Th1-xUxO2+y and ThO2 samples |
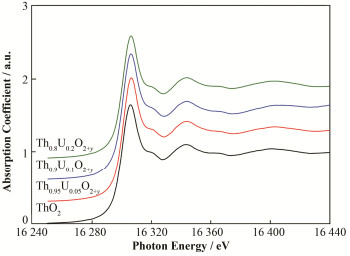
Th1-xUxO2+y样品与ThO2的Th L3边XANES数据见图 2,从图 2可以看出,Th1-xUxO2+y与ThO2的XANES谱图几乎是一样的,这说明Th1-xUxO2+y样品中Th的局域结构与ThO2中的相同。这一点与预期一致,因为XAFS技术提供的是平均结构信息,Th1-xUxO2+y样品中大多数的Th都不与U发生直接相互作用,保持了与ThO2一致的局域结构。与钍氧化物一般只有正四价(ThO2)一种化学态相比,铀氧化物存在多种价态且结构灵活多变,例如UO2、U4O9、U3O7和U3O8等。由于Th1-xUxO2+y中的U含量比Th低得多,Th-U相互作用更容易反映在U的局域结构上。因此,U L3边XAFS提供的平均结构信息中应该包含有更大比例的Th-U相互作用信息。
|
图 2 ThO2、Th0.95U0.05O2+y、Th0.9U0.1O2+y、Th0.8U0.2O2+y的Th L3边XANES实验数据 Figure 2 Th L3-edge XANES of ThO2, Th0.95U0.05O2+y, Th0.9U0.1O2+y and Th0.8U0.2O2+y |
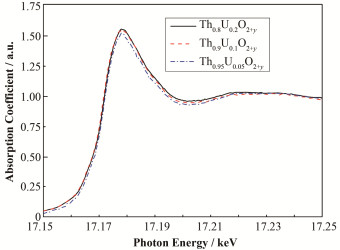
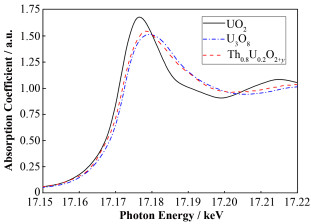
Th1-xUxO2+y样品的U L3边XANES实验数据见图 3。XANES谱中17180 eV附近的强峰(白线峰)对应于从2p轨道到6d轨道的电子跃迁。Th1-xUxO2+y样品之间展现出很相似的XANES谱形,说明Th1-xUxO2+y样品具有很接近的U局域结构。通过与UO2和U3O8相对照,Th0.8U0.2O2+y样品表现出与U3O8更相似的XANES谱形(图 4),表明Th0.8U0.2O2+y中的U具有与U3O8相似的主导局域结构。但是,Th0.8U0.2O2+y样品与U3O8标样之间存在的XANES谱形差异也是可以被明显观察到,二者的白线峰形状存在差异,且XANES谱上不同峰之间的相对位置也存在差异,这些差异可以认为是由于Th0.8U0.2O2+y存在Th-U相互作用导致其U局域结构不完全等同于纯U3O8。仔细观察Th0.8U0.2O2+y的XANES谱形,可以发现其存在少量趋向于UO2的谱形特征。
|
图 3 Th1-xUxO2+y的U L3边XANES实验数据 Figure 3 The U L3-edge XANES of Th1-xUxO2+y |
|
图 4 Th0.8U0.2O2+y样品与UO2和U3O8的U L3边XANES实验数据的对比 Figure 4 Comparison of Th0.8U0.2O2+y, UO2 and U3O8 at the U L3-edge XANES |
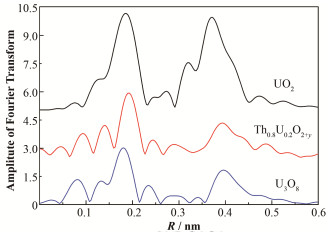
Th0.8U0.2O2+y样品与UO2和U3O8标样相对照的U L3边EXAFS傅里叶变换数据见图 5。可以看出,Th0.8U0.2O2+y样品具有与U3O8更相似的峰型,0.15~ 0.25 nm之间的主峰归属于U-O的散射贡献。由于Th和U的散射相移接近,很难完全区分U-Th和U-U散射贡献,所以0.35~0.45 nm之间的主峰归属于U-U/Th的散射贡献。值的注意的是,虽然Th0.8U0.2O2+y和U3O8的U-U/Th散射峰很相似,但是Th0.8U0.2O2+y的U-O散射峰的位置与U3O8相比存在明显的向右移动,暗示着平均U-O键长增加。
|
图 5 Th0.8U0.2O2+y样品与UO2和U3O8在U L3边EXAFS傅里叶变化数据上的对比 Figure 5 Comparison of Th0.8U0.2O2+y, UO2 and U3O8 under Fourier transform at the U L3-edge EXAFS |
为了进一步得到配位数和键长等局域结构参数,对Th0.8U0.2O2+y样品和ThO2、UO2、U3O8标样的Th或U L3边EXAFS实验进行了拟合。由于Th0.9U0.1O2+y和Th0.95U0.05O2+y的U L3边EXAFS数据信噪比差,没有对其进行EXAFS数据拟合,只是对Th0.8U0.2O2+y样品的EXAFS数据进行了拟合。对ThO2和UO2标样进行拟合时,考虑到Th-O和U-O都是8配位,Th-Th和U-U单重散射路径都是12重简并(相当于12配位),因此,对这些标样进行拟合时先将这些配位数固定下来。同理,对U3O8进行拟合时,也是先根据晶体结构判断U-O和U-U单重散射路径的种类和简并度,然后将U-O和U-U配位数设定为理想值。对Th0.8U0.2O2+y、ThO2的Th L3边EXAFS谱和Th0.8U0.2O2+y、UO2、U3O8的U L3边EXAFS谱进行数据拟合后得到的结果汇编在表 1中,获得了配位数和键长等局域结构信息。
| 表 1 拟合Th0.8U0.2O2+y、ThO2、UO2及U3O8的Th和U L3边EXAFS实验数据得到的结构参数 Table 1 Structural parameters obtained from the analysis of fitting the EXAFS spectra at Th and U L3-edge for Th0.8U0.2O2+y, ThO2, UO2 and U3O8 |
从表 1可以知道,Th0.8U0.2O2+y样品的Th局域结构很接近于ThO2标样,其Th-Th/U键长比ThO2略微短一点。Th0.8U0.2O2+y样品中U的局域结构与U3O8的相似,特别是存在相似的U-U散射路径,这说明Th0.8U0.2O2+y样品中存在局域U3O8结构。由于U3O8具有与ThO2不一样的晶格对称性结构,微观U3O8结构会从ThO2晶格结构中析出,出现XRD难以观察到的局域相分离。然而,Th0.8U0.2O2+y样品U-O配位结构与U3O8之间仍存在一些明显的差异,两者具有不同的U-O配位情况和U-O键长,这说明局域U3O8成分与ThO2成分存在Th-U相互作用,导致U-O结构发生变化。从表 1可以看出,Th0.8U0.2O2+y样品有两种U-O配位,键长分别为0.210 nm和0.232 nm,其中0.232 nm的U-O键长是U3O8中不具备的U-O键长,该U-O键是接近于UO2的U-O键(0.234 nm),这些特点可以看成是Th0.8U0.2O2+y样品中的局域U3O8成分与ThO2成分存在Th-U相互作用,该相互作用导致U出现了类似UO2的U-O结构,即UO2特征。
3 结语用同步辐射XAFS技术研究钍铀混合氧化物的钍和铀的局域结构,提供了与XRD技术互补的结构信息,包括钍和铀的价态、配位数、键长等。通过对共沉淀法制备得到的Th1-xUxO2+y混合氧化物样品的Th和U的L3边XAFS实验数据进行分析,结果表明:Th1-xUxO2+y混合氧化物的主导结构是ThO2成分与局域U3O8成分的混合,出现了微观相分离。进一步对Th0.8U0.2O2+y样品的EXAFS实验数据进行分析和拟合,发现ThO2成分与局域U3O8成分之间存在Th-U相互作用,实验结果表明:Th-U相互作用的存在会导致Th0.8U0.2O2+y中Th-Th/U键长与纯ThO2相比有略微缩短,同时,ThO2成分通过Th-U相互作用对局域U3O8成分的U-O结构进行调制,使Th0.8U0.2O2+y样品出现了与纯UO2中U-O键长接近的U-O配位成分。
致谢 感谢上海光源提供XAFS实验机时及BL14W1线站职工在调光和数据采集上给予的帮助。| [1] |
Myllykyla E, Koivula L, Tanhua-Tyrkko M, et al. Direct alpha spectrometry for analysing leached ThO2 pellets[J]. Journal of Nuclear Materials, 2017, 493: 69-76. DOI:10.1016/j.jnucmat.2017.06.003 |
| [2] |
Vauchy R, Belin R C, Robisson A C, et al. Actinide oxidation state and OM ratio in hypostoichiometric uranium-plutonium-americium U0.750Pu0.246Am0.004 O2-x mixed oxides[J]. Inorganic Chemistry, 2016, 55(5): 2123-2132. DOI:10.1021/acs.inorgchem.5b02533 |
| [3] |
Ma J J, Du J G, Wan M J, et al. Molecular dynamics study on thermal properties of ThO2 doped with U and Pu in high temperature range[J]. Journal of Alloys and Compounds, 2015, 627: 476-482. DOI:10.1016/j.jallcom.2014.11.223 |
| [4] |
Strach M, Belin R C, Richaud J C, et al. Influence of phase separation on the oxidation of (U, Pu)O2-x[J]. Journal of Physical Chemistry C, 2015, 119(40): 23159-23167. DOI:10.1021/acs.jpcc.5b07407 |
| [5] |
Ghosh P, Kuganathan N, Galvin C, et al. Melting behavior of (Th, U)O2 and (Th, Pu)O2 mixed oxides[J]. Journal of Nuclear Materials, 2016, 479: 112-122. DOI:10.1016/j.jnucmat.2016.06.037 |
| [6] |
Wen X D, Martin R L, Roy L E, et al. Effect of spin-orbit coupling on the actinide dioxides AnO2 (An=Th, Pa, U, Np, Pu, and Am):a screened hybrid density functional study[J]. Journal of Chemical Physics, 2012, 137(15): 416. DOI:10.1063/1.4757615 |
| [7] |
Petit L, Svane A, Szotek Z, et al. Electronic structure and ionicity of actinide oxides from first principles[J]. Physical Review B, 2010, 81(4): 045108. DOI:10.1103/PhysRevB.81.045108 |
| [8] |
Shein I R, Ivanovskii A L. Thorium compounds with non-metals:electronic structure, chemical bond, and physicochemical properties[J]. Journal of Structural Chemistry, 2018, 49(2): 348-370. DOI:10.1007/s10947-008-0134-0 |
| [9] |
Neck V, Altmaier M, Muller R, et al. Solubility of crystalline thorium dioxide[J]. Radiochimica Acta, 2003, 91(5): 253-262. DOI:10.1524/ract.91.5.253.20306 |
| [10] |
Purans J, Heisbourg G, Dacheux N, et al. XAFS study of local structure with picometer accuracy:Th1-xUxO2 and Th1-xPuxO2 solid solutions[J]. Physica Scripta, 2015, T115: 925-927. DOI:10.1238/Physica.Topical.115a00925 |
| [11] |
Cakir P, Eloirdi R, Hubei F, et al. Thorium effect on the oxidation of uranium:photoelectron spectroscopy (XPS/UPS) and cyclic voltammetry (CV) investigation on (U1-xThx)O2 (x=0 to 1) thin films[J]. Applied Surface Science, 2017, 393: 204-211. DOI:10.1016/j.apsusc.2016.10.010 |
| [12] |
Ghigna P, Spinolo G. High-energy X-ray absorption spectroscopy in materials chemistry[J]. Science of Advanced Materials, 2015, 7(10): 2216-2233. DOI:10.1166/sam.2015.2270 |
| [13] |
Ankudinov A L, Ravel B, Rehr J J, et al. Real-space multiple-scattering calculation and interpretation of X-ray-absorption near-edge structure[J]. Physical Review B, 1998, 58(12): 7565-7576. DOI:10.1103/PhysRevB.58.7565 |
| [14] |
Shi W Q, Yuan L Y, Wang C Z, et al. Exploring actinide materials through synchrotron radiation techniques[J]. Advanced Materials, 2014, 26(46): 7807-7848. DOI:10.1002/adma.201304323 |
| [15] |
Hubert S, Purans J, Heisbourg G, et al. Local structure of actinide dioxide solid solutions Th1-xUxO2 and Th1-xPuxO2[J]. Inorganic Chemistry, 2006, 45(10): 3887-3894. DOI:10.1021/ic050888y |
| [16] |
Yu H S, Wei X J, Li J, et al. The XAFS beamline of SSRF[J]. Nuclear Science and Techniques, 2015, 26(5): 050102. DOI:10.13538/j.1001-8042/nst.26.050102 |
| [17] |
Ravel B, Newville M. Athena, artemis, hephaestus:data analysis for X-ray absorption spectroscopy using IFEFFIT[J]. Journal of Synchrotron Radiation, 2005, 12: 537-541. DOI:10.1107/S0909049505012719 |


