2. 中国科学院大学 北京 100049
2. University of Chinese Academy of Sciences, Beijing 100049, China
干法后处理技术因具有耐辐照、放射性废物少等优点,使其成为了适合钍基熔盐堆燃料盐在线处理的首选分离技术[1]。相比于传统的水法后处理技术,干法技术是一种建立在以液态金属、卤化物熔盐等为介质的乏燃料高温化学工艺过程,由于高温、强腐蚀性、辐射的存在以及熔盐化学过程的复杂性,干法后处理技术发展过程中仍有许多基础科学问题和关键技术瓶颈有待阐明和突破[2]。在常见的干法分离技术中,减压蒸馏通常被用来回收载体盐,由于裂变产物化合物与盐在蒸发行为上的差异从而实现它们的分离和盐的回收净化。
美国橡树岭国家实验室在20世纪60年代就开展了针对氟盐体系的减压蒸馏技术的研究,主要用于解决熔盐实验堆(Molten Salt Reactor Experiment, MSRE)燃料载体盐分离回收过程中所涉及的科学和技术问题[3−8]。Kelly[4]提出用减压蒸馏法可以去除熔盐中的稀土裂变产物,并有效回收LiF及BeF2。另外,当80%的熔盐被蒸馏时,Eu的分离因子超过1000;当98%的盐被蒸馏分离后,Eu的去污系数则变为50。Singh等[5]证明了减压蒸馏法可有效分离LiF和Ca、Mg、Mn等氟化物。Hightower等[6]在1273 K、67~200 Pa下测定了一系列的氟化物相对于载体盐LiF-BeF2的挥发度,结果表明:载体熔盐LiF-BeF2的挥发度比稀土元素(Ce、La、Nd、Sm、Ba、Sr、Pr、Eu、Y)氟化物挥发度高三个数量级,为在工程量级上验证蒸馏分离熔盐堆载体盐提供了重要的基础数据。Cantor等[7]使用气体雾沫法在1273~1333 K范围内研究了LiF-BeF2-LaF3熔盐混合物的减压蒸馏行为。在1273 K和1301 K时测量得LaF3的去污因子分别为910和1150。Scott[8]在1173~1323 K的温度范围内,测量了Nd、Sm、Eu、Pr等物质相对LiF的挥发度,大部分三价稀土氟化物的相对挥发度在0.01~0.05,且这一数值随着温度的升高而降低。
近年来,由于快堆的发展,美、韩等国开展氯化物熔盐的干法分离研究[9−10]。韩国原子能研究院利用带有称重元件的减压蒸馏装置,研究了不同熔盐体系中氯化物在蒸馏过程中的动态变化[11−14]。Kim等[12]对电解还原后的LiCl-Li2O熔盐(约含有20%的碱土金属)在1173 K、13 Pa条件下的蒸馏行为进行了研究。结果表明:仅有30%的BaCl2、SrCl2伴随着LiCl一同被蒸发,且加入BaCl2、SrCl2、Li2O物质后,盐的蒸发速率明显降低。Cho等[13]通过向熔盐中鼓入氧气使氯化稀土转变为不溶性的氧化稀土或氯氧化稀土沉淀,由于氧化稀土与LiCl-KCl熔盐存在较大的蒸气压差异,因此二者可以实现有效的分离。
尽管氟化物和氯化物熔盐在低压下的蒸馏行为已经得到了比较广泛的研究,但研究重点都集中在稀土等阳离子的存在对蒸发行为的影响,体系中的阴离子都是氟或氯,对于含有氟化物的氯盐体系的减压蒸馏行为研究则鲜有报道。我们在前期的研究过程中发现,将含有氟化钍的氟化物熔盐溶解在氯化物熔盐中,能有效地利用电解沉积的方法实现金属钍的回收并得到较高的分离度[15−16]。然而电解产物总是不可避免地夹带少量的熔盐,影响了钍的进一步重构和再利用。美国阿贡国家实验室提出了基于减压蒸馏的产物净化技术,得到了较好的分离纯化效果[8]。另一方面,伴随着钍电解的同时会产生大量含有裂变产物氟化物的氯化物熔盐,它们的净化和回收对于放射性废物的最小化有着重要的意义。鉴于混合体系的减压蒸馏行为尚未得到足够的重视,我们拟以含有NdF3、CeF3、EuF3、LaF3、SrF2、ZrF4等氟化物的LiCl-KCl熔盐体系为对象,确定氟化物存在的情况下蒸发比例以及氟化物种类对LiCl-KCl熔盐减压蒸馏行为的影响,初步阐明氟氯混合熔盐体系的基本规律。
1 实验及方法 1.1 试剂及仪器试剂:NdF3、CeF3、EuF3、LaF3、SrF2、ZrF4、LiCl、KCl,纯度99.99%,均采购自Sigma-Aldrich;氩气,纯度99.999%,上海娄氧气体罐装有限公司;硝酸,规格/SPEC:UPS级(68%),苏州晶瑞化学股份有限公司。
仪器:电感耦合等离子体原子发射光谱仪(Inductively Coupled Plasma-Atomic Emission Spectrometry, ICP-AES),型号Optima 8000,美国PerkinElmer公司;X射线多晶衍射仪(X-ray Diffraction, XRD),X' Pert Pro MPD,荷兰帕纳科公司;电热恒温加热板,型号ER-35S,协郝(上海)仪器科技有限公司。
1.2 实验装置各熔盐的制备在与氩气气氛的手套箱相连的电加热炉中进行,电阻炉的参数详见文献[17]。减压蒸馏装置采用卧式真空蒸发炉,由刚玉材质炉膛、蒸发坩埚、加热器、不锈钢薄板收集器和真空系统组成。蒸馏时抽真空,盐蒸气在不锈钢薄板上冷凝收集,而剩余盐仍残留于坩埚内。刚玉管长600 mm,加热长度为250 mm,内径为25 mm。镍质蒸发坩埚截面积为9.12 cm2。
1.3 样品的制备LiCl-KCl熔盐的熔融:手套箱内将干燥好的LiCl、KCl按摩尔比为58.5%:41.5%准确称量于镍坩埚内,置于手套相连的电阻炉中,于823 K下保温8 h降为室温后取出,机械粉碎成粉末。
质量分数5% CeF3的LiCl-KCl熔盐:将一定量的CeF3与LiCl-KCl以5:95质量分数比混合均匀,置于与手套箱相连的电加热炉中,至973 K下保温6 h,使其充分熔融后自然冷却,降为室温后取出,对盐的不同部位取样进行均匀性分析。
同样的方法制备不同氟化物的LiCl-KCl熔盐,将混合盐粉碎后保存于手套箱内备用。
1.4 掺杂氟化物的LiCl-KCl盐的蒸馏在氩气气氛的手套箱内称取4 g掺杂氟化物的LiCl-KCl盐于蒸发坩埚内,坩埚置于卧式蒸发炉中,密封后抽真空,蒸发炉以10 K∙min−1的速率升至823K后,关闭真空泵,通入氩气至2.0×104 Pa,以抑制盐的蒸发,并保温30 min,使熔盐充分熔融且除去炉膛内的水汽,继续以6 K∙min−1的速率升至蒸发温度,并开启真空泵,蒸发一定时间后关闭泵通入氩气至常压从而抑制盐的蒸发。待温度降为室温后取出,对蒸馏收集盐进行成分分析测定。
1.5 样品分析样品中的Ce、Nd、Eu、La、Sr、Zr、K、Li等元素含量均采用ICP-AES分析确定。每次实验后将收集到的盐样品粉碎成粉末,准确称量三份熔盐粉末平行样于聚四氟乙烯罐中,样品质量50~60mg,用浓HNO3在473 K溶解2 h,用去离子水稀释至相应浓度进行测试,实验结果为平行样测试结果的平均值。熔盐样品整体蒸发量由实验前后熔盐质量差获得。
熔盐的蒸发比例的计算公式为:
| $ \mathit{\Phi} ={{m}_{1}}/{{m}_{0}} $ | (1) |
式中:m0为实验前含有氟化物熔盐中的总质量;m1为实验后冷却收集盐的质量,g。
收集盐中金属元素的去污系数DF来表征目标元素的分离情况:
| $ \text{DF}={{C}_{0}}/{{C}_{1}} $ | (2) |
式中:C0与C1分别为原料盐中金属元素及冷凝收集盐中金属元素的质量分数,wt%。
2 结果与讨论 2.1 蒸发比例对LiCl-KCl蒸馏行为的影响由于温度是影响物质蒸发的主要因素之一,首先参考文献[18]确定了1000~1150 K下纯LiCl-KCl熔盐的蒸发条件。结果表明:LiCl-KCl熔盐的平均蒸发速率在压力为130 Pa、温度为1000 K、1050 K、1100 K时分别为0.008 g∙min−1∙cm2、0.014g∙min−1∙cm2、0.024 g∙min−1∙cm2。为便于通过控制蒸发时间来改变蒸发比例,实验中选用的氟氯混合盐的质量约4 g,蒸发坩埚面积约9.3 cm2,蒸发温度为1050 K,蒸发时间控制在30 min以内,通过改变蒸馏时间以获得不同蒸发比例。
以含有5% CeF3的LiCl-KCl熔盐为对象,研究了它在1050 K、130 Pa条件下的蒸发行为。表 1给出了不同蒸发比例下收集盐中Ce的含量与去污系数。通过对不同蒸发比例下得到的收集盐进行化学分析可以发现,随着蒸发比例的增大,收集盐中的稀土含量逐渐升高。例如,在蒸发比例为24%的情况下,蒸馏收集盐中Ce的质量分数仅为0.0015%,其去污系数为2.3×103。随着原料盐的蒸发比例进一步增大,剩余盐中Ce的浓度增大,部分的Ce会夹带在LiCl-KCl中一起蒸发,尽管其所占质量分数仍然维持在较低的水平。当蒸发比例达到95%时,收集盐中Ce的质量分数增加了一倍,这也导致其去污系数下降为1.1×103。
| 表 1 不同蒸发比例下5% CeF3-LiCl-KCl蒸馏收集盐中Ce的去污系数(1050 K,130 Pa) Table 1 DFs of Ce in the collected salts from low pressure distillation of 5% CeF3-LiCl-KCl at different evaporation ratios (1050 K, 130 Pa) |
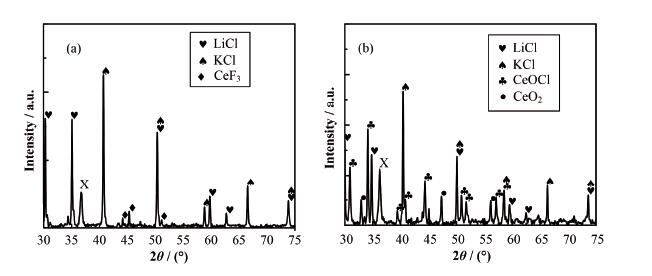
利用XRD分析蒸发比例分别为24%和90%时剩余盐的组成,如图 1所示。在手套箱内将剩余盐研磨均匀,取约0.5 g样品于载玻片上,为防止吸潮,用聚乙烯薄膜包裹,XRD谱图表现为37°附近的薄膜峰X。蒸发比例为24%(图 1(a))时主要出现了分别位于30.10°、34.88°、50.12°、59.60°和28.35°、40.51°、50.17°、58.64°等位置的LiCl、KCl特征衍射峰,以及27.90°、44.05°、45.21°、51.02°等处的CeF3特征衍射峰;当蒸发比例进一步提高到90%时(图 1(b)),剩余盐中除了LiCl和KCl的衍射峰信号,还有CeOCl、CeO2的特征衍射峰。这说明随着蒸发比例的增大,受到微量氧的影响,稀土进一步转化为氯氧化物或氧化物。
|
图 1 5% CeF3-LiCl-KCl蒸发剩余盐的XRD图谱 (a)蒸发比例24%,(b)蒸发比例90%,X:聚乙烯膜 Figure 1 XRD spectra of the collected salt from the low pressure distillation of 5% CeF3-LiCl-KCl mixture (a) Evaporation ratio 24%, (b) Evaporation ratio 90%, X: polythene film |
对于真实的熔盐堆乏燃料盐,其中涉及的氟化物远不止CeF3一种。前期开展的氟化物蒸发行为研究表明,不同氟化物对载体氟盐的蒸发行为存在着一定的影响[19],因此有必要对含有不同氟化物的氯盐蒸发行为进行研究。除了§2.1中提到的CeF3,我们选取了其他几种典型的氟化物,如稀土氟化物LaF3、NdF3、EuF3、碱土氟化物SrF2以及ZrF4。之所以选取ZrF4是由于熔盐堆载体盐中除了氟化锂铍,还含有一定浓度的氟化锆[6]。表 2列出了含有5%氟化物的LiCl-KCl熔盐在蒸发比例约为95%时,收集盐中各元素的浓度及去污系数。可以看出,大部分稀土氟化物和SrF2的去污系数都比较接近,均能达到103,这与它们相比于氯盐具有较低的蒸气压是一致的。相比之下,Eu的去污系数明显低于其他稀土,这一结果与FLiNaK体系中得到的结果相似[19],表明在氯化物熔盐体系中EuF3也是容易还原为EuF2,EuF2的存在导致了铕的去污系数降低。对于ZrF4来说,已有的实验结果表明,在LiF-BeF2-REF3的混合物中,氟化稀土相对氟化锂的挥发度在10−3~10−5级,而氟化锆相对氟化锂的挥发度为1.4[6],而且ZrF4在1050 K时,饱和蒸气压为4000Pa,远高于LiCl和KCl的饱和蒸气压(130 Pa和70Pa)[20],这也是造成锆的去污系数非常低的重要原因。
| 表 2 蒸发比例为95%时蒸馏收集盐中金属氟化物的去污系数(1050 K,130 Pa) Table 2 DFs of metal fluorides in the collected salts after low pressure distillation at the evaporation ratio of 95% (1050 K, 130 Pa) |
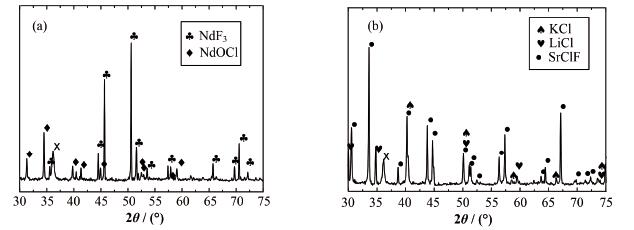
对蒸馏后剩余盐的XRD谱图分析(图 2(a))表明,含有5% NdF3的LiCl-KCl盐在蒸发比例为95%时,剩余盐中基本观察不到LiCl及KCl的衍射峰,出现了位于25.73°、31.43°、34.58°、45.02°、41.40°、57.99°及59.14°的NdOCl的特征衍射峰以及NdF3。Eun等[21]通过研究发现,氧气鼓泡可以使LiCl-KCl熔盐中的NdCl3转变为Nd2O3及NdOCl,并且其转化率与通入氧气的时间及反应温度有关。由于设备的密封性,蒸馏过程中含有NdF3的LiCl-KCl熔盐体系可能与泄露进入系统内的氧气反应从而生成卤氧化物。另外,已有研究表明,氯化稀土在923 K且有氧的环境中可转变为氯氧化物,继续升高温度导致氯氧化稀土脱氯并转化成稀土氧化物[11]。氯化钕与氧气反应的吉布斯自由能变小于0,表明转化反应在高温下是可以发生的[22]。
|
图 2 蒸发剩余盐的XRD图谱 (a) NdF3-LiCl-KCl,(b) SrF2-LiCl-KCl,X:聚乙烯膜 Figure 2 XRD spectra of the collected salts from low pressure distillation of NdF3-LiCl-KCl (a), SrF2-LiCl-KCl (b), X: polythene film |
含有碱土金属SrF2的蒸馏剩余盐的XRD谱图(图 2(b)B)显示了KCl、LiCl的存在,但并没有观察到SrCl2或SrF2的衍射峰。相反,在谱图中出现了氟氯混合物SrClF的特征衍射峰,其特征信号峰为25.70°、25.58°、30.62°、33.67°、40.32°、43.85°、56.41°。含有LaF3、EuF3的氯盐经蒸馏后所得剩余盐的XRD谱图显示,这些稀土元素仍以氟化物的形式存在。在ZrF4-LiCl-KCl的蒸馏剩余盐中没有出现氟化锆的信号,这与ZrF4容易挥发的性质一致。
对于CeF3-LiCl-KCl蒸发收集盐的分析结果表明,收集盐中LiCl和KCl的摩尔分数分别为59.25%和40.75%,其摩尔比与初始盐的摩尔比相近。进一步利用离子色谱分析收集盐中的氟离子浓度,确定氟离子浓度低于0.3%,表明利用减压蒸馏收集得到的LiCl-KCl盐满足回收再利用的要求。
3 结语本工作采用了减压蒸馏方法研究了NdF3、CeF3、EuF3、LaF3、SrF2、ZrF4等氟化物掺杂的LiCl-KCl混合盐在1050 K、130 Pa条件下的蒸发行为。研究结果表明:随着蒸发比例的增大,5% CeF3-LiCl-KCl混合盐经蒸馏后得到的剩余盐中Ce的去污系数逐渐减小,而剩余盐中CeF3的量逐渐减小,同时出现了CeOCl和CeO2。含有氟化物NdF3、CeF3、LaF3、SrF2的LiCl-KCl盐在蒸发比例为95%时,收集盐的去污系数约为103,而EuF3和ZrF4的去污系数则明显低于其他氟化物。EuF3在高温下发生还原反应形成了相对易挥发的EuF2,导致了收集盐中Eu的去污系数偏低。ZrF4则由于其较高的蒸气压导致ZrF4和LiCl-KCl同时蒸发,使其去污系数明显降低。对蒸发剩余盐的分析表明,La、Eu等稀土元素仍以氟化物的形式存在,Nd的剩余盐中出现了NdOCl而Sr的剩余盐中出现了SrClF。在ZrF4-LiCl-KCl的蒸馏剩余盐中没有出现氟化锆的信号,这与ZrF4容易挥发的性质是一致的。从CeF3-LiCl-KCl蒸发收集盐的分析结果来看,利用减压蒸馏收集得到的LiCl-KCl盐满足回收再利用的要求。由于EuF3与ZrF4在同等条件下的去污系数较低,无法通过减压蒸馏净化含这两种氟化物的氯盐,因此还需要与其他技术相结合才能提高这两种元素的去污效果。
| [1] |
Goff K M, Simpson M F. Dry processing of used nuclear fuel[C]. Proceedings of Global 2009, INL/Con-09-15984, 2009.
|
| [2] |
刘学刚. 乏燃料干法后处理技术研究进展[J]. 核化学与放射化学, 2009, 31(s1): 35-44. LIU Xuegang. Research on dry reprocessing technology of spent nuclear fuel[J]. Journal of Nuclear and Radiochemistry, 2009, 31(s1): 35-44. |
| [3] |
Rosenthal M W, Haubenreich P N, Briggs R B. The development status of molten-salt breeder reactors[R]. ORNL-4812, USA: ORNL, 1972.
|
| [4] |
Kelly M J. Recovery of carrier salt by distillation[R]. ORNL-3789, USA: ORNL, 1965.
|
| [5] |
Singh A J, Ross R G, Thoma R E. Vacuum distillation of LiF[J]. Journal of Applied Physics, 1964, 36(4): 1367-1370. DOI:10.1063/1.1714310 |
| [6] |
Hightower J, McNeese L E. Measurement of the relative volatilities of fluorides of Ce, La, Pr, Nd, Sm, Eu, Ba, Sr, Y and Zr in mixtures of LiF and BeF2[R]. ORNL-TM-2058, USA: ORNL, 1968.
|
| [7] |
Cantor S. Transpiration studies in support of the vacuum distillation process[R]. ORNL-4037, USA: ORNL, 1967: 140-142.
|
| [8] |
Scott C D, Carter W L. Preliminary design study of a continuous fluorination-vacuum distillation system for regenerating fuel and fertile streams in a molten salt breeder reactor[R]. ORNL-3791, Tennessee, USA: Oak Ridge National Laboratory, 1966.
|
| [9] |
Lacquement J, Bourg S, Boussier H, et al. Pyro-chemistry assessment at CEA-last experimental results[C/CD]. Proceedings of Global 2007, Boise, Idaho, 2007.
|
| [10] |
Lee H, Park G, Kang K, et al. Pyroprocessing technology development at KAERI[J]. Nuclear Engineering & Technology, 2011, 43(4): 317-328. DOI:10.5516/NET.2011.43.4.317 |
| [11] |
Eun H C, Cho Y Z, Park H S, et al. Study on a recovery of rare earth oxides from a LiCl-KCl-RECl3 system[J]. Journal of Nuclear Materials, 2011, 408: 110-115. DOI:10.1016/j.jnucmat.2010.11.021 |
| [12] |
Kim I S, Chung D Y, Park M S, et al. Evaporation of CsCl, BaCl2, and SrCl2 from the LiCl-Li2O molten salt of the electrolytic reduction process[J]. Journal of Radioanalytical and Nuclear Chemistry, 2014, 303: 223-227. DOI:10.1007/s10967-014-3330-8 |
| [13] |
Cho Y Z, Lee T K, Eun H C, et al. Purification of used eutectic (LiCl-KCl) salt electrolyte from pyroprocessing[J]. Journal of Nuclear Materials, 2013, 437(1-3): 47-54. DOI:10.1016/j.jnucmat.2013.01.344 |
| [14] |
Eun H C, Choi J H, Kim N Y, et al. A reactive distillation process for the treatment of LiCl-KCl eutectic waste salt containing rare earth chlorides[J]. Journal of Nuclear Materials, 2016, 480: 69-74. DOI:10.1016/j.jnucmat.2016.07.063 |
| [15] |
Wang X B, Huang W, Gong Y, et al. Electrochemical behavior of Th(IV) and its electrodeposition from ThF4 -LiCl-KCl melt[J]. Electrochimica Acta, 2016, 196: 286-293. DOI:10.1016/j.electacta.2016.02.184 |
| [16] |
徐千惠, 朱铁建, 郑海洋, 等. ThF4-LiCl-KCl熔盐体系中F-浓度对Th(Ⅳ)电解提取的影响[J]. 辐射研究与辐射工艺学报, 2018, 36(3): 030301. XU Qianhui, ZHU Tiejian, ZHENG Haiyang, et al. Effect of F-concentration on the electrolysis of Th(IV) in ThF4-LiCl-KCl[J]. Journal of Radiation Research and Radiation Processing, 2018, 36(3): 030301. DOI:10.11889/j.1000-3436.2018.rrj.36.030301 |
| [17] |
贾昀澎, 王子豪, 耿俊霞, 等. FLiNaK熔盐中CsF的蒸发与分离[J]. 核技术, 2016, 39(2): 020602. JIA Yunpeng, WANG Zihao, GENG Junxia, et al. Evaporation and separation of CsF in FLiNaK molten salt[J]. Nuclear Techniques, 2016, 39(2): 020602. DOI:10.11889/j.0253-3219.2016.hjs.39.020602 |
| [18] |
Yang H C, Eun H C, Kim I T. Study on the distillation rates of LiCl-KCl eutectic salt under different vacuum conditions[J]. Vacuum, 2009, 84: 751-755. DOI:10.1016/j.vacuum.2009.06.011 |
| [19] |
Wang Z H, Fu H Y, Yang Y, et al. The evaporation behaviors of rare earth doped FLiNaK melts during low pressure distillation[J]. Journal of Radioanalytical and Nuclear Chemistry, 2017, 311(1): 637-642. DOI:10.1007/s10967-016-5110-0 |
| [20] |
Yaws C L. Handbook of vapor pressure: inorganic compounds and elements[M]. Gulf Professional Publishing, 1995, Vol 4.
|
| [21] |
Eun H C, Yang H C, Cho Y Z, et al. Vacuum distillation of a mixture of LiCl-KCl eutectic salts and RE oxidative precipitates and a dechlorination and oxidation of RE oxychlorides[J]. Journal of Hazardous Materials, 2008, 160: 634-637. DOI:10.1016/j.jhazmat.2008.03.079 |
| [22] |
Katayama Y. Precipitation of rare earth compounds in LiCl-KCl eutectic[J]. Journal of the Electrochemical Society, 1995, 142(7): 2174-2178. DOI:10.1149/1.2044271 |


