LiF-NaF-KF (FLiNaK)熔盐在高温时稳定,与常见的结构材料兼容,并具有良好的传热性能,被认为是一种很有应用前景的传热介质,可作为第四代先进高温堆和熔盐堆的二回路传热流体或作为聚变堆中氚的增殖包层[1-4]。由于熔盐堆及聚变堆中氚的产量大且高温时有很强的渗透性,因此在使用FLiNaK熔盐作为传热介质或包层材料时,往往需要考虑氚在FLiNaK熔盐中的扩散、渗透和溶解等相关行为性质。此外,高温时,FLiNaK熔盐中的溶解氚可透过其包容材料,进入其他系统或环境中,从而危害环境和人身安全[5]。研究FLiNaK熔盐中氚的扩散、渗透和溶解等行为性质,可为熔盐堆中氚的分布控制以及聚变堆增殖包层中氚的提取提供数据支持和理论依据。
目前,针对FLiNaK熔盐中氚的渗透扩散行为,国内外研究者通常采用氚的稳定同位素(氢)作为研究对象,通过研究其在FLiNaK熔盐中的渗透扩散行为,从而评估熔盐中氚的相关行为性质[6-7]。基于之前开展的FLiNaK熔盐中氢的渗透行为研究[8],本研究将进一步开展FLiNaK熔盐中氢的行为性质研究,同时对FLiNaK熔盐中氘的渗透扩散行为进行了测量。通过对比分析,探讨FLiNaK熔盐中氢的渗透扩散行为及方式,并研究同位素效应对FLiNaK熔盐中氢渗透扩散行为的影响,从而为FLiNaK熔盐中氚的行为性质研究提供参考依据。
1 实验方法通过氢同位素在熔盐中的扩散渗透特性测试系统(图 1),开展本研究的相关实验。氢同位素在熔盐中的扩散渗透特性测试系统以及使用该测试系统进行实验时的实验方法和过程,均在之前发表的文章中有详细的描述[8],此处不再赘述。此外,本研究使用的熔盐、实验时熔盐的装填厚度,以及熔盐的净化处理过程等均与之前实验相同[9]。

|
图 1 氢同位素在熔盐中的扩散渗透特性测试系统 Figure 1 Testing system for diffusion and permeation characteristics of hydrogen isotope in molten salts. |
本研究的实验内容主要包括:1)采用熔盐侧充氢的实验方式(区别于之前实验中金属侧充氢的实验方式),测定不同温度(500 ℃、550 ℃、600 ℃、650 ℃、700 ℃)下FLiNaK熔盐中H2的渗透扩散行为,通过与金属侧充氢的实验结果比较,探讨充氢方法对FLiNaK熔盐中氢渗透扩散行为的影响;2)采用金属侧充氘的实验方式,测定不同温度(500 ℃、550 ℃、600 ℃、650 ℃、700 ℃)下FLiNaK熔盐中D2的渗透扩散行为,通过与氢渗透扩散实验结果的比较,研究同位素效应对FLiNaK熔盐中氢渗透扩散行为的影响。
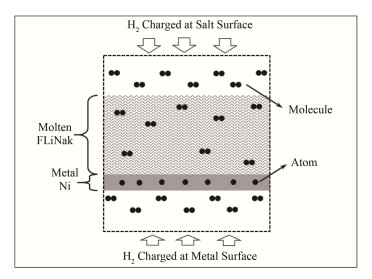
图 2给出了熔盐侧充氢和金属侧充氢时,氢在FLiNaK熔盐和金属Ni构成体系中的渗透过程。其中,氢在金属和熔盐界面的渗透过程可参考文献[10]。当利用熔盐侧充氢方式进行实验时,H2首先以分子的形式溶于FLiNaK熔盐中,溶解的H2通过扩散进入熔盐和金属Ni的接触界面,随后H2裂解成氢原子进入金属Ni中,氢原子在金属Ni中扩散并在另一侧复合为H2;而对于金属侧充氢方式进行的实验,H2首先在金属侧裂解为氢原子,氢原子在金属Ni中扩散并在熔盐和金属Ni的接触界面复合为H2,H2以分子的形式溶于FLiNaK熔盐并进行扩散,最后H2将在熔盐侧进行释放。
|
图 2 熔盐侧充氢和金属侧充氢示意图 Figure 2 A schematic diagram for H2 charged at salt surface and metal surface. |
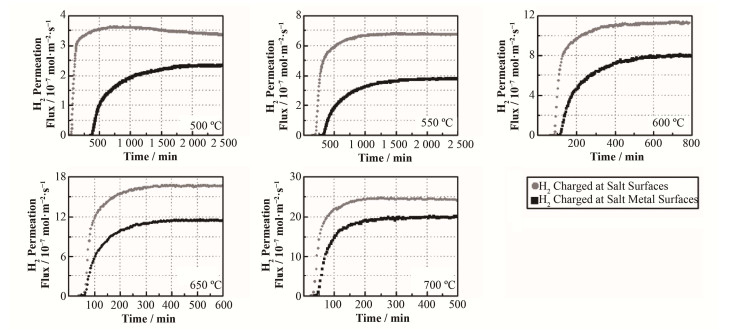
图 3给出的是熔盐侧充氢和金属侧充氢时,500-700 ℃的FLiNaK熔盐中H2渗透通量的测量结果。从图 3可看出,熔盐侧充氢的渗透通量在各温度下均大于金属侧充氢的渗透通量,即在FLiNaK熔盐和金属Ni构成的体系中,H2透过熔盐和金属的渗透通量大于其逆向渗透时的渗透通量。一般而言,在FLiNaK熔盐和金属Ni构成的体系中,金属Ni对氢渗透的阻力要远小于FLiNaK熔盐对氢的渗透阻力[6]。因此,采用熔盐侧充氢方式进行实验时,可忽略氢在金属Ni中的渗透,简化为氢在FLiNaK熔盐中的渗透过程。对于金属侧充氢方式进行的实验,由于氢优先透过金属Ni,导致氢分压在FLiNaK熔盐侧的降低,因此,在简化模型中,熔盐渗透前端的实际氢分压要小于实验中的充氢分压。而熔盐渗透前端氢分压的降低,将导致H2渗透通量的降低,这一结论与图 3显示的结果是吻合的。
|
图 3 500-700 ℃时FLiNaK熔盐中H2渗透通量的测量结果 Figure 3 H2 permeation fluxes with time through molten FLiNaK at 500-700 ℃. |
基于上述分析,可认为熔盐侧充氢方式进行的实验可更好反映FLiNaK熔盐中H2的渗透扩散行为及其性质。因此,本研究将通过熔盐侧充氢的实验结果对FLiNaK熔盐中H2的渗透扩散行为进行研究。根据之前研究提供的计算方法[8],对熔盐侧充氢的实验结果进行拟合,从而获得H2在FLiNaK熔盐中的扩散系数与溶解度。
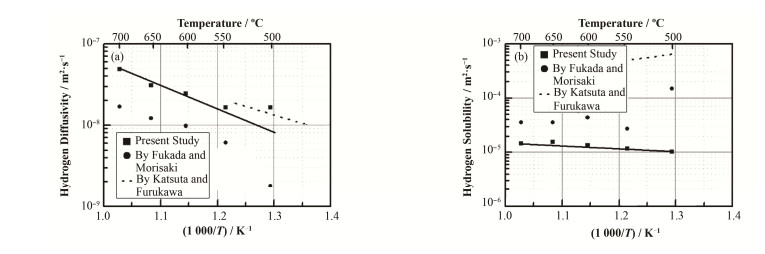
图 4是基于熔盐侧充氢的实验结果拟合计算后得到的FLiNaK熔盐中H2的扩散系数与溶解度常数。同时,图 4也给出了其他相关的文献数值[6, 10]。在本研究与Fukada等[6]的实验中,500 ℃的实验数据均有一定的偏差。例如,本研究500 ℃时获得的扩散系数偏大;而Fukada等在500 ℃时获得的扩散系数则偏小。此外,尽管本研究500 ℃时获得的扩散系数与Katsuta等[11]得到的扩散系数较为接近,但其溶解度常数却存在较大的差异。通过上述相关实验及数据,一方面无法确定500 ℃时FLiNaK熔盐中H2扩散系数和溶解度常数的正确值;另一方面则可能是本研究的实验装置与方法无法准确反映500 ℃时H2在FLiNaK熔盐中的渗透扩散行为(例如,低温时金属对氢渗透阻力的增大)。基于上述原因,在对FLiNaK熔盐中H2的扩散系数和溶解度常数进行处理时,对500 ℃的实验结果均不予考虑。通过计算,FLiNaK熔盐中H2的扩散系数和溶解度常数可分别拟合为以下的Arrhenius方程:
| $ {{D}_{{{\rm{H}}_{\rm{2}}}}}=1.62\times 1{{0}^{-5}}{\rm{exp}}\left(-\frac{48.20\times 1{{0}^{3}}}{{{R}_{\rm{g}}}T} \right) $ |
| $ {{K}_{{{\rm{H}}_{\rm{2}}}}}=6.18\times 1{{0}^{-5}}{\rm{exp}}\left(-\frac{11.14\times 1{{0}^{3}}}{{{R}_{\rm{g}}}T} \right) $ |
|
图 4 FLiNaK熔盐中H2的扩散系数(a)、溶解度常数(b)与温度的关系 Figure 4 Diffusivity (a) and solubility (b) of H2 in molten FLiNaK as the functions of the reciprocal of temperature. |
式中:DH2为FLiNaK熔盐中H2的扩散系数,m2·s-1;KH2为FLiNaK熔盐中H2的溶解度常数,mol·m-3·Pa-1;Rg为理想气体常数,J·mol-3·K-1;T为温度,K。
另外,从图 4可看出,本研究的扩散系数比文献[6]的实验结果偏大,而溶解度常数则比前者偏小。文献[6]采用金属侧充氢方式进行实验,其在降低熔盐中氢渗透通量的同时,将导致拟合计算时扩散系数的减小。在作者之前进行的金属侧充氢实验中,其扩散系数与文献[6]的实验结果相近,同样小于上述熔盐侧充氢的实验结果[9]。至于溶解度常数,根据其计算方法(渗透系数=溶解度常数×扩散系数),可认为FLiNaK熔盐中H2的溶解度常数受FLiNaK熔盐中H2的渗透系数和扩散系数的共同影响。在金属侧充氢的实验中,氢透过金属Ni后导致氢分压的降低,但在实际计算过程中可能仍采用充氢分压作为熔盐渗透的前端分压,从而导致渗透系数的计算值偏小。在计算溶解度常数时,偏小的渗透系数会导致溶解度常数偏大,但扩散系数的减小又导致溶解度常数增大。因此,通过金属侧充氢实验获得的H2溶解度常数可能大于熔盐侧充氢实验获得的H2溶解度常数,即图 4显示的溶解度结果。
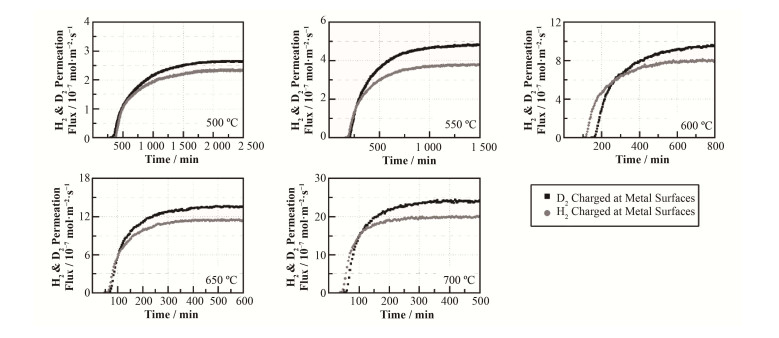
2.2 金属侧充氢和金属侧充氘图 5是金属侧充氢和金属侧充氘时500-700 ℃的FLiNaK熔盐中H2和D2渗透通量的测量结果。对比两者的渗透通量结果,可发现D2在FLiNaK熔盐中的渗透通量要普遍大于H2的渗透通量。但是,上述的差异并不显著,可认为FLiNaK熔盐中H2和D2的渗透扩散行为大体是一致的,即同位素效应对FLiNaK熔盐中氢的渗透扩散行为及其性质的影响可能不会特别显著。
|
图 5 500-700 ℃时FLiNaK熔盐中H2和D2渗透通量的测量结果 Figure 5 H2 and D2 permeation fluxes with time through molten FLiNaK at 500-700 ℃. |
采用熔盐侧充氢(氘)方式可更好地反映FLiNaK熔盐中H2(D2)的渗透扩散行为及其性质。但受实验条件限制,本文仅给出了金属侧充氢(氘)的实验结果,为获得更加完善的FLiNaK熔盐中氘的渗透扩散行为及其性质,可进一步开展熔盐侧充氘实验。本文在对金属侧充氢和金属侧充氘的实验结果进行比较时,意在说明H2和D2在FLiNaK熔盐中的渗透扩散行为及其性质的差异,从而更好的获得同位素效应对FLiNaK熔盐中氢的渗透扩散行为的影响,为FLiNaK熔盐中氚的渗透扩散行为及其性质研究提供指导。
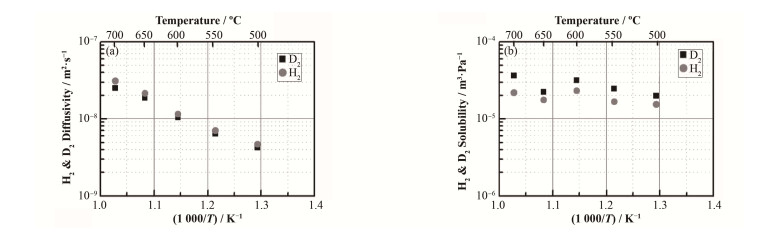
在不考虑金属Ni中H2和D2的渗透过程,分别对金属侧充氢和金属侧充氘的实验结果进行计算分析,从而获得FLiNaK熔盐中H2和D2的扩散系数与溶解度常数,如图 6所示。从图 6可看出,简化计算后得到的FLiNaK熔盐中H2和D2扩散系数在各温度下均非常接近,说明FLiNaK熔盐中H2和D2的扩散行为不同于氢同位素原子在金属材料点阵间隙间的热振动而造成的扩散[12]。此外,根据斯托克斯-爱因斯坦(Stocks-Einstein)方程,溶剂中溶质分子的扩散速率与溶剂的黏度和溶质分子的直径成反比,这一结论可认为与上述实验结果是一致的,即氢在FLiNaK熔盐中主要以氢分子(溶质分子)的形式进行扩散。因此,可基本排除同位素效应对FLiNaK熔盐中氢扩散行为的影响。
|
图 6 FLiNaK熔盐中H2和D2的扩散系数(a)、溶解度常数(b)与温度的关系 Figure 6 Diffusivity (a) and solubility (b) of H2 and D2 in molten FLiNaK with temperatures. |
至于溶解度常数,从图 6可看出,FLiNaK熔盐中H2的溶解度常数要普遍小于D2的溶解度常数,但两者的差异总体上并不明显。在实验过程中,熔盐中溶解的H2(D2)在向熔盐上方的气相释放后,气相中的H2(D2)会透过金属侧壁向外渗透,这部分H2(D2)因无法计入溶解度的计算过程,造成溶解度常数的计算值偏小。由于H2透过金属侧壁的渗透量大于D2的渗透量,因此H2的溶解度常数将比D2的溶解度常数更小。基于上述考虑以及氢和氘溶解度的差异,可认为同位素效应对FLiNaK熔盐中氢溶解度的影响是非常小的。
3 结语通过氢同位素在熔盐中的扩散渗透特性测试系统,对FLiNaK熔盐中氢的渗透扩散行为进行了研究。通过对比熔盐侧充氢和金属侧充氢的实验结果,分析两种充氢方式下FLiNaK熔盐中氢渗透扩散行为的差异。通过比较,确定了以熔盐侧充氢方式进行的实验可更好的反映FLiNaK熔盐中氢的渗透扩散行为及其性质。基于上述熔盐侧充氢的实验,得到550-700 ℃时FLiNaK熔盐中氢的扩散系数与溶解度常数,两者可分别拟合为以下Arrhenius方程:DH2 =1.62×10-5exp(-48.20×103/RgT)和KH2=6.18× 10-5exp(-11.14×103/RgT)。此外,本文通过对比分析金属侧充氢与金属侧充氘的实验结果,确定了同位素效应对FLiNaK熔盐中氢渗透扩散行为及其性质的影响,为FLiNaK熔盐中氚的渗透扩散行为及其性质研究提供参考与指导。
| [1] |
Ambrosek J, Anderson M, Sridharan K, et al. Current status of knowledge of the fluoride salt (FliNaK) heat transfer[J]. Nuclear Technology, 2009, 165(2): 166-173. DOI:10.13182/nt165-166 |
| [2] |
Khokhlov V, Ignatiev V, Afonichkin V. Evaluating physical properties of molten salt reactor fluoride mixture[J]. Journal of Fluorine Chemistry, 2009, 130: 30-37. DOI:10.1016/j.jfluchem.2008.07.018 |
| [3] |
Office of Energy Efficiency and Renewable Energy. FY 2005 annual progress report for the DOE hydrogen program[R]. Office of Scientific and Technical Information (OSTI), 2005. DOI: 10.2172/862311.
|
| [4] |
Yamanishi H, Sagara A. Annual report of national institute for fusion science[R]. Japan, April 1999-March 2000.
|
| [5] |
Briggs R B. Tritium in molten-salt reactors[J]. Reactor Technology, 1971-1972, 14(4): 335-342. |
| [6] |
Satoshi Fukada, Akio Morisaki. Hydrogen permeability through a mixed molten salt of LiF, NaF, and KF (Flinak) as a heat-transfer fluid[J]. Journal of Nuclear Materials, 2006, 358(2): 235-242. DOI:10.1016/j.jnucmat.2006.07.011 |
| [7] |
Ohshima T, Kondo M, Tanaka M, et al. Hydrogen transport in molten salt FLiNaK measured by solid electrolyte sensors with Pd electrode[J]. Fusion Engineering and Design, 2010, 85(10): 1841-1846. DOI:10.1016/j.fusengdes.2010.06.008 |
| [8] |
Zeng Y S, Wu S W, Qian Y, et al. Apparatus for determining permeability of hydrogen isotopes in molten-salt[J]. Nuclear Science and Techniques, 2014, 25(4): 040602. DOI:10.13538/j.1001-8042/nst.25.040602 |
| [9] |
曾友石, 杜林, 皮力, 等. 氢在FLiNaK(LiF-NaF-KF)熔盐中的渗透行为[J]. 核技术, 2015, 38(2): 020603. ZENG Youshi, DU Lin, PI Li, et al. Permeability of hydrogen in molten salt FLiNaK (LiF-NaF-KF)[J]. Nuclear Techniques, 2015, 38(2): 020603. DOI:10.11889/j.0253-3219.2015.hjs.38.020603 |
| [10] |
Maeda Y, Edao Y, Yamaguchi S, et al. Solubility, diffusivity, and isotopic exchange rate of hydrogen isotopes in Li-Pb[J]. Fusion Science and Technology, 2008, 54(1): 131-134. DOI:10.13182/fst54-131 |
| [11] |
Katsuta Hiroji, Furukawa Kazuo. Diffusivity and solubility of hydrogen in molten fluoride mixture (LiF-NaF-KF)[J]. Journal of Nuclear Materials, 1978, 71(2): 375-376. DOI:10.1016/0022-3115(78)90439-7 |
| [12] |
Gomer R, Wortman R, Lundy R, et al. Mobility and adsorption of hydrogen on tungsten[J]. Journal of Chemical Physics, 1957, 24(5): 1147-1164. DOI:10.1063/1.1743484 |


