微生物是土壤生态系统中最活跃的组成部分,是土壤中养分循环的重要驱动力[1–2]。土壤生物学性状 (微生物群落结构、生物量、酶活性等) 可以反映土壤质量与土壤肥力的演变趋势,并作为评价土壤健康的重要指标之一[3–4]。施肥由于直接或间接改变了农田生态系统的养分平衡与供应状况,从而对土壤的物理、化学以及生物学特性产生了深远的影响。因此,明确不同种植制度、土地利用类型以及土壤特性 (酸度) 下施肥对土壤生物学性状的影响程度,对于农田土壤培肥、养分资源的高效利用均具有重要意义。
大量研究表明,施肥对土壤生物学特性的影响存在一定的不确定性。李清华等[5]研究表明,长期施肥能显著增加土壤微生物总量以及磷脂脂肪酸 (PLFA) 的种类,而Stark等[6]研究却发现,施肥对土壤微生物特性没有产生明显影响。颜慧等[7]研究认为,施用氮磷钾 (NPK) 化肥显著提高了土壤微生物总PLFA以及细菌 (Bacteria) 和放线菌 (Actinomycetes)PLFA含量,而白震等[8]研究却发现NPK化肥的施用抑制了大多数菌群的生长。有研究发现施用有机物料能显著提高土壤微生物量以及菌群数[9–10],但对不同菌群的影响程度有所差异[11–12]。另一方面,土壤微生物分泌的酶在有机物质分解以及养分循环中有重要作用,其活性大小可作为衡量土壤质量的重要指标之一。研究表明,施肥可显著提高土壤β-葡萄糖苷酶 (β-Glucosidase,BG) 与乙酰氨基葡萄糖苷酶 (N-Acetyl-glucosamidase,NAG) 活性[13–14],但李子川[15]通过对稻田土壤的研究发现长期施肥并未改变土壤中BG活性。
综上所述,以往大多数研究均基于某个特定试验点进行分析,因而其结果均由于特定的生物地理环境与施肥措施而存在较大差异,导致施肥对土壤生物学特性的影响存在一定的不确定性。为了进一步明确施肥的影响,本研究基于数据整合分析方法 (Meta-analysis) 的原理,通过已发表相关文献的数据收集,定量分析不同施肥措施对土壤生物学特性的影响,为农田土壤培肥和耕地质量提升提供科学依据。
1 研究方法 1.1 数据来源本研究收集的数据来自于web of science和中国知网2个文献数据库。数据收集过程中,设置“中国农田”、“施肥”和“微生物群落结构”三个关键词进行搜索,筛选条件如下:1) 试验点为中国农田;2) 同一试验包含配对的对照组与处理组,对照组为不施肥,处理组分为化肥 (氮、磷、钾和氮磷钾等) 和有机物料 (单施或配施) 处理;3) 试验处理重复数大于或等于3。数据收集内容主要包括:施肥处理、土壤微生物量碳 (Soil microbial biomass carbon,SMBC)、微生物量氮 (Soil microbial biomass nitrogen,SMBN)、总磷脂脂肪酸含量、各菌群磷脂脂肪酸含量以及酶活性等,还包括每个试验点对应的相关信息如种植制度、土地利用方式以及土壤pH等,其中种植制度分为一年一熟与一年两熟,土地利用方式分为水田、旱地和水旱轮作,土壤pH分为pH < 6、6 < pH < 8和pH > 8。在数据收集过程中,如果数据是以图的形式展示,采用GetData Graph Digitizer 2.24 软件来获得。共获得符合条件的已发表文献40篇,相匹配的有效数据185组。由于G +与G-同属于细菌属,因此在研究施肥对不同pH的土壤中微生物群落结构影响时,只分析真菌、细菌和放线菌这三类菌群。在所收集的数据中,一年一熟种植制度主要集中在西北和东北地区,一年两熟则主要集中在华北、华中和华东地区;水田与水旱轮作措施主要集中在南方。
如图1所示,所收集的SMBC、SMBN以及总PLFA数据经对数 (ln) 转换后均符合正态分布 (P < 0.01),其中SMBC样本数为244组,SMBN样本数为131组,总PLFA样本数为185组,满足Meta分析的必要条件。
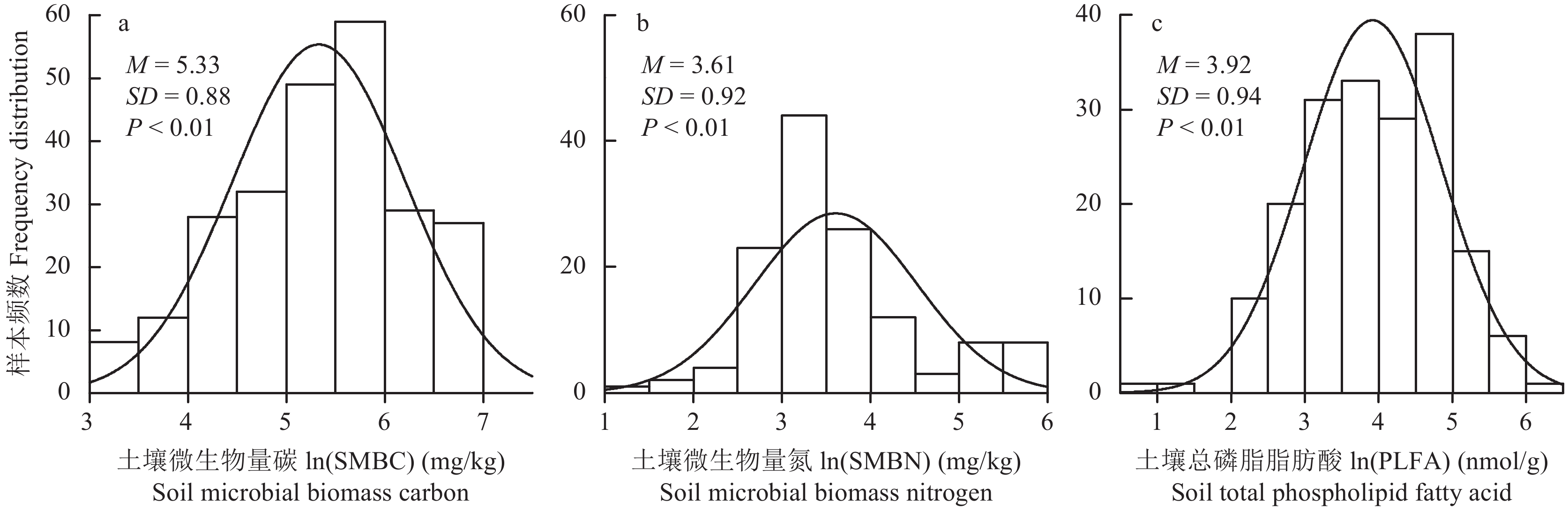 |
| 图1 土壤微生物量碳 (a)、氮 (b) 以及总磷脂脂肪酸 (c) 的分布 Fig. 1 Distribution of soil microbial biomass carbon (a), microbial biomass nitrogen (b) and total PLFA (c) [注(Note):ln(x) 为原始数据经ln转换后的数值;曲线代表数据的高斯分布,P 为显著性检验。ln(x) is the value of the original data after in conversion. The curve is a Gaussian distribution fitted to frequency data and P < 0.01 suit for the distribution.] |
整合分析 (Meta-analysis) 是针对具有共同研究目的且相互独立的多个研究结果进行系统合并分析,定量综合评价研究结果的统计方法,适用于对大尺度生态现象进行研究[16]。本研究主要利用MetaWin2.1软件进行整合分析,定量研究不同施肥措施对微生物量、群落结构以及酶活性的影响。在检验差异性时,每组数据中都需要同时包括平均值 (mean,M)、标准差 (standard deviation,SD) 和样本数 (samples size,n)。若文献提供的数据是标准误 (standard errors,SE),则可通过式 (1) 转换成SD。
| ${S\!D = S\!E}\sqrt {n} $ | (1) |
统计学指标采用合并计数资料响应比 (Response ratio,RR) 表示,并计算其95%置信区间 (95% CI),其中 RR 计算公式为:
| $R\!R = M\!t/M\!c$ | (2) |
式中:Mt代表处理组平均值;Mc代表对照组平均值。
在分析的过程中,需要将RR进行对数化,采用自然对数响应比 (lnRR) 来反映不同施肥措施对生物学特性的影响程度并通过式 (3) 实现[17]:
| $\ln \!R\!R = \ln \!\left( {\frac{{M\!t}}{{M\!c}}} \right) = \ln\! M\!t - \ln\! M\!c$ | (3) |
平均值的变异系数V、权重Wij、权重响应比RR++、RR++的标准误S以及95% CI可通过如下计算获得[18]:
| $V = \frac{{SD_t^2}}{{{n_t}\,M_t^2}} + \frac{{SD_c^2}}{{{n_c}\,M_c^2}}$ | (4) |
| $Wij = 1/V$ | (5) |
| ${R\!R\!_{{}_{ + + }}} = \sum\nolimits_{i = 1}^m \sum\nolimits_{j = 1}^{ki} {W_{\!ij}}R\!{R_{\!ij}}/\sum\nolimits_{i = 1}^m \sum\nolimits_{j = 1}^{ki} {W_{\!ij}}$ | (6) |
| $S({R\!R_{{}_{\!++ }}}) = 1/\sqrt {\sum\nolimits_{i = 1}^m \sum\nolimits_{j = 1}^{ki} {W_{\!ij}}} $ | (7) |
| $95{{\%}} CI = {R\!R_{{}_{\! + + }}}1.96\,S({R\!R_{{}_{ \!+ + }}})$ | (8) |
式 (4) 中:
数据分析处理前,数据库的各研究结果须进行异质性检验,若P > 0.1,表明多个研究具有同质性,此时选择固定效应模型进行分析 (fixed effect model,FEM),反之则选择随机效应模型 (random effect model,REM)。
权重响应比 (weighted response ratio,RR++) 及其95%的置信区间 (95% CI) 通过 (eRR++–1) × 100%来转化。如果95% CI包含零值表明该变量中处理与对照没有显著差异 (P > 0.05) [19]。
2 结果与分析 2.1 不同施肥措施对土壤微生物量的影响整合分析结果表明,与不施肥相比,施肥显著提高了土壤微生物量碳、氮和土壤微生物总PLFA的含量,提高幅度分别为30.9%、41.6%和28.5% (图2)。施用 (单施或配施) 有机物料对土壤微生物总PLFA含量的提高幅度为47.3%,显著高于施用化肥的提高幅度 (12.1%)。施用有机物料显著提高了土壤SMBC和SMBN,提高幅度分别为50.4%和58.7%,相当于施用化肥提高幅度的2.8和2.4倍 (图2)。研究结果表明,施用有机物料对土壤微生物量的提升幅度显著高于单施化肥。
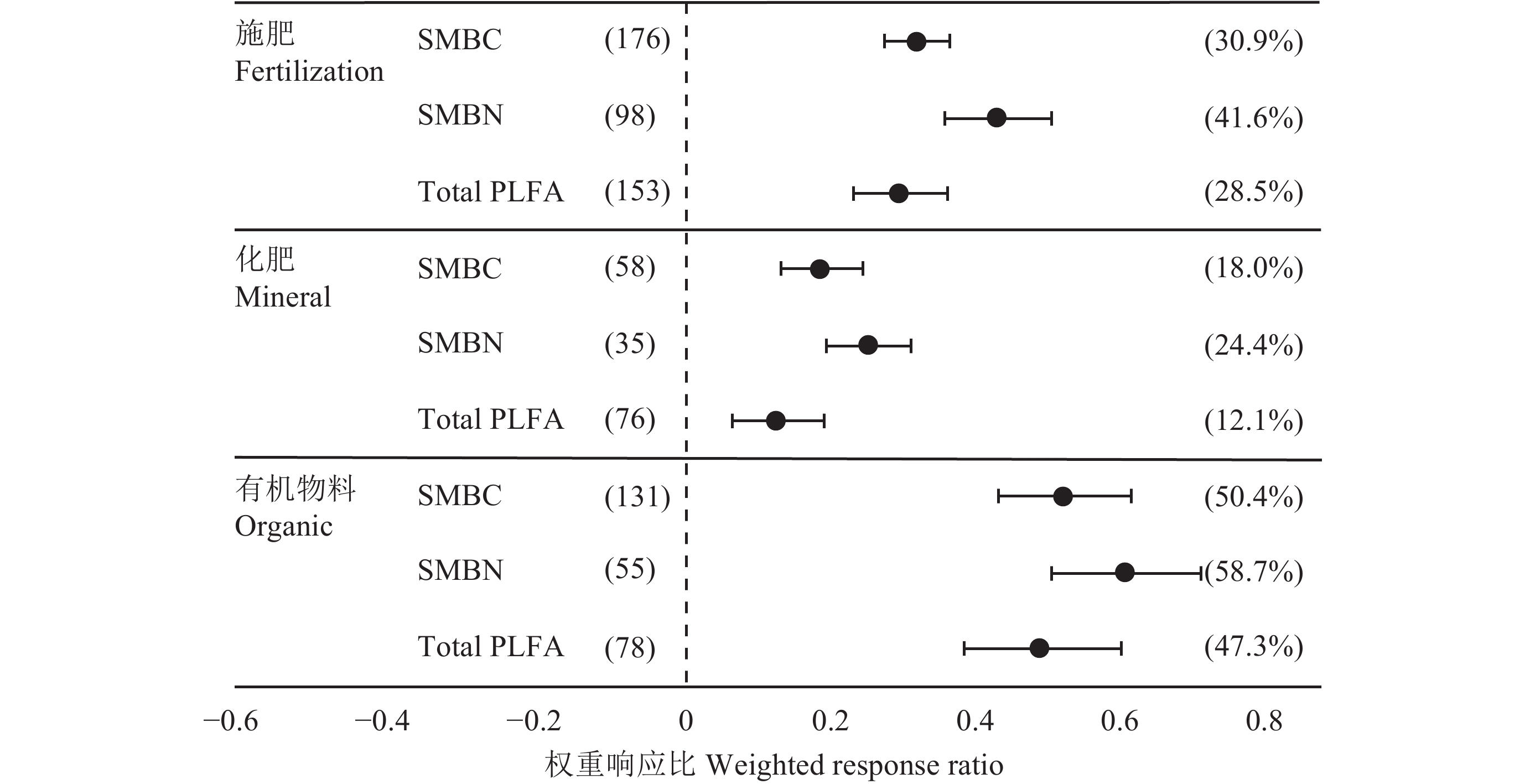 |
| 图2 施肥措施对微生物量的权重响应比 Fig. 2 Weighted response ratio of soil microbial biomass to fertilization [注(Note):SMBC—土壤微生物量碳 Soil microbial biomass carbon;SMBN—土壤微生物量氮 Soil microbial biomass nitrogen. Total PLFA—总磷脂脂肪酸 Total phospholipid fatty acid. 括号内数字分别代表样本数以及施肥相应的百分数 The digitals and percentages in parentheses represent independent sample size and percent response to fertilization,respectively.] |
种植制度和农田利用方式对土壤微生物量具有明显的影响。分析结果表明,不同种植制度、土地利用类型以及土壤pH下,施肥对土壤微生物量 (总PLFA) 的影响程度存在一定差异 (图3)。
总体上,施肥显著提高了一年两熟和一年一熟制区土壤微生物总PLFA含量,提高幅度分别为29.5%和26.6% (图3a)。一年两熟制区,施用化肥对土壤微生物总PLFA含量的提高幅度为17.9%,但在一年一熟制区,施用化肥对土壤微生物总PLFA无显著影响 (图3b)。而一年两熟和一年一熟制区,施用有机物料均显著提升微生物总PLFA含量,提高幅度分别为44.0%和53.5% (图3c)。
农田水分管理措施由于直接影响了土壤的通气和养分状况,从而对土壤微生物产生影响。分析结果表明,总体上,施肥显著提高了水田 (28.0%)、旱地 (24.1%) 和水旱轮作 (36.4%) 下土壤微生物总PLFA的含量 (图3a)。施用化肥显著提高了水田和水旱轮作下土壤微生物总PLFA含量,提高幅度为18.3%~27.6%,二者无显著差异。但在旱地条件下,施用化肥对于土壤微生物总PLFA的提升效果不显著 (图3b)。在不同土地利用类型下施用有机物料均能显著提高微生物总PLFA含量,提高幅度均值为45.3%,水田、旱地与水旱轮作三者之间无显著差异 (图3c)。
土壤酸度是影响微生物群落的重要因素之一,大部分微生物群落具有一定适宜的pH值范围。本研究结果表明,施肥对pH < 6、6 < pH < 8和pH > 8的土壤上微生物总PLFA含量提升幅度并无显著差异,提升幅度为23.0%~32.9% ( 图3a)。施用化肥显著提升了6 < pH < 8的土壤上微生物总PLFA含量,提高幅度为15.6%,在pH > 8的土壤上提升效果不显著 ( 图3b)。在不同酸度的土壤上施用有机物料对微生物总PLFA含量均有显著的提升作用,提高幅度为33.6%~52.2% (图3c)。研究结果表明,在偏酸性和偏碱性的土壤上,施用有机物料对微生物总PLFA含量的提升幅度显著高于单施化肥。
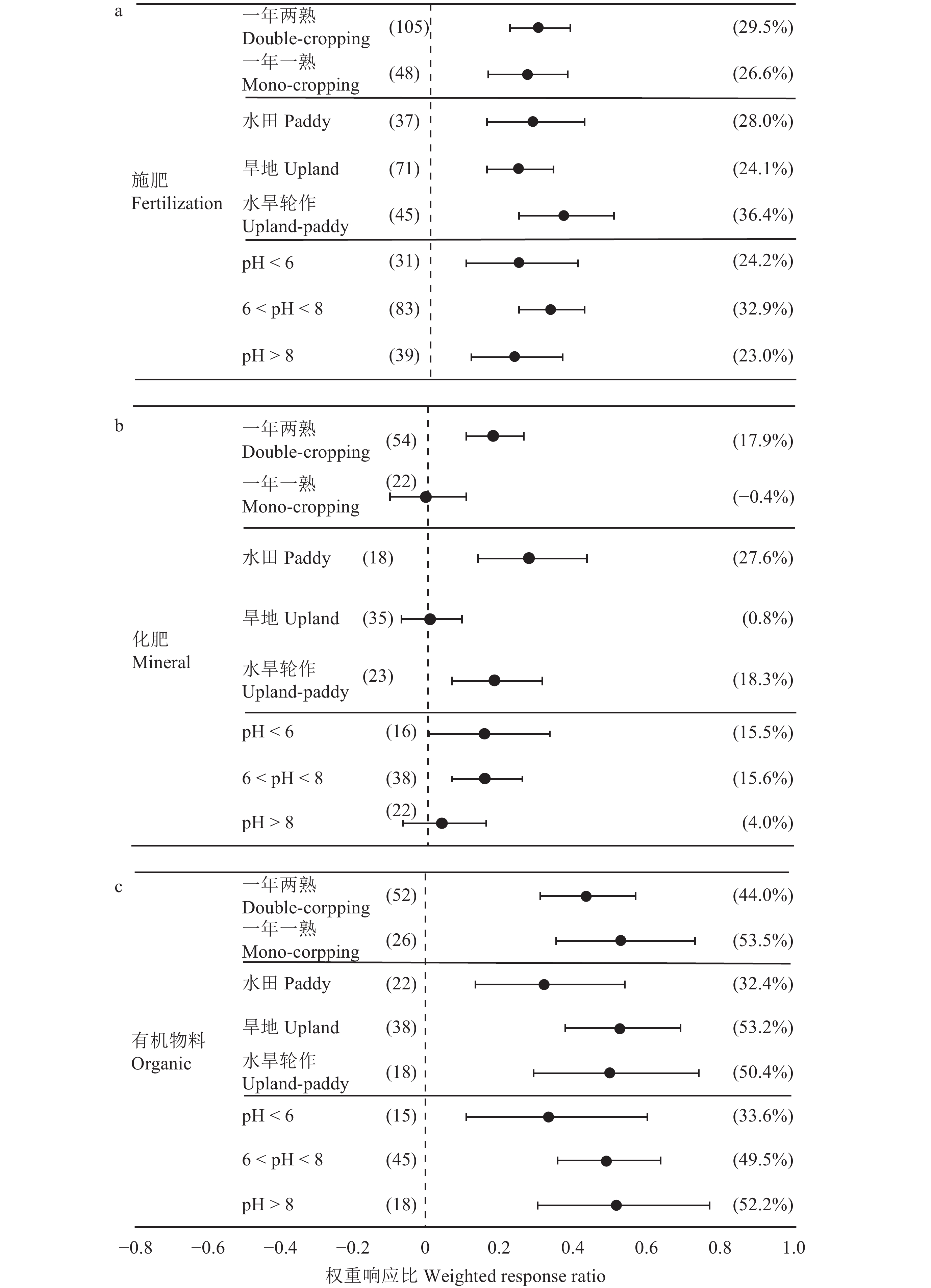 |
| 图3 不同种植制度、土地利用类型和土壤pH下施肥 (a)、施化肥 (b) 和施有机物料 (c) 对总PLFA的权重响应比 Fig. 3 Weighted response ratio of soil total PLFA to fertilization (a), mineral (b) and organic (c) fertilization in different cropping systems, land-use types and soil pH [注(Note):括号内数值和百分数分别代表样本数和施肥相应的百分数 The digitals and percentages in parentheses represent independent sample size and percent response to fertilization, respectively.] |
不同施肥措施对土壤微生物群落结构的影响程度存在一定差异 (图4)。分析结果表明,施肥能显著提高微生物各菌群PLFA的含量,其中,施肥对真菌、细菌、放线菌PLFA含量的提高幅度范围为23.8%~30.4%,对革兰氏阳性菌 (G+)、革兰氏阴性菌 (G–)PLFA含量的提高幅度为37.8%~43.2%。但施肥对土壤微生物的真菌细菌比 (F∶B) 和革兰氏阳性菌革兰氏阴性菌比 (G+∶G–) 无显著影响。以上研究结果表明,尽管施肥显著提高了微生物的总量,但并未引起微生物群落结构的差异。
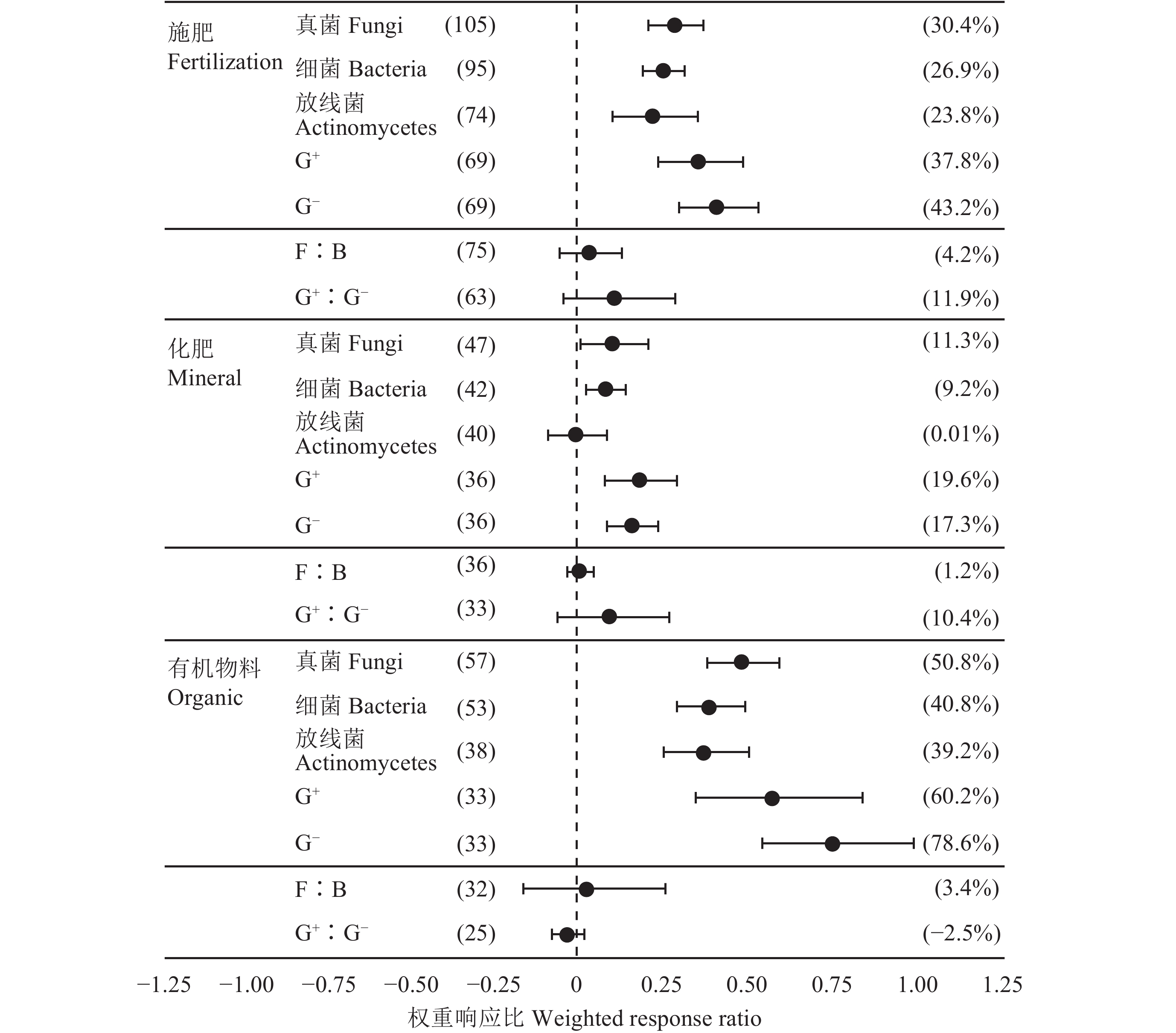 |
| 图4 不同施肥措施对土壤微生物群落结构的权重响应比 Fig. 4 Weighted response ratio of soil microbial structure to fertilization [注(Note):括号内数字分别代表样本数以及施肥相应的百分数 The digitals and percentages in parentheses represent independent sample size and percent response to fertilization, respectively.] |
施用有机物料显著提高了各菌群PLFA含量,且提高幅度均高于施化肥处理。施用有机物料对真菌和细菌PLFA含量的提高幅度为50.8%和40.8%,是施用化肥 (11.3%和9.2%) 的4.5和4.4倍。施用有机物料也显著提高了放线菌PLFA含量,提高幅度为39.2%,而施化肥对放线菌PLFA含量没有显著影响。另外,施用有机物料显著提高了G+和G− PLFA的含量,提高幅度为60.2%和78.6%,是施化肥处理 (19.6%和17.3%) 的3.1和4.5倍。施用化肥与有机物料对土壤微生物的F∶B和G+∶G− 均无显著影响,说明不同施肥措施对土壤微生物群落结构无显著影响。
2.4 不同土壤酸度下施肥对土壤微生物群落结构的影响土壤微生物群落结构与环境的酸度 (pH) 值密切相关。本研究表明,在不同pH的土壤上,施肥对微生物各菌群PLFA的影响存在一定差异 (图5a)。总体上,在pH < 6的土壤上,施肥能显著提高真菌、细菌和放线菌PLFA的含量,提高幅度分别为18.5%~25.8%。在6 < pH < 8的土壤中,施肥也显著提高了真菌、细菌和放线菌PLFA的含量,提高幅度为 32.6%~36.8%。在这两种pH的土壤上,施肥对三者的提升幅度均无显著差异。在pH > 8的土壤上,施肥仅提高了真菌和细菌PLFA含量,提高幅度为34.5%和16.2%,对放线菌PLFA含量无显著影响。
在不同pH的土壤上施用化肥对微生物菌群PLFA含量的影响也有所差异 (图5b)。在pH < 6的土壤上,施用化肥对真菌、细菌和放线菌PLFA含量均未产生显著影响。在6 < pH < 8的土壤上,施用化肥提高了真菌和细菌PLFA含量,提高幅度为24.9%和12.0%,对放线菌PLFA含量无显著影响。在pH > 8的土壤上,施用化肥显著降低了放线菌PLFA含量,降低幅度为12.2%,对真菌和细菌PLFA含量无显著影响。
在不同pH的土壤上施用有机物料显著提高了微生物菌群PLFA含量 (图5c)。其中,在6 < pH < 8的土壤中施用有机物料对真菌、细菌以及放线菌PLFA含量的提高幅度 (48.1%~75.2%) 显著高于在pH < 6(27.0%~35.2%) 和pH > 8(26.1%~34.4%) 的土壤中施用有机物料的提高幅度。
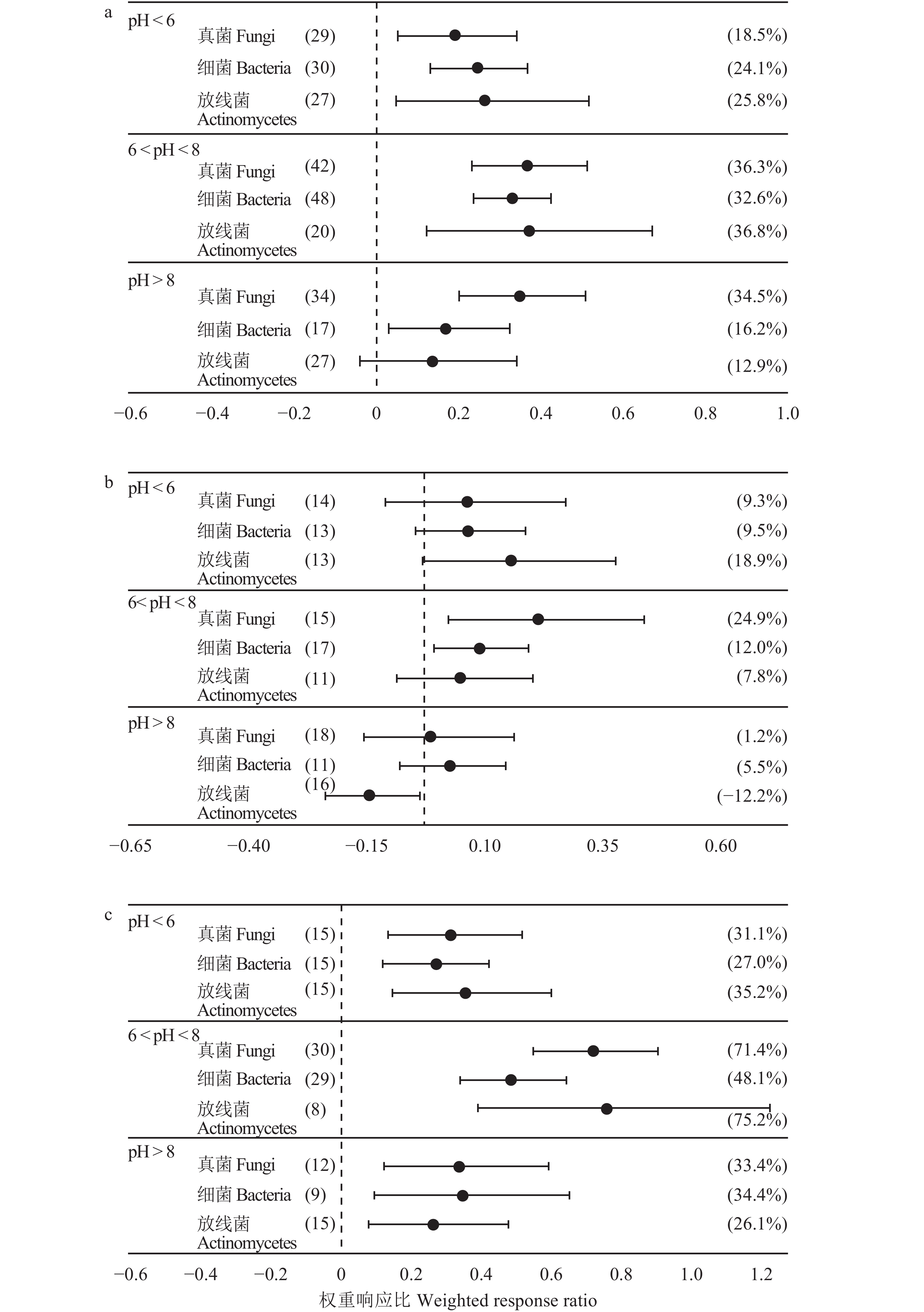 |
| 图5 不同土壤pH下施肥 (a)、施化肥 (b) 和施有机物料 (c) 对微生物群落结构的权重响应比 Fig. 5 Weighted response ratio of soil microbial structure in response to fertilization (a), mineral (b) and organic (c) fertilization in different soil pH [注(Note):括号内数值和百分数分别代表样本数和施肥相应的百分数 The digitals and percentages in parentheses represent independent sample size and percent response to fertilization, respectively.] |
施肥显著改变了土壤微生物量和菌群丰度,从而影响了土壤酶活性。研究表明,与不施肥相比,施肥显著提高了与土壤有机质分解相关的β-葡萄糖苷酶 (β-Glucosidase,BG) 和乙酰氨基葡萄糖苷酶 (N-Acetyl-glucosamidase,NAG) 活性,提高幅度为42.4%和174.5%,对与土壤氮循环相关的亮氨酸氨基肽酶 (leucine aminopeptidase,LAP) 活性没有产生明显影响 (图6)。
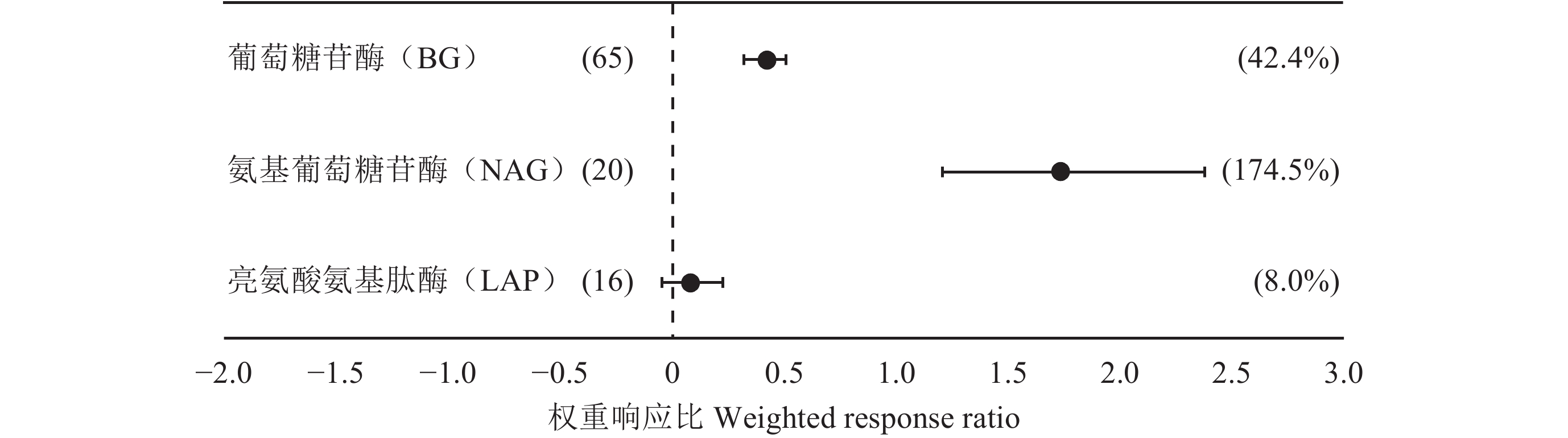 |
| 图6 施肥对土壤酶活性的权重响应比 Fig. 6 Weighted response ratio of soil enzyme activities to fertilization [注(Note):括号内数值和百分数分别代表样本数和施肥相应的百分数 The digitals and percentages in parentheses represent independent sample size and percent response to fertilization,respectively.] |
施肥是土壤微生物演变的重要驱动因子之一[20]。整体而言,与不施肥相比,施肥能够显著提高SMBC、SMBN和总PLFA含量,这与Cruz等[20]研究结果一致。施用有机物料对SMBC、SMBN和总PLFA的提高幅度分别是施用化肥的2.8倍、2.4以及3.9倍。主要的原因是有机物料本身含有多种营养元素,可以促进作物根系和地上部的生长,增加了外源碳的输入,增加了土壤微生物数量,增强了微生物的活性[21]。另外,有机物料的施用有助于促进团聚体结构的形成,改善土壤物理性状,为微生物生长繁殖提供了良好的条件[22–23]。
水分、温度和土壤酸碱性能直接影响微生物活性[24–25],调控植物生长特性,从而影响植物残体质量和归还量[26],促进微生物生长繁殖。在不同种植制度、土地利用类型和土壤pH下,施肥对土壤微生物总PLFA含量的提高幅度有一定差异。在一年两熟制区,施肥对土壤微生物总PLFA含量的提高幅度高于一年一熟制区,施用化肥在一年两熟制区对微生物总PLFA含量的提高幅度也显著高于一年一熟制区。可能的原因是一年两熟的种植制度主要集中在华北、华中和华东地区 (表1),这些地区水热条件充足,年均温高于东北及西北等一年一熟制区,有利于微生物生长繁殖。施肥对水田和水旱轮作下土壤微生物总PLFA含量的提高幅度高于旱地,其中施化肥处理在水田和水旱轮作条件下对微生物总PLFA含量的提高幅度也显著高于旱地,主要的原因是水田和水旱轮作两种利用方式下,土壤的水分含量与养分含量均高于旱地。首先,微生物生长对水分条件有严格要求,淹水能增加土壤微生物对底物的利用效率,加快土壤碳周转速率,促进微生物生长[27];其次,水田及水旱轮作主要集中在中国南方地区,积温高于旱地[16]。最后,水旱轮作发生的干湿交替频率高,对土壤有机质分解产生激发效应,同时土壤的孔隙度发生变化[28],促进了微生物对有机物质的利用和微生物生长繁殖[29],而旱地水分含量相对较低盐分含量相对较高,一定程度上抑制了微生物的数量及多样性[30]。在不同pH的土壤上,施肥显著提高了微生物总PLFA含量,施用化肥仅在6 < pH < 8的土壤中显著提高微生物总PLFA含量,主要原因是绝大多数土壤微生物适宜在中性环境中生长,过酸或过碱的环境使得微生物活性均受到不同程度地抑制 [31],而研究表明单施化肥容易导致土壤酸化,不适宜微生物生长繁殖[32]。在不同种植制度、土地利用类型和土壤pH下,施有机物料均显著提高微生物总PLFA含量,主要的原因是由于土壤肥力提高能够减缓不适宜的水分含量、酸碱度对微生物群落产生的负面影响[33–34]。有机物料的施用不仅提供了营养物质和能源物质,还改善了土壤结构、持水能力以及理化性质[35–36],增强了土壤的抗干扰能力。
| 表1 不同地区、种植制度和土地利用类型条件下施肥对土壤总PLFA影响的样本数分布 Table 1 The distribution of sample sizes regarding fertilization impacts on soil total PLFA in different cropping systems and land-use types in different regions of China |
 |
土壤pH值是影响土壤微生物群落结构及其多样性的重要环境因子[37]。在不同pH值的土壤中,不同施肥措施对微生物各菌群PLFA含量提升幅度有一定差异。本研究表明,施肥在pH > 8的土壤上能显著提升真菌PLFA含量,而对细菌、放线菌PLFA含量无显著影响。主要的原因可能是由于细菌的最佳生长pH值范围较窄,而真菌的最佳生长范围更宽,因此在相同的pH值范围内,pH值对细菌群落的影响更为显著 [38]。施有机物料对真菌、细菌PLFA含量的提高幅度是施化肥的4.5、4.4倍,且在不同施肥措施下,真菌PLFA含量的提高幅度均高于细菌。Zhang等[39]的研究结果也表明,随着土壤肥力的提升,土壤微生物细菌和真菌含量都有所提高,且真菌的提高幅度更大。施用有机物料显著提高了放线菌PLFA含量,而施化肥没有产生影响,说明有机物料的施用提高了土壤微生物的多样性。同时施用化肥在不同pH的土壤中对放线菌PLFA含量无正面影响甚至显著降低,主要是由于放线菌适宜的生长pH为中性或偏碱性,施用化肥,尤其是施用氮肥容易导致土壤酸化,从而抑制了放线菌的生长。孙凤霞等[10]研究也表明,在红壤中施用有机肥能在一定程度上缓解土壤的pH下降,甚至提高土壤pH。施肥显著增加了革兰氏阴性 (G–) 与革兰氏阳性 (G+)PLFA的含量。在施用有机物料的情况下,G–PLFA含量的增加幅度是施化肥条件下的4.5倍,主要的原因G–更倾向于在富营养的环境中生长[40],有机物质的大量投入更有利于G–的生长和繁殖[41]。
土壤中微生物的F∶B可反映真菌与细菌相对含量的变化范围和相对丰度[42],能够反映土壤肥力与健康状况,可以用来表征微生物对周围环境的响应,以及农田生态系统的稳定程度[43–44]。Buyer等[45]研究表明,施用有机肥能增加F∶B,化肥处理则降低F∶B,而Bardgett等[46]研究表明,连续施用六年的化肥并没有显著降低土壤微生物F∶B。本研究大样本统计结果表明,不同施肥措施下土壤微生物F∶B没有显著变化,这与Dong等[47]和毕明丽等[48]的研究结果一致,表明由于不同施肥造成养分配比的差异虽然显著改变了微生物群落的量,但并未引起微生物细菌群落结构发生明显变化。
土壤酶活性代表微生物的活性,是土壤活性功能最重要的指标,在土壤有机质分解和物质循环中起到重要作用[49]。BG与NAG属于碳水化合物分解酶类,与土壤有机质分解转化密切相关[50]。本研究结果表明,施肥显著提高了土壤BG与NAG活性,这与范淼珍等[14]研究结果相似。主要的原因是有机物料能够直接增加碳源,为微生物提供充足的养分,促进土壤微生物数量增加和酶活性增强。施用化肥则是通过增加养分投入,提高作物生产力,增加了作物根系分泌物,从而向微生物提供一定量碳源,且化肥中无机氮能调节土壤碳氮比 (C/N),为提高酶活性创造了条件[51]。因此,施肥直接或间接增加了碳源,促进微生物活动,加速土壤碳循环,提高了土壤中与有机质分解相关酶 (BG和NAG) 的活性。
4 结论整合分析不同施肥措施对土壤微生物学特性的影响结果表明,施肥显著提高了土壤微生物量、菌群丰度以及与有机质分解转化相关酶的活性。在不同种植制度、土地利用类型以及土壤pH下,施用有机物料对土壤微生物总量的提高幅度显著高于施用化肥,在一年一熟种植区、旱地以及偏酸或偏碱性的土壤上配施有机物料,可以显著提高土壤微生物活性,从而提升土壤肥力水平。
| [1] |
宋长青, 吴金水, 陆雅海, 等. 中国土壤微生物学研究10年回顾[J].
地球科学进展, 2013, 28(10): 1087–1105.
Song C Q, Wu J S, Lu Y H, et al. Advances of soil microbiology in the last decade in China[J]. Advances in Earth Science, 2013, 28(10): 1087–1105. DOI:10.11867/j.issn.1001-8166.2013.10.1087 |
| [2] | Zhong W H, Gu T, Wang W, et al. The effects of mineral fertilizer and organic manure on soil microbial community and diversity[J]. Plant and Soil, 2010, 326: 511–522. DOI:10.1007/s11104-009-9988-y |
| [3] | Diacono M, Montemurro F. Long-term effects of organic amendments on soil fertility: A review[J]. Agronomy for Sustainable Development, 2010, 30(2): 401–422. DOI:10.1051/agro/2009040 |
| [4] | Geisseler D, Linquist B A, Lazicki P A. Effect of fertilization on soil microorganisms in paddy rice systems-A meta-analysis[J]. Soil Biology & Biochemistry, 2017, 115: 452–460. |
| [5] |
李清华, 王飞, 林诚, 等. 长期施肥对黄泥田土壤微生物群落结构及团聚体组分特征的影响[J].
植物营养与肥料学报, 2015, 21(6): 1599–1606.
Li Q H, Wang F, Lin C, et al. Effects of long-term fertilization on soil microbial community structure and aggregate composition in yellow clayey paddy field[J]. Journal of Plant Nutrition and Fertilizer, 2015, 21(6): 1599–1606. |
| [6] | Stark C H, Condron L M, O'Callaghan M, et al. Differences in soil enzyme activities, microbial community structure and short-term nitrogen mineral resulting from farm management history and organic matter amendments[J]. Soil Biology & Biochemistry, 2008, 40(6): 1352–1363. |
| [7] |
颜慧, 钟文辉, 李忠佩, 等. 长期施肥对红壤水稻土磷脂脂肪酸特性和酶活性的影响[J].
应用生态学报, 2008, 19(1): 71–75.
Yan H, Zhong W H, Li Z P, et al. Effects of long term fertilization on PLFA and enzyme activities in paddy red soil[J]. Chinese Journal of Applied Ecology, 2008, 19(1): 71–75. |
| [8] |
白震, 张明, 宋斗妍, 等. 不同施肥对农田黑土微生物群落的影响[J].
生态学报, 2008, 28(7): 3244–3253.
Bai Z, Zhang M, Song D Y, et al. Effects of different fertilization on microbial community in an arable mollisol[J]. Acta Ecologica Sinica, 2008, 28(7): 3244–3253. |
| [9] | Zhong W H, Cai Z C. Long term effects of inorganic fertilizers on microbial biomass and community functional diversity in a paddy soil derived from quaternary red clay[J]. Applied Soil Ecology, 2007, 36: 84–91. DOI:10.1016/j.apsoil.2006.12.001 |
| [10] |
孙凤霞, 张伟华, 徐明岗, 等. 长期施肥对红壤微生物生物量碳氮和微生物碳源利用的影响[J].
应用生态学报, 2010, 21(11): 2792–2798.
Sun F X, Zhang W H, Xu M G, et al. Effects of long-term fertilization on microbial biomass carbon and nitrogen and on carbon source utilization of microbes in a red soil[J]. Chinese Journal of Applied Ecology, 2010, 21(11): 2792–2798. |
| [11] |
于树, 汪景宽, 李双异. 应用PLFA方法分析长期不同施肥处理对玉米地土壤微生物群落结构的影响[J].
生态学报, 2008, 28(9): 4221–4227.
Yu S, Wang J K, Li S Y. Application of PLFA method to analyze the effects of long-term different fertilization treatments on soil microbial community structure in corn field[J]. Acta Ecologica Sinica, 2008, 28(9): 4221–4227. DOI:10.3321/j.issn:1000-0933.2008.09.019 |
| [12] |
卜洪震, 王丽宏, 尤金成, 等. 长期施肥管理对红壤稻田土壤微生物量碳和微生物多样性的影响[J].
中国农业科学, 2010, 43(16): 3340–3347.
Pu H Z, Wang L H, You J C, et al. Effects of long-term fertilization management on soil microbial biomass carbon and microbial diversity in red soil[J]. Scientia Agricultura Sinica, 2010, 43(16): 3340–3347. DOI:10.3864/j.issn.0578-1752.2010.16.009 |
| [13] | Zhao S, Li K, Zhou W, et al. Changes in soil microbial community, enzyme activities and organic matter fractions under long-term straw return in north central China[J]. Agriculture Ecosystems & Environment, 2016, 216: 82–88. |
| [14] |
范淼珍, 尹昌, 范分良, 等. 长期不同施肥对红壤碳、氮、磷循环相关酶活性的影响[J].
应用生态学报, 2015, 26(3): 833–838.
Fan M Z, Yin C, Fan F L, et al. Effects of different long-term fertilization on the activities of enzymes related to carbon, nitrogenand phosphorus cycles in a red soil[J]. Chinese Journal of Applied Ecology, 2015, 26(3): 833–838. |
| [15] |
李子川. 不同管理下稻田土壤有机碳及土壤胞外酶活性变化研究[D]. 南京: 南京农业大学博士学位论文, 2016.
Li Z C. Changes in organic carbon and extracellular enzyme activity of paddy soils with different field managements[D]. Nanjing: PhD Dissertation of Nanjing Agricultural University, 2016. |
| [16] |
蔡岸冬, 张文菊, 杨品品, 等. 基于Meta-analysis研究施肥对中国农田土壤有机碳及其组分的影响[J].
中国农业科学, 2015, (15): 2995–3004.
Cai A D, Zhang W J, Yang P P, et al. Effects degree of fertilization practices on soil organic carbon and fraction of croplands in China-based on meta-analysis[J]. Scientia Agricultura Sinica, 2015, (15): 2995–3004. DOI:10.3864/j.issn.0578-1752.2015.15.009 |
| [17] | Hedges L V, Gurevitch J, Curtis P S. The Meta-analysis of response ratios in experimental ecology[J]. Ecology, 1999, 80(4): 1150–1156. DOI:10.1890/0012-9658(1999)080[1150:TMAORR]2.0.CO;2 |
| [18] | Curtis P S, Wang X. A meta-analysis of elevated CO2 effects on woody plant mass, form, and physiology [J]. Oecologia, 1998, 113(3): 299–313. DOI:10.1007/s004420050381 |
| [19] | Niu L A, Hao J M, Zhang B Z, et al. Influences of long-term fertilizer and tillage management on soil fertility of the north China plain[J]. Pedosphere, 2011, 21(6): 813–820. DOI:10.1016/S1002-0160(11)60185-9 |
| [20] | Cruz A F, Hamel C, Hanson K, et al. Thirty-seven years of soil nitrogen and phosphorus fertility management shapes the structure and function of the soil microbial community in a brown chernozem[J]. Plant & Soil, 2009, 315(1-2): 173–184. |
| [21] | Powlson D S, Brookes P C, Christensen B T. Measurement of soil microbial biomass provides an early indication of changes in total soil organic matter due to straw incorporation[J]. Soil Biology & Biochemistry, 1987, 19(2): 159–164. |
| [22] | Lal R. World crop residues production and implications of its use as a bibful[J]. Environment International, 2005, 31(4): 575–584. DOI:10.1016/j.envint.2004.09.005 |
| [23] | Zhang P, Zheng J, Pan G, et al. Changes in microbial community structure and function within particle size fractions of a paddy soil under different long-term fertilization treatments from the Taihu Lake region, China[J]. Colloids & Surfaces Biointerfaces, 2007, 58(2): 264–270. |
| [24] | Santruckova H, Bird M I, Lloyd J. Microbial processes and carbon-isotope fractionation in tropical and temperate grassland soils[J]. Functional Ecology, 2000, 14(1): 108–114. DOI:10.1046/j.1365-2435.2000.00402.x |
| [25] |
黄瑞农. 环境土壤学[M]. 北京: 高等教育出版社, 1994, 145–146.
Huang R N. Environmental soil science[M]. Beijing: Higher Education Press, 1994, 145–146. |
| [26] | Díaz-Raviña M, Acea M J, Carballas T. Seasonal changes in microbial biomass and nutrient flush in forest soils[J]. Biology & Fertility of Soils, 1995, 19(2-3): 220–226. |
| [27] | Pal D, Broadbent F E. Influence of moisture on rice straw decomposition in soils[J]. Soil Science Society of America Journal, 1975, 39(1): 59–63. DOI:10.2136/sssaj1975.03615995003900010018x |
| [28] |
尧水红. 干湿交替强度对旱地土壤结构形成及水稻秸秆分解过程的相互作用的影响[D]. 南京: 南京农业大学硕士学位论文, 2005.
Yao S H. Soil biophysical processes involved in decomposition of rice straw incorporated in upland soils under wetting and drying cycles for stabilization of soil carbon pools and soil structure[D]. Nanjing: MS Thesis of Nanjing Agricultural University, 2005. |
| [29] |
任凤玲, 张旭博, 孙楠, 等. 施用有机肥对中国农田土壤微生物量影响的整合分析[J].
中国农业科学, 2018, 51(1): 119–128.
Ren F L, Zhang X B, Sun N, et al. A Meta-analysis of manure application impact on soil microbial biomass across China’s croplands[J]. Scientia Agricultura Sinica, 2018, 51(1): 119–128. |
| [30] |
沈冰洁, 祝贞科, 袁红朝, 等. 不同种植方式对亚热带红壤微生物多样性的影响[J].
环境科学, 2015, 36(10): 3839–3844.
Shen B J, Zhu Z K, Yuan H C, et al. Effects of different plantation type on the abundance and diversity of soil microbes in subtropical red soils[J]. Environmental Science, 2015, 36(10): 3839–3844. |
| [31] |
白军红, 邓伟, 张玉霞, 等. 洪泛区天然湿地土壤有机质及氮素空间分布特征[J].
环境科学, 2002, 23(2): 77–81.
Bai J H, Deng W, Zhang Y X, et al. Spatial distribution characteristics of soil organic matter and nitrogen in the natural floodplain wetland[J]. Environmental Science, 2002, 23(2): 77–81. DOI:10.3321/j.issn:0250-3301.2002.02.016 |
| [32] |
孙凤霞. 长期施肥对中国3种典型土壤微生物量碳氮和微生物碳源利用率的影响[D]. 呼和浩特: 内蒙古农业大学硕士学位论文, 2010.
Sun F X. Effects of Long-term fertilization on microbial biomass carbon, nitrogen and microbial utilization ratio of carbon source in three tropical soils of China[D]. Hohhot: MS Thesis of Inner Mongolia Agricultural University, 2010. |
| [33] | Li W T, Wu M, Liu M, et al. Responses of soil enzyme activities and microbial community composition to moisture regimes in paddy soils under long term fertilization practices[J]. Pedosphere, 2018, 28(2): 323–331. DOI:10.1016/S1002-0160(18)60010-4 |
| [34] |
蔡泽江, 孙楠, 王伯仁, 等. 长期施肥对红壤pH、作物产量及氮、磷、钾养分吸收的影响[J].
植物营养与肥料学报, 2011, 17(1): 71–78.
Cai Z J, Sun N, Wang B R, et al. Effects of long-term fertilization on pH of red soil, crop yields and uptakes of nitrogen, phosphorous and potassium[J]. Plant Nutrition and Fertilizer Science, 2011, 17(1): 71–78. |
| [35] | Kagawa M, Matsubara K, Kimura K, et al. Impacts of organic matter amendments on carbon and nitrogen dynamics in grassland soils[J]. Soil Biology & Biochemistry, 2014, 68(1): 52–61. |
| [36] | Ng E L, Patti A F, Rose M T, et al. Do organic inputs alter resistance and resilience of soil microbial community to drying?[J]. Soil Biology & Biochemistry, 2015, 81: 58–66. |
| [37] | Geisseler D, Scow K M. Long-term effects of mineral fertilizers on soil microorganisms-A review[J]. Soil Biology & Biochemistry, 2014, 75: 54–63. |
| [38] | Rousk J, Bååth E, Brookes P C, et al. Soil bacterial and fungal communities across a pH gradient in an arable soil[J]. Isme Journal, 2010, 4(10): 1340–1351. DOI:10.1038/ismej.2010.58 |
| [39] | Zhang P, Li L, Pan G, et al. Influence of long-term fertilizer management on topsoil microbial biomass and genetic diversity of a paddy soil from the Tai Lake region, China[J]. Acta Ecologica Sinica, 2004, 24(12): 2818–2824. |
| [40] | Saetre P, Baath E. Spatial variation and patterns of soil microbial community structure in a mixed spruce-birch stand[J]. Soil Biology & Biochemistry, 2000, 32(7): 909–917. |
| [41] | Shi P, Wang S, Jia S, et al. Effect of 25-year fertilization on soil microbial biomass and community structure in a continuous corn cropping system[J]. Archives of Agronomy & Soil Science, 2015, 61(9): 1303–1317. |
| [42] | Ftde V, Hoffland E, Nvan E, et al. Fungal/bacterial ratios in grasslands with contrasting nitrogen management[J]. Soil Biology & Biochemistry, 2006, 38(8): 2092–2103. |
| [43] | Michaels S, Johannes R. Considering fungal : bacterial dominance in soils-Methods, controls, and ecosystem implications[J]. Soil Biology & Biochemistry, 2010, 42(9): 1385–1395. |
| [44] | Bailey V L, Peacock A D, Smith J L, et al. Relationships between soil microbial biomass determined by chloroform fumigation-extraction, substrate-induced respiration and phospholipid fatty acid analysis[J]. Soil Biology & Biochemistry, 2002, 34(9): 1385–1389. |
| [45] | Buyer J S, Teasdale J R, Roberts D P, et al. Factors affecting soil microbial community structure in tomato cropping systems[J]. Soil Biology & Biochemistry, 2010, 42(5): 831–841. |
| [46] | Bardgett R D, Mcalister E. The measurement of soil fungal : bacterial biomass ratios as an indicator of ecosystem self-regulation in temperate meadow grasslands[J]. Biology & Fertility of Soils, 1999, 29(3): 282–290. |
| [47] | Dong W Y, Zhang X Y, Dai X Q, et al. Changes in soil microbial community composition in response to fertilization of paddy soils in subtropical China[J]. Applied Soil Ecology, 2014, 84(3): 140–147. |
| [48] |
毕明丽, 宇万太, 姜子绍, 等. 利用PLFA方法研究不同土地利用方式对潮棕壤微生物群落结构的影响[J].
中国农业科学, 2010, 43(9): 1834–1842.
Bi M L, Yu W T, Jiang Z S, et al. Study on effects of different land use patterns on microbial community structure in aquic brown soil by utilizing PLFA method[J]. Scientia Agricultura Sinica, 2010, 43(9): 1834–1842. DOI:10.3864/j.issn.0578-1752.2010.09.009 |
| [49] | Yan J, Pan G, Li L, et al. Adsorption, immobilization, and activity of beta-glucosidase on different soil colloids[J]. Journal of Colloid and Interface Science, 2010, 348(2): 565–570. DOI:10.1016/j.jcis.2010.04.044 |
| [50] | Gispert M, Emran M, Pardini G, et al. The impact of land management and abandonment on soil enzymatic activity, glomalin content and aggregate stability[J]. Geoderma, 2013, 202: 51–61. |
| [51] |
鲁艳红, 杨曾平, 郑圣先, 等. 长期施用化肥、猪粪和稻草对红壤水稻土化学和生物化学性质的影响[J].
应用生态学报, 2010, 21(4): 921–929.
Lu Y H, Yang Z P, Zhen S X, et al. Effects of long-term application of chemical fertilizer, pig manure and rice straw on chemical and biochemical properties of reddish paddy soil[J]. Chinese Journal of Applied Ecology, 2010, 21(4): 921–929. |
 2018, Vol. 24
2018, Vol. 24  doi:
doi: 

