2. 陕西沃德金鈅匙生物科技有限公司,陕西西安 610102
2. Shanxi Ward Gold Key Biological Technology Co. Ltd, Xian, Shaanxi 610102, China
化肥利用率低,面源污染严重是我国农业发展中急需解决的问题[1]。根据酶功能的专一性与催化反应的高速度来推断,将外源酶引入土壤是否对农业土壤环境起到积极作用?纤维素酶是由多种水解酶组成的一个复杂酶系,广泛存在于自然界的生物体中,其主要作用就是在分解纤维素时起生物催化作用,使纤维素成为单体葡萄糖,其应用于饲料、酒精、纺织、食品等领域,具有巨大的市场潜力[2],但在农业土壤上的应用却鲜有报道。土壤纤维素酶的活性与土壤纤维素分解细菌和真菌的活动有关,它与土壤腐殖质、氮、磷及某些微量元素的含量呈正相关,在一定程度上反映了土壤形成的生物气候及生态学条件、生物化学过程的强度及土壤肥力水平[3]。本研究旨在通过添加外源纤维素酶,在提高土壤本身纤维素酶活性的同时,影响其它土壤酶及土壤微生物,从而改变整体土壤环境,提高土壤肥力,为工厂化生产的有益酶早日用于土壤改良提供科学依据。
1 材料与方法 1.1 试验地点试验地点位于宁夏海原县高崖乡宁夏旱作节水高效农业科技园的槽式日光温室内 (105°09′ E,37°02′ N),海拔1363 m,地处黄土高原西北部,属黄河中游黄土丘陵沟壑区,宁夏中部干旱带。年平均降水量为286.0 mm,且降水分布不均衡,集中于5~9月,年均蒸发量2180 mm,年平均太阳总辐射量5642 × 109 J/m2,年日照时数2710 h,年均气温7.0℃,昼夜温差12~16℃,无霜期149~171 d。
1.2 试验材料供试土壤为典型的黏壤土。前茬为礼品西瓜,其0—20 cm表层土壤碱解氮肥力为偏低的5级水平 (30~60 mg/kg),有机质为极缺的6级水平 (< 6 g/kg),有效磷为中等偏低的4级水平 (5~10 mg/kg),速效钾为极丰富的1级水平 (> 160 mg/kg)[4],全盐含量1.32 g/kg,pH为8.31。表明所供试的土壤养分贫瘠、偏碱性、有机质含量少,为低产田土壤。
纤维素酶制剂由陕西沃德生物酶有限公司提供,主要由内切葡聚糖酶 (C1酶)、外切葡聚糖酶 (CX酶和CMC酶) 和 β-葡萄糖苷酶等组成,其中CMC酶活力为120万。
1.3 试验设计试验时间为2014年7月~2015年3月,以番茄‘芬达’为试材,采用随机区组设计,根据番茄定植前施入纤维素酶制剂的质量梯度设计6个处理,分别为未施入 (CK)、3 kg/hm2 (T1)、6 kg/hm2 (T2)、9 kg/hm2 (T3)、12 kg/hm2 (T4)、15 kg/hm2 (T5),小区面积为16 m2,三次重复,水肥及其它田间管理一致。于番茄结果初期测不同处理番茄的光合指标,并按照结果初期、结果盛期、采收盛期取土样进行土壤酶 (脲酶、蔗糖酶、SOD、碱性磷酸酶) 活性及土壤微生物 (细菌、真菌、放线菌) 的测定,并于番茄采收初期测定株高、茎粗,果实成熟期分批测产,确定小区最终产量。
1.4 测定指标与方法番茄植株的光合指标采用TPS-2便携式光合测定仪测定。
土样测定方法:取植株根部0—20 cm深的土样,每个处理小区内按“S”型进行多点取样,分别混合,混匀后一部分置于4℃冰箱保存,用于土壤微生物种群数量的调查,一部分土样风干粉碎过1 mm筛,用于土壤酶活性分析。土壤微生物数量的测定采用稀释平板计数法[5],细菌采用牛肉膏蛋白胨培养基10–4;真菌采用马丁孟加拉红–链霉素选择性培养基10–2 (1000 mL培养基中加1%孟加拉红水溶3.3 mL、1%链霉素3 mL);放线菌采用改良高氏一号培养基10–2 (每300 mL培养基中加入3%重铬酸钾1 mL,以抑制细菌和霉菌生长)。每处理按四分法称取10 g样土,溶于装有90 mL灭菌水的三角瓶中,置于空气浴震荡器上振荡摇匀30 min后静止,取上清液1 mL,溶于装有9 mL灭菌水的试管中,依次稀释至10–1、10–2、10–4梯度的菌悬液备用。用移液枪量取1 mL土壤菌悬液分别置于温度为50℃左右的培养基中与之混匀,凝结成平板后倒置于28℃恒温培养箱中培养。培养2~7天统计各处理真菌、细菌、放线菌菌落总数量。
土壤酶活性测定[6]:脲酶采用苯酚–次氯酸钠比色法,蔗糖酶采用3,5-二硝基水杨酸比色法,碱性磷酸酶采用磷酸苯二钠比色法,SOD (超氧化物歧化酶) 采用氮蓝四唑法。
采用Excel 2003和DPS 7.05对试验数据进行方差分析,采用Duncans新复极差法进行多重比较。
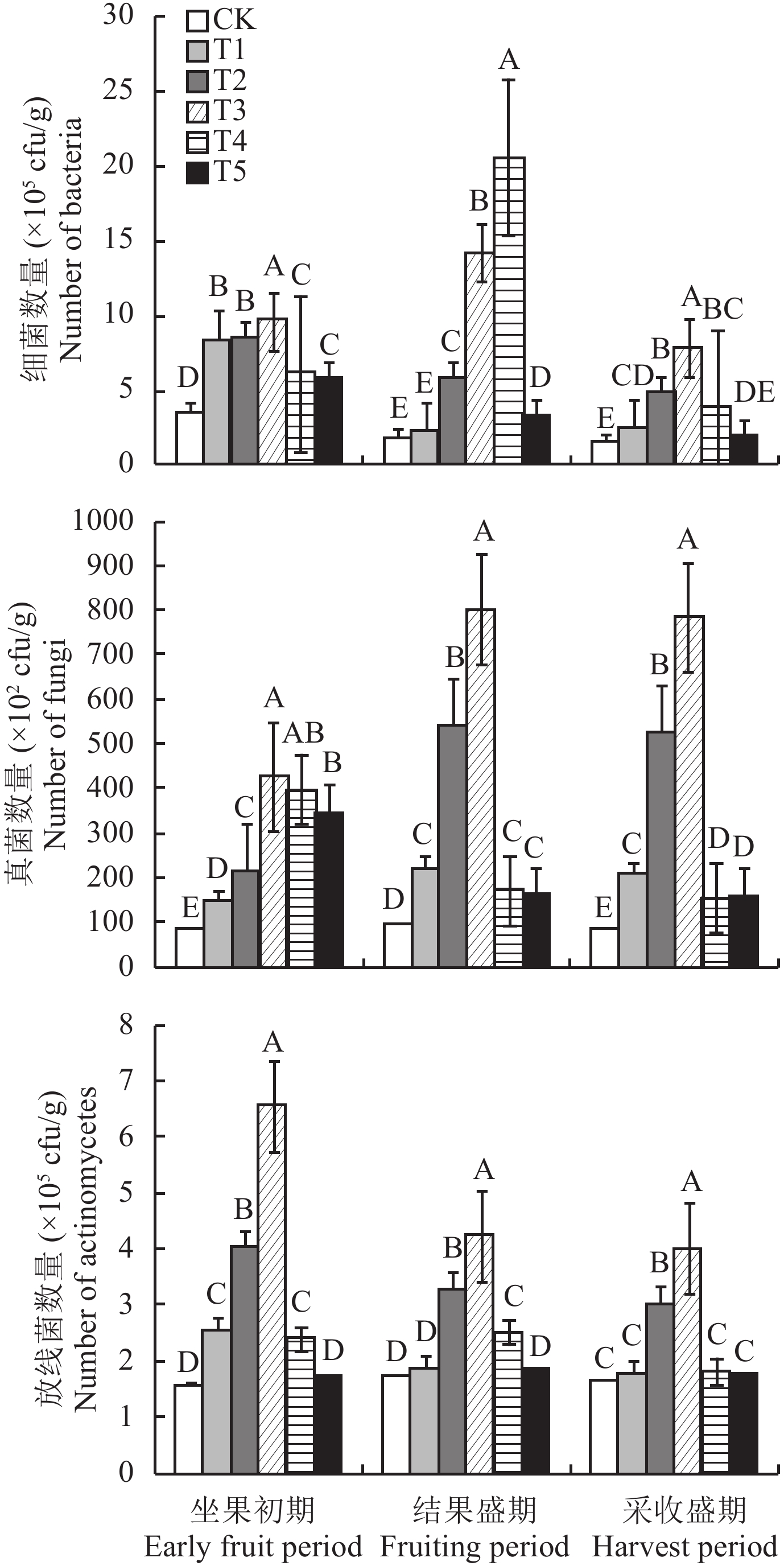
2 结果与分析 2.1 不同外源纤维素酶添加量对土壤微生物数量的影响由图1可见,添加外源纤维素酶后,与坐果初期相比,结果盛期T3、T4处理的土壤细菌数量增加,其中T4处理的增加幅度最大,数量最多,由坐果初期的6.20 × 105 cfu/g 增加到结果盛期的20.62 × 105 cfu/g,其他处理的土壤细菌数量降低,CK和T1处理的细菌数量最低,分别为1.88 × 105 cfu/g和2.23 × 105 cfu/g;采收盛期相对于结果盛期,采收盛期各处理细菌数量均大幅减少,其中T3处理数量最多,为1.88 × 105 cfu/g,CK最低,仅1.55 × 105 cfu/g,T1和T5处理细菌数量相差不大。同一时期不同处理随酶制剂用量的增加细菌数量先增加后降低,均以CK最低,坐果初期和采收盛期T3处理最高,分别较CK高出165.8%和408.4%,结果盛期则是T4处理细菌数量最多,较CK多出996.8%。
结果盛期与坐果初期相比,T2、T3处理的真菌数量急剧增加,分别由初期的215.59 × 102 cfu/g和426.35 × 102 cfu/g增加到539.28 × 102 cfu/g和802.46 × 102 cfu/g,分别增加97.8%和48.8%;CK、T1处理增加较少,T4、T5处理则显著减少;采收盛期较结果盛期,各处理真菌数量均略有减少,但差异不显著。同一时期不同处理随酶制剂用量的增加真菌数量先增加后降低,三个时期均是CK最低、T3处理最高,分别较CK高出368.4%、752.9%和801.4%,坐果初期时T4、T5与T3处理相差不大,结果盛期和采收盛期T3处理显著高于其他处理,其次是T2处理。
随着植株生长,T1、T2、T3处理放线菌数量持续减少,CK、T4、T5处理先减少后略有增加,但数量变化不显著;同一时期不同处理随酶制剂用量的增加放线菌数量先增加后降低,三个时期均是T3处理最高,分别为6.55 × 105、4.25 × 105、4.02 × 105 cfu/g,分别较CK高出314.6%、147.1%和145.1%,其次是T2处理,各个时期数量最低的均为CK 。
 |
|
图1
不同外源纤维素酶添加量下番茄不同生育期土壤中细菌、真菌、放线菌数量
Fig. 1
Population of bacteria, fungi and actinomycetes in one gram of soil under different amount of exogenous cellulase addition at different growing stages of tomato
|
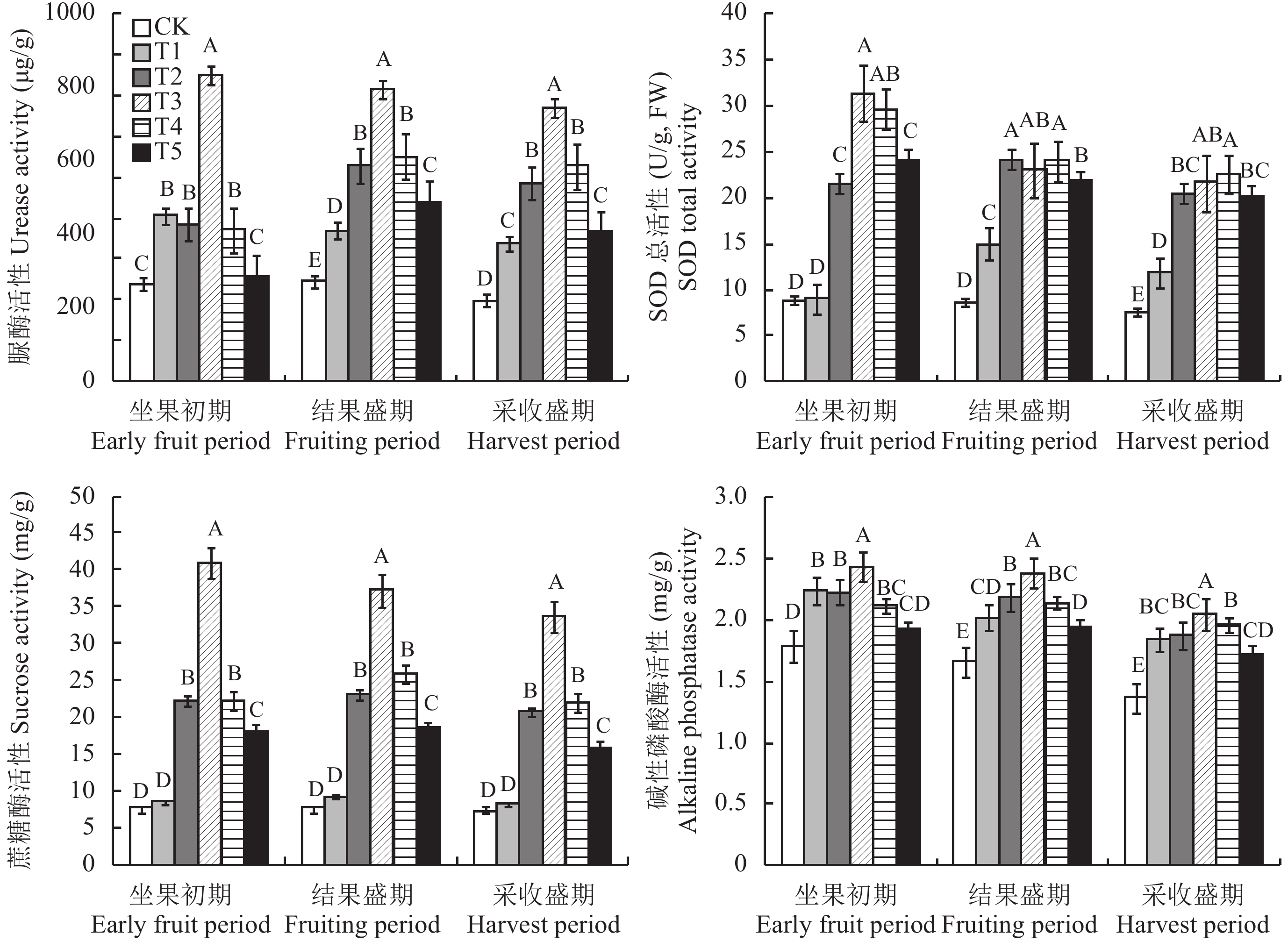
由图2可见,纤维素酶制剂对土壤脲酶、蔗糖酶、SOD及碱性磷酸酶活性的影响几乎趋于一致。随着酶制剂用量的增加,各个土壤酶活性均表现为先增加后降低,T3处理的脲酶、蔗糖酶活性在每个时期都极显著高于其他处理,脲酶活性分别为749.5、715.0、671.5 μg/g,蔗糖酶活性分别为40.8、37.2、33.5 mg/g,T2、T4处理的脲酶、蔗糖酶活性仅次于T3处理;T3处理的SOD总活性在番茄坐果初期最高,为31.4 U/g FW,T4处理略低于T3处理,在结果盛期T3处理则低于T2和T4处理,且T2、T4处理二者无显著差异,采收盛期则T4处理最高,为22.6 U/g FW,T3处理略低于T4处理;各处理的碱性磷酸酶活性在番茄坐果初期和结果盛期变化均不大,各处理之间除T3处理活性较高和CK活性较低外,其他处理差异不大。土壤脲酶、蔗糖酶、SOD及碱性磷酸酶活性最高时较CK分别增加了214.3%、424.3%、254.0%和44.0%。随着番茄生长期的延长,同一处理的以上各种酶活性均有所降低。
 |
|
图2
不同添加量外源纤维素酶对土壤脲酶、蔗糖酶、SOD酶、碱性磷酸酶活性的影响
Fig. 2
Impact of the exogenous cellulase on soil urease, sucrose, SOD and alkaline phosphatase activities
|
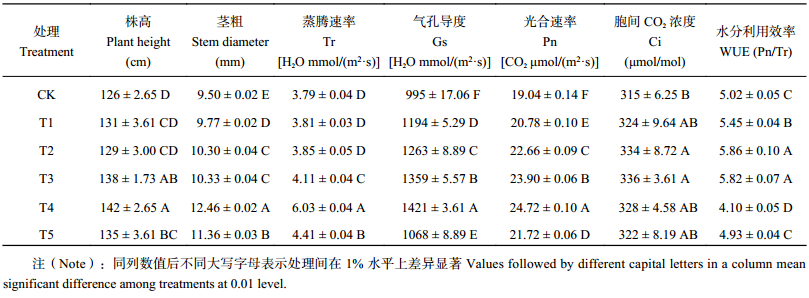
由表1可以看出,随着酶制剂用量的增加,番茄株高和茎粗均表现为先增加后降低,T4处理的番茄株高和茎粗均最大,说明其生长势最强,CK和T1处理的番茄株高和茎粗较小,且二者差别不大。光合指标中,番茄叶片的蒸腾速率、气孔导度、光合速率和胞间CO2浓度均随酶制剂用量的增加而升高,其中前三个指标均以T4处理最高,而胞间CO2浓度以T2、T3处理最高,且二者差异不显著,CK的各个光合指标均最低。T2、T3处理的水分利用效率最高,且二者无差异。
| 表1 不同添加量外源纤维素酶对番茄生长及光合指标的影响 Table 1 Effects of exogenous cellulase rate on tomato growth and photosynthesis |
 |
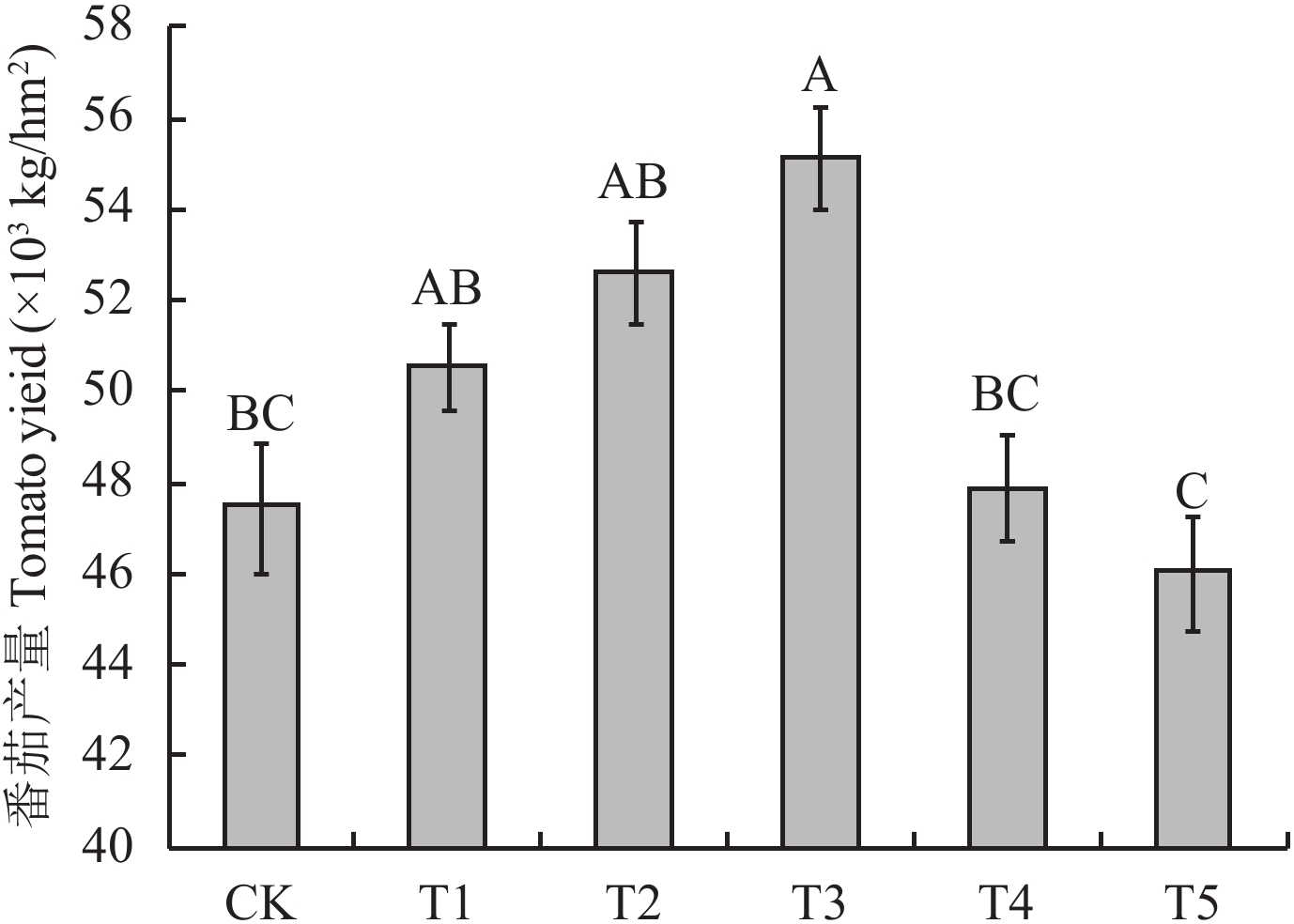
由图3可见,随着酶制剂用量的增加番茄产量先增加后降低,T3处理的番茄产量最高,为55188 kg/hm2,其次是T2处理,为52621 kg/hm2,T3处理与T2、T1处理无显著差异;T5处理产量最低,仅为46058 kg/hm2。
 |
|
图3
不同添加量外源纤维素酶对番茄产量的影响
Fig. 3
Effects of the exogenous cellulase rate on tomato yield
|
土壤酶在生态系统的有机质腐解、养分循环与迁移等代谢反应中起着非常重要的作用,是土壤质量的潜在敏感性指标[7–8],可以作为土壤肥力、土壤质量和微生物活性的重要指标[9–10]。纤维素酶主要是在分解纤维素时起生物催化作用[11]。向土壤中施加外源纤维素酶,有助于提高土壤原生纤维素酶活性[12]。本实验中,添加外源纤维素酶有利于土壤中细菌、真菌、放线菌数量的增加,并增强了土壤脲酶、蔗糖酶、SOD及碱性磷酸酶活性,对番茄植株生长及光合作用有一定的促进作用,增加了番茄产量。原因可能是,外源纤维素酶在分解纤维素的过程中,促使土壤中的微生物大量繁殖,而土壤酶主要来源于土壤中的微生物及作物,微生物数量的增多势必会增加土壤中酶的活性,根际微生物的适度生长以及土壤酶可加快根际土壤有效养分的转化与储存,并刺激植物根系对养分的吸收[13–14],从而促进番茄生长和产量提高。
但是同一植物的不同生育期,其根际微生物的数量、种类等存在很大差异,这可能与植物根系释放的有机物质有关[15],同时,根分泌物通过改变根际环境,如pH、氧化还原电位等间接地影响根际微生物的类型[16]。当纤维素酶的添加量提高时,土壤中纤维素酶活力也会有所提高,相应的微生物和土壤酶也随之增加,但当外源酶增加到一定用量时 (12 kg/hm2和15 kg/hm2),微生物和土壤酶以及作物部分农艺指标反而出现不同程度的降低,这可能是因为当提高添加的纤维素酶水平时,土壤对纤维素酶的无效吸附也有相应增加所致[17],也可能与外源纤维素酶、根际微生物种群数量、土壤酶活性三者的单效以及互作关系有关,而此过程中主效因素的确定有待于进一步研究。
随着外源纤维素酶制剂施用量的增加,番茄株高、茎粗和产量以及光合速率、蒸腾速率、气孔导度、胞间CO2浓度等农艺和光合生理指标均呈现先增加再下降的变化规律,其中T3处理番茄农艺性状和生理指标表现效果最优,因此外源纤维素酶制剂的使用量以9 kg/hm2为宜。
| [1] |
楚骏莹. 农业面源污染现状及建议措施[J].
北京农业, 2016, (2): 156–157.
Chu J Y. Current situation and suggestions of agricultural non-point source pollution[J]. Beijing Agriculture, 2016, (2): 156–157. |
| [2] |
武秀琴. 纤维素酶及其应用[J].
微生物学杂志, 2009, 29(2): 89–92.
Wu X Q. Cellulase and its application[J]. Journal of Microbiology, 2009, 29(2): 89–92. |
| [3] |
李飒. 不同温度、pH、底物下外源纤维素酶对土壤原生酶活性及酶解率的影响[D]. 山东泰安: 山东农业大学硕士学位论文, 2006.
Li S. Effect of the out–cellulase on soil enzyme activity and enzymatic hydrolysis under different temperature, pH and substrates [D]. Tai'an, Shandong: MS Thesis of Shandong Agricultural University, 2006. |
| [4] |
全国土壤普查办公室. 中国土壤[M]. 北京: 中国农业出版社, 1998.
National Soil Survey Office. Chinese soils [M]. Beijing: China Agriculture Press, 1998. |
| [5] |
李振高, 骆永明, 腾应. 土壤与环境微生物研究法[M]. 北京: 科学出版社, 2008.
Li Z G, Luo Y M, Teng Y. Soil and environmental microbiology research methods [M]. Beijing: Science Press, 2008. |
| [6] |
鲍士旦. 土壤农化分析(第三版)[M]. 北京: 中国农业出版社, 2000.
Bao S D. Soil and agrochemical analysis (Third edition) [M]. Beijing: China Agriculture Press, 2000. |
| [7] | Nayak D R, Babu Y J, Adhya T K. Long-term application of compost influences microbial biomass and enzyme activities in a tropical Aeric Endoaquept planted to rice under flooded condition[J]. Soil Biology and Biochemistry, 2007, 39(8): 1897–1906. DOI:10.1016/j.soilbio.2007.02.003 |
| [8] | Aon M A, Colaneri A C. Temporal and spatial evolution of enzymatic activities and physico-chemical properties in an agricultural soil[J]. Applied Soil Ecology, 2001, 18(3): 255–270. DOI:10.1016/S0929-1393(01)00161-5 |
| [9] |
侯雪莹, 韩晓增, 王树起, 等. 土地利用方式对黑土酶活性的影响[J].
中国生态农业学报, 2009, 17(2): 215–219.
Hou X Y, Han X Z, Wang S Q, et al. Effect of landuse type on enzyme activity in black soil[J]. Chinese Journal of Eco-Agriculture, 2009, 17(2): 215–219. |
| [10] | Caravaca F, Alguacil M M, Figueroa D, et al. Re-establishment of retama sphaerocarpa as a target species for reclamation of soil physical and biological properties in a semi-arid Mediterranean area[J]. Forest Ecology and Management, 2003, 182: 49–58. DOI:10.1016/S0378-1127(03)00067-7 |
| [11] |
刘晓晶, 李田, 翟增强. 纤维素酶的研究现状及应用前景[J].
安徽农业科学, 2011, 39(4): 1920–1921, 1924.
Liu X J, Li T, Zhai Z Q. The status and application prospect of cellulase[J]. Journal of Anhui Agriculture Science, 2011, 39(4): 1920–1921, 1924. |
| [12] |
李飒, 聂俊华. 不同温度下外源纤维素酶对土壤原生纤维素酶活性的影响[J].
安徽农业科学, 2010, 38(21): 11359–11360, 11449.
Li S, Nie J H. Effect of the exogenous cellulase on the activity of its native enzyme in soil under different temperature condition[J]. Journal of Anhui Agriculture Science, 2010, 38(21): 11359–11360, 11449. DOI:10.3969/j.issn.0517-6611.2010.21.118 |
| [13] |
倪国荣, 涂国全, 魏赛金, 等. 稻草还田配施催腐菌剂对晚稻根际土壤微生物与酶活性及产量的影响[J].
农业环境科学学报, 2012, 31(1): 149–154.
Ni G R, Tu G Q, Wei S J, et al. Effects of straw-returning using agent on microbe and enzyme activity in rhizosphere soils and yield of late rice[J]. Journal of Agro-Environment Science, 2012, 31(1): 149–154. |
| [14] |
王茹华, 张启发, 周宝利, 等. 浅析植物根分泌物与根际微生物的相互作用关系[J].
土壤通报, 2007, 38(1): 167–172.
Wang R H, Zhang Q F, Zhou B L, et al. Analysis on the interaction between root exudates and rhizosphere microbes[J]. Chinese Journal of Soil Science, 2007, 38(1): 167–172. |
| [15] | Kapoor R. Root exudation and its implication on rhizosphere mycoflora[J]. Advances in Microbial Biotechnology, 1999, 44(2): 351–362. |
| [16] |
张淑香, 高子勤. 连作障碍与根际微生态研究 Ⅱ.根系分泌物与酚酸物质[J].
应用生态学报, 2000, 11(1): 152–156.
Zhang S X, Gao Z Q. Continuous cropping obstacle and rhizospheric microecology Ⅱ. Root exudates and phenolic acids[J]. Chinese Journal of Applied Ecology, 2000, 11(1): 152–156. |
| [17] |
韩玮, 聂俊华, 李飒. 外源纤维素酶对秸秆降解速率及土壤速效养分的影响[J].
中国土壤与肥料, 2006, (5): 28–32.
Han W, Nie J H, Li S. Influences of outer cellulase on degradation rates of straws and available nutrients of soil[J]. Soil and Fertilizer Sciences in China, 2006, (5): 28–32. DOI:10.11838/sfsc.20060508 |
 2017, Vol. 23
2017, Vol. 23  doi:
doi: 
