2. 河南省粮食作物协同创新中心,河南郑州 450002;
3. 河南农业大学植物保护学院,河南郑州 450002
2. Collaborative Innovation Center of Food Crops in Henan, Zhengzhou 450002, China;
3. College of Plant Protection, Henan Agricultural University, Zhengzhou 450002, China
小麦是世界上第三大粮食作物,蚜虫是影响小麦生产的主要害虫。据全国农技推广中心历年公布的数据,我国麦蚜常年发生面积约为 0.1~0.17 亿公顷,造成小麦减产 10% 左右[1],其中麦长管蚜 (Sitobion avenae F.) 是我国黄淮麦区的优势种[2],不仅直接吸食麦株汁液,同时通过传播病毒,对小麦产量造成极大的影响。
提高作物抗虫性是降低虫害发生、对虫害进行综合防治的重要技术途径,也是农业领域中极具挑战性的研究课题[3]。研究表明,施肥等农艺措施对作物抗虫性具有重要影响[4–5],其中施用钾肥在降低作物虫害发生方面效果突出。Waring 等[6]通过综述前人研究结果指出,有 50% 和 40% 试验中高钾供应与蚜虫或刺吸性虫害发生呈正相关;Perrenouds[7]对国际钾肥研究所 2000 多项钾肥试验结果进行总结后发现,63% 的施用钾肥试验能够降低虫害的发生率;钾缺乏延长大麦蚜虫生命历期和增加繁殖能力[8];土壤或叶片钾含量较低时大豆蚜虫群体密度、蚜虫净增值率和内禀增长率较高[9–11]。
碳水化合物是植物和植食性昆虫共同的能量来源,而氨基酸作为植物主要的氮素形态,不仅是制约植食性昆虫生长的食物,也是重要的防御性物质的前体物质[12],而可溶性蛋白作为植物另一类含氮化合物,不仅可以酶的形式参加植物的各种代谢活动和作为渗透调节物[13],而且也是植食性昆虫的营养物质[14]。因而,对上述物质进行调控对控制植食性昆虫的发生具有重要意义。
研究表明,供钾水平对植株碳氮代谢有重要影响。例如 Van Emden 等[15]发现,施钾可降低甘蓝可溶性氮的含量;Hu 等[16]研究认为,缺钾的棉花植株游离氨基酸含量较高;低钾胁迫条件下,玉米可溶性蛋白含量降低,而可溶性糖含量增加[13]。植食性昆虫取食亦可诱导植物基本代谢物质尤其是碳水化合物和氨基酸的变化。蚜虫取食可诱导小麦韧皮部必需氨基酸含量的升高[17–18];蚜虫取食日本花楸后植株游离氨基酸含量比未取食植株高约 4 倍[19],但关于蚜虫取食条件下供钾水平对植株碳氮代谢相关物质积累的影响研究较少,尤其是将上述变化与蚜虫发生相联系的研究还鲜见报道。
本研究通过对不同钾水平下小麦植株分别进行不接虫和接虫处理,探讨了供钾水平和蚜虫取食对麦株游离氨基酸、可溶性蛋白质和可溶性糖影响的主效及其交互效应,在此基础上分析了供钾水平对蚜虫取食过程中上述物质变化的影响及其与蚜虫密度的关系,为田间麦蚜的生态调控提供科学依据。
1 材料与方法 1.1 试验设计本试验采用水培试验,在光照培养室中进行,采用钾水平和蚜虫侵染水平 5 × 2 设计,其中 5 个供钾 (K+) 水平分别为 0.005、0.05、0.5、2、10 mmol/L;蚜虫侵染分为不接虫和接虫两个水平。植物所需要的钾用氯化钾提供 (其中钾水平低于 2 mmol/L 处理中 Cl– 用 NaCl 补充)。营养液配方采用杨振明营养液:Ca (NO3)2·4H2O 0.6 mmol/L, NH4NO3 0.8 mmol/L, CaCl2 2.6 mmol/L, MgSO4·7H2O 0.3 mmol/L, (NH4)2HPO4 0.28 mmol/L, NH4H2PO4 0.64 mmol/L, CuSO4·5H2O 0.001 mmol/L, ZnSO4·7H2O 0.001 mmol/L, H3BO3 0.033 mmol/L,MnSO4 0.01 mmol/L, (NH4)6Mo7O2·4H2O 0.0002 mmol/L。螯合铁:EDTA-Fe2+ 0.02 mmol/L。培养过程中每 2 天更换 1 次营养液。小麦五叶一心开始接种蚜虫 (5 头/株),蚜虫选用虫龄一致的健壮成虫,每个处理 15 株为一个重复,共设 3 个重复。为防止蚜虫从接虫植株上迁出,用上端开口的玻璃纸罩将植株罩住,开口处再盖上用 80 目 (
于接种蚜虫后的第 4 天和第 8 天取样之前先调查蚜虫数量,然后称取对应小麦植株的地上部干重,计算单位干物质重的蚜虫数目。
1.3 游离氨基酸、可溶性糖和可溶性蛋白质含量的测定于接种蚜虫后的第 4 天和第 8 天取样,各处理接虫植株取接虫部位叶片,不接虫植株取同叶位叶片。游离氨基酸测定采用水合茚三酮法,可溶性糖测定采用蒽酮法,可溶性蛋白质测定采用考马斯亮蓝法。
1.4 数据处理数据处理采用 Excel 2010 和 SPSS statistics 19.0 进行数据计算与统计分析;相关性采用双变量相关性分析。
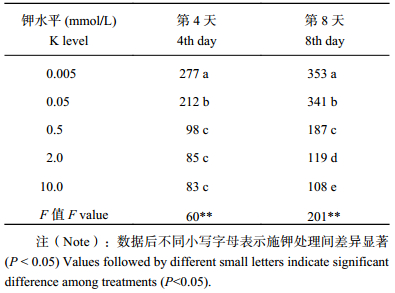
2 结果与分析 2.1 不同供钾水平对麦株蚜虫数量的影响随着时间的推移,各施钾水平蚜虫数量均呈增加趋势;随着钾水平的提高,麦株上蚜虫数量整体呈降低趋势 (表 1)。接虫后第 4 天,蚜虫数量在 K 0.005~0.5 mmol/L 范围内显著下降,继续提高钾水平蚜虫数量无显著变化;接虫后第 8 天,蚜虫数量在 K 0.005~10 mmol/L 范围内显著下降。由此可以看出,随着蚜虫侵染时间的延长,降低蚜虫数量所需的供钾水平随之增加。
| 表1 处理 4 天、8 天后麦株蚜虫数量 (No./g, DW) Table 1 Number of aphids in wheat under different K treatments on the 4th and 8th day after the infestation |
 |
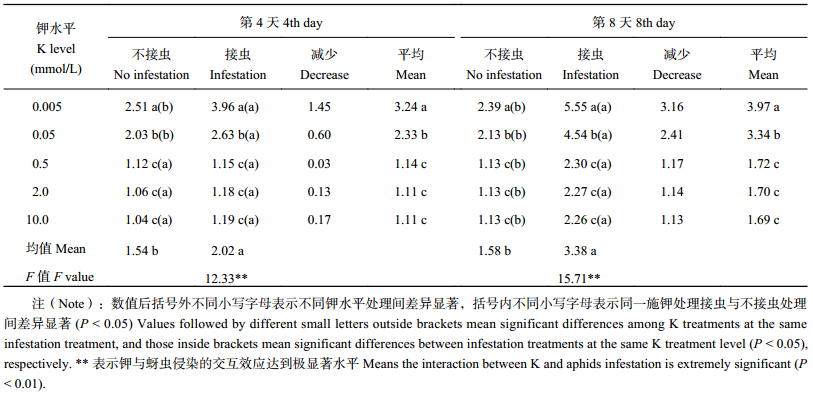
在两个时间节点上,钾水平和接虫水平对小麦游离氨基酸影响的主效应及其交互效应均达显著水平 (表 2)。同一接虫水平下,叶片游离氨基酸含量均随着钾水平的提高呈先降低后趋于稳定的趋势,其转折点在 K0.5 水平。钾水平相同时,与不接虫处理相比,接虫植株叶片游离氨基酸含量均呈增加趋势,但接虫植株与不接虫植株两者差值随钾水平的增加而缩小,其中在接虫后第4天 K 0.005、0.05 mmol/L 水平下,接虫与不接虫植株叶片游离氨基酸含量差异达显著水平;而在接虫后第8天,各供钾水平下接虫与不接虫植株叶片游离氨基酸含量差异均达显著水平。两个时间点相比,随时间推移,不接虫处理植株游离氨基酸的增加幅度较小,为–4.8%~10.8%,平均增幅为 2.6%;而接虫处理不同钾水平下植株游离氨基酸含量增加幅度较大,为 40.2%~100.0%,平均增幅为 67.3%。
| 表2 接虫后第 4 天和第 8 天不同钾水平处理小麦游离氨基酸含量 (mg/g) Table 2 Free amino acids content of wheat after the aphids infestation under different K levels on the 4th and the 8th day |
 |
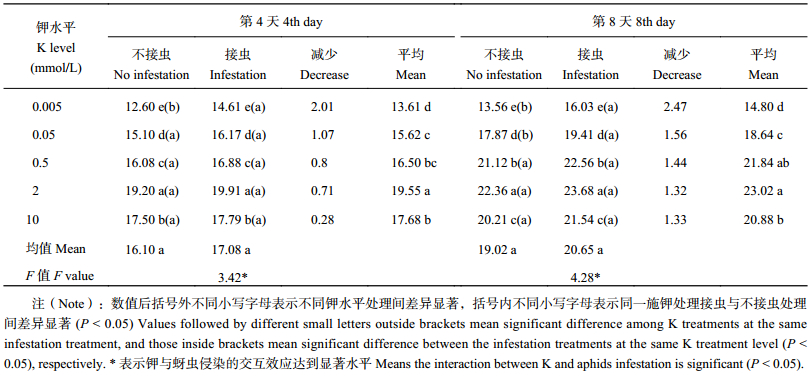
在两个时间节点上,钾水平对小麦可溶性蛋白质含量的影响的主效应达显著水平,接虫水平对小麦可溶性蛋白质影响的主效应未达显著水平,但钾水平和接虫水平对小麦可溶性蛋白质影响的交互效应达显著水平 (表 3)。接虫水平相同时,叶片可溶性蛋白质含量均随着钾水平的提高呈先增加后减少的趋势,其中在 K2 水平下叶片可溶性蛋白质含量达最高。同一钾水平下,与不接虫处理相比,接虫后植株叶片可溶性蛋白含量均呈增加趋势,但接虫植株与不接虫植株叶片可溶性蛋白含量的差值随钾水平的提高而缩小,在接虫后第 4 天 K 0.005 mmol/L 水平下、在第 8 天 K 0.005 和 0.05 mmol/L 水平下,接虫与不接虫植株叶片可溶性蛋白含量差异均达显著水平。两个时间点下相同处理间叶片可溶性蛋白质含量均随时间推移呈增加趋势。其中,不接虫处理间植株可溶性蛋白含量增加 7.6%~31.3%,平均增幅为 18.1%;接虫处理间植株可溶性蛋白含量增加 9.7%~33.7%,平均增幅为 20.7%。
| 表3 接虫后第 4 天和第 8 天不同钾水平处理小麦可溶性蛋白质含量 (mg/g) Table 3 Effect of K levels on total soluble protein content of wheat under different K treatment levels on the 4th and the 8th day after the aphids infestation |
 |
在两个时间节点上,钾水平和接虫水平对小麦可溶性总糖含量的影响的主效应及其交互效应均达显著水平 (表 4)。不接虫时,小麦叶片可溶性总糖含量均随着钾水平的提高呈先增加后趋于稳定的变化规律,其转折点为 K 0.05 mmol/L,进一步提高钾水平可溶性糖含量变化不显著。接虫时,在第 4 天小麦叶片可溶性总糖含量随着钾水平的变化规律与不接虫相同,但转折点钾水平提高到 K 0.5 mmol/L。在第 8 天小麦叶片可溶性总糖含量随着钾水平的提高而升高。供钾水平相同时,与不接虫相比,接虫后小麦叶片可溶性总糖增加量随钾水平增加而提高,其中在第 4 天的 K 2 和 10 mmol/L 水平下,在第 8 天的各供钾水平下,可溶性总糖的增加量均达显著水平。两个时间点相比,不接虫处理叶片可溶性总糖含量随时间推移增加较少,增加幅度为–3.7%~4.4%,平均增幅为 2.0%;接虫处理叶片可溶性总糖含量随时间推移增加较多,增加幅度为 17.8%~29.9%,平均增幅为 22.9%。
| 表4 接虫第 4 天和第 8 天不同钾水平处理小麦可溶性总糖含量 (mg/g) Table 4 Total soluble sugar content of wheat affected by the K treatment levels on the 4th and the 8th day after the aphids infestation |
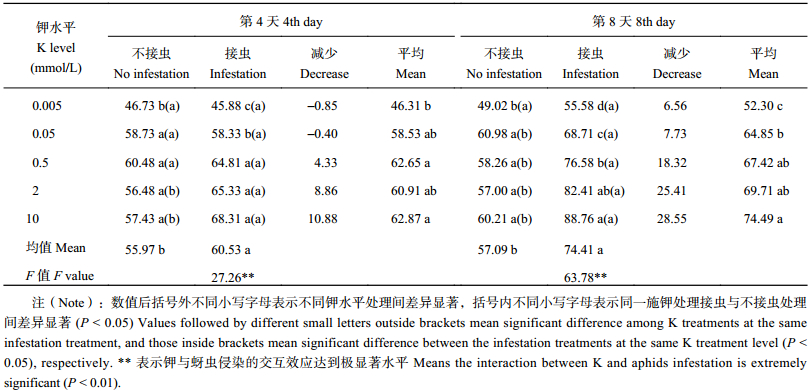 |
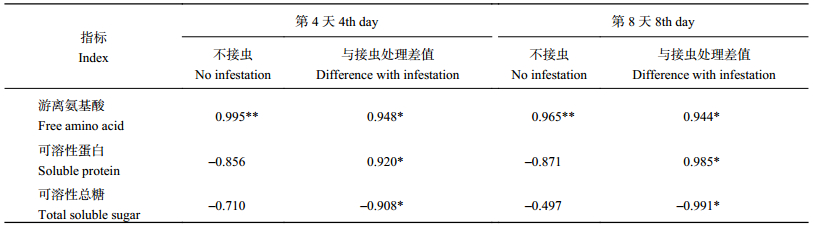
表 5 表明,在接虫后第 4 天和第 8 天,随着钾水平的增加,小麦蚜虫密度与不接虫小麦叶片游离氨基酸含量呈极显著正相关关系,与可溶性蛋白和可溶性糖含量相关性不显著;与蚜虫取食诱导的游离氨基酸积累量、可溶性蛋白积累量呈显著的负相关关系,而与蚜虫取食诱导的可溶性糖的增加量呈显著的正相关关系。
| 表5 接虫后第 4 天和第 8 天各测定指标与蚜虫密度的相关性分析 Table 5 Correlation analysis of the measured items and aphid population density on the 4th and 8th day after the aphids infestation |
 |
植物的抗性,既涉及到植物本身的组成抗性,也包括遭受植食性昆虫进攻后所表现出来的诱导抗性[20]。植物的抗虫性外在表现为昆虫种群降低和为害减少,其内在机理既与植物基础代谢相关,也与其次生代谢有关。本研究涉及的施钾可以增强小麦抗蚜水平的可能的生理机制,就是从植物基础代谢的角度开展的研究。
本试验结果表明,在接虫后 8 天内,两个时间节点小麦植株单位干重的蚜虫群体密度均受供钾水平的影响,且在一定供钾浓度范围内随供钾水平的提高呈降低趋势,这与前人在大豆、甘蓝等作物上发现的土壤或叶片钾含量较低时植株蚜虫群体密度、蚜虫净增值率和内禀增长率繁殖率较高的研究结果相一致[9–11, 14]。进一步证明提高供钾水平可降低蚜虫密度,同时研究也发现,随着时间的推移,有效降低蚜虫密度所需要的钾水平增加。
前人关于供钾水平对植株游离氨基酸、可溶性蛋白和可溶性糖含量的影响已进行过较多研究。多数研究结果均表明缺钾增加植株游离氨基酸水平,这在大豆、棉花、甘蓝等作物上均得到证明[11, 14-15],本研究结果与前人结论基本一致,且进一步发现,供钾水平在 0.5 mmol/L 以下植株游离氨基酸含量显著降低,而钾水平高于 0.5 mmol/L,进一步增加供钾水平植株游离氨基酸含量变化较小。前人关于供钾水平对植株可溶性蛋白质、可溶性糖含量的影响的研究结果不尽一致,有的结果甚至相反。如闫洪奎等[16]和 Mengel 等[21]发现低钾胁迫使植物可溶性蛋白含量降低,而 Rashid 等[22]则发现,增施钾肥可以使水稻组织内可溶性蛋白含量降低。而本研究发现,供钾水平过低和过高对小麦可溶性蛋白质含量均有不利影响。Marschner 等[23]认为,供钾不足会引起植物体内可溶性糖含量的升高,Rashid 等[22]的研究也表明,提高水稻组织中的含钾量会降低可溶性糖含量。但是,柳洪鹃等[24]研究表明,钾肥可以促进植物组织中淀粉水解,从而提高组织可溶性糖含量。本研究结果表明,小麦可溶性蛋白随供钾水平的增加呈先上升后降低的趋势;在钾水平低至 0.005 mmol/L 时,小麦可溶性糖含量虽显著降低,但在该水平以上,进一步提高钾水平,可溶性糖含量变化不显著。与前人研究不尽一致。笔者认为,植株可溶性蛋白和可溶性糖含量对钾水平的响应可能受作物类型和品种、外部环境条件等多种因素的影响,而本试验条件与其它研究可能有所差异。
相关分析表明,未接虫时,仅植株游离氨基酸的含量与相应时间节点蚜虫密度呈显著的正相关关系,而可溶性蛋白质和可溶性糖的含量与相应时间节点蚜虫密度均未达到显著水平,似乎说明植株中后两种物质积累的多少不是限制蚜虫生长的主要因子。但这一结果似乎难以解释前人的研究,人们发现,抗蚜品种西瓜幼苗的可溶性蛋白含量明显低于感蚜材料[25];小麦抗蚜性与可溶性蛋白含量呈负相关[26]。棉株体内可溶性糖含量与其抗蚜性呈正相关[27];冬小麦体内平均可溶性糖含量越高,麦蚜密度或生殖力越低[26]。朱永峰等[28]对燕麦的研究发现,高抗蚜品种受到蚜虫危害后体内可溶性糖含量的增加显著高于感蚜品种。Karley 等[29]和 Pompon 等[30]研究认为,植物韧皮部可溶性糖浓度足够高时会导致蚜虫的取食液和血淋巴渗透势升高,从而引起蚜虫脱水和死亡。蔗糖的浓度显著影响蚜虫的进食,当蔗糖的浓度超过20%以后,蚜虫的进食严重减弱[31]。
笔者分析发现,供钾水平和蚜虫取食对植株游离氨基酸、可溶性蛋白质含量和可溶性糖含量影响的交互效应亦达显著水平,也就是说,寄主植物中受蚜虫取食所诱导的上述物质积累因供钾水平不同而异。其中随着供钾水平的增加,蚜虫取食诱导的游离氨基酸和可溶性蛋白含量显著降低,而蚜虫取食诱导的可溶性糖含量显著增加。相关分析表明,随着钾水平的提高,寄主蚜虫取食诱导的氨基酸、可溶性蛋白质的增加量与蚜虫密度呈显著的正相关关系,而可溶性糖的增加量与蚜虫密度呈显著的负相关关系。该结果与前人研究所得的氨基酸、可溶性蛋白以及可溶性糖与蚜虫密度的关系基本吻合,所以我们推测,供钾水平对蚜虫密度的影响一方面是降低了植株体内组成型和诱导型游离氨基酸的含量,另一方面降低了诱导型可溶性蛋白含量和增加了诱导型可溶性糖的含量,共同降低麦长管蚜密度。
关于施钾增强植株抗虫性的机理,前人从钾对植物基础代谢的影响角度虽进行过阐述,例如 Van Emden 提出,施钾降低甘蓝蚜虫繁殖力机理与降低了植株游离氨基酸含量有关[15];Walter 等[11]提出,施钾降低大豆蚜虫发生与降低了植株韧皮部中的天冬氨酸含量有关,但上述研究主要基于施钾对未感虫植株的生理代谢的影响进行分析,因而未涉及施钾对虫害诱导植物抗蚜性的影响。而本研究通过对不同钾水平下小麦植株分别进行不接虫和接虫处理,在探讨供钾水平和蚜虫取食对麦株游离氨基酸、可溶性蛋白质和可溶性糖影响的主效及其交互效应基础上,分析了供钾水平对蚜虫取食过程中麦株上述物质变化的影响及其与蚜虫密度的关系,既探讨了施钾对植株组成型抗性的影响,也探讨了施钾对蚜虫取食诱导抗性的影响,更为深入地阐述供钾水平—植株基础代谢—蚜虫发生的关系。
目前认为,虫害的早期信号传到细胞内后,植物将通过三种主要的激素茉莉酸 (JA)、水杨酸 (SA)、乙烯 (ET) 等信号物质介导的信号通路,启动一系列防御反应[32]。因此需要进一步深入分析钾水平对上述过程的调控机理,以揭示施钾如何通过影响植物基础代谢而影响植物的防御反应。另外,本试验是在室内水培条件下严格控制蚜虫迁移的前提下开展的,且只应用了一个小麦品种,因此,该试验仅反映了无翅蚜虫在不同钾水平的矮抗 58 小麦幼苗上的生长发育与植株体内碳氮代谢相关物质含量的关系,其结果有待在更多的品种、土壤培育小麦和田间进一步验证。
总之,从植物基础代谢角度分析,提高钾水平可能通过降低小麦组成型游离氨基酸的含量,降低蚜虫取食诱导型游离氨基酸和可溶性蛋白积累,提高诱导型可溶性糖的积累,共同降低小麦苗期麦长管蚜密度。
| [1] |
胡想顺, 赵惠燕. 我国小麦抗蚜机理研究进展[J].
应用昆虫学报, 2014, 51(6): 1459–1469.
Hu X S, Zhao H Y. The reviews of wheat resistant mechanism to cereal aphid in China[J]. Chinese Journal of Applied Entomology, 2014, 51(6): 1459–1469. DOI:10.7679/j.issn.20951353.2014.170 |
| [2] |
王美芳, 原国辉, 陈巨莲, 等. 麦蚜发生危害特点及小麦抗蚜性鉴定的研究[J].
河南农业科学, 2006, (7): 58–60.
Wang M F, Yuan G H, Chen J L, et al. Research advances of occurrence pattern, damage characteristics of wheat aphid and resistance identification of wheat[J]. Journal of Henan Agricural sciences, 2006, (7): 58–60. |
| [3] | Dogimont C, Bendahmane A, Chovelon V, et al. Host plant resistance to aphids in cultivated crops: Genetic and molecular bases, and interactions with aphid populations[J]. Comptes Rendus Biologies, 2010, 333: 566–573. DOI:10.1016/j.crvi.2010.04.003 |
| [4] | Altieri M A, Nicholls C I. Soil fertility management and insect pests: harmonizing soil and plant health in agroecosystems[J]. Soil & Tillage Research, 2003, 72: 203–211. |
| [5] |
庞淑婷, 董元华. 土壤施肥与植食性害虫发生为害的关系[J].
土壤, 2012, 44(5): 719–726.
Pang S T, Dong Y H. Effects of soil fertilization on herbivores infestation[J]. Soils, 2012, 44(5): 719–726. |
| [6] | Waring G L, Cobb N S. The impact of plant stress on herbivore population dynamics[J]. Insect-plant Interactions, 1992, 4: 167–226. |
| [7] | Perrenoud S. Potassium and plant health[M]. Bern, Switzerland: International Potash Institute, 1990. |
| [8] | Havlickova H, Smetankova M. Effect of potassium and magnesium fertilization on barley preference by the bird cherry-oat aphid (Rhopalosiphum padi) [J]. Rostlinna Vyroba, 1998, 44(8): 379–383. |
| [9] | Myers S W, Gratton C, Wolkowski R P, et al. Effect of soil potassium availability on soybean aphid (Hemiptera: Aphididae) population dynamics and soybean yield [J]. Journal of Economic Entomology, 2005, 98(1): 113–120. DOI:10.1093/jee/98.1.113 |
| [10] | Myers S W, Gratton C. Influence of potassium fertility on soybean aphid, aphis glycines matsumura (Hemiptera: Aphididae), population dynamics at a field and regional scale [J]. Physiological Ecology, 2006, 35(2): 219–227. |
| [11] | Walter A J, Difonzo C D. Soil potassium deficiency affects soybean phloem nitrogen and soybean aphid populations[J]. Physiological Ecology, 2007, 36(1): 26–33. |
| [12] | Zhou S Q, Lou Y R, Tzin V, Jander G. Alteration of plant primary metabolism in response to insect herbivory[J]. Plant Physiology, 2015, 169: 1488–1498. |
| [13] |
闫洪奎, 刘祥, 王会广, 等. 低钾胁迫下耐低钾玉米可溶性蛋白、可溶性糖和钾含量的变化及其关系[J].
玉米科学, 2012, 20(6): 81–84.
Yan H K, Liu X, Wang H G, et al. Changes and relation of soluble protein, soluble sugar and potassium in low-potassium tolerant maize under low-potassium condition[J]. Journal of Maize Sciences, 2012, 20(6): 81–84. |
| [14] |
李田田, 姜文芝, 谷停停, 等. 黄瓜叶片营养物质与抗蚜性的关系研究[J].
山东农业科学, 2016, 48(10): 44–47.
Li T T, Jiang W Z, Gu T T, et al. Relationship between aphid resistance and leaf nutrient content of cucumber[J]. Shandong Agricultural Sciences, 2016, 48(10): 44–47. |
| [15] | Van Emden H F. Studies on the relations of insect and host plant. III. A comparison of the reproudution of Brevicoryne Brassicae and Myzus Presicae (Hemiptera Aphididae) on brussels sprout plants supplied with different rates of nitrogen and potassium [J]. Entomologia Experimentalis et Applicata, 1966, 9(4): 444–460. DOI:10.1111/eea.1966.9.issue-4 |
| [16] | Hu W, Zhao W Q, Yang J S, et al. Relationship between potassium fertilization and nitrogen metabolism in the leaf subtending the cotton (Gossypium hirsutum L.) boll during the boll development stage [J]. Plant Physiology and Biochemistry, 2016, 101: 113–123. DOI:10.1016/j.plaphy.2016.01.019 |
| [17] | Dorschner K W, Ryan J D, Johnson R C. Modification of host nitrogen levels by the greenbug (Homoptera: Aphididae): its role in resistance of winter wheat to aphids[J]. Environmental Entomology, 1987, 16(4): 1007–1011. DOI:10.1093/ee/16.4.1007 |
| [18] | Sandström J, Telang A, Moran N A. Nutritional enhancement of host plants by aphids—A comparison of three aphid species on grasses[J]. Journal of Insect Physiology, 2000, 46(1): 33–40. DOI:10.1016/S0022-1910(99)00098-0 |
| [19] | Koyama Y, Yao I, Akimoto S I. Aphid galls accumulate high concentrations of amino acids: a support for the nutrition hypothesis for gall formation[J]. Entomologia Experimentalis et Applicata, 2004, 113(1): 35–44. DOI:10.1111/eea.2004.113.issue-1 |
| [20] |
娄永根, 程家安. 植物的诱导抗虫性[J].
昆虫学报, 1997, 40(3): 320–330.
Lou Y G, Cheng J A. Induced plant resistance to phytophagous insects[J]. Acta Entomologica Sinica, 1997, 40(3): 320–330. |
| [21] | Mengal K, Kirkby E A, Appel T, et al. Principles of plant nutrition(5th edition) [M]. The Netherlands: Dordrecht, 2001. |
| [22] | Rashid M M, Jahan M, Islam K S. Impact of nitrogen, phosphorus and potassium on Brown[J]. Rice Science, 2016, 23(3): 119–131. DOI:10.1016/j.rsci.2016.04.001 |
| [23] | Marschner H. Mineral nutrition of higher plants (2nd edition) [M]. New York: Academic Press, 1995. |
| [24] |
柳洪鹃, 史春余, 张立明, 等. 钾素对食用型甘薯糖代谢相关酶活性的影响[J].
植物营养与肥料学报, 2012, 18(3): 724–732.
Liu H J, Shi C Y, Zhang L M, et al. Effect of potassium on related enzyme activities in sugar metabolism of edible sweet potato[J]. Plant Nutrition and Fertilizer Science, 2012, 18(3): 724–732. DOI:10.11674/zwyf.2012.11253 |
| [25] |
吴梅梅, 杨丽荣, 张显. 蚜虫侵染对西瓜幼苗生理生化指标的影响[J].
果树学报, 2015, 32(5): 943–949.
Wu M M, Yang L R, Zhang X. Effect of aphid invasion on physiological and biochemical indexes in watermelon seedling stage[J]. Journal of Fruit Science, 2015, 32(5): 943–949. |
| [26] |
王祎, 张月玲, 苏建伟, 等. 氮硅配施对冬小麦生育后期蚜虫密度及抗虫生化物质含量的影响[J].
植物营养与肥料学报, 2013, 19(4): 832–839.
Wang Y, Zhang Y L, Su J W, et al. Effect of nitrogen application combined with silicon on density of Sitobion avenae and contents of biochemical materials of winter wheat at the late growth stage [J]. Journal of Plant Nutrition and Fertilizer, 2013, 19(4): 832–839. DOI:10.11674/zwyf.2013.0408 |
| [27] |
刘旭明, 杨奇华. 棉花抗蚜的生理生化机制及其与棉蚜种群数量消长关系的研究[J].
植物保护学报, 1993, 20(1): 25–29.
Liu X M, Yang Q H. Physiological and biochemical mechanism of cotton aphid resistance and its relationship with the growth and decline of the cotton aphid populations[J]. Acta Phytophylacica Sinica, 1993, 20(1): 25–29. |
| [28] |
朱永峰, 陈明, 刘长仲. 蚜虫为害对五个燕麦品种苗期体内几种物质的影响[J].
植物保护, 2011, 37(2): 55–58, 66.
Zhu Y F, Chen M, Liu C Z. Variations of several substances in the seedlings of five oat varieties infested by aphids[J]. Plant Protection, 2011, 37(2): 55–58, 66. |
| [29] | Karley A J, Ashford D A, Minto L M. The significance of gut sucrase activity for osmoregulation in the pea aphid, Acyrthosiphon pisum[J]. Journal of Insect Physiology, 2005, 51(12): 1313–1319. DOI:10.1016/j.jinsphys.2005.08.001 |
| [30] | Pompon J, Quiring D, Joyer C. A phloem-sap feeder mixes phloem and xylem sap to regulate osmotic potential[J]. Journal of Insect Physiology, 2011, 57(9): 1317–1322. DOI:10.1016/j.jinsphys.2011.06.007 |
| [31] | Mittler T E. Effect of amino acid and sugar concentrations on the food uptake of the aphid Myzus persicae [J]. Entomologia Experimentalis et Applicata, 1967, 10(1): 39–51. DOI:10.1111/eea.1967.10.issue-1 |
| [32] | Gao L L, Jonathan P A, Klingler J P, et al. Involvement of the octadecanoid pathway in bluegreen aphid resistance in Medicago truncatula [J]. Molecular Plant-microbe Interactions, 2007, 20(1): 82–93. DOI:10.1094/MPMI-20-0082 |
 2017, Vol. 23
2017, Vol. 23  doi:
doi: 

