文章信息
- 张倩, 辛军
- 卵巢透明细胞癌PET/CT的影像表现
- PET/CT Manifestations of Ovarian Clear Cell Carcinoma
- 中国医科大学学报, 2018, 47(8): 763-765
- Journal of China Medical University, 2018, 47(8): 763-765
-
文章历史
- 收稿日期:2017-09-04
- 网络出版时间:2018-07-12 11:54
卵巢透明细胞癌(ovarian clear cell carcinoma,OCCC)是一种是起源于苗勒管的卵巢上皮恶性肿瘤,临床上比较少见,发病率仅占卵巢上皮恶性肿瘤的5%~10%[1-2],其恶性程度高,对化疗药物不敏感,治疗后易复发和转移,是卵巢上皮性恶性肿瘤中预后最差的一个亚型。目前关于OCCC的PET/CT表现鲜有报道。本研究回顾性分析了15例OCCC的PET/CT表现,以期提高本病的影像诊断水平。
1 材料与方法 1.1 临床资料搜集我院2011年11月至2017年5月OCCC 15例。年龄范围32~64岁,平均(49.73±10.7)岁,中位年龄为51岁,其中以体检意外发现2例,宫颈癌意外发现2例,腹痛4例,腹部肿块就诊2例,尿频就诊1例。相关肿瘤标志物检查,11例患者血清CA125升高(36~2 309 U/mL)。患者均经手术获得最终病理结果,全部为OCCC。
1.2 检查方法所有患者于术前行PET/CT检查,18F-FDG显像剂的制备采用医用回旋加速器GE MINItraceⅡ及合成器GE Tracelab FDG。检查前患者空腹6 h以上,控制血糖在7.0 mmol/L以内。静脉注射18F-FDG 8~12 mCi后平卧休息40~60 min后采集图像。使用GE Discovery PET/CT Elite进行PET/CT扫描。扫描范围:颅顶至股骨中段。PET使用3D+飞行时间技术(TOF) +点扩展函数(SharpIR)采集及重建技术,矩阵:192×192,2 min/床位。CT扫描参数:全身螺旋扫描,120 kV,自动曝光控制技术(automatic exposure control,AEC) (30~210 mA,噪声指数25),层厚3.25 mm。经CT衰减校正、OSEM迭代法重建,分别得到全身或局部的冠状、矢状以及横断位的CT、PET以及PET/CT融合图像。
1.3 图像分析由2位或2位以上PET/CT中心医师复习患者临床资料,采用盲法共同阅片,结合PET代谢图像从CT上观察病灶部位、大小、形态、密度与周围组织的关系,在PET图像上自动勾画肿瘤FDG高代谢感兴趣区,测量SUVmax值,观察肿瘤FDG摄取情况,FDG代谢水平与肝脏相比较,高于、等于及低于肝脏代谢水平分别为FDG高度、中度及低度摄取,并分析主病灶SUVmax与临床分期相关性。
1.4 统计学分析采用SPSS 17.0软件进行统计学分析,符合正态分布的计量资料用x±s表示,不同临床分期肿瘤SUVmax均值比较采用单因素方差分析,P < 0.05为差异有统计学意义。
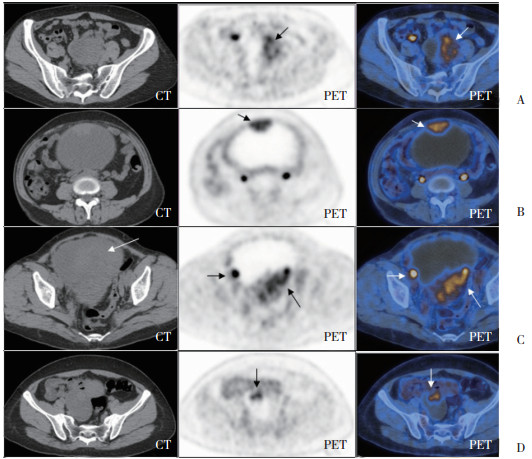
2 结果PET/CT表现:CT显示15例均为单侧附件发生(左7例、右8例);14例表现为囊实混杂性肿块,囊性成分为主,另有实性肿物1例。肿块最大径3~17 cm,平均(8.70±4.36) cm;肿块形态规则呈类圆形8例,分叶者7例;囊性成分呈单囊或多囊,有5例囊内见分隔,实性成分表现为囊内不规则乳头状结节或团块样肿块向腔内突出,平均CT值(38.8±6.86) HU。PET图像可见14例囊实混合型肿块呈不均匀高代谢区与低或无代谢区混杂影像,分别对应实性及囊性成分(图 1)。另有1例实性肿块,代谢均匀一致。SUVmax值为2.96~32.85,平均SUVmax值为9.26±7.57,中位SUVmax值为7.11;轻中度摄取2例,SUVmax值分别为2.96和3.02,其余13例均呈不同程度FDG高摄取,平均SUVmax值为10.22±7.70,中位SUVmax值为7.51;3例可见腹膜腔内多发高代谢结节,怀疑转移,术后病理均证实为转移灶。同时伴有子宫肌瘤7例,伴有子宫内膜异位6例,另有伴发宫颈癌2例,子宫内膜癌1例。根据国际妇产联盟FIGO分期Ⅰ期8例,平均SUVmax值7.49±4.89,Ⅱ期3例,平均SUVmax值为6.66±2.47,Ⅲ期4例,平均SUVmax值14.77±12.33,主病灶的代谢程度与临床分期无明显相关性(F = 1.574,P > 0.05)。
|
| A,女,55岁,CT左侧附件区见囊实性肿块,实性部分FDG代谢不均匀增高,周边为著(箭头所示),囊性成分代谢稀疏缺损;B,C,女,52岁,CT腹盆腔发现巨大囊实性包块,囊性为主,PETCT融合图像显示内见软组织实性成分呈不均匀高代谢区(箭头所示),囊性成分代谢缺损,内见片状稍高密度出血灶(CT图中白箭头所示);D,女,50岁,CT平扫右侧附件区囊实性包块,PETCT融合图像显示内见乳头状高代谢壁结节(箭头所示),囊性部分呈代谢稀疏缺损区. 图 1 OCCC患者18F-FDG PET/CT显像图 |
3 讨论
OCCC发生率低,是卵巢上皮恶性肿瘤中预后最差和致死率最高的妇科恶性肿瘤[3],多发生于围绝经期妇女,单侧多见;OCCC有早期发病的趋势,Ⅰ期及Ⅱ期患者占60%以上[4-5]。本组病例年龄范围32~64岁,50岁以上占60% (9例),与报道基本符合。本研究12例为早期,这可能与OCCC细胞本身的倍增时间长,进展时间缓慢有关,患者长时间停留在早期阶段[6-7]。OCCC的临床表现多不特异,有报道称腹痛为最常见症状[8]。OCCC与子宫内膜异位症关系紧密[9-10],这也可能是以腹痛为常见症状的原因。本组病例中有6例(40%)病理证实存在子宫内膜异位症。在子宫内异症的恶变病例中有90.0%左右来源于上皮,因此可以认为子宫内膜异位症也被看成是OCCC、卵巢子宫内膜样癌的高危因素[9-10]。73.3% (11/15)的CA125高于正常值(36~2 309 U/mL),可在一定程度上提示卵巢上皮来源恶性肿瘤倾向。
OCCC在就诊时往往发现盆腔肿块较大[8, 11],本组病例中肿瘤最长径≥10 cm有5例,最大径17 cm。肿块以囊实混合型为多见,本组14例(93.3%)为囊实性,仅1例(6.7%)为实性,与文献[8]报道相仿。囊性部分的CT值相对较高,常常提示合并出血,子宫内膜异位的存在。PET影像13例肿块呈不均匀高代谢区,2例为不均匀中轻度代谢区,均表现为不同代谢程度的壁结节或肿块,对应于病理所见的肿瘤实质成分,囊性成分或坏死区FDG代谢摄取缺损。笔者认为,由于肿瘤的异质性及肿瘤组织常常伴发坏死,可能致代谢水平欠均匀。国外KONISHI等[12]报道了27例OCCC的FDG代谢情况,SUVmax范围在1.53~12.17,中位SUVmax值为4.9,低于本组病例的7.11,笔者认为,原因可能在于OCCC在临床上仍然是少见的肿瘤,样本量较少,FDG代谢情况统计存在一定的偏倚,还有可能部分病例合并子宫内膜异位症,肿瘤SUVmax欠精确,有待进一步收集病例,加大样本量细致研究。
| [1] |
ANGLESIO MS, CAREY MS, KÖBEL M, et al. Clear cell carcinoma of the ovary:a report from the first ovarian clear cell symposium, June 24th, 2010[J]. Gynecol Oncol, 2011, 121(2): 407-415. DOI:10.1016/j.ygyno.2011.01.005 |
| [2] |
刘国艳, 袁碧波, 糜若然. 卵巢透明细胞癌诊治进展[J]. 国际妇产科学杂志, 2012, 39(4): 364-367, 372. |
| [3] |
SIEGEL R, NAISHADHAM D, JEMAL A. Cancer statistics, 2012[J]. CA Cancer J Clin, 2012, 62(1): 10-29. DOI:10.3322/caac.20138 |
| [4] |
SUGITA S, MORISHITA Y, KANO J, et al. IGFBP-1 is expressed specifically in ovarian clear cell adenocarcinoma[J]. Histopathology, 2011, 8(5): 729-738. DOI:10.1111/j.1365-2559.2011.03817.x |
| [5] |
WIEGAND KC, SHAH SP, AL-AGHA OM, et al. ARID1A mutations in endometriosis-associated ovarian carcinomas[J]. N Engl J Med, 2010, 363(16): 1532-1543. DOI:10.1056/NEJMoa1008433 |
| [6] |
KURMAN RJ, SHIH IEM. Molecular pathogenesis and extra ovarian origin of epithelial ovarian cancer-shifting the paradigm[J]. Human Patho, 2011, 42(7): 918-931. DOI:10.1016/j.humpath.2011.03.003 |
| [7] |
张君, 王言奎. 血清CA125在卵巢癌诊断及预测分期中的应用价值[J]. 齐鲁医学杂志, 2012, 27(6): 479-481, 484. |
| [8] |
张家云, 江魁明. 卵巢透明细胞癌的CT表现[J]. 中国医学影像技术, 2010, 26(10): 1943-1945. |
| [9] |
热娜, 季菲, 艾星子, 等. 卵巢子宫内膜异位症与卵巢恶性肿瘤的相关性分析[J]. 中国妇产科临床杂志, 2011, 12(5): 331-334. |
| [10] |
宋建平. 子宫内膜异位症与卵巢癌相关性临床分析[J]. 现代肿瘤医学, 2015, 23(10): 1432-1434. DOI:10.3969/j.issn.1672-4992.2015.10.32 |
| [11] |
UEKURI C, SHIGETOMI H, ONO S, et al. Toward an understanding of the pathophysiology of clear cell carcinoma of the ovary[J]. Oncol Lett, 2013, 6(5): 1163-1173. DOI:10.3892/ol.2013.1550 |
| [12] |
KONISHI H, TAKEHARA K, KOJIMA A, et al. Maximum standardized uptake value of fluorodeoxyglucose positron emission tomography is a prognostic factor in ovarian clear cell adenocarcinoma[J]. Int J Gynecol Cancer, 2014, 24(7): 1190-1194. DOI:10.1097/IGC.0000000000000180 |
 2018, Vol. 47
2018, Vol. 47