文章信息
- 裴祎, 张晓晶, 郑珂, 王巍, 邱恩铎, 李盛龙
- PEI Yi, ZHANG Xiaojing, ZHENG Ke, WANG Wei, QIU Enduo, LI Shenglong
- miR-212抑制骨肉瘤细胞恶性生物学行为的实验研究
- Inhibitory Effect of miR-212 on the Malignant Biological Behavior of Osteosarcoma Cells
- 中国医科大学学报, 2018, 47(10): 924-928
- Journal of China Medical University, 2018, 47(10): 924-928
-
文章历史
- 收稿日期:2017-08-06
- 网络出版时间:2018-09-27 10:50
骨肉瘤是起源于间叶组织的原发性恶性肿瘤,恶性程度较高,早期就发生肺转移,多在青少年发病,严重危害着青少年的健康,亟待寻找有效方式对其进行预测和治疗[1-3]。锌指蛋白133(zinc finger protein-133,ZNF133)是一种具有逆转录抑制活性的KRAB型C2H2锌指蛋白,在真核生物的转录调控中发挥重要作用。它可以参与调节胚胎发育、细胞周期、细胞凋亡、细胞侵袭转移、细胞分化等多种生物学功能,与肿瘤的发生发展密切相关。有研究[4-5]指出,在慢性粒细胞白血病和神经母细胞瘤中ZNF133均处于高表达的状态;在骨肉瘤中其表达较高,可能参与骨肉瘤的发生发展。
微小RNA(microRNA,miRNA)是长度为18~25个核苷酸的内源性非编码小分子RNA,在进化上高度保守,具有多种生物学功能,对生长发育等生理功能具有调节作用,对各种病理过程也有重要影响。miRNA很适合作为肿瘤标记物,也可以作为肿瘤治疗的潜在靶点[6-9]。本研究通过体外实验探讨miR-212通过调节ZNF133蛋白对骨肉瘤细胞增殖和迁移能力的影响。
1 材料与方法 1.1 主要试剂MG63细胞,实验室冻存,使用DMEM培养基(美国Gibco公司)加10%胎牛血清(天津灏洋公司)在37 ℃细胞培养箱内于5% CO2环境下培养至对数生长期。ZNF133、CDK4、CDK6、MMP2、GAPDH抗体及相关二抗购自美国Santa Cruz公司。ZNF133 WT、ZNF133MUT(突变与miR-212结合位点的序列)引物均合成于上海生工公司。荧光素酶报告基因试剂盒购自上海英拜生物。miR-212 mimic/control、miR-212 inhibitor/control及miR-212 antisense(AS)购于广州锐博生物公司。
1.2 方法 1.2.1 荧光素酶报告基因实验分别将miRNA拟似物等及ZNF133 WT/MUT共同转染到处于对数生长期的MG63细胞中,转染24 h后使用双荧光素酶报告实验测得荧光值并计算统计结果。
1.2.2 MTT实验分别在MG63细胞中转染不同miRNA,转染24 h后将细胞消化使用培养基混匀,以1×104/孔接种于96孔培养板中。分别于0、12、24、36、48 h通过MTT检测细胞增殖情况。具体检测步骤为不同时间点分别加入10 μL MTT(5 mg/mL),置于孵箱内培养4 h后使用1 mL注射器吸去上清,加入DMSO 200 μL溶解结晶,溶解后在490 nm处记录吸光值。
1.2.3 Transwell实验MG63细胞转染不同处理因素24 h后,将无血清培养基中的MG63细胞以1×105/孔接种于Transwell小室上室中,下室添加600 μL含10 %胎牛血清的培养基。培养18 h后,95%乙醇固定,0.4 %台盼蓝染色,棉签擦去小室内细胞。200倍显微镜下观察。
1.2.4 Western blotting检测MG63细胞转染24 h后,使用RIPA裂解细胞提取蛋白。取等量蛋白在10 %的SDS-PAGE胶内进行电泳(110~130 V)、电泳结束后4 ℃下100 V转膜1 h,洗膜3次,5 %脱脂奶粉室温封闭1 h,对应一抗4 ℃孵育过夜,洗膜3次,二抗室温1 h,ECL发光仪发光。
1.3 统计学分析采用SPSS 17.0软件进行统计学分析,组间比较采用完全随机设计t检验,P < 0.05为差异有统计学意义。
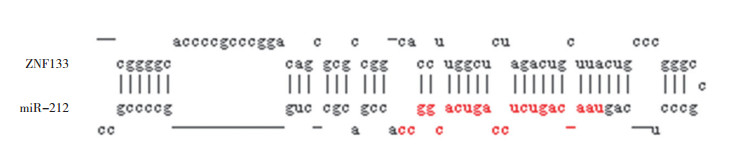
2 结果 2.1 miR-212和ZNF133之间的关系ZNF133可以促进骨肉瘤进程,通过生物学软件(MIRDB)预测寻找到miR-212可能打靶ZNF133,如图 1所示,miR-212与ZNF133的3’UTR区域具有结合位点。
|
| 图 1 miR-212与ZNF133的结合位点预测 Fig.1 Prediction of binding sites between miR-212 and ZNF133 |
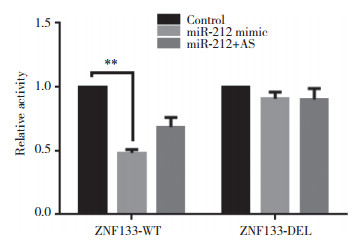
为了进一步探索miR-212是否可以直接调控ZNF133表达,本研究进行了荧光素酶报告基因实验,结果显示,当miR-212与ZNF133共同转染时,ZNF133的活性显著下调,但是转入miR-212反义链后此作用消失,而且当miR-212与ZNF133 MUT共同转染时,不影响ZNF133的活性,这说明miR-212可以直接作用于ZNF133,见图 2。
|
| ** P < 0.05 vs control group. 图 2 miR-212与ZNF133的关系 Fig.2 The relationship between miR-212 and ZNF133 |
2.2 miR-212对MG63细胞增殖的影响
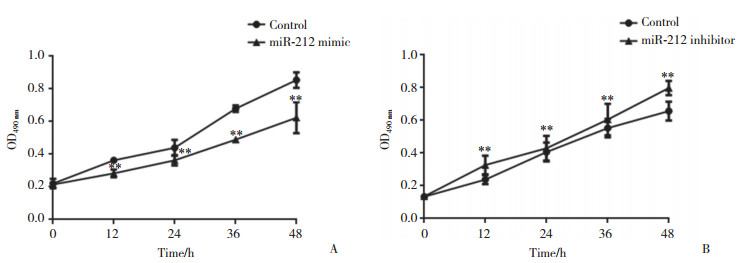
ZNF133可以调节骨肉瘤细胞增殖,分别将miR-212 mimic和control转染到MG63细胞后,得到miR-212过表达的细胞系。通过MTT的方法检测细胞增殖,结果显示,miR-212对MG63细胞的增殖具有一定抑制作用,见图 3A。分别将miR-212 inhibitor和对照转染到MG63细胞后,得到miR-212低表达的细胞系。MTT方法检测细胞增殖结果显示,miR-212对MG63细胞的增殖具有显著的促进作用,见图 3B。
|
| A, the proliferation of MG63 was inhibited by miR-212, ** P < 0.05 vs control group; B, the proliferation of MG63 was promoted when miR-212 was inhibited. ** P < 0.05 vs control group. 图 3 miR-212对MG63细胞增殖的影响 Fig.3 The proliferation of cells treated with miR-212 |
2.3 miR-212对骨肉瘤细胞迁移能力的调节
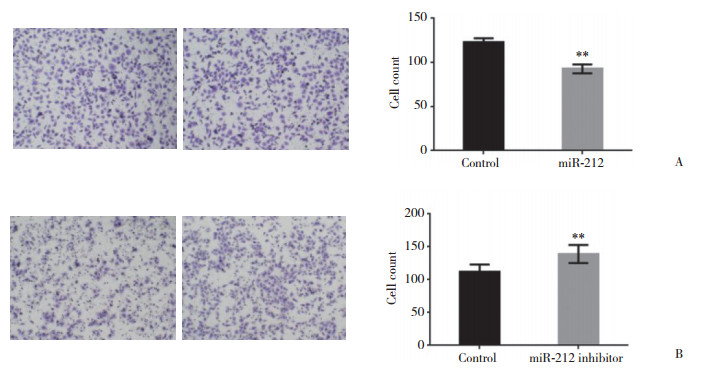
在MG63细胞中过表达了miR-212,Transwell实验结果显示,miR-212过表达可以抑制MG63细胞迁移;利用MG63细胞构建了miR-212低表达的细胞系,Transwell实验结果显示,miR-212表达下调可以促进MG63细胞迁移,见图 4。
|
| A, the migration of MG63was inhibited by miR-212;B, the migration of MG63 was promoted when miR-212 was inhibited.** P < 0.05 vs control group. 图 4 miR-212对MG63迁移能力的影响×400 Fig.4 The effect of miR-212 on the migration of MG63 cells ×400 |
2.4 miR-212过表达对ZNF133、CDK4/6和MMP蛋白的作用
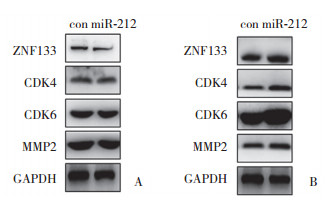
ZNF133可以通过调节蛋白来调节细胞的生长与侵袭转移。本研究构建了miR-212过表达的MG63细胞系,结果发现miR-212对ZNF133、CDK4/6和MMP2蛋白均有一定的抑制作用,见图 5A。本研究构建了miR-212稳定低表达的MG63细胞系,结果发现miR-212表达下调后ZNF133、CDK4/6和MMP2蛋白表达均上调,见图 5B。
|
| A, the expression of the proteins was inhibited by miR-212;B, the expression of the proteins was promoted when miR-212 was inhibited. 图 5 miR-212对ZNF133、CDK4/6和MMP蛋白的作用 Fig.5 The effect of miR-212 on the ZNF133, CDK4/6 and MMP2 expressions |
3 讨论
近年来,随着新辅助化疗、保肢手术的开展,骨肉瘤5年生存率提高到60%~70%,但仍是一种死亡率和致残率极高的恶性肿瘤,严重威胁着青少年的身心健康[10]。国内外很多研究[10]指出,多种蛋白与骨肉瘤的进程密切相关。ZNF133可以促进慢性粒细胞性白血病的进程,也在神经母细胞瘤中高度扩增[11]。有研究[5]指出,在INF-γ的作用下,ZNF133可以过表达,进而激活MAPK等信号通路,促进肿瘤进程。有研究[11-12]指出在骨肉瘤中ZNF133表达较高,可以通过影响细胞周期和细胞的侵袭转移来促进骨肉瘤进展。
研究[13-14]指出miR-212可以抑制多种肿瘤的发生发展。食管癌中miR-212的表达较低,当上调细胞系中miR-212的含量,食管癌细胞的生长和迁移功能受到抑制;miR-212过表达可以显著抑制肺癌细胞的增殖,它与肺癌中组蛋白的修饰相关,并且miR-212的含量与肺癌的预后密切相关;miR-212也被证明可以通过抑制过度激活的信号通路来抑制肝细胞癌的生长;miR-212可以通过影响H3K4的去甲基化来调节视网膜母细胞瘤的增殖和衰老;同样也有报道[13-15]指出miR-212在胃癌中表达下调,可以通过抑制DNA的甲基化来抑制胃癌的发展。
因此,ZNF133和miR-212在肿瘤中均发挥重要作用,而且ZNF133也可以调节骨肉瘤的发生发展。本研究通过生物学软件预测发现miR-212与ZNF133蛋白的3’UTR区域有一定的结合位点,进一步荧光素酶报告基因实验证实,miR-212可以抑制ZNF133蛋白表达。MTT实验和Transwell实验证实miR-212过表达可以抑制骨肉瘤细胞的增殖和侵袭转移,当miR-212受到抑制后,MG63细胞的增殖与迁移受到促进。蛋白检测发现miR-212可以通过调节ZNF133蛋白,进一步影响细胞周期相关蛋白CDK4和CDK6的表达,进而起到抑制MG63细胞增殖作用。同时也发现miR-212可以通过影响ZNF133蛋白进而调节细胞迁移相关蛋白MMP2的表达,起到抑制MG63细胞侵袭转移的作用。
综上所述,miR-212可以通过抑制ZNF133蛋白进而调节细胞增殖和侵袭相关蛋白来抑制骨肉瘤细胞的增殖和迁移,为骨肉瘤的治疗提供了新的理论基础。
| [1] |
YUAN Z, MO H, MO L, et al. Suppressive effect of microRNA-138 on the proliferation and invasion of osteosarcoma cells via targeting SIRT1[J]. Exp Ther Med, 2017, 13(6): 3417-3423. DOI:10.3892/etm.2017.4426 |
| [2] |
HE Y, YU B. MicroRNA-93 promotes cell proliferation by directly targeting P21 in osteosarcoma cells[J]. Exp Ther Med, 2017, 13(5): 2003-2011. DOI:10.3892/etm.2017.4204 |
| [3] |
HEISHIMA K, ICHIKAWA Y, YOSHIDA K, et al. Circulating microRNA-214 and -126 as potential biomarkers for canine neoplastic disease[J]. Sci Rep, 2017, 7(1): 2301. DOI:10.1038/s41598-017-02607-1 |
| [4] |
SHEN AL, MORAN SA, GLOVER EA, et al. Association of a chromosomal rearrangement event with mouse posterior polymorphous corneal dystrophy and alterations in Csrp2bp, Dzank1, and Ovol2 gene expression[J]. PLoS One, 2016, 11(6): e0157577. DOI:10.1371/journal.pone.0157577 |
| [5] |
LI Y, LIANG Q, WEN YQ, et al. Comparative proteomics analysis of human osteosarcomas and benign tumor of bone[J]. Cancer Genet Cytogenet, 2010, 198(2): 97-106. DOI:10.1016/j.cancergencyto.2010.01.003 |
| [6] |
ZHAO D, CHEN Y, CHEN S, et al. MiR-19a regulates the cell growth and apoptosis of osteosarcoma stem cells by targeting PTEN[J]. Tumour Biol, 2017, 39(5): 1010428317705341. DOI:10.1177/1010428317705341 |
| [7] |
GAI P, SUN H, WANG G, et al. miR-22 promotes apoptosis of osteosarcoma cells via inducing cell cycle arrest[J]. Oncol Lett, 2017, 13(4): 2354-2358. DOI:10.3892/ol.2017.5674 |
| [8] |
LI CH, YU TB, QIU HW, et al. miR-150 is downregulated in osteosarcoma and suppresses cell proliferation, migration and invasion by targeting ROCK1[J]. Oncol Lett, 2017, 13(4): 2191-2197. DOI:10.3892/ol.2017.5709 |
| [9] |
SONG L, DUAN P, GAN Y, et al. MicroRNA-340-5p modulates cisplatin resistance by targeting LPAATβ in osteosarcoma[J]. Braz J Med Biol Res, 2017, 50(5): e6359. DOI:10.1590/1414-431X20176359 |
| [10] |
CAO Y, WU T, LI D, et al. MicroRNA-336 directly targets Sox-2 in osteosarcoma to inhibit tumorigenesis[J]. Mol Med Rep, 2017, 15(6): 4217-4224. DOI:10.3892/mmr.2017.6493 |
| [11] |
NIMMANON T, ZILIOTTO S, MORRIS S, et al. Phosphorylation of zinc channel ZIP7 drives MAPK, PI3K and mTOR growth and proliferation signalling[J]. Metallomics, 2017, 9(5): 471-481. DOI:10.1039/c6mt00286b |
| [12] |
TSUJI T, KUROKAWA Y, CHICHE J, et al. Dissecting the process of activation of cancer-promoting zinc-requiring ectoenzymes by zinc metalation mediated by ZNT transporters[J]. J Biol Chem, 2017, 292(6): 2159-2173. DOI:10.1074/jbc.M116.763946 |
| [13] |
PRONINA IV, LOGINOV VI, BURDENNYY AM, et al. DNA methylation contributes to deregulation of 12 cancer-associated microRNAs and breast cancer progression[J]. Gene, 2017, 604: 1-8. DOI:10.1016/j.gene.2016.12.018 |
| [14] |
WU Z, ZHOU L, DING G, et al. Overexpressions of miR-212 are associated with poor prognosis of patients with pancreatic ductal adenocarcinoma[J]. Cancer Biomark, 2017, 18(1): 35-39. DOI:10.3233/CBM-160671 |
| [15] |
FU W, TAO T, QI M, et al. MicroRNA-132/212 upregulation inhibits TGF-β -mediated epithelial-mesenchymal transition of prostate cancer cells by targeting SOX4[J]. Prostate, 2016, 76(16): 1560-1570. DOI:10.1002/pros.23241 |
 2018, Vol. 47
2018, Vol. 47