| P204从高铝粉煤灰硫酸浸液中萃取除铁 |
2. 东北大学多金属共生矿生态化冶金教育部重点实验室,沈阳 110819
2. Key Laboratory for Ecological Metallurgy of Multimetallic Mineral, Ministry of Education, Northeastern University, Shenyang 110819, China
粉煤灰作为煤炭燃烧后留下的固体废弃物,如何处理一直以来受到广泛关注。由于地质原因,我国一些地区产出的煤炭含有大量的Al、Si以及一些稀土元素,燃烧后可形成氧化铝含量为38%~50%的高铝粉煤灰。作为最大的发展中国家,煤炭一直以来是我国主要能源之一,因此我国粉煤灰的年排放量和堆存量巨大,对生态环境造成了严重危害[1]。对于可视作潜在提铝资源的高铝粉煤灰,碱法提铝和酸法提铝是目前主要的提取氧化铝的方法[2-4]。由于碱法提铝不仅对粉煤灰原料的要求比较高,且在生产过程中需要消耗大量的能源并对环境造成污染,不利于当前的可持续发展战略。相反,酸法提铝由于对原料要求比较低、过程简单、消耗能源少等优点近些年受到越来越多的关注。
酸法处理粉煤灰主要是以粉煤灰为原料,采用无机酸(盐酸、硫酸)与粉煤灰反应,得到含有铝、铁为主要有价金属元素的混合溶液[5-7]。若直接将该混合溶液加工制造铝产品,会使得产品中夹杂大量的杂质铁,而铁的掺入会严重影响铝产品的质量,限制铝产品在高端领域的应用。由于铁的存在大大限制了该工艺中铝的回收,所以从酸浸液中除铁是制得优质铝产品前必不可少的一步。
从粉煤灰酸浸液中除铁近年来主要通过沉淀法、离子交换树脂法以及溶剂萃取法3种渠道。沉淀法[8]通常应用于对除铁效率要求不高的分离提纯工艺中,一般除铁率为60%,并不能达到深度除铁的效果。此外,在沉淀过程中,其他有价金属会不可避免地与铁发生共沉淀,从而造成损失。离子交换树脂[9-10]具有高效性和高选择性,但由于传质速率比较低以及载铁能力有限,所以只有在铁含量比较低的情况下才具有经济可行性。溶剂萃取法[11-12]除铁具有选择性和萃取效率高、负载能力大、污染少、能耗低等优点,一直以来被广泛关注。其中,酸性磷酸酯类、中性萃取剂及胺类萃取剂等有机试剂在溶剂萃取法除铁中表现效果比较优异。在酸性磷酸酯类萃取剂中,WANG等采用1.5 mol/L的P507萃取粉煤灰硫酸酸浸液中的Fe3+,Fe3+的萃取率可达到97.60%[13]。磷酸三丁酯(TBP)作为中性磷类萃取剂中的代表,其在氯化物溶液中有着良好的萃取效果,YI等用50%TBP+20%2-octanol+30%煤油萃取体系可以有效萃取含Ni-Co-Fe盐酸溶液中的Fe[14]。胺类萃取剂的萃取能力与其结构相关[15],而伯胺作为胺类萃取剂中萃取效果最优的有机试剂,LI等用伯胺N-1923作为萃取剂萃取工业硫酸铝溶液(C(Fe3+)=2.3 g/L,C(Al3+)=89.4 g/L)中的铁,在一定条件下,铁的萃取率可达到99%[16]。
P204作为酸性磷酸酯类中最具代表性的萃取试剂,在对Fe3+的萃取过程中表现非常突出,但对萃取后有机相中Fe3+反萃时表现效果不佳。由于关于P204在硫酸铝溶液中萃取除铁的研究文献非常少而且比较久远,本文拟通过配置之前研究的粉煤灰硫酸浸液(C(Fe3+)=5.1 g/L,C(Al3+)=37.1 g/L)确定出较优工艺条件。在对载铁有机相反萃研究中,选用H2SO4和HCl作为反萃剂考察其在不同条件下对载铁有机相反萃效果的影响。
1 实验方法 1.1 试剂萃取剂:二(2-乙基己基)磷酸酯(P204),分子式: C16H35O4P,化学纯;
稀释剂:260#溶剂油,化学纯;
其他试剂均为分析纯,在试验过程中没有任何其他处理。
1.2 实验步骤将配制好的(C(Fe3+)=5.1 g/L,C(Al3+)=37.1 g/L)硫酸铁、硫酸铝混合溶液置于数显集热式磁力搅拌器中,加入一定量P204和260#溶剂油,升高温度搅拌一定时间后倒入分液漏斗中,静置约30 s待油水相完全分层,取下层水相萃余液,用EDTA滴定法滴定测出水相中的Fe3+,Al3+含量,通过差减法计算得出有机相中Fe3+和Al3+含量,研究不同P204体积分数、萃取温度、初始溶液pH、反应时间及相比(有机相体积V(O)和水相体积V(A)之比)V(O): V(A)对Fe3+、Al3+萃取率的影响。
1.3 萃取原理P204作为酸性磷酸酯类萃取试剂,在萃取金属离子时根据金属离子结构和溶液pH不同,有着不同的选择性和萃取能力。从溶液中萃取金属离子时,pH由低到高的萃取顺序为Fe3+ > Zn2+ > Ca2+ > Al3+ > Cu2+ > Mn2+ > Co2+ > Ni2+ > Mg2+[17]。
在酸性条件下,P204一般以二聚体的形式参与反应,其萃取Fe3+的反应式为[18]:
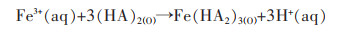
|
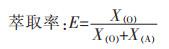
|
(1) |
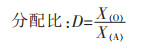
|
(2) |
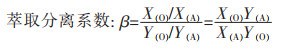
|
(3) |
式(1)-式(3)中:X(O)、X(A)和Y(O)、Y(A)分别表示X、Y在有机相和水相中的含量。分配比D的大小代表着物质X在萃取过程中,从溶液中被萃取到有机相的难易程度,D越大,表示物质X越容易进入有机相。β是衡量物质X、Y分离难易时的重要数据参数,若β远远大于1或远小于1,说明两种物质越容易分离,而β=1则说明两者不能分离。
2 萃取结果与结论 2.1 P204体积分数对萃取效果的影响为了探究P204体积分数对Fe3+、Al3+分离效果的影响,取萃取温度60 ℃,水相pH=0.4,反应时间30 min,相比V(O): V(A)=1:1,萃取结果如图 1和图 2所示。
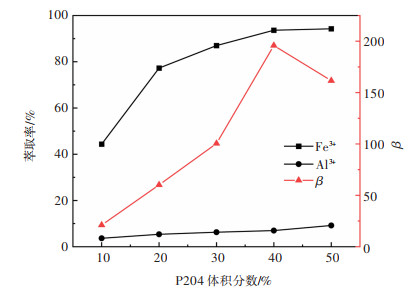 |
| 图 1 P204体积分数对萃取效果的影响 Fig. 1 Effect of volume fraction of P204 on extraction performance |
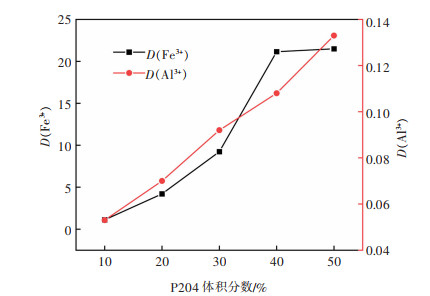 |
| 图 2 P204体积分数对分配比的影响 Fig. 2 Effect of the volume fraction of P204 on the distribution ratio |
由图 1可知,随着P204体积分数提高,Fe3+萃取率的增加趋势逐渐变缓,40%时已达93.00%。继续提高P204的体积分数,萃取率变化不大,而且体系将会变得黏稠,不利于分子扩散,进而影响萃取反应的反应速率。同时,从β随着P204体积分数变化趋势来看,β随着P204体积分数升高不断增加,在P204体积分数为40%时达到195.0,之后开始减小。说明Fe和Al在P204体积分数为40%时最容易分离。另由图 2可以看出,铁的分配比D(Fe3+)随P204体积分数升高不断增大,且在P204体积分数为40%时达到最大21.1。因此,随P204体积分数升高,Fe3+更容易进入有机相。
2.2 萃取温度对萃取效果的影响在P204体积分数40%,相比V(O): V(A)=1:1,水相pH=0.4,反应时间30 min的条件下,不同温度对萃取效果的影响如图 3、图 4所示。
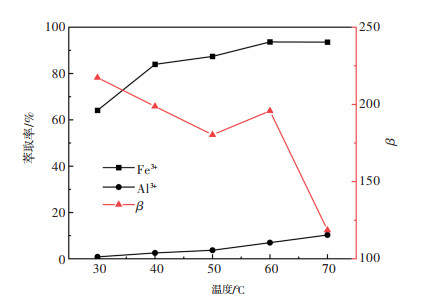 |
| 图 3 温度对萃取效果的影响 Fig. 3 Effect of temperature on extraction performance |
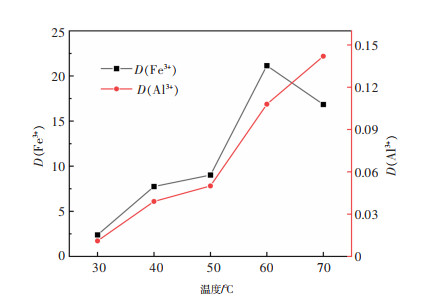 |
| 图 4 温度对Fe3+、Al3+分配比的影响 Fig. 4 Effect of temperature on the distribution ratio |
由图 3可以看出,Al3+和Fe3+的萃取率在温度为30~60 ℃时增加明显,在60 ℃时Fe3+萃取率达最高。随着温度继续升高,Fe3+萃取率基本不变,而Al3+萃取率持续增加。若继续升高温度,在萃取过程更多Al3+随着Fe3+一起共萃到有机相中,造成Al3+损失。
由图 4所示,Fe3+的分配比D(Fe3+)随着萃取温度的升高不断增加,在60 ℃时达到最大21.1,之后开始减小。说明Fe3+在萃取温度为60 ℃时更容易从水相被萃取到有机相。在温度为60 ℃时,Fe和Al的分离系数β为195,可以达到良好的分离效果。
2.3 反应时间对萃取效果的影响在P204体积分数为40%,相比V(O): V(A)=1:1,水相pH=0.4,温度为60 ℃的条件下,考察不同反应时间对萃取效果的影响如图 5及图 6所示。
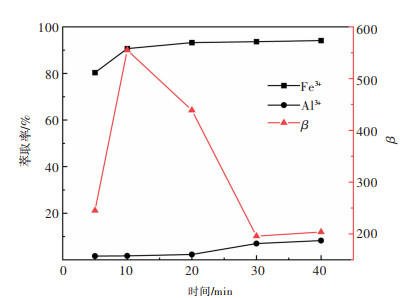 |
| 图 5 时间对萃取效果的影响 Fig. 5 Effect of time on extraction performance |
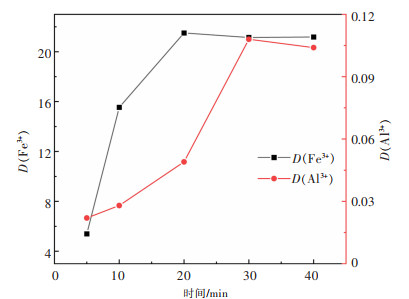 |
| 图 6 时间对Fe3+、Al3+分配比的影响 Fig. 6 Effect of time on distribution ratio |
在萃取过程中,反应时间越短意味着传质速率越快。由图 5可以看出,5 min时Fe3+的萃取率已达80.34%,说明P204萃取Fe3+反应在初始时传质速率很快。随着反应时间延长,Fe3+萃取率增加趋势减缓,20 min后,Fe3+的萃取率基本不再变化,而Al3+的萃取率在20 min后开始出现缓慢增加趋势。
由图 6所示,D(Fe3+)随着反应时间延长逐渐增加,20 min时,D(Fe3+)达到最大,随着反应时间继续增加,D(Fe3+)基本趋于稳定。在20 min时β达438,虽然小于10 min时的分离系数,但此时不仅有更多Fe3+被萃取进入有机相,而且共萃进有机相的Al3+较30 min也明显减少,故后续萃取反应的反应时间选为20 min。
2.4 水相pH对萃取效果的影响在P204体积分数为40%,温度为60 ℃,相比V(O): V(A)=1:1,反应时间为20 min的条件下,研究水相pH对萃取效果的影响如图 7、图 8所示。
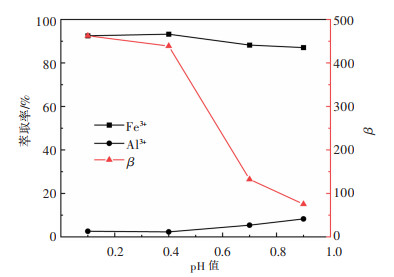 |
| 图 7 pH对萃取效果的影响 Fig. 7 Effect of pH on extraction performance |
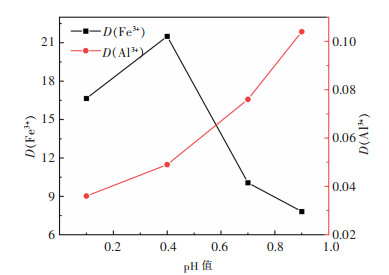 |
| 图 8 pH对Fe3+、Al3+分配比的影响 Fig. 8 Effect of pH on distribution ratio |
P204在不同pH下对有价金属元素萃取顺序不同。由图 7可知,当初始水相的pH值从0.1升高到0.4,Fe3+、Al3+萃取率变化并不明显,随着pH继续升高,P204对金属离子的萃取选择性开始发生变化,Fe3+的萃取率逐渐下降,Al3+的萃取率开始缓慢增加。
根据图 8所示,D(Fe3+)随着pH增加先增大后减小,在pH值为0.4时达到最大,说明此时Fe3+最容易从水相被萃取到有机相。而D(Al3+)随着pH增加一直在增大,意味着pH越大,Al3+越容易进入有机相,即造成水相中Al3+损失。在萃取过程中,在保证更多Fe3+被萃取到有机相的同时,减少共萃进有机相的Al3+,达到更理想分离效果,选择pH=0.4为后续萃取实验水相初始pH,此时Fe、Al的分离系数β值为438。
2.5 相比V(O): V(A)对萃取效果的影响在P204体积分数为40%,温度为60 ℃,pH值为0.4,反应时间为20 min的条件下,考察相比对萃取效果的影响如图 9、图 10所示。
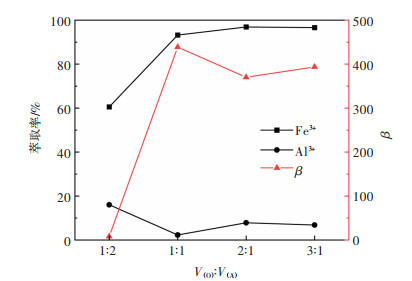 |
| 图 9 相比V(O): V(A)对萃取效果的影响 Fig. 9 Effect of the phase ratio V(O): V(A) on the extraction performance |
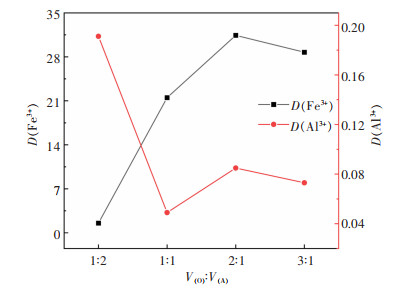 |
| 图 10 相比V(O): V(A)对Fe3+、Al3+分配比的影响 Fig. 10 Effect of the phase ratio V(O): V(A) on the distribution ratio |
由图 9所示,Fe3+的萃取率在初始时随着相比V(O): V(A)提高呈线性增加。当相比V(O): V(A)=1:1时,Fe3+的萃取率达到93.24%,继续提高相比,Fe3+的萃取率变化不大,Al3+的萃取率进一步提高。根据图 10可以看出,V(O): V(A)=1:1时,Al3+的分配比最小,说明此时Al3+在萃取过程中难以从水相进入有机相。若进一步提高相比,不仅会导致水相中铝额外损失,还会增加后续有机相回收难度,造成有机相损失,因此选择有机相和水相体积比V(O): V(A)=1:1作为单级萃取实验相比。
为考察试验效果的重现性,在较优反应条件P204体积分数为40%,萃取温度60 ℃,初始水相pH=0.4,相比V(O): V(A)=1:1,反应时间20 min下重复3组试验,Fe、Al的萃取率如图 11所示。试验结果显示试验数据基本保持稳定,此时有机相中Fe3+浓度约为4.76 g/L。由于在萃取过程中只有极少量的Al3+与Fe3+一同被共萃进有机相,Fe、Al在萃取阶段已到达理想的分离效果,因此在反萃时主要考虑载铁有机相中Fe3+的反萃。
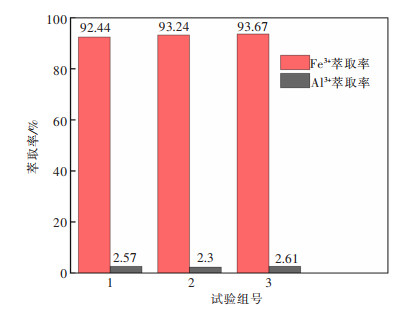 |
| 图 11 重复性实验 Fig. 11 Repeatability of the experiments |
2.6 萃取前后有机相红外光谱分析
为研究P204萃取Fe3+时的反应机理,在较优反应条件下,萃取前后的有机相红外光谱如图 12所示。随着萃取反应的进行,P204的P=O基团与Fe形成了新的配位键P=O→Fe,从而削弱了P=O基团的电子云,因此P=O基团在1 230 cm-1处的伸缩振动萃取后转移至1 196 cm-1,强度也逐渐变低。P204中1 035 cm-1左右的伸缩振动归因于P204中的P-O-C以及P-O-H,在萃取时,H+被Fe3+取代,峰位发生红移,因此在萃取之后主峰不仅向波数稍低的位置转移并且峰形逐渐变宽。光谱图中1 690 cm-1处的P-O-H由于面内弯曲振动在萃取后强度增大,逐渐向波数较低的方向移动,最终由于被1 464 cm-1主峰所掩盖而消失。同样,P204中P-O-H基团在2 311 cm-1处的伸缩振动在萃取后也完全消失,而这是由于随着萃取的发生,其逐渐向高波数移动,强度显著增加造成的。通过光谱分析可以看出,Fe3+通过与P204中的P=O和P-O-H结合进而被萃取进有机相。
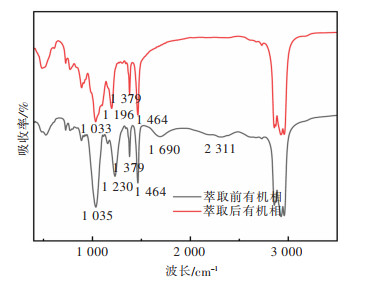 |
| 图 12 萃取前后有机相红外光谱 Fig. 12 IR spectra of the organic phase before and after extraction |
2.7 载铁有机相的反萃
在对载铁有机相中的Fe3+反萃时,研究H2SO4、HCl作为反萃剂对载铁有机相中Fe3+反萃的效果差异。在使用体积分数为40%的H2SO4作为反萃剂时,通过单级反萃的试验结果表明,在温度为60 ℃,相比V(O): V(A)=1:1,反萃时间为10 min的条件下,Fe3+的反萃率仅为37.00%,反萃效果不佳。在同样的反应条件,即使经四级反萃,Fe3+的反萃率也仅达到76.74%,这与先前的研究结果一致[19]。而在采用5 mol/L的盐酸,在相比V(O): V(A)=1:1时,在室温下经过10 min的反应,Fe3+的反萃率达72.35%,在其他条件不变的情况下,当相比V(O): V(A)=1:3时,Fe3+的单级反萃率可达92.96%。
为了研究反萃后的有机相的重复利用性,在温度为60 ℃,水相初始pH值为0.4,相比V(O): V(A)=1:1的条件下,经过20 min的反应,Fe3+萃取率为89.60%,Al3+的萃取率为2.06%,有机试剂的萃取性能良好。
3 结论通过模拟粉煤灰硫酸浸液(配制Al3+浓度为37.1 g/L,Fe3+浓度为5.10 g/L的硫酸铝溶液),系统研究了P204萃取体系在萃取分离含铁硫酸铝溶液中Fe、Al时,P204体积分数、萃取温度、反应时间、水相pH、相比V(O): V(A)对Fe、Al分离效果的影响以及载铁有机相的反萃效果。
1) 在P204体积分数为40%、萃取温度为60 ℃、水相pH为0.4、相比V(O): V(A)=1:1,经过20 min的反应时间,Fe3+的萃取率约为93.24%,Al3+的萃取率约为2.30%,分离系数β为438,Fe、Al可达到很好的分离效果。
2) 通过萃取前后有机相的红外光谱图分析可以看出,在萃取过程中,Fe3+通过与P204中的P=O和P-O-H基团结合进而被萃取进有机相中。
3) 在对载铁有机相中的Fe3+反萃时,用体积分数为40%硫酸在温度为60 ℃,相比V(O): V(A)=1:1,反萃时间为10 min的条件下对载铁有机相的单级反萃效果不佳,即使经四级萃取,Fe3+的反萃率也仅为76.74%。而采用5 mol/L的盐酸作为反萃剂,当相比V(O): V(A)=1:3,在室温下经10 min反应,单级反萃率即达92.96%。
| [1] |
白光辉, 王香港, 郭继萍, 等. 粉煤灰硫酸法提铝的新工艺参数研究[J].
煤炭科学技术, 2008(9): 106–109.
|
| [2] |
DING J, MA S, SHEN S, et al. Research and industrialization progress of recovering alumina from fly ash: A concise review[J].
Waste Management, 2016(6): 375–387. |
| [3] |
王勇, 申立苗, 朱应宝. 高铝粉煤灰预脱硅碱石灰烧结法提铝硅钙渣脱碱工艺研究[J].
轻金属, 2015(8): 10–14.
|
| [4] |
吴永峰. 粉煤灰提取氧化铝的除铁工艺研究进展[J].
中国资源综合利用, 2017, 35(8): 58–61.
DOI: 10.3969/j.issn.1008-9500.2017.08.022.
|
| [5] |
王丽萍, 李超, 郭昭华, 等. 酸浸法生产氧化铝过程除铁技术新进展[J].
无机盐工业, 2018, 50(9): 7–9.
|
| [6] |
赵爱春, 张廷安, 吕国志, 等. 低温酸浸高铁铝土矿中铁和铝的溶出规律研究[J].
功能材料, 2012, 43(增刊1): 105–108.
|
| [7] |
吕国志, 张廷安, 赵爱春, 等. 酸浸及萃取对高铁铝土矿中有价元素分离特性的影响[J].
东北大学学报(自然科学版), 2013, 34(10): 1442–1445.
DOI: 10.3969/j.issn.1005-3026.2013.10.018.
|
| [8] |
刘汇东, 孙琦, 赵利军, 等. 粉煤灰脱硅液FeSx-CuS共沉淀法深度除铁实验[J].
科学技术与工程, 2017, 17(33): 369–373.
DOI: 10.3969/j.issn.1671-1815.2017.33.059.
|
| [9] |
WANG G, ZHAO Y, YANG B, et al. Removal of trace iron from cobalt electro-refining electrolytes using monophos resin[J].
Hydrometallurgy, 2018, 176: 69–72. DOI: 10.1016/j.hydromet.2018.01.008. |
| [10] |
ZHANG Y, LIU Q, LI L. Removal of iron from synthetic copper leach solution using a hydroxy-oxime chelating resin[J].
Hydrometallurgy, 2016, 164: 154–158. DOI: 10.1016/j.hydromet.2016.06.004. |
| [11] |
薛茹君, 兰伟兴, 李森, 等. 萃取除铁法在粉煤灰制取高纯氧化铝中的应用研究[J].
中国矿业大学学报, 2010, 39(6): 907–910.
|
| [12] |
SUN X X, SUN Y Z, YU J G. Removal of ferric ions from aluminum solutions by solvent extraction, part I: Iron removal[J].
Separation and Purification Technology, 2016, 159: 18–22. DOI: 10.1016/j.seppur.2015.12.054. |
| [13] |
WANG L J, WANG Y, LI C, et al. A sustainable approach for advanced removal of iron from CFA sulfuric acid leach liquor by solvent extraction with P507[J].
Separation and Purification Technology, 2020, 251: 1–10. |
| [14] |
YI X T, HUO G S, TANG W. Removal of Fe(Ⅲ) from Ni-Co-Fe chloride solutions using solvent extraction with TBP[J].
Hydrometallurgy, 2020, 192: 1–6. |
| [15] |
何朝晖, 易文武, 刘一平. 伯胺萃取法生产无铁硫酸铝工艺研究[J].
无机盐工业, 2001(6): 29–30.
|
| [16] |
LI M Y, HE Z M, LI Z. Removal of iron from industrial grade aluminum sulfate by primary amine extraction system[J].
Hydrometallurgy, 2011, 106: 170–174. DOI: 10.1016/j.hydromet.2010.12.018. |
| [17] |
李凡, 朱军, 白苗苗, 等. 用溶剂萃取法从硫酸镍溶液中去除钙、铁[J].
湿法冶金, 2016, 35(2): 132–135.
|
| [18] |
冯雪茹, 吕国志, 张廷安, 等. P204萃取硫酸体系中V(Ⅳ)、Fe(Ⅲ)的分离性能研究[J].
钢铁钒钛, 2017, 38(2): 23–29.
|
| [19] |
YU S Q, CHEN J Y. Stripping of Fe(Ⅲ) extracted by Di-2-ethylhexyl phosphoric acid from sulfate solutions with sulfuric acid[J].
Hydrometallurgy, 1989, 22: 267–272. DOI: 10.1016/0304-386X(89)90057-1. |
 2022, Vol. 13
2022, Vol. 13

