| 单晶型LiNi0.8Co0.1Mn0.1O2正极材料的制备及性能对比 |
b. 江西理工大学,资源与环境工程学院,江西 赣州 341000;
c. 江西理工大学,江西省动力电池及其材料重点实验室,江西 赣州 341000
b. School of Resources and Environmental Engineering, Jiangxi University of Science and Technology, Ganzhou 341000, Jiangxi, China;
c. Jiangxi Key Laboratory of Power Battery and Materials, Jiangxi University of Science and Technology, Ganzhou 341000, Jiangxi, China
近年来,能源和环境问题一直是技术发展的热点话题,新型的、绿色能源的开发和利用变得越来越重要。在新能源发展进程中,锂离子电池作为新型储能技术,在新型电动汽车等领域发挥着重要作用。早在20世纪末,有着不同结构的钴酸锂,锰酸锂,磷酸铁锂等材料的电池已经被商品化[1]。而目前,对于锂离子电池的应用不论是具有储能功能的电力领域,还是便利社会、代表着时代发展的新兴产业和产品,例如智能电子设备,电动汽车等都有着相当大的应用前景和市场需求[2-4]。近年来,传统锂离子电池在实际应用中,逐渐暴露出其比能量低的短板,这就意味着锂离子电池以后的发展趋势必然以研究开发比容量高的电极材料为先决条件。正极作为锂离子电池材料的关键材料,它的容量密度的大小是整个电池体系性能是否优异的重要指标[5-6]。锂离子电池正极材料的种类很多,不同种类的正极材料有着不同的特点,其中具有层状结构的钴酸锂,因为其优异的循环性能和较高的电压平台,成为商业化最早的正极材料。但是由于钴金属价格昂贵,资源储量较少,极大的限制了钴酸锂材料的发展,就目前而言,钴含量对锂离子电池的容量衰减速率有着直接影响[7]。磷酸铁锂具有橄榄石结构,安全性高,而且价格低廉。但是其在电化学性能测试中充放电电压较低,能量密度小,跟钴酸锂有着显著区别[8-12]。此外,还有近些年新兴的镍钴锰三元正极材料等。NCM三元材料兼备上述几种电极材料的特点,其生产成本低、环境污染小、毒性低、能量密度和电压平台高,在一定程度上弱化三者的缺点,因此三元材料在锂离子电池行业迅速成长起来[13]。
三元材料制备方法通常有以下几种:①高温固相法。将锂盐、锰盐、钴盐、镍盐按一定比例并通过不同的方法混合,研磨均匀后高温煅烧制得粉体材料。该法主要优点有:工艺简单、晶体结构完整。缺点主要有:烧成温度高[14]、能耗大、固相中离子扩散速度慢,难于保证元素分布均匀。由于该种材料自身结构特性和较差的热稳定性,温度过高会导致阳离子混排加剧[15];②溶胶凝胶法(Sol-gel)。通过金属离子与某些有机酸的络合作用,再进一步酯化和聚合形成凝胶前驱体,前驱体高温下烧结制成材料粉体,该法能使元素达到原子级混合,从而降低后续烧制温度、减小无电化学活性的岩盐相产生及减少锂盐挥发造成的损失,结晶性能很好[16];③共沉淀法。首先将3种盐类充分溶解在水中,在施加其合成条件,得到沉淀的同时析出溶液,待经过充分干燥后的沉淀可作为前驱体,再将前驱体经混锂高温烧结以后制备成所需材料[17-19]。该法制备的颗粒大小均一,振实密度高,且可通过调节工艺参数来调整其形貌;④水热法。是利用锂离子与镍、钴、锰离子在一定条件下能在液相中生长的特性,继而得到结晶态样品的方法,但该法不好控制反应条件,且生长过程条件为高温、高压,过程能耗高、成本高[19-21]。
高镍的LiNi0.8Co0.1Mn0.1O2材料,一般因Ni含量的占比较大,会造成阳离子混排(Ni2+与Li+有着相当的离子半径,会出现部分Ni2+占据Li+位置的现象,影响Li+的脱嵌)[22]。镍离子的还原和氧化反应若不彻底,将对其材料性能造成影响,其中高价镍离子在被还原的过程中有一定的几率会与电解液反应,且Ni2+在氧化过程中容易形成氧化层,造成离子迁移障碍。这就使得在电池的充放电性能测试时,存在容量衰减突出,库伦效率过低等缺陷,极大地降低实用价值。所以对材料的改性相当有必要[23-29]。主要的改性方法有2种:一种是包覆改性,顾名思义,根据材料的特性(溶解度、熔点、稳定性)在所需材料表层包覆合适的惰性物质,不仅可以避免电解液的侵蚀,还能使离子交换达到最大化,可以有效抑制活性物质在电解质中的溶解。此外,包覆改性能够更直观的改善NCM材料的镍锂混排,更应该注意包覆量(过量包覆影响电化学性能)对材料带来的影响[30-33]。此外还有离子掺杂,离子掺杂分为2种,阳离子掺杂和阴离子掺杂。前文已经提到因材料自身原因造成混排,合理的阳离子掺杂是解决此类现象很有效的一种方式,原本由于Ni2+抢占Li+通道而造成的影响会因加入新的阳离子得到改善。不仅如此,阳离子的大小迥异,可以利用离子尺寸差来改变层状间距,构造新的离子通道方便锂离子嵌入和脱出[34-35],并与锂离子大小相近的离子相互支撑,还可以通过价态较高的阳离子对镍离子进行价态转变来达到目的。而阴离子掺杂则是通过改变元素与元素之间的键能,防止氧的外溢[36-37]。
近年来多数团队通过掺杂锰、铁、铝等金属元素制备高镍材料,进一步降低钴的含量来节约成本,且仍保持优异的电化学性能,多数方法采用高温固相法,溶胶凝胶法来制备,而这些方法若要得到结晶良好的材料往往实现过程较为复杂[38]。
就目前而言,多晶形态的富镍正极材料虽然充放电速度快,但是经过多次循环后,晶体结构破裂,而且小晶体的集合体比单晶更容易受到外界因素的影响。PNNL团队利用高温熔融食盐中生长高性能晶体的工艺制备出一种单晶的高镍正极材料来规避该问题。他们还估计,与电动汽车所使用的锂离子电池相比,该种单晶材料容量至少可增加25%[39]。郭乾坤等用共沉淀-高温固相法合成了单晶型LiNi0.83Co0.1Mn0.07O2正极材料,通过降低材料与电解液的接触面积而减小电池工作时的副反应。在电极制作过程中,正极材料要经过一定的压实密度和机械破碎强度来保证极片的质量[40]。Liu等在实验过程中发现,单晶结构材料不仅机械强度高,压实密度更大,而且光滑的单晶颗粒可以充分与导电剂接触,有效地减小内阻并降低极化损失,而多晶材料由于二次球形颗粒的破碎易造成材料结构崩塌[41]。此外,商业NCM中往往以附聚物形状存在,Kim在研究中发现,在液相通量存在的情况下,每个NCM粒子可以单独生长,因此可以获得单个物体的颗粒形状,利用助溶剂和高温体系制备出单晶型正极材料不仅高温储存过程中显示出更少的气体排放,而且该材料颗粒光滑,形貌均一,在900 ℃烧制的样品的容量与商用NCM523相当[42]。
本文主要通过较为简单的熔盐合成的方式来获得单晶物质,以LiNO3为熔盐作为熔剂,在多个烧结温度下合成LiNi0.83Co0.1Mn0.07O2正极材料,并研究其结构、形貌及电化学性能,同时还以固相法制备相同温度下对应的参照组,最终得出熔盐法可以显著的提高NCM811材料的循环性能。
1 材料制备及测试主要设备和试剂如下:
设备:烧杯,电子天平,球磨仪,马弗炉,真空泵玛瑙研钵,漏斗,抽滤瓶,滤纸,鼓风干燥箱,48 μm筛网,涂布机,对辊机,冲片机,真空干燥箱,手套箱,电化学工作站。
试剂:无水乙醇,氢氧化镍,氧化亚钴,二氧化锰,LiOH·H2O,LiNO3,去离子水,炭黑(Super-P),聚偏氟乙烯(PVDF),N-甲基吡咯烷酮(NMP)。
1.1 样品制备按物质的量0.05 mol,以8:1:1的配比计算、称量所需氢氧化镍、氧化亚钴、二氧化锰,再加入1.05倍的LiOH·H2O,记为Sp,混合均匀后用无水乙醇浸没,加入大小不同的转子,以12 Hz的频率球磨12~14 h后取出烘干,适当研磨以后放入马弗炉中在氧气气氛下烧制。另取1份相同配比的氢氧化镍、氧化亚钴、二氧化锰,以F=4(0.38LiOH·H2O+0.62·NO3)的助熔体系加入混合锂盐,混合均匀后重复以上步骤,记为Ms。待炉子冷却至室温后,取出样品适当研磨后过滤、洗涤、干燥。干燥后再研磨过48 μm筛网,在氧气气氛下回火。
烧成制度:从室温升温到320 ℃,保温3 h;升温到750 ℃,保温3 h;升温到900 ℃,保温3 h;降温到750 ℃,保温12 h;随炉冷却。回火时从室温升温到600 ℃,保温6 h。升温速率均为3 ℃/min。
1.2 电池组装配置40:1的PVDF的NMP溶液,将涂炭铝箔裁成直径为1.2 cm的圆片并称量其质量,按质量比80:10称取所制备的活性物质NCM811、导电剂Super-P置于研钵中,然后加入一定量的PVDF溶液和适量的NMP,经研磨后用刮刀将其均匀涂布在集流体表面。然后置于鼓风干燥箱中(120 ℃)干燥后取出,辊压后称量其质量,置于真空干燥箱12 h以上即可取出组装电池。以金属锂片作为负极,隔膜采用微孔聚丙烯膜(PP),加入一定量1 mol/L的LiPF6电解液,在充满氩气的手套箱中组装成扣式半电池。然后常温下静置8 h即可测试电化学性能。
1.3 材料结构测试在Cu Kα辐射的Bruker粉末X射线衍射仪(XRD)样品进行物相分析。用ZEISS横梁340扫描电镜分析仪(SEM)对样品表面形貌表征图像进行采集。借助FEITecnaiG2F20透射电子显微镜(TEM)对材料纳米级别的形貌结构进行表征。
1.4 充放电测试用恒电流充放电测试系统对电池进行测试。拟定2.75~4.3 V为电压测试区间进行充放电测试,首次充放电性能测试时,先恒流充电至4.3 V,再恒压充电30 min,然后恒流放电至2.75 V。再搁置5 min。循环性能测试时,将使用不同的倍率进行循环,依次为0.1,0.5,1,3,5,0.1 C。先在指定倍率下恒流充电至4.3 V,再压充电30 min,继而于同一倍率下恒流放电至2.75 V,再搁置5 min,重复以上工作。
1.5 循环伏安测试(CV)用电化学工作站来进行循环伏安分析研究,在环境温度25 ℃恒温条件下,在2.5~4.5 V电压范围内以0.1 mV/s的速度进行扫描得到CV图。
2 材料结构测试结果及分析Ms-NCM811(熔盐法)和Sp-NCM811(固相法)样品的XRD衍射图谱中(图 1),二者所得材料的特征峰型为典型的尖峰,证明其材料空间结构是α-NaFeO2结构,空间群R-3m。而在(006)/(012),(018)/(110)位置出现明显的分裂峰,说明NCM三元正极材料属于层状结构并且结晶度都很高。
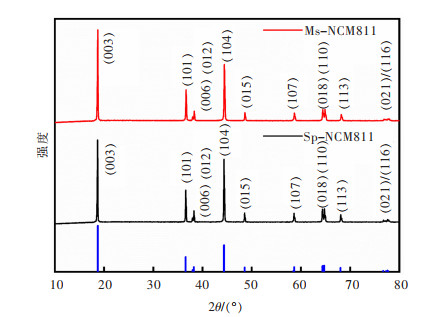 |
| 图 1 Ms-NCM811和Sp-NCM811样品的XRD图谱 Fig. 1 XRD patterns of Ms-NCM811 and Sp-NCM811 samples |
在三元材料中,镍锂混排程度是材料稳定性最常见的判别标准之一,在XRD衍射图谱中,(003)和(104)晶面的衍射强度会因为锂离子和过渡金属离子之间的晶面迁移而发生改变。经计算得出采用熔盐法制备的材料值为1.957,明显大于传统固相法合成的材料值1.665,而一般来说,I(003)/I(104)比值增加,意味着镍离子在锂层中的混乱占位的比例降低,表明Ms-NCM811材料镍锂混排程度更小,有着较好的层状结构,从而得到更为优异的电化学性能[43]。
通过扫描电镜(图 2),可以进一步更清楚的看到材料的表面特征。图 2(a)和图 2(b)是研磨混合均匀后通过固相反应高温梯度煅烧得到的Sp-NCM811材料表面形貌图像,可以看到材料中许多细小颗粒发生了团聚现象,且颗粒形状不规则,反应不充分,材料导电性不强,致使SEM不够清晰。由熔盐法结合高温固相法制备合成的Ms-NCM811材料图 2(c), 图 2(d)可以明显看出,较固相法相比,不论是小颗粒还是较大的颗粒,尺寸差异较小,均匀的分散开来,在观察过程中,可以看到明显的单晶结构,且大多数颗粒呈规则的菱方形状。固相法下呈现的材料颗粒较小,相互之间黏接聚集在一起,导致形状不规则,晶体结构不明显,相反Ms-NCM811下的粒径明显比固相法制备的要大,能达到微米级别的颗粒数量多,导电性良好,SEM观察图像清晰,边界明显。可以佐证XRD得到的结论,使用熔盐法制备的材料具有更好的循环性能与储存性能。
 |
| 图 2 Sp-NCM811和Ms-NCM811样品的扫描电镜图像 Fig. 2 The SEM images of Sp-NCM811 and Ms-NCM811 samples |
图 3所示为样品在透射电子显微镜下的形貌结构,在助溶剂作用下(F=4),Ms-NCM811在200 nm条件下有着460 nm的完整形貌图 3(a),表现出较为典型的微观尺寸。更高倍率下,其侧面微弱透光层析出保护薄膜图 2(b),而Sp-NCM811材料侧面所示结构证明Li+在过渡金属层间的状态为层间运动图 2(d)。此外,图 3(c)和图 3(f)可看出Ms-NCM811和Sp-NCM811材料明显的晶格条纹,其相对应的晶面间距分别为0.492 nm和0.202 nm,Ms-NCM811较为清晰明显,对应X射线光谱中具有离子传输活性的(003)晶面,且熔盐法下材料的晶格间距较常规三元材料的间距(0.474 nm)略大,可以更好的实现锂离子的脱嵌,提高倍率性能。Sp-NCM811条纹致密紧凑,对应(104)晶面。
 |
| 图 3 Ms-NCM811和Sp-NCM811样品的透射电镜图像 Fig. 3 The TEM images of Ms-NCM811and Sp-NCM811samples |
设定测试范围0.01~100 kHz,分别取在经过0.1 C倍率下化成后的2种扣式电池进行交流阻抗测试,在用软件拟合后的图谱中(图 4)可以看出,图像大致可以分为3个阶段。在距离实轴最近的低频截距区,代表着锂离子在内部溶液中迁移时产生的溶液内阻。显然Ms-NCM811较Sp-NCM811斜率较小。小半圆中频区域则反映锂离子在扩散至边界SEI膜时的迁移状态。而小半圆之后的高频区大半圆则为锂离子材料中固态扩散电阻的表征,3个阶段都较为清晰的反映出材料内部的电荷转移状态,且在等效电路拟合结果中得到映证。不论是在经过正极的界面接触阻抗,还是高频电导率以及低频区内部结构是否发生变化,都能够在此得到初步判断。证明用此种方法所制备的材料的离子在迁移过程中保持良好的状态[44-45]。
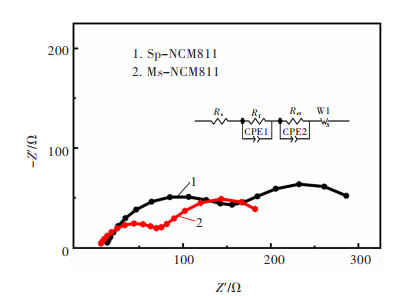 |
| 图 4 Sp-NCM811和Ms-NCM811材料的电化学阻抗谱(插图为等效电路模型) Fig. 4 Electrochemical impedance spectra of Sp-NCM811 and Ms-NCM811 materials The inset shows the corresponding equivalent circuit model |
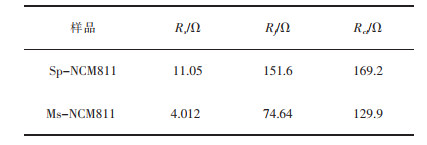
表 1所列为用ZView软件拟合出来的等效电路中元件的电阻值。表 1中Rs、Rf、Rct分别对应着锂离子电池中的溶液阻抗,界面阻抗,以及电荷转移阻抗。就液体环境中的迁移电阻而言,固相法和熔盐法2种所示阻值虽然不大,但熔盐法所制材料在电解液中电阻为4.012 Ω,小于固相法2倍之余,同样的,对比其在固体界面阻值以及锂离子在电极表面固体中的阻值,熔盐法所得阻值都远小于固相法。从而直观的说明在电池性能测试在拥有更小的内阻时,会减少因材料结构而造成的界面附加反应,表现出更好的导电性,大大地提高电池比容量及循环性能[46]。
| 表 1 Sp-NCM811和Ms-NCM811的阻抗拟合结果 Table 1 Impedance fitting results of Sp-NCM811 and Ms-NCM811 |
 |
| 点击放大 |
图 5所示为2种方法得到材料在电压区间为2.5~4.5 V之间,并将扫描速率设为0.1 mV/s,连续扫描5次后的循环伏安曲线,可以看到,2种方法下的氧化还原峰的出现都介于3.2~4.5 V之间,证明3.2 V以后才在电极表面发生了Ni3+的氧化还原反应。而在氧化还原峰前的平直曲线范围所对应电压区间内并没有实际反应,且在电化学测试中平台电压的设置范围也应与其相对应[47]。另外,在实轴上所得的有效电压差不仅可以作为判断材料内部电极表面是否发生极化的依据,还可以推测所测样品潜在容量的大小。从图 5中可以看出Ms-NCM811的ΔV为0.276 V,低于Sp-NCM811的0.332V,说明Ms-NCM811在循环过程中有效的抑制相变降低电极极化,进一步体现熔盐法所制备的样品材料晶体结构的稳定。这也是锂离子电池再循环测试保持良好稳定性的前提。
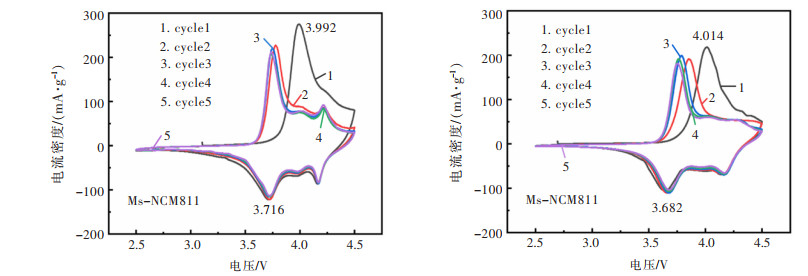 |
| 图 5 Ms-NCM811和Sp-NCM811在0.1mV/s扫速下的循环伏安曲线 Fig. 5 CV curves of Ms-NCM811 and Sp-NCM811 at a scan rate of 0.1mV/s |
图 6所示为2种材料在0.2~5 C倍率性能测试,在0.2 C低倍率下固相法和熔盐法制备的材料有着相近的放电比容量,这种趋势在0.5 C倍率下表现尤为明显,随着测试倍率的提高,熔盐法合成的材料逐渐表现出好的电化学性能。在较大充放电倍率(1,3,5 C)下,Ms-NCM811材料有着明显的优势。且在5 C充放电后,Ms-NCM811可以保持有比Sp-NCM811更高的比容量,再低至0.2 C倍率时较最初时放电比容量相差更大。
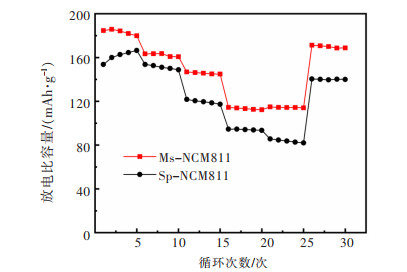 |
| 图 6 Sp-NCM811和Ms-NCM811样品的倍率性能对比 Fig. 6 Comparison of rate capability of Sp-NCM811 and Ms-NCM811 materials |
这说明熔盐法制备的大单晶结构材料,即使在大电流下也能保持很好的晶体结构,同时在大电流充放电后仍能保持很好的稳定性。
图 7所示为Ms-NCM811和Sp-NCM811材料在0.1 C倍率下的首次充放电曲线。熔盐法Ms-NCM811的首次放电比容量201.848 mAh/g, 固相法Sp-NCM811的首次放电比容量为173.813 mAh/g,较熔盐法略低一些。另一方面,Ms-NCM811的首次充放电效率为68.41%,比Sp-NCM811的67.46%要略高一点,总体上二者的首次库伦效率都偏低,且相差不大。
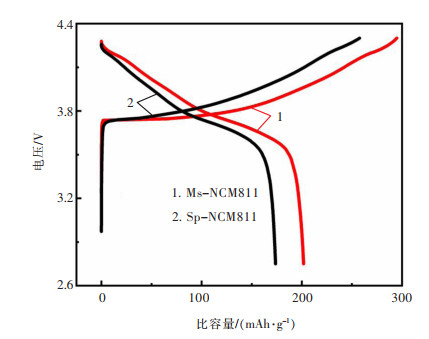 |
| 图 7 Ms-NCM811和Sp-NCM811样品化成充放电比容量对比 Fig. 7 Comparison of charge-discharge specific capacity of single Ms-NCM811 and Sp-NCM811 samples |
这可能是由于:
1) 有副反应发生。脱锂时有部分容量是电极与电解液的反应,且不可逆。
2) 残留锂盐较多,造成的不可逆相变。
3) 用熔盐法和固相法制得正极材料时,由于体系中充满大量的Ni,在首次脱锂之后,材料表面不仅会形成SEI膜,还会生成Li2NiO2,这会显著降低材料动力学特性,阻碍Li+重新嵌入材料[48]。
图 8所示为Ms-NCM811和Sp-NCM811 2种材料在不同电流密度下放电比容量的循环次数之间的变化关系。0.2 C倍率下,Ms-NCM811的首圈放电比容量为184.628 mAh/g,59圈时为168.812 mAh/g,容量保有率为91.43%。而Sp-NCM811首圈放电比容量为153.643 mAh/g,59圈为140.022 mAh/g,保持率为91.13%。这说明在低倍率下2种材料的循环稳定性较好且相差不大(图 8(a))。0.5 C倍率下,Ms-NCM811首次放电比容量为148.078 mAh/g,但在第2~6圈时回升至163.606 mAh/g,这是因为首次放电不完全造成的,之后到100圈时仍有146.751 mAh/g,容量保有率可达89.70%。Sp-NCM811的首圈放电比容量为163.95 mAh/g,第100圈仅有106.556 mAh/g,保持率仅有65.00%(图 8(b))。1 C时,Ms-NCM811在经过100次充放电测试后,比容量可达127.632 mAh/g,保有率80.93%。同倍率下,Sp-NCM811在100圈之后放电比容量仅有71.969mAh/g,容量保持率仍有78.98%(图 8(c))。而在3 C倍率下,Ms-NCM811第100圈时放电比容量为98.996 mAh/g,保有率80.09%。Sp-NCM811的首圈放电比容量仅有100.815 mAh/g,但保有量达83.54%(图 8 (d))。5 C时,Ms-NCM811的200圈容量保持率为80.49%。Sp-NCM811比容量在200次循环后由100.347 mAh/g下降至40.125 mAh/g,保持率仅有39.99%(图 8(e))。
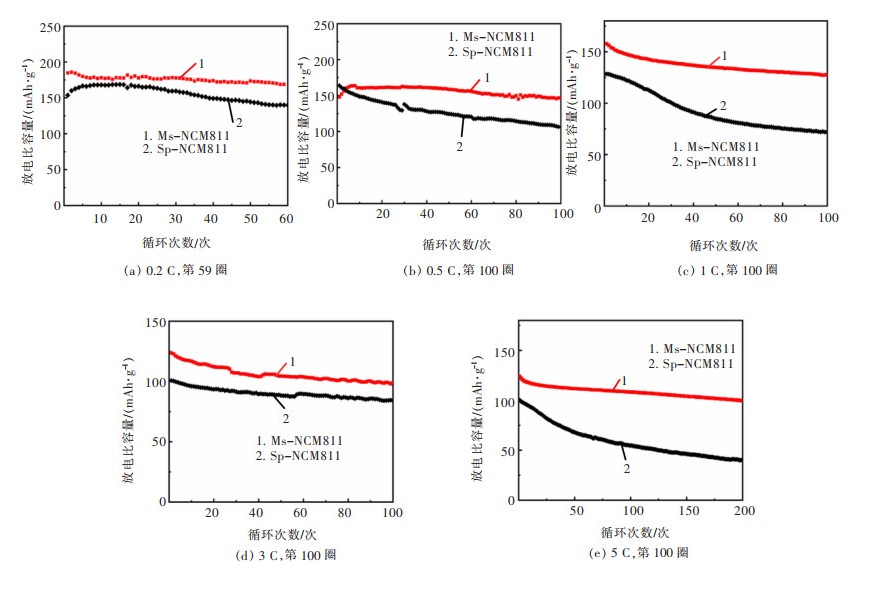 |
| 图 8 Ms-NCM811和Sp-NCM811在不同电流密度下的循环曲线 Fig. 8 Ms-NCM811和Sp-NCM811 Cycling performances at different current density |
总之,在以上几种倍率下Ms-NCM811的循环稳定性优于Sp-NCM811,尤其在0.2 C倍率的容量保持率都在90%以上,而Sp-NCM811比容量保持率变化幅度较大,在5 C下不足50%。且随着倍率的增大,二者可逆比容量的差距的增大佐证了循环和倍率变化趋势的一致性, 进一步体现了单晶样品材料的循环稳定性。
3 结论1) 通过熔盐法制备的LiNi0.8Co0.1Mn0.1O2正极材料,层状结构明显,符合LiNi0.8Co0.1Mn0.1O2材料的结构特征,并且该材料阳离子混排程度很低,晶体尺寸达到微米级,且具有良好的单晶体结构。
2) 熔盐法制备的NCM811具有更好的高倍率循环性能。在低倍率充放电下,熔盐法制备的LiNi0.8Co0.1Mn0.1O2材料电化学性能与固相反应制备的类似,放电比容量可达184.63 mAh/g, 保有率高达90%以上,且在1 C及以上倍率下,熔盐法制备的NCM811材料优异得循环性能更加突出,尤其在5 C倍率下,保持率仍高达80.49%。
3) 虽然熔盐法和固相法所得材料首次充放电效率不高,仅有68.41%和67.46%,但在4.3 V电压上限下,放电比容量可提高至少7.1 mAh/g以上,而通过熔盐法制备的LiNi0.8Co0.1Mn0.1O2正极材料,给NCM正极材料制备中遇到的阳离子无序等问题提供了新思路。
| [1] |
赖春艳, 雷轶轲, 蒋宏雨, 等. 锂离子电池NCM三元正极材料的研究进展[J].
上海电力学院学报, 2020, 36(1): 11–16.
|
| [2] |
JUNG C H, SHIM H, EUM D G, et al. Challenges and recent progress in LiNixCoy Mn 1-x-y O2 (NCM) cathodes for lithium ion batteries[J].
Journal of the Korean Ceramic Society, 2021, 58(prepublish): 1–27. |
| [3] |
FRIEDRICH F, STREHLE B, FREIBERG A, et al. Editors' choice-capacity fading mechanisms of NCM[J].
Journal of The Electrochemical Society, 2019, 166(15): 3760–3774. DOI: 10.1149/2.0821915jes. |
| [4] |
CHOI K H, LIU X Y, DING X H, et al. Design strategies for development of nickel-rich ternary lithium-ion battery[J].
Ionics: International Journal of Ionics: The Science and Technology of Ionic Motion, 2020, 26(29): 1063–1080. |
| [5] |
SUN X, LUO X L, ZHANG Z, et al. Life cycle assessment of lithium nickel cobalt manganese oxide (NCM) batteries for electric passenger vehicles[J].
Journal of Cleaner Production, 2020, 273: 123006. DOI: 10.1016/j.jclepro.2020.123006. |
| [6] |
CHAKRABORTY A, KUNNIKURUVAN S, DIXIT M, et al. Review of computational studies of NCM cathode Ma terials for Li-ion Batteries[J].
Israel Journal of Chemistry, 2020, 60(8/9): 850–862. |
| [7] |
GAO S, CHENG Y T, SHIRPOUR M. Effects of cobalt deficiency on nickel-rich layered LiNi0.8Co0.1Mn0.1O2 positive electrode materials for lithium-ion batteries[J].
ACS Applied Materials & Interfaces, 2018, 11(1): 982–989. |
| [8] |
孙嘉遥, 黄超, 郭双桃. 锂离子全电池研究综述[J].
新材料产业, 2019(5): 51–57.
|
| [9] |
宗意恒. 熔盐法制备高镍三元正极材料及其在锂电池领域的应用[D]. 徐州: 中国矿业大学, 2019.
|
| [10] |
陈军, 丁能文, 李之峰, 等. 锂离子电池有机正极材料[J].
化学进展, 2015, 27(9): 1291–1301.
|
| [11] |
刘浩, 吴江, 陈浩. 高比能量富镍三元正极材料的研究进展[J].
化学工程师, 2020, 34(7): 58–64.
|
| [12] |
王亚龙. 纯电动城市物流车动力电池温度稳定性研究[D]. 太原: 太原理工大学, 2017.
|
| [13] |
韩彬. 锂电池三元正极材料的最新研究进展[J].
电源技术, 2020, 44(2): 285–290.
DOI: 10.3969/j.issn.1002-087X.2020.02.037.
|
| [14] |
孙淑婷. 锂离子电池三元正极材料LiNi0.6Co0.2Mn0.2O2的制备与改性[D]. 天津: 天津大学, 2015.
|
| [15] |
熊聪. 锂离子电池LiNi0.8Co0.1Mn0.1O2正极材料的制备与改性研究[D]. 广州: 华南理工大学, 2020.
|
| [16] |
廖大健. 锂离子电池LiNi0.6Co0.2Mn0.2O2高镍三元正极材料的制备与改性研究[D]. 广州: 华南理工大学, 2020.
|
| [17] |
PARK S, KU H, LEE K J, et al. The effect of NH; Concentration during co-precipitation of precursors from leachate of lithium-ion battery positive electrode active materials[J].
Journal of the Korean Institute of Resources Recycling, 2015, 24(6): 9–16. DOI: 10.7844/kirr.2015.24.6.9. |
| [18] |
LIU P C, YANG X R, LI X, et al. Preparation of ternary trecursor derived from spent LiNixCoy Mn1-x-yO2 materials[J].
JOM, 2019, 71(12): 4492–4499. DOI: 10.1007/s11837-019-03789-x. |
| [19] |
房子魁. 纳米LiMnPO4/C正极材料的可控合成及其掺杂改性研究[D]. 马鞍山: 安徽工业大学, 2017.
|
| [20] |
施方长. 水热法合成高镍三元正极材料的研究[D]. 镇江: 江苏科技大学, 2020.
|
| [21] |
郭家瑞, 泮思赟, 桂培培, 等. 三元正极材料制备及其改性研究进展[J].
山东化工, 2020, 49(1): 44–45.
DOI: 10.3969/j.issn.1008-021X.2020.01.019.
|
| [22] |
章亚飞. 富镍三元正极材料的表面改性及储锂性能研究[D]. 石家庄: 河北科技大学, 2019.
|
| [23] |
郭家瑞, 泮思赟, 桂培培, 等. 三元正极材料制备及其改性研究进展[J].
山东化工, 2020, 49(1): 44–45.
DOI: 10.3969/j.issn.1008-021X.2020.01.019.
|
| [24] |
钟盛文, 金柱, 梅文捷, 等. 高容量锂离子正极材料LiNi0.5Co0.3Mn0.2O2的制备与性能[J].
电源技术, 2016, 40(1): 24–27.
DOI: 10.3969/j.issn.1002-087X.2016.01.006.
|
| [25] |
CHEN B Z, ZHAO B C, ZHOU J F, et al. Surface modification with oxygen vacancy in Li-rich layered oxide Li1.2Mn0.54Ni0.13Co0.13O2 for lithium-ion batteries[J].
Journal of Materials Science & Technology, 2019, 35(6): 994–1002. |
| [26] |
韩彬. 锂电池三元正极材料的最新研究进展[J].
电源技术, 2020, 44(2): 285–290.
DOI: 10.3969/j.issn.1002-087X.2020.02.037.
|
| [27] |
赵星. 高倍率三元正极材料的制备及性能研究[D]. 成都: 西南石油大学, 2017.
|
| [28] |
郭家瑞, 泮思赟, 桂培培, 等. 三元正极材料制备及其改性研究进展[J].
山东化工, 2020, 49(1): 44–45.
DOI: 10.3969/j.issn.1008-021X.2020.01.019.
|
| [29] |
赵星, 李星, 王明珊, 等. 锂离子电池正极材料LiNi0.8Co0.1Mn0.1O2的研究进展[J].
电源技术, 2016, 40(12): 2469–2471.
DOI: 10.3969/j.issn.1002-087X.2016.12.051.
|
| [30] |
KIM Y J, RAJESH R, RYU K S. Study of LiNi0. 6Co0. 2Mn0. 2O2 coated with Li2ZrO3 nanolayers in all-solid-state lithium ion batteries[J].
Science of Advanced Materials, 2020, 12(3): 412–421. DOI: 10.1166/sam.2020.3653. |
| [31] |
张晶波. LiAlO2和PPy包覆改性LiNi0.8Co0.1Mn0.1O2材料及电化学性能研究[D]. 哈尔滨: 哈尔滨工业大学, 2019.
|
| [32] |
武建鑫. 锂离子电池高镍正极材料LiNi0.8Co0.1Mn0.1O2的制备及其包覆改性研究[D]. 北京: 北京交通大学, 2019.
|
| [33] |
王同振. 高容量锂离子电池正极材料的包覆改性及循环性能研究[D]. 合肥: 合肥工业大学, 2020.
|
| [34] |
SON H B, JEONG M Y, HAN J G, et al. Effect of reductive cyclic carbonate additives and linear carbonate co-solvents on fast chargeability of LiNi0.6Co0.2Mn0.2O2/graphite cells[J].
Journal of Power Sources, 2018, 400: 147–156. DOI: 10.1016/j.jpowsour.2018.08.022. |
| [35] |
李子晨. 锂离子电池正极补锂添加剂的制备及其性能研究[D]. 哈尔滨: 哈尔滨工业大学, 2020.
|
| [36] |
张登科. 富镍系LiNi0.8Co0.1Mn0.1O2电极材料的制备及改性研究[D]. 上海: 上海应用技术大学, 2020.
|
| [37] |
杨慧平. 掺杂与包覆双重修饰锂离子电池高镍正极材料的研究[D]. 长沙: 长沙理工大学, 2019.
|
| [38] |
范凤松, 徐唱, 钟盛文, 等. 电池材料LiNi0.7Mn0.3O2在熔盐中的生长与电化学性能[J].
电源技术, 2017, 41(2): 177–180.
DOI: 10.3969/j.issn.1002-087X.2017.02.001.
|
| [39] |
靳爱民. 单晶技术为下一代锂离子电池带来了希望[J].
石油炼制与化工, 2021, 52(4): 32.
|
| [40] |
郭乾坤, 黄吉丽, 周苗苗, 等. 单晶LiNi0.83Co0.1Mn0.07O2正极材料的合成及电化学性能[J].
有色金属科学与工程, 2020, 11(4): 23–28.
|
| [41] |
LIU W, OH P, LIU X, et al. Nickel-rich layered lithium transition-metal oxide for high-energy lithium-ion batteries[J].
Angewandte Chemie International Edition, 2015, 54(15): 4440–4458. DOI: 10.1002/anie.201409262. |
| [42] |
KIM Y. Lithium nickel cobalt manganese oxide synthesized using alkali chloride flux: morphology and performance as a cathode material for lithium ion batteries[J].
ACS Applied Materials & Interfaces, 2012, 4(5): 2329–2333. |
| [43] |
宗意恒. 熔盐法制备高镍三元正极材料及其在锂电池领域的应用[D]. 徐州: 中国矿业大学, 2019.
|
| [44] |
庄全超, 杨梓, 张蕾, 等. 锂离子电池的电化学阻抗谱分析研究进展[J].
化学进展, 2020, 32(6): 761–791.
|
| [45] |
徐婷婷. 高镍三元正极材料单晶体的制备及其电化学性能[D]. 徐州: 中国矿业大学, 2019.
|
| [46] |
宋美霖, 王东晨, 罗珑玲, 等. 制备工艺对LiNi0.5Co0.2Mn0.3O2正极材料微结构和电化学性能的影响[J].
广西大学学报(自然科学版), 2018(2): 710–715.
|
| [47] |
张佳卫. 锂硫电池用碳/硫复合正极材料的制备及电化学性能研究[D]. 杭州: 浙江理工大学, 2016.
|
| [48] |
ZHOU H, XIN F X, PEI B, et al. What limits the capacity of layered oxide cathodes in lithium batteries?[J].
ACS Energy Letters, 2019, 4(8): 1902–1906. DOI: 10.1021/acsenergylett.9b01236. |
 2021, Vol. 12
2021, Vol. 12


