| 过渡金属有机框架结构构件及电解水研究进展 |
2. 广东石油化工学院化学工程学院, 广东 茂名 525000
2. School of Chemical Engineering, Guangdong University of Petrochemical Technology, Maoming 525000, Guangdong, China
目前,开发清洁高效的可再生能源来代替传统的化石能源对我国经济的可持续发展有着重大意义[1]。氢能由于其燃烧热值高、无毒无害和来源广等优势成为了目前最理想的清洁能源[2-3]。其中,电催化水分解是用来开发氢能的较理想的方法之一[4]。整体水分解是由两个半反应组成,即析氢反应(HER)和析氧反应(OER)[5]。但析氢反应(2H2O+2e-→H2+2OH-)和析氧反应(4OH-→O2+2H2O+4e-)都存在动力学迟缓等问题,特别是析氧反应,由于涉及到4个电子的转移而需要更大的能耗。因此,人们通过引入催化剂来降低过电位,从而提高能源的转化效率。目前作为电化学水分解的高效催化剂多为贵金属及其氧化物(Pt,RuO2和IrO2等)[6-7],这类贵金属及其氧化物由于价格高且稀缺,在大规模的工业应用过程中受到了极大的限制[8],而过渡金属(如Ni,Co和Fe基异质结构)在理论上具有较高的电催化活性[9-11],且成本低,已被证明可以作为有效的非贵金属电催化剂。但目前非贵金属催化剂来代替贵金属催化剂也存在反应效率低下的问题,提高其催化性能非常关键。
金属有机框架(Metal-Organic Framework,简称MOF)是一种利用金属离子与有机配体设计合成的一种高孔隙率的晶体材料[12-13]。由于MOFs具有独特的配位连接方式,可以选择不同的金属中心和有机配体进行配对,因此,MOFs在组成和结构上可以表现出不同维度的结构从而应用在不同的领域上,尤其在作为电解水阳极催化剂上显示出巨大的应用潜力。本文从MOFs的结构出发,总结了以不同合成方式制备的零维、一维和二维MOF结构,并对基于过渡金属构建的MOFs材料在电催化水分解的应用进展和面临的挑战进行了分析讨论。
1 过渡金属有机框架结构1995年,YAGHI等将过渡金属Co和均苯三甲酸反应合成了二维结构的材料,第一次提出了金属有机框架的概念[14]。金属有机框架材料是一种由有机配体和金属离子或团簇通过配位键自组装形成的具有分子内孔隙的有机-无机杂化材料,具有比表面积大、孔道可调控和可功能化等特性[15-18]。因此,MOF及其衍生物目前广泛应用于吸附、气体存储、生物催化、光催化、化学催化等领域[19-24]。但是在电催化析氢(HER)、析氧(OER)及氧还原(ORR)中应用较少[25-27]。主要原因有2个:较差的导电性和结构不稳定性。由于在电催化过程中的动力学过程缓慢,导电性差和结构不稳定等问题会导致电解质离子传输行为不良和不稳定,从而使得有效的MOF析氧电催化剂无法得到很好的探索。因此,为了减少导电性和稳定性对MOF在电催化中应用的影响,研究者们通过让不同的金属离子/簇与不同的有机配体相结合来调控组合物的结构以满足不同场景下的需要[28-32]。如将MOF的结构限定在纳米尺度范围内,制备不同维度的纳米材料,如零维纳米颗粒、一维纳米棒、二维超薄纳米片等。
1.1 零维MOF材料的合成迄今为止,零维MOF材料已经通过多种方式合成,这些合成方式主要依赖于在溶剂热或水热条件下MOF晶体成核和生长的空间和时间控制。2006年,Ni等提出了一种名为“微波辅助溶剂热合成”的新合成方法,该方法利用微波加热使含有反应物的有机溶剂和水的混合溶液迅速蒸发,在1 min内合成高质量的金属有机骨架晶体[33]。Ni和同事利用极性溶剂如二乙基甲酰胺(DEF)的高介电吸收能力,使反应溶液能快速进行热能转换和有效的局部加热,从而实现快速成核和晶体生长,成功合成了IRMOF-1、IRMOF-2和IRMOF-3纳米颗粒。自此,许多研究者也成功地采用这种方法来高效和选择性地合成各种MOF纳米颗粒[34-36]。
除了通过不同类型的能量转换控制尺寸外,零维MOF纳米粒子还可以通过利用界面反应和限制反应区的形状来控制合成。ZHAO等使用表面活性剂限制合成MOF颗粒的尺寸,并将表面活性剂作为中孔分子筛的模板来形成微孔MOF结构[37]。由于CO2和碳氟化合物表面活性剂尾部之间的相互作用很强,N-乙基全氟辛基磺酰胺(N-EtFOCA)和离子液体(ILs)在超临界CO2(SCCO2)中形成微乳液。在合成过程中,将Zn(NO3)2、1, 4-苯二甲酸和N-EtFOCA添加到1, 1, 3, 3-乙酸四甲基胍盐(TMGA)中,并在16.8 MPa CO2压力下的高压槽中加热。从扫描和透射电子显微镜像(如图 1所示)可以观察到,纳米颗粒的直径约为80 nm,尺寸分布均匀,高倍率的透射图像中可以观察到MOF纳米球中包含有序的孔道,这些MOF纳米球的微孔和中孔的存在可以增强材料的传质过程,在气体分离和催化中具有潜在的应用。
1.2 一维MOF材料的合成
一维(1D)体系结构由于具有良好的一维导向通道, 能够为电子传递和离子扩散提供便利等特性,近年来受到了研究人员的广泛关注[38]。此外,组织良好且紧密排列的MOF阵列可改善电导率,增强电化学活性表面积,在电催化领域的应用中展现出较大的潜力。目前,1D MOF的合成方法主要有2种:模板合成和无模板合成。
1.2.1 模板合成模板法可以有效的控制纳米材料合成的尺寸和组成[39],被广泛应用于一维材料的合成。近年来,已经报道了多种利用模板法合成的一维纳米材料,如模板水热法合成1D分层空心Co3O4纳米管、电沉积模板合成单晶铜纳米线以及碲纳米线等[40-42]。早在1994年,MARTIN和同事就利用轨迹蚀刻聚碳酸酯(PCTE)膜作为硬模板合成聚合物、1D金属和无机材料[33-45]。最近,ARBULU等发现使用轨道蚀刻聚碳酸酯膜,可以通过改变模板孔的大小和反应物的类型或浓度来定制ZIF-8 1D纳米结构和超结构,从而形成独特的形态[46]。通过轨迹蚀刻聚碳酸酯(PCTE)膜为模板,Zn(NO3)2·6H2O和2-甲基咪唑为反应物界面合成,在100 nm膜孔内形成了多晶沸石咪唑盐骨架(ZIF-8)纳米棒ZIF8-100-N(图 2(a),图 2(d)),当用Zn(Ac)2代替Zn(NO3)2·6H2O反应时,形成了ZIF8-100-A纳米管(图 2(b),图 2(e)),这可能是由于PCTE孔内ZIF-8晶体的生长速率降低所致。此外,使用具有30 nm较小孔尺寸的PCTE膜为模板,则制备出了单晶ZIF8-30-N纳米线(图 2(c),图 2(f)),纳米线结构的形成可能归因于PCTE通道中表面张力的增加,这导致小的ZIF-8种子快速溶解和重结晶,从而在单个通道中形成了大而稳定的晶体种子。这个发现为控制MOF纳米材料的尺寸,形态和晶格取向提供了一种通用方法。
 |
| 图 2 ZIF8-100-N纳米棒, ZIF8-100-A纳米管和ZIF8-30-N纳米线的TEM像和SAED像[46] Fig. 2 TEM images and SAED images of ZIF8-100-N nanowires, ZIF8-100-A nanowires and ZIF8-30-N nanowires[46] |
这种硬模板合成法通常需要在模板上进行特定的表面修饰,从而限制MOF在模板表面上的生长,但是即使如此,也不能防止MOF在溶液中的直接成核和生长。相比之下,基于金属氧化物或氢氧化物纳米结构的自模板合成策略也是一种有效可控的合成方法。因为金属氧化物或氢氧化物模板可以通过牺牲自身来提供金属离子,使MOF固定生长而无需进行任何表面修饰。Zhan等基于自我模板策略成功合成了具有核-壳结构的ZnO@ZIF-8纳米棒,其中ZnO纳米棒不仅充当模板,而且还提供用于形成ZIF-8的Zn2+[47]。实验表明,溶剂组成和反应温度对ZnO @ ZIF-8纳米棒的良好控制至关重要,因为它们都对ZnO纳米棒的溶出速率和2-甲基咪唑与释放的Zn2+离子的配位速率之间的平衡有很大影响。同时,ZnO在金属氧化物中具有最丰富的纳米形态(纳米棒、纳米带、纳米环等),可以通过类似的合成方法获得更多的ZnO @ ZIF-8异质结构。因此,这种自我模板合成策略为合成与MOF相关的核-壳异质结构开辟了一条新途径。
1.2.2 无模板合成尽管模板方法具有广泛的适用性,但繁琐的模板合成和移除模板的步骤阻碍了其大规模应用。近年来,“芯片实验室(Lab on a chip)”设备用于合成一维纳米结构已成为合成化学家的关注点。与传统方法相比,当缩小微反应器中的尺寸时,将显示出卓越而独特的性能。PUIGMART?魱S等提出了在微流体环境中利用界面化学制备一维聚合物纳米线的方法(图 3)[48]。PUIGMART?魱S通过将反应物溶液平行注入微流体芯片中,形成层流的反应物溶液,使MOF的成核和生长限制在纳米级的通道界面中,从而实现对反应界面区域的控制,成功合成了Cu-Asp、Ag(l)-Cys和Zn(Ⅱ)-4, 40-bipy 3种纳米线。除此之外,添加配位调节剂指导MOF的成核和生长过程也是一种简单有效的方法。PACHFULE等使用水杨酸作为调节剂稳定MOF晶体表面上的活性金属位点,使MOF以棒状形态生长,但当未加入水杨酸时,形成了微晶MOF-74[49]。除水杨酸外,乙酸和多金属氧酸盐[50-51]也可作为调节剂控制MOF合成。
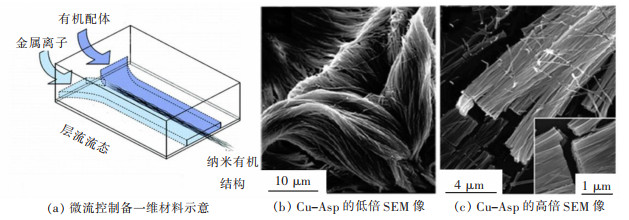 |
| 图 3 微流控制备纳米线的示意和Cu-Aps的SEM像[48] Fig. 3 Schematic diagram of microfluidic preparation of nanowires and SEM image of Cu-Aps[48] |
1.3 二维MOFs材料的合成
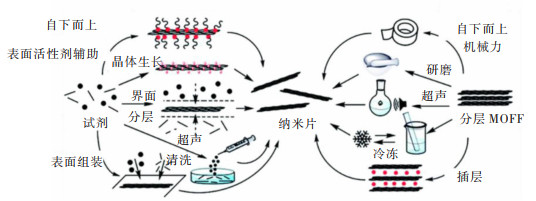
二维材料独特的各向异性和电子特性就引起了人们对其在电化学等领域应用的极大兴趣[52]。其中,二维MOF纳米材料由于其可调的孔位结构和功能,高度有序的空洞排列及大的比表面积提供的活性位点。特别是厚度为几纳米的二维MOF材料不仅可以提供快速的电子转移通道,还由于具有较大的比表面积和有效活性位点而提高了材料的性能。目前合成二维MOF材料的方法主要分为自上而下和自下而上2种方法(图 4)[53]。
1.3.1 自上而下合成法
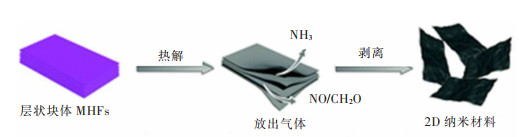
自上而下合成方式主要通过施加一个机械力(如超声处理或电化学手段)将分层的MOFs剥离为单层或少层的纳米片。2008年,NIELSEN等首次报道了Zn(C12H14O4)在小的高极性分子溶液(如丙酮和乙醇)中分层。Zn(C12H14O4)在室温下超声处理约3 h,伴随着丙酮的蒸发,可以观察到重新堆叠的层状化合物和分层的单层[54]。其中大多数颗粒的厚度约为2 nm,相当于2层。晶体学分析证明了金属有机化合物层之间的弱范德华键[55]。GALLEGO等仅通过将层状MOF[Cu(μ-pym2S2)(μ-Cl)]n·nY(其中Y可以是甲醇、水和乙醇)浸入在水中进行完全分层[56]。这种现象是由于这种MOF结构层与层之间的相互作用和空腔较弱,夹层腔可被溶剂分子填充,从而以简单且可重复的方式产生分层。这种方法比传统的剥离法所获得的片层更加均匀,并能获得更大更完整的薄片。除此之外,Liu等发现层状金属-六胺(HMT)可以进行热剥离,并同时转化为二维碳基纳米材料[57]。在快速的加热过程中,HMT的部分分解会产生大量的气体(如NH3, NO等),从而破坏HMT中的氢键,实现剥离(图 5)。
在实际应用中,自上而下法利用超声辅助和电化学手段来对层状的MOF进行分层确实是一种简单可行的方法,但也具有明显的缺点。超声所施加外力无法精确调控所获得MOF纳米片的大小尺寸,除此之外,在剥离过程中,剥离的单层或少层MOF会出现碎裂或者重新堆叠等问题,使得到的MOF纳米片的厚度难以控制。
1.3.2 自下而上法与自上而下法不同,自下而上法是有机配体和金属点反应直接合成二维MOFs纳米片。自下而上法主要通过限制配位聚合物在一个方向上的生长或通过限制/抑制合成过程中的结晶层间相互作用来实现MOF NS的合成[58],如利用表面活性剂或基材限制MOF晶体的生长方向。Zhao等开发了一种简便的表面活性剂辅助合成法来制备一系列厚度小于10 nm的超薄二维M-TCPP(M = Zn,Cu,Cd或Co,TCPP =四(4-羧基苯基)卟啉)纳米片[59]。实验中,在表面活性剂聚乙烯吡咯烷酮(PVP)的存在下,PVP选择性的附着在MOF的表面上,限制MOF沿着垂直方向生长,从而获得了稳定的超薄二维纳米片。除此之外,十六烷基三甲基溴化铵(CTAB)[60-61]和N, N-二甲基甲酰胺(DMF)[62]也可以作为表面活性剂调控二维MOF纳米片的合成。
除采用表面活性剂辅助合成二维MOF纳米片外,利用液体/液体或液体/空气界面来限制MOF纳米片的生长的界面合成法也是近来被广泛应用的方法。Li等通过使用自下而上的溶剂热法在不同溶剂中合成了厚度只有几个原子层的Ni-M-MOF NSs(M=Fe,Al,Co,Mn,Zn和Cd)[63]。如图 6(a)所示,当仅用水作溶剂时,会生成装饰有纳米颗粒的无定形纳米花;当仅用DMAC作溶剂时,制备的粉末具有多孔蓬松的形态(图 6(b));在DMAC和水的混合溶剂中,水通过占据金属有机配合物每一层表面上的金属配位部位,限制配位聚合物的生长,从而合成了超薄的MOF NS(图 6(c))。这一结果也说明了只有对有机配体具有良好溶解性的溶剂才能实现Ni-Fe-MOF NS的合成。但如果要合成超薄或者是单层的MOF纳米片,液/气界面合成法的适用更加广泛。作为一个典型的例子,MAKIURA等报告了在液/气界面合成Co-TCPP纳米片。MAKIURA将含有Co-TCPP配体和吡啶的氯仿和甲醇的混合物分散在Langmuir-Blodgett(LB)槽中的CuCl2·H2O溶液[64]。为了确保配体的单层分散,水的表面没有被完全覆盖。等到氯仿和甲醇蒸发后,2个阻隔壁开始压缩表面的配体,形成一个密堆积的配体单层(图 6(d))。最后,通过Cu2+与Co-TCPP配体的配位,在水/空气界面形成了单层Co TCPP-Cu纳米片。这种方法通过在水/空气界面合成的单层Co TCPP-Cu纳米片的逐层过渡,可以制备出很少的MOF纳米片。此外,他们还使用这种方法通过改变有机配体来合成其他MOF纳米片,如TCPP-Cu, ZnTPyP等[65-66]。
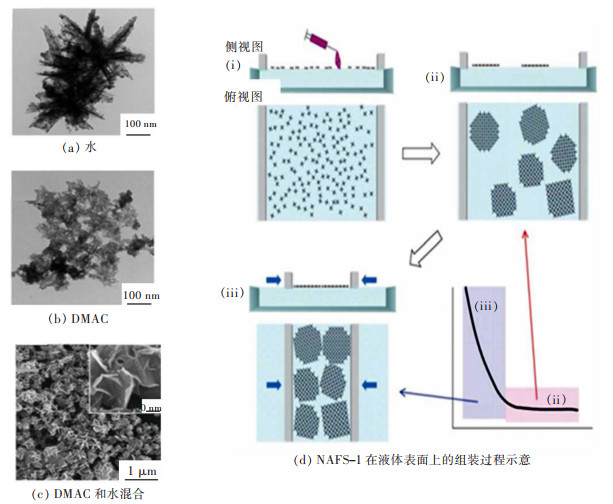 |
| 图 6 不同溶剂条件下合成的Ni-Fe-MOF NSs的TEM和NAFS-1组装示意[63-64] Fig. 6 TEM images of Ni-Fe-MOF NSs synthesized under different solvent conditions and assembly diagram of NAFS-1[63-64] |
近年来,二维MOF材料由于其独特的尺寸和超薄特性,在各种环境和能源领域展现出巨大的应用前景。尽管人们通过研究改进自上而下和自下而上等方法促进二维MOF纳米片的合成,但仍然存在很多关键性问题,其中最大的挑战就是二维MOF材料的合成和表征。二维MOF材料的合成极易受到到初始环境条件、生长方式以及金属离子和有机配体的选择等问题的制约。除此之外,MOF纳米片由于结构稳定性差在酸性或碱性溶液中不能长期稳定的存在,这也大大的限制了它们的应用。因此,改进MOF纳米片的合成方法,提高其分散性和电导率是我们迫切需要解决的问题。经过多次实验表明,上述的设计和合成方法有效的改善了MOF存在的稳定性差和活性位点暴露不足等问题。
2 过渡金属电催化剂分类Pt是HER活性最高的催化剂,Ir和Ru及其氧化物IrO2和RuO2是OER活性最高的电催化剂。特别是IrO2在酸性和碱性环境中都具有极好的催化性能[67-68]。但是贵金属材料存在成本高和稀缺等问题不能大规模的应用,因此,越来越多的研究者们开始寻找活性高,价格低廉的非贵金属催化剂来替代贵金属催化剂。
过渡金属(如Co,Ni和Fe基异质结构)在理论上具有较高的电催化活性,可作为有效的OER电催化剂。在过去的十余年间,过渡金属硫化物、硒化物、磷化物、硼化物等非贵金属基OER电催化剂被大量的研究及报道并取得了长足发展。总体而言,这些催化剂主要根据其金属组成进行分类,即Ni基、Fe基和Co基化合物。这些催化剂在析氧过电位、耐久性方面正趋接近甚至超越RuO2和IrO2等贵金属催化剂。然而,这些过渡金属催化剂在OER催化过程中会产生一些中间物(如M-OH、M=O和M-OOH, 其中M为催化活性中心),中间物的迅速降解为游离过渡金属离子导致分子催化剂稳定性变差,这也是过渡金属在OER中发展的主要障碍之一[69]。
2.1 Ni基催化剂Ni基材料,特别是Ni泡沫,通常用作碱性电解质中的商业电催化中的电极材料。除此之外,Ni的资源丰富且理论催化活性较高,作为电催化剂具有一定的优势。目前广泛研究的Ni基催化剂有Ni基氧化物、Ni基氢氧化物和基于Ni的钙钛矿氧化物。然而,作为催化剂,Ni的效率低且稳定性差。因此,用其他过渡金属和非金属元素掺杂Ni金属或其氧化物也是目前提高Ni基材料最常见的方法。
氧化镍作为一种资源丰富且不可缺少的半导体氧化物,已广泛应用于电池、超级电容器和电催化等方向。Zhang及同事通过阳离子交换方法在导电基体上原位制备了具有可调氧空位的NiO NR[70]。根据实验和理论结果,Zhang证明了在NiO NRs表面引入大量的O空位可增强电子传导并促进HER通路,从而使NiO NRs具有出色的碱性HER活性。2019年,Qiu等在NiO/NF掺入铁元素,使得Fe-NiO/NF电极对HER和OER的性能得到了很大的提高[71]。从拉曼光谱中发现,掺入铁有助于改变在施加电势下产生有益活性表面相的能力,从而导致在给定的超电势下催化活性增强。除此之外,EIS表征中,Fe-NiO/NF具有较低的电荷转移电阻,这是由于Ni和Fe在移动电位下生成羟基氧化物的协同元素效应。
除此之外,Ni(OH)2也具有较高的活性。Liu通过用N, O和S掺杂的碳泡沫的生长Ni(OH)2纳米片成功地设计了3D分层Ni(OH)2/NOSCF电极(图 7)[72]。实验发现,用约3.3 nm尺寸的CeO2 NP装饰的Ni(OH)2纳米片在NOSCF上表现出增强的OER性能。与Ni(OH)2/NOSCF相比,CeO2NP装饰的Ni(OH)2/NOSCF的起始电位从270 mV降至240 mV,Tafel斜率从65 mV/(°)降至57 mV/(°),比基准Ir/C好得多。OER性能增强归因于CeO2NP与Ni(OH)2纳米片之间的协同作用,并提供了有关稀土CeO2基纳米材料增强OER催化能力的见解。BABAR通过以泡沫镍为集流体和前体,使用简单且可扩展的热氧化方法在泡沫镍表面生长多孔氧化镍(NiO)[73]。由于骨架的支撑,以及不需要使用黏结剂,负载在泡沫镍表面的多孔氧化镍直接作为OER催化剂表现出良好的稳定性。
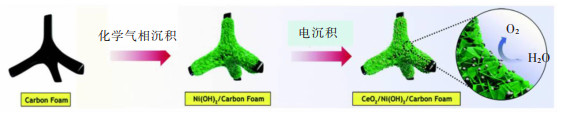 |
| 图 7 自支撑CeO2/ Ni(OH)2/ NOSCF电极的设计过程及在析氧反应中的应用[72] Fig. 7 Process for designing of self-supported CeO2/Ni(OH)2/NOSCF electrode and application for oxygen evolution reaction[72] |
含镍的钙钛矿氧化物因其低成本和高的OER活性而备受关注。钙钛矿型金属氧化物有一个通用的ABO3公式,其中“A”为稀土或碱金属离子,“B”点为过渡金属离子,因此, 具有调整电子结构和金属阳离子的灵活性、含氧空缺和过量的缺陷结构、优越的氧释放/吸收动力学等优点[74]。最近,ZENG及其同事合成了一系列Ruddlesden-Popper钙钛矿镍酸盐LanSrNinO3n+1(n=1、2、3和∞)以研究尺寸对OER的作用[75]。维数随n的增加,镍酸盐显示出增强的OER活性。研究人员发现,通过增加尺寸来减弱Ni 3d电子之间的电子相关性会导致绝缘体到金属的转变以及增强Ni-O的杂化,这两者都加速了OER动力学。这项工作为高效的析氧催化剂提供了指导。
2.2 Co基催化剂钴基OER催化剂由于其对环境友好、储量丰富、热稳定性好、成本低等原因,已被广泛用于研究在碱性环境中通过电催化过程进行的催化[76]。目前,最常见的Co基催化剂可分为尖晶石型氧化物,层状氢氧化物和钙钛矿氧化物[77]。
Co3O4作为典型的Co基尖晶石氧化物,其结构是围绕紧密排列的O2-离子阵列构建,Co2+和Co3+分别占据部分或全部的四面体和八面体空位。Co3O4的理化性能高度依赖与其组成,结构参数以及Co的氧化态和阳离子组成[78]。2D结构和多孔性质可以有效地为电化学反应提供更多的暴露活性位点,并促进了离子在整个薄片上的转移。Li等以氧化石墨烯为牺牲模版成功制备了多孔的Co3O4纳米片,显示出良好的电催化活性[79]。随后Xu等通过等离子刻蚀策略设计了一种高效的基于Co3O4的OER电催化剂(图 8),该催化剂在二维Co3O4纳米片表面产生了更多的Co2+氧空位,并增加了Co3O4表面积确保了具有更多的OER位置[80]。Co3O4表面上产生的氧空位改善了电子电导率并为OER产生了更多的活性缺陷。与原始的Co3O4相比,等离子刻蚀的Co3O4纳米片具有更高的电流密度和更低的启动电位。
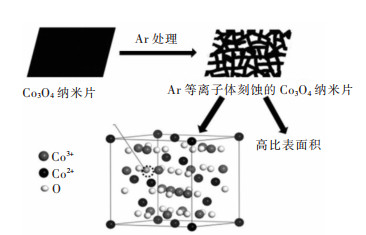 |
| 图 8 具有氧空位和高表面积的Ar等离子体刻蚀Co3O4的合成示意[80] Fig. 8 Illustration of the preparation of the Ar-plasma-engraved Co3O4 with oxygen vacancies and high surface area [80] |
除此之外,一维Co3O4纳米线作为OER电催化剂也获得了显著的关注。与Co3O4颗粒和薄膜相比,一维Co3O4纳米线具有较大的界面面积、高效的活性位点和优异的传质性能[81]。Xu等合成了3种用于氧释放反应(OER)的不同形态的Co3O4电极。通过比较Co3O4的3种形态,电催化性能表明,Co3O4电极的海胆状球具有较低的过电势和良好的电催化稳定性,表明海胆状Co3O4球的结构显示出易于水分解的OER[82]。
众所周知,由于Co(OH)2和基于Co的层状双氢氧化物中的Co处于氧化物态,因此具有较大OER潜力。Co(OH)2具有2种多晶型物,即α和β有Co(OH)2。β形式与水镁石样化合物是同构的,由六边形的氢氧根离子组成,其中Co(II)占据了八面体空隙位置[83-84]。不仅如此,由于β形式比α形式的结构稳定性更好,它经常被选作有希望的电化学催化剂候选者[85]。ZHANG等以液态金属为介质,报道了一种新颖的涂漆-脱合金策略在Co板上合成了柔性、自支撑的六角形β-Co(OH)2纳米片阵列[86]。β-Co(OH)2/Co不含任何黏合剂和导电剂、具有独特的超薄纳米片形态和开放的阵列结构,在碱性电解液中具有出色的电催化活性和稳定性。除此之外,由于液态金属的优点,可以方便地设计和调节集成电极的图案和形状,而不会影响OER活性。
研究表明,降低钙钛矿中的电荷转移间隙或增加金属-氧共价、半导体氧化物的电子转移的能垒和含氧中间体的吸附强度,可以有效的改善OER动力学[87-88]。但是,减小这些钙钛矿的电荷转移间隙也会降低费米能级的绝对能级,这种变化会产生更多带负电荷的表面,从而导致更弱的氢氧化物亲和力,也就是对电解质中氢氧根离子的表面反应性变弱。KUZNETSOV等在SrCoO3的A部位引入了高负电/路易斯酸性离子(Bi3+)元素,从而通过感应效应可以维持Co-O的高价态。对于Bi取代的SrCoO3,获得了25mV/(°)的异常低的Tafel斜率[89]。这归因于通过引入Bi3+可能增加了催化剂表面的氢氧化物亲和力,并促进了OER的动力学过程。除此之外,也有人报道了相关A位电负性对催化中所选钙钛矿活性的强烈影响[90]。
2.3 Fe基催化剂与Co和Ni相比,Fe具有使用成本低、毒性小等优点。因此,Fe基材料在作为电催化剂催化水分解具有一定的优势。但是,大多数铁氧化物为半导体材料,不适合直接作为催化剂进行催化。因此,一般情况下,Fe作为掺杂剂/杂质注入到Ni基和Co基催化材料中,显著改善其电催化性能。
目前,Fe和Ni的复合物催化剂是活性最好、最有前途的的贵金属替代催化剂,它们表现出非常低的过电位和较好的催化活性[91-92]。1987年,Corrigan发现在溶液中有极少量的Fe对Ni(OH)2的活性有极大的提高[93]。作者使用Moessbauer谱检测到,Fe(Ⅲ)的部分电子转移走能够形成部分的高价态,可能是在Ni(Ⅱ)的氧化过程中导致了高价态Fe的生成,对OER的活性有重要的作用。2017年,Wu等制备了由含有三价镍的超薄纳米片组装而成的分层Fe掺杂NiOx纳米管(图 9)[94]。发现在掺杂Fe后氧化镍的纳米结构中形成了Ni(Ⅲ)并出现了更多的氧空位,更有利于在催化过程中氧的吸附,制备的分层Fe掺杂NiOx纳米管对碱性电解质中的氧释放反应(OER)表现出显着的催化活性。随后, Yan等通过简单的水热法制备了不同量的Fe掺杂入三元NiCo2O4,经对比其他样品发现Fe0.5Ni0.5Co2O4的Tafel斜率更小,OER活性提高可能归因于三元混合金属(尤其是Fe掺杂)的协同效应[95]。Liang等将Fe掺入mCo3O4(Fe-mCo3O4)通过破坏整体介孔结构和形成狭缝状孔而产生不同寻常的协同效应。Fe-mCo3O4复合材料显示出显着增强的氧释放催化活性[85]。
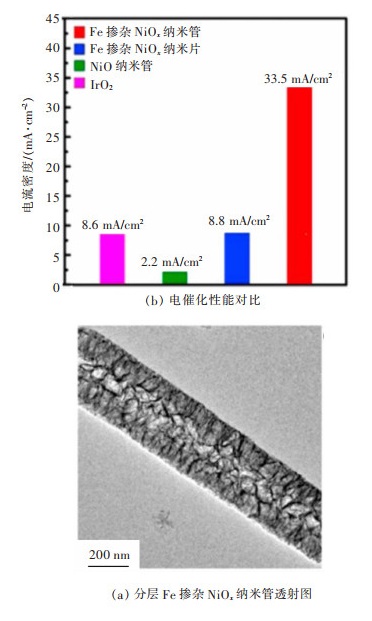 |
| 图 9 分层Fe掺杂NiOx纳米管透射图和性能测试对比图[94] Fig. 9 TEM images of the hierarchical Fe-doped NiOx nanotubes and performance test results[94] |
2.4 双金属催化剂
尽管贵金属/金属氧化物电催化剂可以显示出高电催化活性,但它们在电催化中的应用受到其高成本和稀有性的限制。为了提高效率并增加其大规模应用可能性,目前,已经进行了很多工作来开发双金属催化剂,因为它们具有丰富的氧化态和结构以及协同作用产生的优势。
LIM及其同事[96]使用简单的水热方法并随后H2还原成功地制备了二元NiFe合金纳米颗粒。然后将纳米颗粒用作OER的电催化剂。与一元Ni或Fe相比,二元NiFe合金电催化剂在10 mA/cm2的电流密度下表现出低得多的298 mV,并且对OER的电催化活性优于最先进的RuO2和IrO2贵金属氧化物催化剂。而且,在1 000次循环伏安法测试之后,合金催化剂表现出显着的长期耐久性。这种卓越的电化学性能主要源于Fe掺入Ni元素的协同作用,从而改善了催化剂的电荷转移动力学和固有活性。这些结果为开发具有成本效益的高性能电催化剂作为能量存储的电极提供了途径。双金属氢氧化物(LDH)在催化中也表现出出色的性能,特别是NiFe LDH和CoFe LDH,通常表现为层状的纳米片结构,具有丰富的活性位点和稳定性,其金属离子之间的协同作用也使得电催化性能比单金属氢氧化物有很大的提高。YANG等通过简便的水热和电沉积方法,合成了一种新型的CoFe层状双氢氧化物与负载在泡沫镍上的NiFe-LDH纳米片阵列耦合(表示为CoFe@ NiFe/NF),所得的CoFe@NiFe/NF结构催化剂对OER和HER都表现出出色的活性和稳定性(图 10)[97]。此外,使用CoFe@NiFe/NF作为催化剂在10 mA/cm2的电流密度下可达到1.59 V的电压,优于许多其他现有的电催化剂。
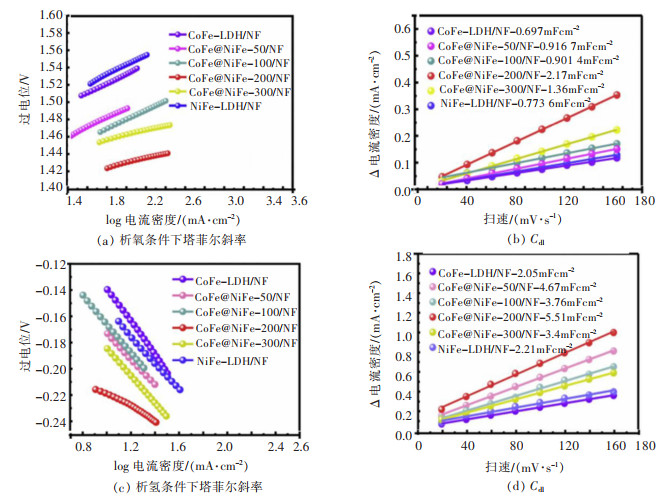 |
| 图 10 不同CoFe @ NiFe / NF在OER和HER下的性能测试[97] Fig. 10 Performance test of different CoFe@NiFe/NF under OER and HER[97] |
综上所述,过渡金属材料作为出色的电催化剂,在催化过程中优异的性能通常不是建立在材料本身,而是取决于在不同环境下对过渡金属基的合理和精心设计。因此,如何获得高效率电催化剂是我们急需解决的问题。研究者们开发了各种方式来提升电催化剂的性能,如通过创建更多活性位点,最大限度地利用活性中心,调节电子结构,提高电导率,以及控制材料的不同晶格面等,经实验证明,对于不同的电化学应用,对材料合理的设计合成可以显著促进催化效率的提升。
3 过渡金属基MOFs作为催化剂在电解水方面的应用 3.1 过渡金属基MOF直接作为催化剂在电解水方面的应用金属有机骨架(MOF)由于其高孔隙率和热稳定性而不同于其他传统的多孔材料。由三维构成MOF是无机金属离子和有机配体的结晶组装体,可实现灵活的结构设计,通过选择不同的结构单元可以定义明确的孔径,表面积和功能。MOFs属性的高度可调控性吸引了许多研究人员的兴趣。目前为止,已经有超过20 000多种不同的MOF结构被报告和研究。如图 11是目前应用较多的MOF结构示意图[98]。
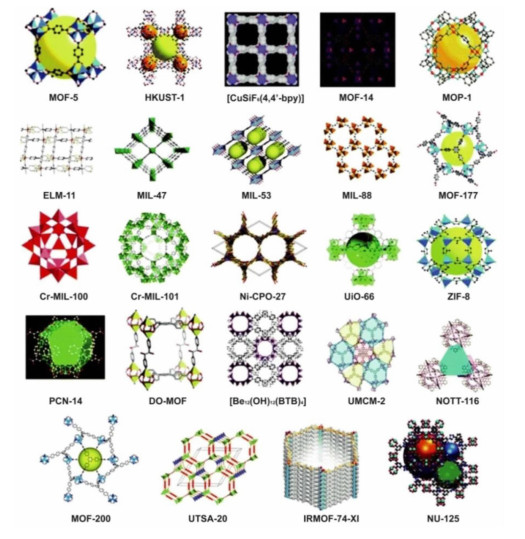 |
| 图 11 不同研究小组合成的不同MOF的纳米孔结构插图[98] Fig. 11 Illustration of nanoporous structures of different MOFs synthesized by different research groups[98] |
3.1.1 MOF中加入黏结剂后负载到电极上
对于直接作为催化剂进行OER催化的材料有2种催化方式,一是将制备好的MOF材料加入黏结剂后负载到导电电极上;另一种是将MOF材料原位生长在导电基体上直接作为催化剂进行反应。由于MOF材料虽具有多孔性有利于分子在材料中进行质子交换,但孔径过小对质子交换具有一定的限制,因此要选择合适孔径的MOF材料进行催化。
Wang等采用铁盐和钴盐为金属离子前体,均苯三酸为有机配体,通过水热法合成了混合金属离子金属有机骨架(MOF(Fe/Co)),所制备的MOF(Fe/Co)具有良好的晶体结构,具有丰富的微孔,较高的比表面积和较高的热稳定性[99]。(MOF(Fe/Co))对OER和ORR具有出色的双功能催化活性。高比表面积和丰富的微孔有利于氧扩散和催化剂中催化位点的利用,这对于OER和ORR是有利的。最近,Rui等通过将电化学惰性的Fe-MOF纳米颗粒引入到活性2D MOF纳米片上,可以显着提高对水氧化催化的催化活性(图 12(a))[100]。Rui将Fe-MOF纳米颗粒引入到Ni-MOF上,在电流密度为10 mA/cm2时,最低过电势为265 mV,优于最先进的OER催化剂IrO2(365 mV)图 12(c)。从图 12(b)可以看出,单纯的Fe-MOF对水氧化反应呈惰性,而与Fe-MOF的杂交可将Ni-MOF(370 mV)的过电势显着降低。此外,Ni-MOF @ Fe-MOF混合体(82 mV/(°))的相应Tafel斜率也低于Ni-MOF(139 mV/(°))和IrO2(158 mV/(°))的Tafel斜率(图 12(d)、图 12(e)),这表明杂交后显着增强的催化反应动力学。除了Ni活性中心和Fe物种之间的2D纳米片形态和协同作用外,杂化MOF在OER期间被原位转化为氧化物纳米粒子,充当了真正的活性中心以及多孔纳米片催化剂的组成部分。随后,Rui制备的活性NiCo-MOF纳米片中也成功证明了类似的性能改进,这项工作为了解基于MOF的水氧化催化催化剂提供了新的见解,也为开发高效的MOF衍生的纳米结构用于电催化开辟了一条新途径。
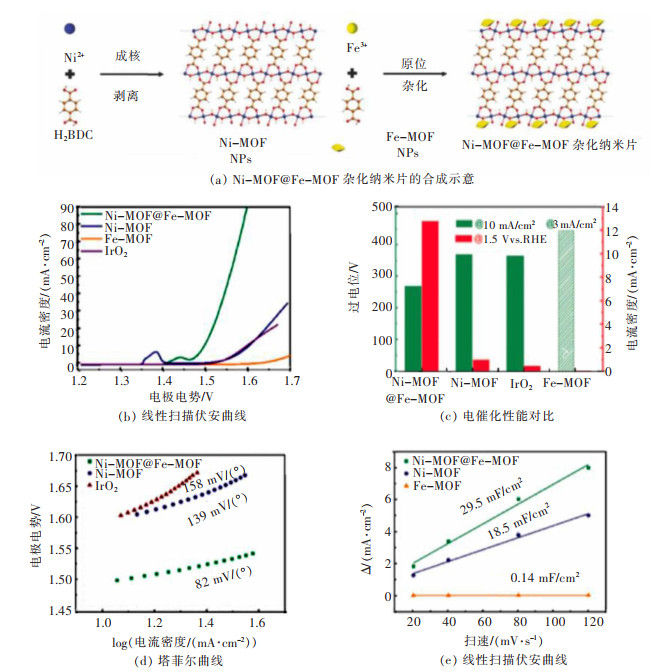 |
| 图 12 Ni-MOF@Fe-MOF杂化纳米片的合成示意和电催化性能测试[100] Fig. 12 Schematic illustration of synthesis of Ni-MOF@Fe-MOF hybrid nanosheets and summary of electrocatalytic performance test[100] |
与单金属催化剂相比,双金属催化剂或多金属催化剂由于不同元素之间的协同作用而具有增强活性和和稳定性潜力。基础研究和理论计算已经证明,引入多种元素应该会显著改善电荷转移以及优化催化剂表面电子结构[101-102]。MOF前体能够相对简单地制造具有可控金属组成的多金属材料。最近,Zhang和同事[103]通过自组装策略设计了普鲁士蓝类似物前体,并通过后硒化方法将其转化为(Fe-Co)Se2。得益于MOFb本身独特的多孔形态,较高的电化学活性表面积和快速的电子转移能力,获得的(Fe-Co)Se2催化剂具有优异的OER和HER性能,其在OER过程中仅需要251 mV的过电位即可达到10 mA/cm2的电流密度,而HER在10 mA/cm2的电流密度下达到90 mV。(Fe-Co)Se2具有高电化学活性,同时具有长期耐用性,这种催化剂的研究可能会鼓励研究者们在可再生能源技术方面进行更实际的催化应用。
3.1.2 MOF原位生长到导电材料上将MOF材料原位生长在导电材料上直接作为电极催化是MOF直接作为催化剂的另一种方式。为提高MOF的导电性、稳定性和电化学性能,很多研究者选择以导电性良好的材料如(泡沫镍、铜网、碳膜等)为基底在上面原位生长MOF材料。Zhang等已经通过水热处理Fe3+和对苯二甲酸溶液成功地合成了NF上的Fe MOF纳米片阵列[104]。这样的Fe-MOF/NF在1 mol/L KOH中对OER表现出优异的电催化性能,在50 mA/cm2下具有240 mV的低过电势和72 mV/(°)的小塔菲尔斜率。这项研究将为设计和利用MOF纳米阵列作为低成本的电化学水分解催化剂材料提供新的机会和传感应用。随后Xing等发现Fe2+/3+对泡沫镍刻蚀,释放出Ni2+参与反应(图 13)[105]。这种自支撑3D电极具有较大的电化学表面积,快速电荷转移能力和机械性能稳定性,除了得益于结构对其性能的影响外,NiFe之间的协同作用也是提高其电催化性能的原因。
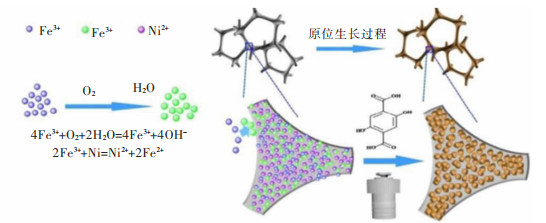 |
| 图 13 在泡沫镍上原位形成NiFe-MOF-74的示意[105] Fig. 13 Schematic diagram of in-situ NiFe-MOF-74 formation on nickel foam[105] |
最近,Duan等以泡沫镍为载体的NiFe-MOF阵列具有极好的OER催化能力。如图 14,当电流密度为10 mA/cm2时,NiFe-MOF的过电位为240 mV是目前活性最高的的双功能催化剂[106],Tafel仅为45 mV/(°)。不仅如此,通过对NiFe-MOF长时间的计时安培测试发现,NiFe-MOF还具有出色的稳定性。对于如此优异的电化学性能,作者认为归功于Ni-Fe的协同作用和该MOF的结构特点包括优异的导电性、亲水性和多孔性。
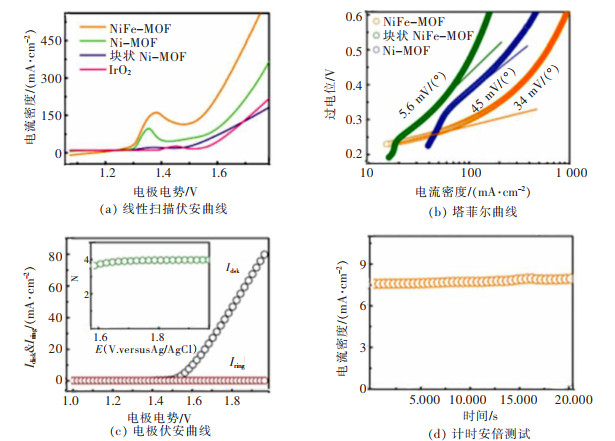 |
| 图 14 NiFe MOF在0.1 mol/L KOH电解液下OER性能汇总[106] Fig. 14 Summary of OER performance of NiFe-MOF in 0.1 mol/L KOH electrolyte[106] |
对于目前的MOF直接作为电催化剂的研究,主要是集中在制备NiFe双金属有机框架催化剂,而Ni一般被认作是活性位点起主要作用。在阳极析氧过程中,MOF内部的MO6会被氧化成MO6/MOOH(M为过渡金属)一起作为活性物质参与催化反应。因此,双金属材料参与催化的主要活性位点是什么还有待进一步研究。
3.2 过渡金属基MOF衍生材料在电解水方面的应用MOF具有纳米级孔和开放通道,可以为小分子进入提供结构条件,因此,有潜力用作合成纳米多孔碳材料的模板[107]。在过去的几年中,MOF已被广泛地用作制备具有规则多孔结构的各种纳米材料的前体,从碳基材料到金属基材料,例如氧化物、碳化物、硫族化物和磷化物等[108-110]。经多年研究发现,使用MOF作为制备各种纳米结构的前体/牺牲模板的一些优势[111]:①通过MOF的受控煅烧,可以制造具有所需拓扑结构和材料特性的MOF衍生纳米结构;②使用MOF作为模板,可以减少煅烧过程中框架的不良结构塌陷,因为它们通常显示出结构坚固性;③易于与其他杂原子和金属/金属氧化物进行功能化,因此能够提高整体性能和效率;④MOF可以在温和的条件和简单的过程中进行制备。
MOF衍生材料的纳米材料得益于MOF材料本身形貌的保持,由于具有高的BET表面,它们呈现出高密度的活性位点,因此可以作为出色且耐用的多相催化剂、助催化剂或催化剂载体,从而应用于各种反应。早在2017年ZHAO等就对基于金属有机框架衍生的多相催化剂做了系统的分析和归纳[112]。在不同的环境下的应用,对于模板的选择尤为重要。
通常,某些MOF结构(例如Cu-BTC和MOF-5)在碳化过程中会塌陷,因此,不适宜作为模板来合成多孔纳米材料,而一些MOF结构(例如ZIF-8和ZIF-67)在提供指导模板来形成的模板方面效果更好。ZHU等通过简单的一系列低温煅烧(150,200,250,300,350,400,450 ℃)实现ZIF-67的部分脱枝,使ZIF-67的结构不会完全分解,从而形成一种类似ZIF-67的结构[113]。通过像差校正TEM和FTIR光谱发现,在350 ℃煅烧的ZIF-67表现出暴露的活性位点,大多数孔尺寸变大,这可能都与ZIF-67结构的部分脱枝有关。经测试,ZIF-67的OER性能表现出对煅烧过程的依赖性。Li等以ZIF-67为前驱体合成了嵌入纳米多孔碳中的钴纳米颗粒(PNC/Co)。虽然前驱体光滑的表面变得粗糙其尺寸明显缩小,热解产物基本保持了ZIF-67晶体的原始形态(如图 15),这可能与退火过程中有机成分的大量损失有关[114]。由此产生的PNC/Co在强碱性介质中对OER表现出很高的活性,达到在电流密度为10 mA/cm2时产生的很小过电位,对OER具有很高的法拉第效率。
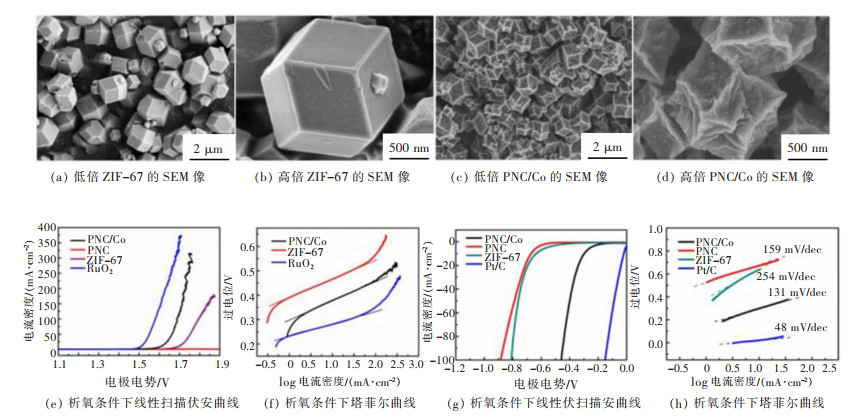 |
| 图 15 ZIF-67和PNC/Co的SEM图像及其电催化性能测试[114] Fig. 15 SEM images of ZIF-67 and PNC/Co and their electrocatalytic performance test drawings [114] |
除此之外,由于MOF易功能化的特点,CHENG等开发了一种原位非均相催化合成方法,用于通过将掺杂有Ni的氮掺杂碳(NC)纳米管接枝到金属有机骨架(MOF)衍生的碳基质上来构建分层的Ni /碳杂化体[115]。遵循原位催化合成过程中涉及的“纳米管尖端生长模型”,可以通过调节热过程中的条件来控制制备的分级镍基碳杂化物的纳米管和包封颗粒的形态和尺寸。这种方法使活性金属位点能够充分的暴露出来且不易团聚,同时,由于稳定的金属Ni活性位和N掺杂的碳载体的协同作用,在HER过程中,优化的Ni@NC6-600样品表现出稳定且高的催化活性,仅需181 mV的过电位即可在碱性介质中获得10 mA/cm2的电流密度。
但有时,各种MOF中的金属原子可能会聚集在一起碳化过程中容易形成不规则分布的大颗粒,在高温下会降低所得产物的电催化活性[116]。为了提高材料的活性,AMIINU等将三维ZIF纳米晶催化转化为具有优越电催化活性和高稳定性的一维Co-Nx/C纳米棒,具有出色的电催化活性和对OER的耐久性(图 16)[117]。一维Co-Nx/C纳米棒最初是由Zn2+团簇和甲基咪唑/ PVP配体的有机金属反应来制备ZIF纳米晶体,然后是纳米棒骨架的共催化结构发展。
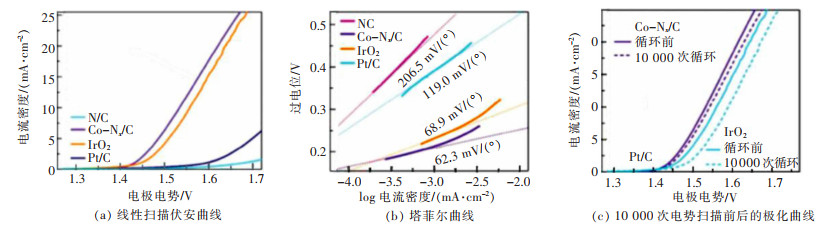 |
| 图 16 Co-Nx/C纳米棒的电催化性能测试[117] Fig. 16 Electrocatalytic performance test diagram of Co-Nx/C nanorods [117] |
MOF衍生的纳米材料具有独特的多维结构和可调功能性能,在OER方面能表现出极好的活性。同时,MOF衍生的纳米材料具有较低的成本和更好的稳定性。然而,对MOF衍生的金属/碳材料的制备及其在催化剂中的应用仍然存在许多关键问题和挑战需要解决。目前,制备MOFs衍生物的主要为热解,这种方法费时费力并且存在合成过程不稳定的现象,因此,开发一步合成或原位转化的方法对未来的研究具有重大的意义。除此之外,MOFs衍生物的稳定性较差,大多数MOFs衍生催化剂的结构都极易破坏,难以循环使用。因此,通过改进催化剂的合成方法、选择合适的有机配体和合适的热处理温度、减少分子团聚带来的不良影响,对未来MOF衍生纳米材料在电催化方面的应用具有重大的意义。从电催化的反应机制来讲,结构的稳定和较大的比表面积也能提供足够多的活性位点来提供场所进行反应。
4 结论近年来,过渡金属构建的MOFs和MOF的衍生材料已经成功的用作电解水的催化剂。与常规的催化剂类似,MOFs的结构空隙率,晶体尺寸和形态都是决定其电催化性能的非常重要的因素,但随着对MOFs的深入了解,对合成的MOFs在电催化方向的应用提出了一些要求:①高的催化活性和稳定性,可以更有效的促进反应物和产物的生成和分解;②高的比表面积和较大的孔结构,可以为反应提供更多的活性位点并保证合成气体的良好运输,有利于性能的提高;③良好的电子传导率。随着对MOFs研究的深入,根据应用环境尝试设计合成MOFs,用不同的方法合成零维、一维、二维MOFs及MOFs衍生材料,可以更大的暴露活性位点和扩大材料的孔隙,有效改善催化活性和稳定性。但同时,在合成和应用过程中也发现了一些问题:①低维的MOFs材料虽然在理论上具有更好的催化活性,但在催化反应中易于扩散并团聚;②双金属催化剂和MOFs的协同作用以及纳米孔结构的限域效应在作为催化剂表现出优异的性能,但催化机理尚不明确,还需进一步研究;③MOFs内单位点催化剂的精确控制仍难以完成,由于表征技术有限,单位点催化剂的精细表征难以实现;④MOF材料在很多情况下为粉末相,在催化时要滴铸在基材表面,在这种情况下,基于MOF的材料和基材表面通常显示出较弱的相容性,从而阻碍了电荷从催化剂表面向基材表面的转移,并削弱了电催化剂的稳定性,通常需要像Nafion溶液那样的黏合剂,在电子转移过程中会部分屏蔽活性位,因此,原位合成和沉积将MOFs用化学键固定在基材上,对未来研究具有很大的意义;⑤在工业应用中,电催化剂通常要在很苛刻的条件下进行反应,如高温和强碱性,实验室制备的材料很少提到关于在这种条件下表现出的活性和稳定性。
综上所述,目前,对于MOFs的研究还尚未进入成熟发展阶段,因而仍具有很大的发展空间。为了解决上述问题,我们可以进行以下研究:①对纳米级的结构和组成进行高度控制,调整纳米级的形貌,从而对尺寸进行调整;②开发原位和非原位表征技术以及理论计算来提供更多的实验数据,便于催化机理的进一步研究。这种有针对性的合成方式,使MOFs在各大领域都有广大的应用前景。总之,MOFs及其衍生材料在电催化领域的探索依然会是当前科研工作者的研究热点。
| [1] |
ABE J O, POPOOLA A P I, AJENIFUJA E, et al. Hydrogen energy, economy and storage: review and recommendation[J].
International Journal of Hydrogen Energy, 2019, 44(29): 15072–15086. DOI: 10.1016/j.ijhydene.2019.04.068. |
| [2] |
DAWOOD F, ANDA M, SHAFIULLAH G M. Hydrogen production for energy: An overview[J].
International Journal of Hydrogen Energy, 2020, 45(7): 3847–3869. DOI: 10.1016/j.ijhydene.2019.12.059. |
| [3] |
叶射稳, 彭文锟, 彭子扬, 等. 氮掺杂碳负载超细碳化钼析氢电催化剂[J].
有色金属科学与工程, 2020, 11(3): 33–38.
|
| [4] |
SUEN N T, HUNG S F, QUAN Q, et al. Electrocatalysis for the oxygen evolution reaction: recent development and future perspectives[J].
Chemical Society Reviews, 2017, 46(2): 337–365. DOI: 10.1039/C6CS00328A. |
| [5] |
JIA Y, ZHANG L, GAO G, et al. A heterostructure coupling of exfoliated Ni-Fe hydroxide nanosheet and defective graphene as a bifunctional electrocatalyst for overall water splitting[J].
Advanced Materials, 2017, 29(17): 1700017–1700023. DOI: 10.1002/adma.201700017. |
| [6] |
ABBAS S A, KIM S H, IQBAL M I, et al. Synergistic effect of nano-Pt and Ni spine for HER in alkaline solution: hydrogen spillover from nano-Pt to Ni spine[J].
Scientific Reports, 2018, 8(1): 2986–2994. DOI: 10.1038/s41598-018-21396-9. |
| [7] |
ZAGALSKAYA A, ALEXANDROV V. Role of defects in the interplay between adsorbate evolving and lattice oxygen mechanisms of the oxygen evolution reaction in RuO2 and IrO2[J].
ACS Catalysis, 2020, 10(6): 3650–3657. DOI: 10.1021/acscatal.9b05544. |
| [8] |
DA SILVA G C, FERNANDES M R, TICIANELLI E A. Activity and stability of Pt/IrO2 bifunctional materials as catalysts for the oxygen evolution/reduction reactions[J].
ACS Catalysis, 2018, 8(3): 2081–2092. DOI: 10.1021/acscatal.7b03429. |
| [9] |
HAN L, DONG S, WANG E. Transition-metal (Co, Ni, and Fe)-based electrocatalysts for the water oxidation reaction[J].
Advanced materials, 2016, 28(42): 9266–9291. DOI: 10.1002/adma.201602270. |
| [10] |
SUN H, YAN Z, LIU F, et al. Self-supported transition-metal-based electrocatalysts for hydrogen and oxygen evolution[J].
Advanced Materials, 2020, 32(3): 1806326–1806343. DOI: 10.1002/adma.201806326. |
| [11] |
ANDRES P P, KAI L N, KIERAN F. Supported transition metal phosphides: activity survey for HER, ORR, OER, and corrosion resistance in acid and alkaline electrolytes[J].
ACS Catalysis, 2019, 9(12): 11515–11529. DOI: 10.1021/acscatal.9b03359. |
| [12] |
XIAO X, ZOU L, PANG H, et al. Synthesis of micro/nanoscaled metal-organic frameworks and their direct electrochemical applications[J].
Chemical Society Reviews, 2020, 49: 301–331. DOI: 10.1039/C7CS00614D. |
| [13] |
翟睿, 焦丰龙, 林虹君, 等. 金属有机框架材料的研究进展[J].
色谱, 2014(2): 107–116.
|
| [14] |
YAGHI O M, LI G, LI H. Selective binding and removal of guests in a microporous metal-organic framework[J].
Nature, 1995, 378(6558): 703–706. DOI: 10.1038/378703a0. |
| [15] |
TIAN D, XU J, XIE Z J, et al. The first example of Hetero-triple-walled metal-organic frameworks with high chemical stability constructed via flexible integration of mixed molecular building blocks[J].
Advanced Science, 2016, 3(10): 1500283–1500283. DOI: 10.1002/advs.201500283. |
| [16] |
XU C, FANG R, LUQUE R, et al. Functional metal-organic frameworks for catalytic applications[J].
Coordination Chemistry Reviews, 2019(388): 268–292. |
| [17] |
DUAN C, YU Y, XIAO J, et al. Water-based routes for synthesis of metal-organic frameworks: A review[J].
Science China Materials, 2020, 63(5): 667–685. DOI: 10.1007/s40843-019-1264-x. |
| [18] |
MCCARTHY B D, BEILER A M, JOHNSON B A, et al. Analysis of electrocatalytic metal-organic frameworks[J].
Coordination Chemistry Reviews, 2020, 406: 213137–213157. DOI: 10.1016/j.ccr.2019.213137. |
| [19] |
WU Q, SIDDIQUE M S, YU W. Iron-nickel bimetallic metal-organic frameworks as bifunctional Fenton-like catalysts for enhanced adsorption and degradation of organic contaminants under visible light: Kinetics and mechanistic studies[J].
Journal of Hazardous Materials, 2020, 401: 123261–123304. |
| [20] |
SINGH DHANKHAR S, SHARMA N, KUMAR S, et al. Rational design of a bifunctional, two-fold interpenetrated ZnⅡ-metal-organic framework for selective adsorption of CO2 and efficient aqueous phase sensing of 2, 4, 6-trinitrophenol[J].
Chemistry-A European Journal, 2017, 23(64): 16204–16212. DOI: 10.1002/chem.201703384. |
| [21] |
CHEN S, LI Y, MI L. Porous carbon derived from metal organic framework for gas storage and separation: the size effect[J].
Inorganic Chemistry Communications, 2020, 118: 107999–108005. DOI: 10.1016/j.inoche.2020.107999. |
| [22] |
CHEN W H, VÁLEZ M, ZOABI A, et al. Biocatalytic cascades driven by enzymes encapsulated in metal-organic framework nanoparticles[J].
Nature Catalysis, 2018, 1(9): 689–695. DOI: 10.1038/s41929-018-0117-2. |
| [23] |
LUO H, ZENG Z, ZENG G, et al. Recent progress on metal-organic frameworks based- and derived- photocatalysts for water splitting[J].
Chemical Engineering Journal, 2020(383): 123196–123287. |
| [24] |
LU X F, XIA B Y, ZANG S Q, et al. Metal-organic frameworks based electrocatalysts for the oxygen reduction reaction[J].
Angewandte Chemie International Edition, 2019, 59(12): 4593–4969. |
| [25] |
DOWNES C A, CLOUGH A J, CHEN K, et al. Evaluation of the H2 evolving activity of benzenehexathiolate coordination frameworks and the effect of film thickness on H2 production[J].
ACS Applied Materials & Interfaces, 2018, 10(2): 1719–1727. |
| [26] |
GUO X, KONG R M, ZHANG X, et al. Ni(OH)2 nanoparticles embedded in conductive microrod array: an efficient and durable electrocatalyst for alkaline oxygen evolution reaction[J].
ACS Catalysis, 2017, 8(1): 651–655. |
| [27] |
GUO J, ZHANG X, SUN Y, et al. Loading Pt nanoparticles on metal-organic frameworks for improved oxygen evolution[J].
ACS Sustainable Chemistry & Engineering, 2017, 5(12): 11577–11583. |
| [28] |
LI D, XU H Q, JIAO L, et al. Metal-organic frameworks for catalysis: state-of-the-art, challenges, and opportunities[J].
Energy Chem, 2019: 100005–100043. |
| [29] |
LIBERMAN I, HE W, SHIMONI R, et al. Spatially confined electrochemical conversion of metal-organic frameworks into metal-sulfides and their in situ electrocatalytic investigation via scanning electrochemical microscopy[J].
Chemical Science, 2020, 11: 180–185. DOI: 10.1039/C9SC04141A. |
| [30] |
WEI X, ZHANG Y, HE H, et al. Carbon-incorporated porous honeycomb NiCoFe phosphide nanospheres derived from a MOF precursor for overall water splitting[J].
Chemical Communications, 2019, 55(73): 10896–10899. DOI: 10.1039/C9CC05225A. |
| [31] |
LI H, KE F, ZHU J. MOF-derived ultrathin cobalt phosphide nanosheets as efficient bifunctional hydrogen evolution reaction and oxygen evolution reaction electrocatalysts[J].
Nanomaterials, 2018, 8(2): 89–100. DOI: 10.3390/nano8020089. |
| [32] |
AHN S H, MANTHIRAM A. Direct growth of ternary Ni-Fe-P porous nanorods onto nickel foam as a highly active, robust bi-functional electrocatalyst for overall water splitting[J].
Journal of Materials Chemistry A, 2017, 5(6): 2496–2503. DOI: 10.1039/C6TA10509B. |
| [33] |
NI Z, MASEL R I. Rapid production of metal-organic frameworks via microwave-assisted solvothermal synthesis[J].
Journal of the American Chemical Society, 2006, 128(38): 12394–12395. DOI: 10.1021/ja0635231. |
| [34] |
FORSYTH C, TARAS T, JOHNSON A, et al. Microwave assisted surfactant-thermal synthesis of metal-organic framework materials[J].
Applied Sciences, 2020, 10(13): 4563–1572. DOI: 10.3390/app10134563. |
| [35] |
BUTOVA V V, VETLITSYNA-NOVIKOVA K S, PANKIN I A, et al. Microwave synthesis and phase transition in UiO-66/MIL-140A system[J].
Microporous and Mesoporous Materials, 2020, 296: 109998–110007. DOI: 10.1016/j.micromeso.2020.109998. |
| [36] |
ARENAS-VIVO A, AVILA D, HORCAJADA P. Phase-selective microwave assisted synthesis of Iron(Ⅲ) aminoterephthalate MOFs[J].
Materials, 2020, 13(6): 1469–1480. DOI: 10.3390/ma13061469. |
| [37] |
ZHAO Y, ZHANG J, HAN B, et al. Metal-organic framework nanospheres with well-ordered mesopores synthesized in an ionic liquid/CO2/surfactant system[J].
Angewandte Chemie International Edition, 2011, 50(3): 636–639. DOI: 10.1002/anie.201005314. |
| [38] |
董超振, 刘文兵, 王新东. 以阵列二氧化钛纳米棒为载体制备一体化析氧电极[J].
有色金属科学与工程, 2017, 8(2): 52–56.
|
| [39] |
陈彰旭, 郑炳云, 李先学, 等. 模板法制备纳米材料研究进展[J].
化工进展, 2010(1): 94–99.
|
| [40] |
YAO M, HU Z, XU Z, et al. Template synthesis of 1D hierarchical hollow Co3O4 nanotubes as high performance supercapacitor materials[J].
Journal of Alloys and Compounds, 2015, 644: 721–728. DOI: 10.1016/j.jallcom.2015.05.028. |
| [41] |
GAO T, MENG G W, ZHANG J, et al. Template synthesis of single-crystal Cu nanowire arrays by electrodeposition[J].
Applied Physics A, 2001, 73(2): 251–254. DOI: 10.1007/s003390100910. |
| [42] |
ZHANG W, WU Z Y, JIANG H L, et al. Nanowire-directed templating synthesis of metal-organic framework nanofibers and their derived porous doped carbon nanofibers for enhanced electrocatalysis[J].
Journal of the American Chemical Society, 2014, 136(41): 14385–14388. DOI: 10.1021/ja5084128. |
| [43] |
MARTIN C R. Nanomaterials: a membrane-based synthetic approach[J].
Science, 1994, 266(5193): 1961–1966. DOI: 10.1126/science.266.5193.1961. |
| [44] |
MARTIN C R. Membrane-based synthesis of nanomaterials[J].
Chemistry of Materials, 1996, 8(8): 1739–1746. DOI: 10.1021/cm960166s. |
| [45] |
MARTIN C R, PARTHASARATHY R, MENON V. Template synthesis of electronically conductive polymers-preparation of thin films[J].
Electrochimica Acta, 1994, 39(8-9): 1309–1313. DOI: 10.1016/0013-4686(94)E0052-2. |
| [46] |
ARBULU R C, JIANG Y B, PETERSON E J, et al. Metal-organic framework (MOF) nanorods, nanotubes, and nanowires[J].
Angewandte Chemie International Edition, 2018, 57(20): 5813–5817. DOI: 10.1002/anie.201802694. |
| [47] |
ZHAN W, KUANG Q, ZHOU J, et al. Semiconductor@ metal-organic framework core-shell heterostructures: a case of ZnO@ ZIF-8 nanorods with selective photoelectrochemical response[J].
Journal of the American Chemical Society, 2013, 135(5): 1926–1933. DOI: 10.1021/ja311085e. |
| [48] |
JOSEP PUIGMART-LUIS, MARTA RUBIO-MART NEZ, HARTFELDER U, et al. Coordination polymer nanofibers generated by microfluidic synthesis[J].
Journal of the American Chemical Society, 2011, 133(12): 4216–4219. DOI: 10.1021/ja110834j. |
| [49] |
PACHFULE P, SHINDE D B, MAJUMDER M, et al. Fabrication of carbon nanorods and graphene nanoribbons from a metal-organic framework[J].
Nature Chemistry, 2016, 8(7): 718–724. DOI: 10.1038/nchem.2515. |
| [50] |
WANG B, LIU W, ZHANG W, et al. Nanoparticles@nanoscale metal-organic framework composites as highly efficient heterogeneous catalysts for size-and shape-selective reactions[J].
Nano Research, 2017, 10(11): 3826–3835. DOI: 10.1007/s12274-017-1595-2. |
| [51] |
XU X, LU Y, YANG Y, et al. Tuning the growth of metal-organic framework nanocrystals by using polyoxometalates as coordination modulators[J].
Science China Materials, 2015, 58(5): 370–377. DOI: 10.1007/s40843-015-0053-2. |
| [52] |
李绍周, 黄晓, 张华. 有机或金属-有机二维纳米材料的制备与应用[J].
化学学报, 2015, 73(9): 913–923.
|
| [53] |
ASHWORTH D J, FOSTER J A. Metal-organic framework nanosheets (MONs): a new dimension in materials chemistry[J].
Journal of Materials Chemistry A, 2018, 6(34): 16292–16307. DOI: 10.1039/C8TA03159B. |
| [54] |
NIELSEN R B, KONGSHAUG K O, FJELLV G H. Delamination, synthesis, crystal structure and thermal properties of the layered metal-organic compound Zn (C12H14O4)[J].
Journal of Materials Chemistry, 2008, 18(9): 1002–1007. DOI: 10.1039/b712479a. |
| [55] |
EDDAOUDI M, MOLER D B, LI H, et al. Modular chemistry: secondary building units as a basis for the design of highly porous and robust metal-organic carboxylate frameworks[J].
Accounts of Chemical Research, 2001, 34(4): 319–330. DOI: 10.1021/ar000034b. |
| [56] |
GALLEGO A, HERMOSA C, CASTILLO O, et al. Solvent-induced delamination of a multifunctional two dimensional coordination polymer[J].
Advanced Materials, 2013, 25(15): 2141–2146. DOI: 10.1002/adma.201204676. |
| [57] |
LIU S, ZHOU J, SONG H. Thermal-exfoliated synthesis of N-rich carbon-based nanosheets from layered bulk crystals of a metal-hexamine framework[J].
Chemical Communications, 2018, 54(70): 9825–9828. DOI: 10.1039/C8CC04988B. |
| [58] |
杨凯, 董必亮, 李绍周, 等. 具有自支撑结构的有机二维纳米材料研究进展[J].
中国科学(技术科学), 2017, 47(1): 1–12.
|
| [59] |
ZHAO M, WANG Y, MA Q, et al. Ultrathin 2D metal-organic framework nanosheets[J].
Advanced Materials, 2015, 27(45): 7372–7378. DOI: 10.1002/adma.201503648. |
| [60] |
JUNGGEBURTH S C, DIEHL L, WERNER S, et al. Ultrathin 2D coordination polymer nanosheets by surfactant-mediated synthesis[J].
Journal of the American Chemical Society, 2013, 135(16): 6157–6164. DOI: 10.1021/ja312567v. |
| [61] |
XU Y, LI B, ZHENG S, et al. Ultrathin two-dimensional cobalt-organic framework nanosheets for high-performance electrocatalytic oxygen evolution[J].
Journal of Materials Chemistry A, 2018, 6(44): 22070–22076. DOI: 10.1039/C8TA03128B. |
| [62] |
CHOI E Y, BARRON P M, NOVOTNY R W, et al. Pillared porphyrin homologous series: intergrowth in metal-organic frameworks[J].
Inorganic Chemistry, 2009, 48(2): 426–428. DOI: 10.1021/ic801677y. |
| [63] |
LI F L, WANG P, HUANG X, et al. Large-scale, bottom-up synthesis of binary metal-organic framework nanosheets for efficient water oxidation[J].
Angewandte Chemie, 2019, 131(21): 7125–7130. DOI: 10.1002/ange.201902588. |
| [64] |
MAKIURA R, TSUCHIYAMA K, SAKATA O. Self-assembly of highly crystalline two-dimensional MOF sheets on liquid surfaces[J].
Cryst Eng Comm, 2011, 13(18): 5538–5541. DOI: 10.1039/c1ce05684k. |
| [65] |
MOTOYAMA S, MAKIURA R, SAKATA O, et al. Highly crystalline nanofilm by layering of porphyrin meta-organic framework sheets[J].
Journal of the American Chemical Society, 2011, 133(15): 5640–5643. DOI: 10.1021/ja110720f. |
| [66] |
MAKIURA R, KONOVALOV O. Bottom-up assembly of ultrathin sub-micron size metal-organic framework sheets[J].
Dalton Transactions, 2013, 42(45): 15931–15936. DOI: 10.1039/c3dt51703a. |
| [67] |
卢立新, 王新东. 石墨烯负载铂催化剂的制备及稳定性[J].
有色金属科学与工程, 2015, 6(3): 40–44.
|
| [68] |
TRASATTI S. Electrocatalysis in the anodic evolution of oxygen and chlorine[J].
Electrochimica Acta, 1984, 29(11): 1503–1512. DOI: 10.1016/0013-4686(84)85004-5. |
| [69] |
PARENT A R, SAKAI K. Progress in base-metal water oxidation catalysis[J].
Chem Sus Chem, 2014, 7(8): 2070–2080. DOI: 10.1002/cssc.201402322. |
| [70] |
ZHANG T, WU M Y, YAN D Y, et al. Engineering oxygen vacancy on NiO nanorod arrays for alkaline hydrogen evolution[J].
Nano Energy, 2018, 43: 103–109. DOI: 10.1016/j.nanoen.2017.11.015. |
| [71] |
QIU Z, MA Y, AND EDVINSSON T. In operando Raman investigation of Fe doping influence on catalytic NiO intermediates for enhanced overall water splitting[J].
Nano Energy, 2019, 66: 104118–104125. DOI: 10.1016/j.nanoen.2019.104118. |
| [72] |
LIU Z, LI N, ZHAO H, et al. Regulating the active species of Ni(OH)2 using CeO2: 3D CeO2/Ni(OH)2/carbon foam as an efficient electrode for the oxygen evolution reaction[J].
Chemical Science, 2017, 8(4): 3211–3217. DOI: 10.1039/C6SC05408K. |
| [73] |
BABAR P T, LOKHANDE A C, GANG M G, et al. Thermally oxidized porous NiO as an efficient oxygen evolution reaction (OER) electrocatalyst for electrochemical water splitting application[J].
Journal of Industrial and Engineering Chemistry, 2018, 60: 493–497. DOI: 10.1016/j.jiec.2017.11.037. |
| [74] |
GHOSH S, BASU R N. Multifunctional nanostructured electrocatalyts for energy conversion and storage: current status and perspectives[J].
Nanoscale, 2018, 10(4): 11241–11280. |
| [75] |
ZENG J, ZHOU S, CAO C, et al. Dimensionality control of electrocatalytic activity in perovskite nickelates[J].
Nano Letter, 2020, 20: 2837–3842. DOI: 10.1021/acs.nanolett.0c00553. |
| [76] |
HE J, PENG Y, SUN Z, ET AL. Realizing high water splitting activity on Co3O4 nanowire arrays under neutral environment[J].
Electrochimica Acta, 2014: 64–71. |
| [77] |
HAN L, DONG S, WANG E. Transition-metal (Co, Ni, and Fe)-based electrocatalysts for the water oxidation reaction[J].
Advanced Materials, 2016, 28(42): 9266–9291. DOI: 10.1002/adma.201602270. |
| [78] |
ZHANG N, FAN Y, FAN H, et al. Cross-linked Co3O4 nanowalls synthesized by electrochemical oxidation of metallic cobalt layer for oxygen evolution[J].
ECS Electrochemistry Letters, 2012, 1(2): 8–10. |
| [79] |
LI Z, YU X Y, PAIK U. Facile preparation of porous Co3O4 nanosheets for high - performance lithium ion batteries and oxygen evolution reaction[J].
Journal of Power Sources, 2016, 310: 41–46. DOI: 10.1016/j.jpowsour.2016.01.105. |
| [80] |
XU L, JIANG Q, XIAO Z, et al. Plasma-engraved Co3O4 nanosheets with oxygen vacancies and high surface area for the oxygen evolution reaction[J].
Angewandte Chemie International Edition, 2016, 55(17): 5277–5281. DOI: 10.1002/anie.201600687. |
| [81] |
LU B, CAO D, WANG P, et al. Oxygen evolution reaction on Ni-substituted Co3O4 nanowire array electrodes[J].
International Journal of Hydrogen Energy, 2011, 36(1): 72–78. DOI: 10.1016/j.ijhydene.2010.09.056. |
| [82] |
XU Q Z, XU Q Z, SU Y Z, et al. Effect of morphology of Co3O4 for oxygen evolution reaction in alkaline water electrolysis[J].
Current Nanoscience, 2014, 11(1): 107–112. DOI: 10.2174/1573413710666140925200938. |
| [83] |
MOCKENHAUPT C, ZEISKE T, LUTZ H D. Crystal structure of brucite-type cobalt hydroxide β-Co{O(H, D)}2— neutron diffraction, IR and Raman spectroscopy[J].
Journal of Molecular Structure, 1998, 443: 191–196. DOI: 10.1016/S0022-2860(97)00388-8. |
| [84] |
BENSON P, BRIGGS G W D, WYNNE-JONES W F K. The cobalt hydroxide electrode—I. Structure and phase transitions of the hydroxides[J].
Electrochim Acta, 1964, 9: 275–280. DOI: 10.1016/0013-4686(64)80016-5. |
| [85] |
LIANG H, RAITANO J M, ZHANG L, et al. Controlled synthesis of Co3O4 nanopolyhedrons and nanosheets at low temperature[J].
Chemical Communications, 2009, 48: 7569–7571. |
| [86] |
ZHANG J, DONG C, WANG Z, et al. Flexible, self-supported hexagonal β-Co(OH)2 nanosheet arrays as integrated electrode catalyzing oxygen evolution[J].
reaction. Electrochimica Acta, 2018, 284: 495–503. DOI: 10.1016/j.electacta.2018.07.182. |
| [87] |
HONG W T, STOERZINGER K A, LEE Y L, et al. Charge-transfer-energy-dependent oxygen evolution reaction mechanisms for perovskite oxides[J].
Energy & Environmental Science, 10(10), 10(10): 2190–2200. |
| [88] |
YAMADA I, TAKAMATSU A, ASAI K, et al. Synergistically enhanced oxygen evolution reaction catalysis for multielement transition-metal oxides[J].
ACS Applied Energy Materials, 2018, 1: 3711–3721. DOI: 10.1021/acsaem.8b00511. |
| [89] |
KUZNETSOV D A, PENG J, GIORDANO L, et al. Bismuth substituted strontium cobalt perovskites for catalyzing oxygen evolution[J].
The Journal of Physical Chemistry C, 2020, 124(12): 6562–6570. DOI: 10.1021/acs.jpcc.0c01401. |
| [90] |
HONG W T, WELSCH R. E, YANG S H. Descriptors of oxygen-evolution activity for oxides: a statistical evaluation[J].
The Journal of Physical Chemistry C, 2016, 120: 78–86. DOI: 10.1021/acs.jpcc.5b10071. |
| [91] |
TROTOCHAUD L, RANNEY J K, WILLIAMS K N, et al. Solution-cast metal oxide thin film electrocatalysts for oxygen evolution[J].
Journal of the American Chemical Society, 2012, 134(41): 17253–17261. DOI: 10.1021/ja307507a. |
| [92] |
LANDON J, DEMETER E, INOGLU N, et al. Spectroscopic characterization of mixed Fe-Ni oxide electrocatalysts for the oxygen evolution reaction in alkaline electrolytes[J].
ACS Catalysis, 2012, 2(8): 1793–1801. DOI: 10.1021/cs3002644. |
| [93] |
CORRIGAN D A. The catalysis of the oxygen evolution reaction by iron impurities in thin film nickel oxide electrodes[J].
Journal of The Electrochemical Society, 1987, 134(2): 377–384. DOI: 10.1149/1.2100463. |
| [94] |
WU G, CHEN W, ZHENG X, et al. Hierarchical Fe-doped NiOxnanotubes assembled from ultrathin nanosheets containing trivalent nickel for oxygen evolution reaction[J].
Nano Energy, 2017, 38: 167–174. DOI: 10.1016/j.nanoen.2017.05.044. |
| [95] |
YAN K L, SHANG X, LI Z, et al. Ternary mixed metal Fe-doped NiCo2O4 nanowires as efficient electrocatalysts for oxygen evolution reaction[J].
Applied Surface Science, 2017, 416: 371–378. DOI: 10.1016/j.apsusc.2017.04.204. |
| [96] |
LIM D, OH E, LIM C, et al. Bimetallic NiFe alloys as highly efficient electrocatalysts for the oxygen evolution reaction[J].
Catalysis Today, 2020, 352: 27–33. DOI: 10.1016/j.cattod.2019.09.046. |
| [97] |
YANG R, ZHOU Y, XING Y, et al. Synergistic coupling of CoFe-LDH arrays with NiFe-LDH nanosheet for highly efficient overall water splitting in alkaline media[J].
Applied Catalysis B: Environmental, 2019, 253: 131–139. DOI: 10.1016/j.apcatb.2019.04.054. |
| [98] |
YAP M H, FOW K L, CHEN G Z. Synthesis and applications of MOF-derived porous nanostructures[J].
Green Energy & Environment, 2017, 2(3): 218–245. |
| [99] |
WANG H, YIN F, LI G, et al. Preparation, characterization and bifunctional catalytic properties of MOF (Fe/Co) catalyst for oxygen reduction/evolution reactions in alkaline electrolyte[J].
International Journal of Hydrogen Energy, 2014, 39(28): 16179–16186. DOI: 10.1016/j.ijhydene.2013.12.120. |
| [100] |
RUI K, ZHAO G, CHEN Y, et al. Hybrid 2D dual-metal-organic frameworks for enhanced water oxidation catalysis[J].
Advanced Functional Materials, 2018, 28(26): 1801554–18015562. DOI: 10.1002/adfm.201801554. |
| [101] |
HUANG Z F, SONG J, LI K, et al. Hollow cobalt-based bimetallic sulfide polyhedra for efficient All-pH-value electrochemical and photocatalytic hydrogen Evolution[J].
Journal of the American Chemical Society, 2016, 138: 1359–1365. DOI: 10.1021/jacs.5b11986. |
| [102] |
WANG T, ZHOU Q, WANG X, et al. MOF-derived surface modified Ni nanoparticles as an efficient catalyst for the hydrogen evolution reaction[J].
Journal of Materials Chemistry A, 2015, 3: 16435–16439. DOI: 10.1039/C5TA04001A. |
| [103] |
ZHANG W, ZHANG H, LUO R, et al. Prussian blue analogues-derived bimetallic iron-cobalt selenides for efficient overall water splitting[J].
Journal of Colloid and Interface Science, 2019, 548: 48–55. DOI: 10.1016/j.jcis.2019.04.029. |
| [104] |
ZHANG X, LIU Q, SHI X, et al. An Fe-MOF nanosheet array with superior activity towards the alkaline oxygen evolution reaction[J].
Inorganic Chemistry Frontiers, 2018, 5(6): 1405–1408. DOI: 10.1039/C8QI00163D. |
| [105] |
XING J, GUO K, ZOU Z, et al. In situ growth of well-ordered NiFe-MOF-74 on Ni foam by Fe2+ induction as an efficient and stable electrocatalyst for water oxidation[J].
Chemical Communications, 2018, 54(51): 7046–7049. DOI: 10.1039/C8CC03112F. |
| [106] |
DUAN J, CHEN S, ZHAO C. Ultrathin metal-organic framework array for efficient electrocatalytic water splitting[J].
Nature Communications, 2017, 8: 15341–15347. DOI: 10.1038/ncomms15341. |
| [107] |
LIU B, SHIOYAMA H, AKITA T, et al. Metal-organic framework as a template for porous carbon synthesis[J].
Journal of the American Chemical Society, 2008, 130(16): 5390–5391. DOI: 10.1021/ja7106146. |
| [108] |
QIAN J, LI T T, HU Y, et al. A bimetallic carbide derived from a MOF precursor for increasing electrocatalytic oxygen evolution activity[J].
Chemical Communications, 2017, 53(97): 13027–13030. DOI: 10.1039/C7CC07853F. |
| [109] |
MING F, LIANG H, SHI H, et al. Hierarchical (Ni, Co) Se2/carbon hollow rhombic dodecahedra derived from metal-organic frameworks for efficient water-splitting electrocatalysis[J].
Electrochimica Acta, 2017, 250: 167–173. DOI: 10.1016/j.electacta.2017.08.047. |
| [110] |
WANG R, DONG X Y, DU J, et al. MOF-Derived bifunctional Cu3P nanoparticles coated by a N, P-codoped carbon shell for hydrogen evolution and oxygen reduction[J].
Advanced Materials, 2018, 30(6): 1703711–1703720. DOI: 10.1002/adma.201703711. |
| [111] |
XIA B Y, YAN Y, LI N, et al. A metal-organic framework-derived bifunctional oxygen electrocatalyst[J].
Nature Energy, 2016, 1(1): 15006–15013. DOI: 10.1038/nenergy.2015.6. |
| [112] |
ZHAO S N, SONG X Z, SONG S Y, et al. Highly efficient heterogeneous catalytic materials derived from metal-organic framework supports/precursors[J].
Coordination Chemistry Reviews, 2017, 337: 80–96. DOI: 10.1016/j.ccr.2017.02.010. |
| [113] |
ZHU R, DING J, YANG J, et al. Quasi-ZIF-67 for boosted oxygen evolution reaction catalytic activity via a low temperature calcination[J].
ACS Applied Materials and Interfaces, 2020, 12(22): 25037–25041. DOI: 10.1021/acsami.0c05450. |
| [114] |
LI X, NIU Z, JIANG J, et al. Cobalt nanoparticles embedded in porous N-rich carbon as an efficient bifunctional electrocatalyst for water splitting[J].
Journal of Materials Chemistry A, 2016, 4(9): 3204–3209. DOI: 10.1039/C6TA00223D. |
| [115] |
CHENG N, WANG N, REN L, et al. In-situ grafting of N-doped carbon nanotubes with Ni encapsulation onto MOF-derived hierarchical hybrids for efficient electrocatalytic hydrogen evolution[J].
Carbon, 2020, 163: 178–185. DOI: 10.1016/j.carbon.2020.03.017. |
| [116] |
TANG J, SALUNKHE R R, LIU J, et al. Thermal conversion of core-shell metal-organic frameworks: a new method for selectively functionalized nanoporous hybrid carbon[J].
Journal of the American Chemical Society, 2015, 137(4): 1572–1580. DOI: 10.1021/ja511539a. |
| [117] |
AMⅡNU I S, LIU X, PU Z, et al. From 3D ZIF nanocrystals to Co-Nx/C nanorod array electrocatalysts for ORR, OER, and Zn-air batteries[J].
Advanced Functional Materials, 2018, 28(5): 1704638–1704646. DOI: 10.1002/adfm.201704638. |
 2021, Vol. 12
2021, Vol. 12