| 硫代硫酸钠浸出贵州卡林型金矿 |
黄金,作为一种稀有且珍贵的金属,不仅是用于储备和投资的特殊通货,更是首饰业、电子业、航天航空业等多领域的重要材料[1-2]。随着全球金矿不断被开采,高品位、易选冶金矿资源日益枯竭,储量巨大的难处理金矿如卡林型金矿正逐渐成为黄金生产行业的重要原材料[3-5]。卡林型金矿,简称“微细浸染型金矿”,是一种在碳酸盐岩-碎屑岩形成过程中所生成的微细浸染型金矿床[6]。贵州省卡林型金矿资源储量丰富,具有很大的开发利用价值。目前,工业上一般采用氰化浸金法从卡林型金矿中提取黄金。氰化浸金法虽然具有成本低、综合回收率高、对矿石类型适用性广等多个优点[7],但该法对难处理金矿的提金效果比较差,受杂质因素干扰比较大,且生产过程中产生的大量含氰废水、废渣对人体和环境危害极大。随着我国绿色环保生产理念的不断推进,开发安全高效、绿色环保的非氰化浸金法已经成为黄金生产行业的研究热点。
目前,难处理金矿的非氰化浸金研究方法主要有硫脲法[8]、氯化法[9]、硫代硫酸盐法[10]、多硫化物法[11]和石硫合剂法[12]。相较于传统的氰化浸金法,硫代硫酸盐浸金法具有反应迅速、低毒高效、环境友好等诸多优点[13-18]。
本文设计并进行了硫代硫酸钠浸出贵州卡林型金矿的试验,研究了Na2S2O3浓度、乙二胺浓度、Cu2+浓度、Na2SO3浓度以及溶液pH值等不同因素对金浸出率的影响,探索硫代硫酸钠浸出贵州卡林型金矿的可行性。
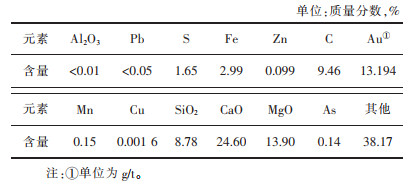
1 试验 1.1 试验原料试验所选用的金矿石均来自贵州省紫金矿业公司,金矿石表面呈深灰色,质地紧密,含金品位为13.194 g/t。将原矿石破碎、球磨、筛分至矿石粒度小于74 μm占92%后,混合烘干备用[9]。矿石的主要化学组成如表 1所列。
| 表 1 原矿化学成分分析结果 Table 1 Analysis results of chemical composition of raw ore |
 |
| 点击放大 |
1.2 试验试剂及仪器
试验使用的主要试剂:硫代硫酸钠、乙二胺、五水合硫酸铜、亚硫酸钠、氢氧化钠(以上试剂均为AR分析纯)。
试验使用的主要仪器:X’Pert PRO MPD型X射线衍射仪(荷兰帕纳科公司)、722型可见光分光度计(上海菁华科技仪器有限公司)、JJ-1型机械搅拌器(常州澳华有限公司)、DK-98-IIA型电子恒温水浴锅(天津泰斯特仪器有限公司)、SHZ-D(III)型循环水式多用真空泵(天津华鑫仪器厂)。
1.3 试验原理及方法在Cu2+-en-S2O32-体系的硫代硫酸盐浸金体系中,Cu2+和乙二胺结合形成化学性质稳定的乙二胺合Cu(Ⅱ)配离子,乙二胺中的2个N原子作为配位原子,可以同时与配位数为4的Cu2+配位,生成具有环状结构的螯合物Cu(en)22+[17]。Cu(en)22+又作为氧化剂,把金氧化成Au+,使之与体系中的S2O32-形成稳定的Au(S2O3)23-,如式(1)。在搅拌桨的作用下,空气中的O2将进入溶液当中,使Cu(en)2+迅速被氧化形成Cu(en)22+,Cu(en)22+又在黄金表面被还原,使得Cu2+被循环利用。
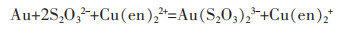
|
(1) |
试验流程:称取50 g矿样,分别按计量加入硫代硫酸钠、乙二胺、五水合硫酸铜、亚硫酸钠等物质,用氢氧化钠调节溶液pH,搅拌浸出一定时间后,抽滤,烘干,用硫代米蚩酮(TMK)分光光度法[9]测定金质量分数,从而计算得到金浸出率。
2 试验结果与讨论 2.1 Na2S2O3浓度对金浸出率的影响取矿样50 g,液固体积质量比5∶1(单位:L/g,下同),浸金液中乙二胺浓度为0.1 mol/L,Cu2+浓度为0.05 mol/L,Na2SO3浓度为0 mol/L,溶液pH值为9.5,室温(25 ℃)浸出4 h。依次调节Na2S2O3浓度分别为0.05,0.15,0.25,0.35,0.45 mol/L。Na2S2O3浓度对金浸出率的影响如图 1所示。
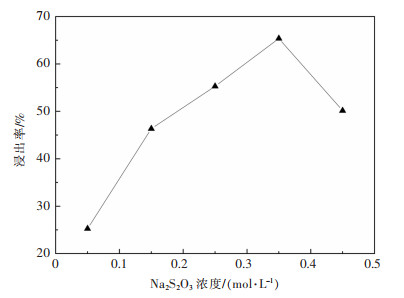 |
| 图 1 Na2S2O3浓度对金浸出率的影响 Fig. 1 The influence of Na2S2O3 concentration on gold leaching rate |
由图 1可知,随着Na2S2O3浓度增加,金浸出率先升高后降低,且当Na2S2O3浓度为0.35 mol/L时,金浸出率达到最高值65.36%。体系中的S2O32-会与Au形成稳定的络合物[Au(S2O3)2]3-,增加适量的硫代硫酸盐浓度,有利于反应正向移动,提高金浸出率[17]。
当体系中Na2S2O3浓度达到0.35 mol/L之后,继续增加Na2S2O3浓度,金浸出率不增反减。[Cu(en)2]2+在浸金过程中起氧化剂的作用,体系中过量的Na2S2O3会与[Cu(en)2]2+反应,造成[Cu(en)2]2+浓度下降,体系的氧化性减弱,最终导致金的浸出率降低。
综合考虑,在后续试验中Na2S2O3浓度取0.35 mol/L为宜。
2.2 乙二胺浓度对金浸出率的影响取矿样50 g,液固体积质量比5∶1,浸金液中Na2S2O3浓度为0.35 mol/L,Cu2+浓度为0.05 mol/L,Na2SO3浓度为0 mol/L,溶液pH值为9.5,室温(25 ℃)浸出4 h。依次改变乙二胺浓度分别为0,0.025,0.050,0.075,0.1,0.125 mol/L。乙二胺浓度对金浸出率的影响如图 2所示。
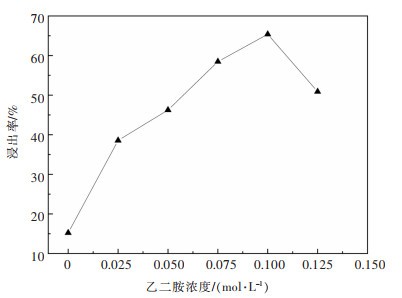 |
| 图 2 乙二胺浓度对金浸出率的影响 Fig. 2 Effect of ethylenediamine concentration on gold leaching rate |
由图 2可知,随着乙二胺浓度增加,金浸出率先升高后降低。当体系中不存在乙二胺时,金浸出率低至15.22%。此时的硫代硫酸盐由于没有乙二胺的干扰,会迅速在金颗粒表面分解生成一层元素硫膜,使金溶解钝化,阻碍金浸出[19]。
之后,随着乙二胺浓度增加,金浸出率也随之升高,且当体系中乙二胺浓度为0.1 mol/L时,金浸出率达到最高值65.36%。当体系中存在适量乙二胺时,乙二胺将优先吸附在金颗粒表面,阻止元素硫膜的生成,并与金发生络合反应,将之带入溶液。随后,Au(en)+将与S2O32-反应生成Au(S2O3)23-。
当体系中乙二胺浓度达到0.1 mol/L之后,继续增加乙二胺浓度,金浸出率不增反减。体系中过量的乙二胺,会导致溶液的混合电位降低,从而使体系中S2O32-,Cu2+的消耗急剧增加,金浸出反应动力学条件被削弱,最终造成金浸出率下降。
综合考虑,在后续试验中乙二胺浓度取0.1 mol/L为宜。
2.3 Cu2+浓度对金浸出率的影响取矿样50 g,液固体积质量比5∶1,浸金液中Na2S2O3浓度为0.35 mol/L,乙二胺浓度为0.1 mol/L,Na2SO3浓度为0 mol/L,溶液pH值为9.5,室温(25 ℃)浸出4 h。依次调节Cu2+浓度分别为0,0.025,0.050,0.075,0.1 mol/L。Cu2+浓度对金浸出率的影响如图 3所示。
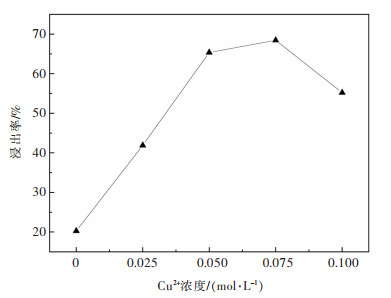 |
| 图 3 Cu2+浓度对金浸出率的影响 Fig. 3 The influence of Cu2+ concentration on gold leaching rate |
由图 3可知,随着Cu2+浓度增加,金浸出率先升高后降低,且当Cu2+浓度为0.075 mol/L时,金浸出率达到最高值68.45%。反应前期,Cu2+浓度比较低,Cu2+能与乙二胺形成[Cu(en)2]2+,该离子具有强氧化性,不易形成硫化物膜,能够打开硫化物的包裹,使金暴露出来,从而使Au与S2O32-的络合反应正向移动,提高金浸出率。
当体系中Cu2+浓度达到0.075 mol/L之后,继续增加Cu2+浓度,金浸出率不增反减。体系中过量的Cu2+会消耗更多的S2O32-,从而使Au与S2O32-的络合反应逆向移动,降低金浸出率[18]。
综合考虑,在后续试验中Cu2+浓度取0.075 mol/L为宜。
2.4 溶液pH值对金浸出率的影响取矿样50 g,液固体积质量比5∶1,浸金液中Na2S2O3浓度为0.35 mol/L,乙二胺浓度为0.1 mol/L,Cu2+浓度为0.075 mol/L,Na2SO3浓度为0 mol/L,室温(25℃)浸出4 h。依次调节溶液pH值分别为8,8.5,9,9.5,10。溶液pH值对金浸出率的影响如图 4所示。
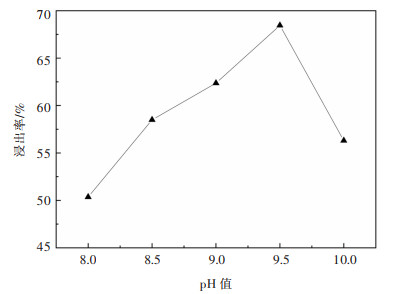 |
| 图 4 浸金液pH值对金浸出率的影响 Fig. 4 Influence of pH of gold leaching solution on gold leaching rate |
由图 4可知,随着Cu2+浓度增加,金浸出率先升高后降低,且当溶液pH值为9.5时,金浸出率达到最高值68.45%。S2O32-在碱性条件下有很强的络合能力,且碱性越强,络合能力越强。随着溶液pH值增大,S2O32-的络合能力随之增强,从而使Au与S2O32-的络合反应正向移动,提高了金浸出率[20]。
当体系中溶液pH值达到9.5之后,继续增大溶液pH值,金浸出率不增反减。体系中过量的OH-会使S2O32-发生歧化反应,生成亚硫酸盐和硫化物。该反应不但会降低体系中S2O32-浓度,从而使Au与S2O32-的络合反应逆向移动,降低金浸出率。而且生成的硫化物会包裹在金表面,阻碍金进一步溶出[21]。
综合考虑,在后续试验中溶液pH值以9.5为宜。
2.5 Na2SO3对金浸出率和Na2S2O3消耗率的影响通过前期试验得出较好浸金条件:液固体积质量比5∶1,浸金液中Na2S2O3浓度为0.35 mol/L,乙二胺浓度为0.1 mol/L,Cu2+浓度为0.075 mol/L,溶液pH为9.5,室温(25 ℃)浸出4 h。在此基础上,研究Na2SO3对金浸出率和Na2S2O3消耗率的影响。
取矿样50 g,液固体积质量比5∶1,浸金液中Na2S2O3浓度为0.35 mol/L,乙二胺浓度为0.1 mol/L,Cu2+浓度为0.075 mol/L,调节溶液pH值为9.5,室温(25 ℃)浸出4 h。依次调节Na2SO3浓度分别为0,0.05,0.10,0.15,0.20 mol/L。Na2SO3浓度对金浸出率以及对Na2S2O3消耗率的影响如图 5所示。
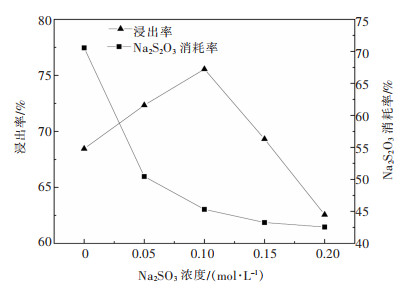 |
| 图 5 Na2SO3浓度对金浸出率以及Na2S2O3消耗率的影响 Fig. 5 The influence of Na2SO3 concentration on gold leaching rate and Na2S2O3 consumption rate |
由图 5可知,随着Na2SO3浓度增加,金浸出率先升高后降低,且当Na2SO3浓度为0.1 mol/L时,金浸出率达到最高值75.56%。硫代硫酸盐在浸金过程中会发生分解反应,生成亚硫酸盐,而亚硫酸盐能加速连多硫酸盐分解生成硫代硫酸盐这一过程[22]。相关反应方程式如下:
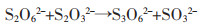
|
(2) |
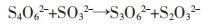
|
(3) |
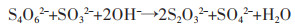
|
(4) |
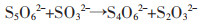
|
(5) |
体系中的亚硫酸盐,不但阻止了硫代硫酸盐自身分解反应的发生,而且促进了连多硫酸盐的分解反应,降低了体系中S2O32-的损失[23]。此外,Na2SO3还可以和元素硫以及硫化物反应生成S2O32-,增加体系中S2O32-的浓度。相关反应方程式如下:
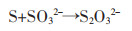
|
(6) |
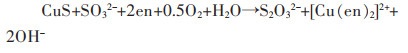
|
(7) |
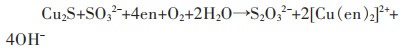
|
(8) |
由上述反应可知,体系中添加适量Na2SO3能够有效遏制硫与硫化物在金表面上沉积,从而提高金浸出率。
而当体系中Na2SO3浓度大于0.1 mol/L之后,继续增加Na2SO3浓度,虽然可以降低Na2S2O3的消耗率,但同时会使金浸出率也随之降低。体系中过量Na2SO3会与溶解氧反应生成SO42-,且影响体系中的铜-乙二胺络离子的生成。相关反应方程式如下:
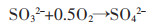
|
(9) |
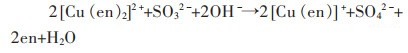
|
(10) |
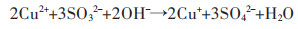
|
(11) |
此外,过量的SO32-还可以与金硫代硫酸盐络合物发生反应,导致金浸出率降低[24]:
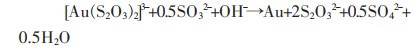
|
(12) |
过量亚硫酸盐一方面会参与反应生成S2O32-,虽然在一定程度上减少了硫代硫酸盐的消耗,但另一方面也增加了体系中溶解氧的消耗,并且使部分Cu2+,[Cu(en)2]2+以及[Au(S2O3)2]3-被还原,导致金浸出率降低。故反应体系中应该添加适量的Na2SO3,使之在降低Na2S2O3消耗率的同时保证金的高浸出率。
由试验结果可知,Na2SO3的添加对提升金浸出率并降低Na2S2O3消耗率均有着良好的效果。
综合考虑,在后续试验中Na2SO3浓度取0.1 mol/L为宜。
2.6 优化扩大试验通过上述试验结果,可以得出较优浸出条件:液固体积质量比5∶1,Na2S2O3浓度为0.35 mol/L,乙二胺浓度为0.1 mol/L,Cu2+浓度为0.075 mol/L,Na2SO3浓度为0.1 mol/L,溶液pH值为9.5,室温(25 ℃)浸出4 h。
在较优浸出条件下,将试验规模同时扩大5倍,进行3组平行试验。取矿样250 g,液固体积质量比5∶1,浸金液中Na2S2O3浓度为0.35 mol/L,乙二胺浓度为0.1 mol/L,Cu2+浓度为0.075 mol/L,Na2SO3浓度为0.1 mol/L,溶液pH值为9.5,室温(25 ℃)浸出4 h。3组试验的金浸出率分别为75.82%,76.04%和75.46%,证明了较优浸出条件下,金较高浸出率具有良好的稳定性。
2.7 浸出前后矿样的XRD分析分别对原矿石、不添加Na2SO3和添加Na2SO3的浸出渣进行XRD分析,XRD分析结果如图 6所示。其中图 6(a)为原矿石;图 6(b)为0.35 mol/L Na2S2O3、0.1 mol/L乙二胺、0.075 mol/L Cu2+、溶液pH值为9.5条件下的浸出渣;图 6(c)为0.35 mol/L Na2S2O3、0.1 mol/L乙二胺、0.075 mol/L Cu2+、0.1 mol/L Na2SO3、溶液pH值为9.5条件下的浸出渣。
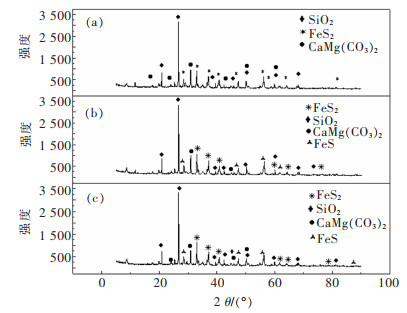 |
| 图 6 原矿、浸出渣的XRD图谱 Fig. 6 Spectra of XRD for raw ore and leaching residues |
通过对比图 6(a)、图 6(b)和图 6(c),在浸出前,原矿XRD图谱中主要为SiO2,FeS2和CaMg(CO3)2等物质的衍射峰。浸出后的图 6(b)和图 6(c)均出现了FeS的衍射峰,这表明在Cu2+-en-S2O32-浸金体系中,有一部分的FeS2分解脱硫生成了FeS。浸出前后矿渣的XRD图谱中均出现了SiO2和CaMg(CO3)2的衍射峰,是因为这2种物质化学性质稳定,不溶于水,也不参与反应。由图 6(a)、图 6(b)和图 6(c)图谱的峰形基本一致,可知二氧化硅、白云石等杂质基本上都留在浸出渣中,而金则被浸出进入浸出液中。通过浸出前后矿样的XRD图谱分析,在较优浸出条件下,硫代硫酸钠能够有效氧化硫化膜并释放出元素Au进入浸出液,对贵州卡林型金矿具有一定的浸出能力。
3 结论1)在较优浸出条件下,液固体积质量比5∶1,浸金液中Na2S2O3浓度为0.35 mol/L,乙二胺浓度为0.1 mol/L,Cu2+浓度为0.075 mol/L,Na2SO3浓度为0.1 mol/L,溶液pH值为9.5,室温(25 ℃)浸出4 h,金浸出率最高可达75.56%,表明硫代硫酸钠浸出贵州卡林型金矿是可行的。
2)在较优浸出条件下,3次优化扩大试验均得到了75%以上的金浸出率,证明了较优浸出条件下,金较高浸出率具有良好的稳定性。
3)浸出前后矿样的XRD图谱分析结果表明,在较优浸出条件下,Cu2+-en-S2O32-浸金体系能够有效氧化硫化膜并释放出元素Au进入浸出液,对贵州卡林型金矿具有一定的浸出能力。
4)硫代硫酸盐对贵州卡林型金矿具有一定的浸出效果,且浸出过程反应迅速、低毒高效、环境友好,值得进一步研究。
| [1] |
刘舒飞, 李亮. 中国黄金产业现状及对策建议[J].
资源与产业, 2016, 18(4): 98–102.
|
| [2] |
谢为, 郑明贵. 世界黄金价格影响因素模型研究[J].
有色金属科学与工程, 2012, 3(3): 90–94.
|
| [3] |
王经北, 魏志成. 新时代我国生态文明建设的战略思考[J].
江西理工大学学报, 2018, 39(2): 12–16.
|
| [4] |
徐水太, 徐晨晨, 张汗青, 等. 我国矿业循环经济的发展方向与思路[J].
江西理工大学学报, 2018, 39(2): 52–56.
|
| [5] |
王威, 杨卉芃, 冯安生, 等. 全球金矿开发利用现状及供需分析[J].
矿产保护与利用, 2016(6): 71–77.
|
| [6] |
古宇声. 我国微细浸染型金矿研究现状[J].
世界有色金属, 2017(10): 209–210.
|
| [7] |
张霜华, 郑雅杰, 曹攀, 等. 砷硫铁的脱除对高砷金精矿氰化浸金的影响[J].
中南大学学报(自然科学版), 2020, 51(6): 1471–1480.
|
| [8] |
肖力, 王永良, 钱鹏, 等. 非氰提金技术研究进展[J].
黄金科学技术, 2019, 27(2): 292–301.
|
| [9] |
黄成戈, 唐道文, 蔡鹏源, 等. 漂白粉浸出贵州难浸金矿的正交试验研究[J].
有色金属科学与工程, 2020, 11(2): 97–103.
|
| [10] |
项朋志, 刘龙江, 黄遥, 等. 硫代硫酸盐-EDTA-铜离子体系浸金工艺研究[J].
稀有金属, 2020, 44(5): 555–560.
|
| [11] |
贾玉娟, 王晓辉, 程伟, 等. 难处理金矿非氰浸金研究进展[J].
工程科学学报, 2019, 41(3): 307–315.
|
| [12] |
张景河. 采用石硫合剂处理某难浸金矿的试验研究[J].
矿业研究与开发, 2020, 40(4): 118–121.
|
| [13] |
SUN C B, ZHANG X L, KOU J, et al. A review of gold extraction using noncyanide lixiviants: Fundamentals, advancements, and challenges toward alkaline sulfur-containing leaching agents[J].
International Journal of Minerals Metallurgy and Materials, 2020, 27(4): 417–431. DOI: 10.1007/s12613-019-1955-x. |
| [14] |
SHI C L, NIE Y H, ZI F T, et al. Effect of tetrathionate on thiosulfate leaching of gold in copper-ammonia system[J].
Asia-Pacific Journal of Chemical Engineering, 2018: e2173. |
| [15] |
XU B, LI K, ZHONG Q, et al. Study on the oxygen pressure alkaline leaching of gold with generated thiosulfate from sulfur oxidation[J].
Hydrometallurgy, 2018: S0304386X17309271. |
| [16] |
赵鹤飞, 杨洪英, 张勤, 等. 硫代硫酸盐浸金各因素影响研究现状[J].
黄金科学技术, 2018, 26(1): 105–114.
|
| [17] |
韩彬, 童雄, 谢贤, 等. 硫代硫酸盐浸金体系研究进展[J].
矿产综合利用, 2015(3): 11–16.
|
| [18] |
高鹏, 唐道文, 唐攒浪. 用硫代硫酸钠从某卡林型金矿石中浸出金试验研究[J].
湿法冶金, 2017, 36(1): 12–15.
|
| [19] |
沈智慧, 张覃, 李先海, 等. 贵州某微细浸染型金矿非氰浸出试验研究[J].
有色金属(选矿部分), 2015(3): 52–56.
|
| [20] |
贾玉娟. 高砷高硫金矿焙砂碱介质物相重构及非氰浸金[D]. 贵阳: 贵州大学, 2019.
|
| [21] |
李骞, 董中林, 张雁, 等. 含硫砷含碳金精矿提金工艺研究[J].
黄金, 2016, 37(11): 41–45.
|
| [22] |
吕奉鹏. 连六硫酸盐亚硫酸化和硫代硫酸化反应动力学[D]. 徐州: 中国矿业大学, 2018.
|
| [23] |
蔡鑫, 崔毅琦, 何建, 等. 铜氨/胺体系下硫代硫酸盐浸金的电化学研究进展[J].
矿产保护与利用, 2019, 39(5): 156–159.
|
| [24] |
贺俊傲, 崔毅琦, 何建, 等. 氨性硫代硫酸盐浸出金银过程中降低硫代硫酸盐消耗量研究进展[J].
矿产保护与利用, 2019, 39(5): 160–166.
|
 2021, Vol. 12
2021, Vol. 12


