| 废加氢催化剂中有价金属回收技术研究进展 |
2. 江西理工大学材料冶金化学学部,江西 赣州 341000;
3. 稀贵金属绿色回收与提取北京市重点实验室,北京 100083
2. Faculty of Materials, Metallurgy and Chemistry, Jiangxi University of Science and Technology, Ganzhou 341000, Jiangxi, China;
3. Beijing Key Laboratory of Green Recycling and Extraction of Metals, Beijing 100083, China
加氢催化剂广泛用于石化行业,其用量约占石油精炼行业催化剂总用量的30%[1]。长期使用后,加氢催化剂会因结构被破坏、活性组分流失或活性组分转化为非活性组分等原因失活。因此在加氢催化剂使用一定时间,活性下降到一定程度,就必须进行再生处理[2-3]。然而当经过多次再生处理的催化剂的活性无法恢复到合理水平,或再生成本过高时,就必须将失活的催化剂报废[4]。一般来说,石油加氢催化剂的使用寿命为2~3年[5]。随着石化行业对加氢催化剂的需求量逐年递增,每年报废的加氢催化剂量也与日俱增,全世界每年报废的加氢催化剂量高达12万t(干基)[6]。
在最新的国家危险废物名录中,废加氢催化剂被列为危险废物[7-8]。废加氢催化剂含有大量的重金属和有机物[9-11],如果未得到有效处理,会对环境和人的健康造成巨大的影响。此外,废加氢催化剂含有大量的有价金属,且含量比天然矿物中的含量高得多,这些金属广泛应用于多个领域。随着金属矿产资源的不断开采,仅靠原生矿产已很难满足金属的需求,这促进了金属二次资源的利用[12]。因此,废加氢催化剂的循环利用对于环境保护和资源的高效利用意义重大[13]。
由于废加氢催化剂物料本身的一些特性,导致各种回收处理工艺面临一些亟待解决的共性问题[14-15]。废加氢催化剂中含有10%~30%的有机物、积碳等,会对提取过程造成极为不利的影响[16]。此外,由于废催化剂中组分极其复杂,含有大量的Al2O3及一定量的SiO2,有价元素以氧化物、硫化物、盐、多金属复合物等多种形式存在,也会导致有价金属回收困难[17-20]。近年来,国内外学者在废加氢催化剂回收方面进行了大量的研究工作,也开发并报道了许多从废加氢催化剂中回收有价金属的方法。废加氢催化剂的回收技术主要分为湿法工艺、火法工艺以及火法湿法联合工艺等3大种类。综述了近年来废加氢催化剂回收的研究进展,重点分析了不同技术的主要过程及其优缺点,最后对废加氢催化剂回收的发展趋势及前景进行了展望。
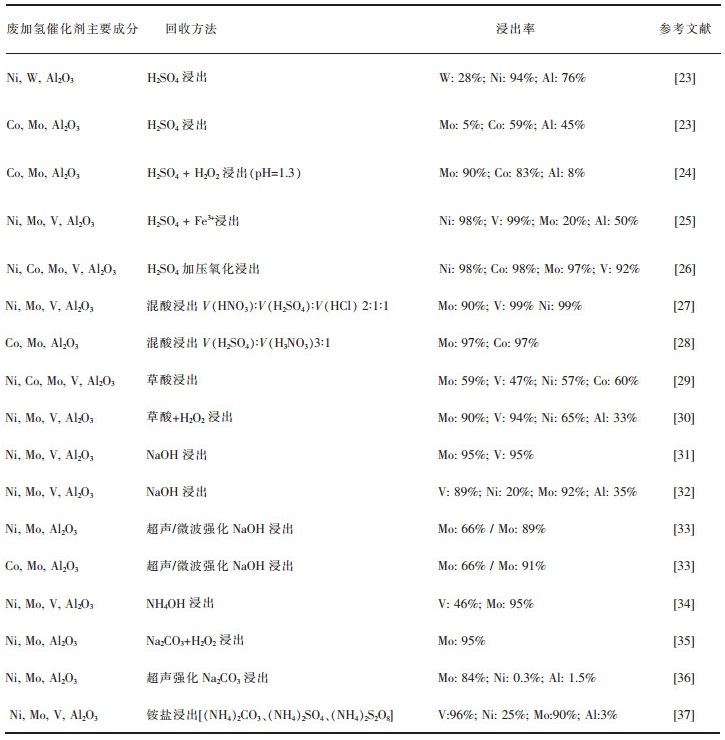
1 废加氢催化剂回收工艺综述 1.1 湿法工艺湿法工艺是指利用浸出剂直接将废加氢催化剂中的有价金属溶出并回收的处理工艺。浸出剂通常采用不同浓度的无机酸(如H2SO4、HCl或HNO3等)、水溶性有机酸(如草酸、柠檬酸)溶液、氨或铵盐溶液以及碱液[21],或利用微生物将固体化合物转化为可溶性化合物然后浸出[22]。表 1列举了采用湿法工艺回收废加氢催化剂中有价金属的主要方法。
| 表 1 采用湿法工艺回收废加氢催化剂中有价金属的主要方法 Table 1 Main method for recovering valuable metals from spent hydrogenation catalyst by hydrometallurgical process |
 |
| 点击放大 |
1.1.1 酸性浸出
在湿法冶金处理中,由于废加氢催化剂中含有的有价金属在酸性条件下比较容易浸出,因此浸出时一般优先使用酸作为浸出剂。Valverde等进行了在相同条件下使用盐酸和硫酸浸出废加氢催化剂的对比研究[38]。结果表明,硫酸对废加氢催化剂中金属的浸出效率要好于盐酸。而且由于盐酸具有挥发性,对环境不友好,因此在浸出剂的选择上,优选使用硫酸而不是盐酸[8]。Siemens等分别对废加氢催化剂中的Co-Mo类催化剂和Ni-W类催化剂进行了硫酸浸出研究[23]。通过研究发现,使用稀硫酸在常压下浸出有价金属时,Mo和W的浸出率分别为5%和28%。由于常压硫酸浸出不能有效浸出Mo、W和V等有价金属,所以有研究采用加入氧化剂和加压等提高有价金属浸出效果。Ruiz等在pH=1.3、固液比(指固体质量与液体体积之比,单位为g/L,下同)为7.5、H2O2浓度为3.75 mol/L的条件下,通过淋滤回收Mo和Co。结果表明,Mo和Co的浸出率分别为90%和83%,而Al的溶解度不超过8%[24]。Veal等开发了一种加压氧化酸浸处理废加氢催化剂的方法[26]。在温度高于148 ℃、O2大于0.4 MPa的条件下,将催化剂中存在的金属硫化物(NiS,V2S3,MoS2,CoS等)氧化成对应的氧化物,再通过与硫酸反应达到浸出有价金属的目的。此方法可浸出98%的Ni和Co、97%的Mo和92%的V。Lai等将混酸浸出和流化床电解工艺相结合,从废加氢催化剂中回收有价金属。研究发现当使用组成体积比为2:1:1 HNO3/H2SO4/HCl的混酸溶液可以达到最好的浸出效果[27]。此混合溶液在实验条件为70 ℃、固液比为40、浸出时间1 h下,Mo、Ni、V的浸出率分别达到90%、99%和99%。
除无机酸外,许多学者也开展了有机酸浸出废加氢催化剂中有价金属的研究。Beuther等分别对草酸、酒石酸和柠檬酸浸出废加氢催化剂中有价金属进行了研究[29]。研究表明在上述有机酸中,草酸对废加氢催化剂中金属的浸出效率最高,但V、Co、Ni和Mo的浸出率也仅为47%、60%、56%和59%。在有机酸浸出过程中,为了提高浸出效率,通常会加入一些氧化剂,例如Al(NO3)3、H2O2和Fe(NO3)3等。通过氧化和螯合反应的协同作用,来提高金属的浸出效率[39]。Mulak等研究了草酸和H2O2混合溶液对废加氢催化剂中Mo、Ni、V和Al等元素的浸取效率[30]。结果表明,在50℃、C2H2O4 0.5 mol/L和H2O2 3.0 mol/L的较优条件下浸取4 h,Mo、V、Ni和Al的浸出率分别为90%、94%、65%和33%。有机酸法相对无机酸法而言,存在金属浸出率较低、浸出剂价格较高等问题,不利于工业应用。
1.1.2 碱性浸出当V、Mo和W之类的有价金属以氧化物的形式存在于废加氢催化剂中时,可以溶解在碱性溶液中。因此可以首先利用碱性溶液选择性地浸出上述金属,然后通过酸浸浸出Ni、Co等有价金属。Rojas-Rodriguez等使用氢氧化钠溶液从废加氢催化剂中回收Mo和V,在氢氧化钠溶液浓度为20%、反应温度为室温、反应时间为2 h的条件下,Mo和V的浸出率均为95%左右[31]。剩余的浸出渣主要成分为NiAlO2,可用于下一步Ni的回收。为在更低NaOH浓度下有效浸出Mo、W和V等有价金属,Isabel等将NaOH浸出和超声、微波等强化方法相结合[33]。当使用常规浸出方法(10 g/L NaOH、80 ℃、2 h、固液比为50)时,可浸出Ni-Mo催化剂中77%的Mo和Co-Mo催化剂中84%的Mo,当使用超声强化在相同条件下浸出时,对于这两种催化剂均可浸出66%左右的Mo,当使用微波强化时,Mo浸出率可分别达到89%和91%。
除了氢氧化钠溶液,氨和碳酸钠[40-42]等碱性试剂也被用于浸出废加氢催化剂中的有价金属。Zhao等将氨浸法用于从废Mo-V催化剂中回收Mo和V[34]。研究表明在较优条件下,V和Mo的浸出率分别达到46.3%和95.1%。Park等利用碳酸钠和过氧化氢混合溶液回收废加氢催化剂。在较优浸出条件下(0.4 mol/L Na2CO3、6%(体积百分数)H2O2、室温、1 h)Mo的浸出率约为85%[35]。
直接使用碱性浸出方法处理废加氢催化剂时,废催化剂中的积碳和有机物会影响浸出效果。同时碱浸会造成部分Al和Si会溶解在溶液中,导致浸出试剂的消耗量增加和后续净化工序的困难。如能在碱性浸出之前将废加氢催化剂中的Al、Si、积碳和油去除,则可发挥碱性浸出选择性好的优势。
1.1.3 生物浸出与化学浸出相比,生物浸出具有低成本、绿色和高金属回收率等优点[43]。生物浸出分为直接和间接生物浸出[44]。在生物直接浸出中,细菌与废加氢催化剂中的金属元素直接相互作用,使其转变为可溶于溶液中的离子态,硫在溶液中也会转化为可溶形式。在生物间接浸出中,首先通过细菌的代谢过程将Fe2+和S元素氧化为Fe3+和H2SO4,然后利用Fe3+作为氧化剂,H2SO4作为溶剂浸出有价金属。在各类细菌中,嗜酸硫杆菌属(即嗜酸氧化亚铁硫杆菌和嗜酸氧化硫硫杆菌)被广泛用于金属的回收[45-46]。Mishra等利用氧化硫硫杆菌直接转化废加氢催化剂中的有价金属[47]。通过研究表明,经过氧化硫硫杆菌一周时间的转变后,可回收废催化剂中94.8%的V、46.3%的Mo和88.3%的Ni。Kim等在使用氧化亚铁硫杆菌处理废加氢催化剂时,用硫酸亚铁作为铁补充剂,利用细菌将Fe2+氧化为Fe3+,然后在Fe3+和H2SO4溶液的共同作用下浸出废催化剂中的有价金属[48]。此方法需要14 d才能实现回收97%的Ni、59%的Al、11%的Mo和27%的V。利用细菌浸出回收有价金属需要的时间比其他方法要长的多,这是生物浸出的一个显著缺点。除此之外,利用生物浸出时有价金属的浸出率也较低。在大多数情况下,使用生物浸出,Mo的浸出率低于Co、Ni和V的浸出率。可能是废加氢催化剂表面上形成的硫层会阻碍细菌与金属特别是Mo之间相互作用的原因[49-50]。此外,细菌的活性和生长也会受到温度、pH、金属的组成和浓度等诸多因素影响,稳定性差。
废加氢催化剂中含有大量的积碳和有机物,不经过脱碳、脱油处理直接湿法浸出会影响有价金属浸出效果。有价金属在废加氢催化剂中的存在方式复杂多样,通过加入氧化剂或采用加压氧化浸出虽然可以有效的浸出如Ni、Co等一些有价金属,但有价金属总体浸出率不高。除此之外,湿法工艺中载体溶解率较高,造成后续分离提取过程较为繁琐,操作性较差。浸出过程会产生部分有毒气体,且提取有价金属后的溶液由于含有机物也较难处理。
1.2 火法工艺废加氢催化剂中含有的积碳和有机物可作为火法工艺中的燃料和还原剂。废加氢催化剂中有价金属以氧化物、硫化物、盐及多金属复合物存在,但均可在熔炼过程中被还原成单质并富集到合金中。同时在熔炼过程中,Al2O3和SiO2等载体会与有价金属分离进入渣中,消除了载体在后续浸出分离过程中的影响。因为火法工艺的上述优势,一些研究者在多年前即开始关注并研究用火法冶金工艺处理废加氢催化剂。
朱兆鹏等用等离子炉熔炼含钼废加氢催化剂回收有价金属[51]。在研究中使用的废加氢催化剂中主要组分的含量(指质量百分数)为:Co 1.74%、Ni 3.09%、Mo 4.7%、V 12.6%、S 11.2%、C 11.6%、Fe 0.4%。以焦炭作为还原剂,氧化铁和石灰石作造渣剂。由于Al2O3的熔点较高,所以此方法利用等离子炉,在1 900 ℃以上的温度进行熔炼。实验结果表明,所得到的多金属合金的主要成分(指质量百分数)为:Co 5%~7%、Ni 9%~11%、Mo 15%~18%、V 30%~35%、Fe 10%~15%,金属的平均回收率达93%。Canham等分别进行了等离子炉熔炼的实验室试验和放大试验(0.2 m3)。两次试验结果表明,合金中Co和Mo的回收率均大于99%,炉渣中各有价金属含量均小于0.05%[52]。Pak等在1 800~2 000 ℃的高温下进行还原熔炼,然后再对熔体采用吹炼的方法,使还原熔炼产生的Fe-V-Ni-Mo熔体中的V被氧化,与氧化钙、氧化铁形成炉渣,此炉渣可加工成Fe-V合金[53]。该方法成功地生产了Fe-V和Fe-Ni-Mo合金,V的回收率超过了90%,Ni和Mo的回收率超过了95%。
Howard等在进行废加氢催化剂还原熔炼之前,先将废加氢催化剂在760~870 ℃的氧化条件下进行煅烧,以除去硫、游离碳、水和碳氢化合物[54]。然后将煅烧后的废加氢催化剂在电弧炉中与废铁一起冶炼,温度为1 800~2 400 ℃。在电弧炉中加入还原剂(例如天然气),将废加氢催化剂中V、Co和Ni的氧化物还原为金属态,从而形成合金。通过密度差将熔融的Al2O3与金属合金分离并定期去除。该工艺可以回收约99%的有价金属,但熔炼温度较高,电弧炉电极消耗快。
传统火法工艺存在反应温度过高、能耗大、只能得到合金中间产品等问题。如能降低熔炼温度同时利用湿法工艺进行后续有价金属的分步回收,则可降低能耗,提高产品的附加值。
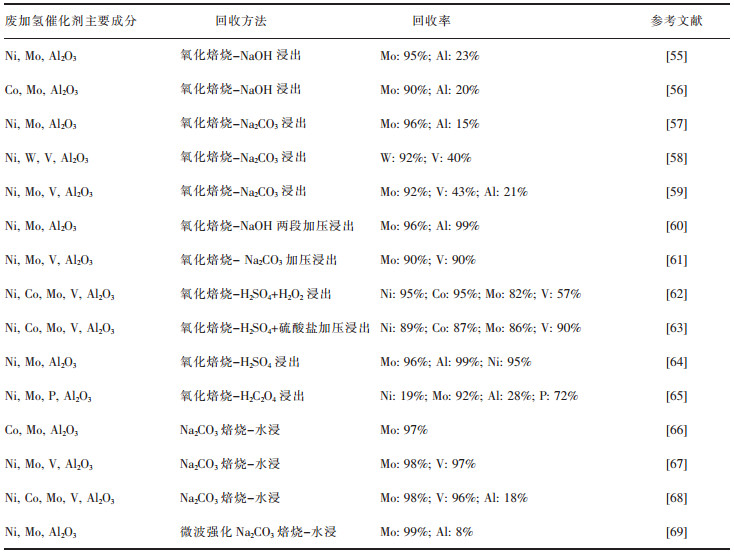
1.3 火法湿法联合工艺针对单独采用湿法工艺的缺点和不足,越来越多的研究人员提出了火法湿法联合工艺。表 2所列为火法湿法联合工艺回收废加氢脱硫催化剂中有价金属的主要方法。火法-湿法联合工艺的典型方案为氧化或钠化(钙化)焙烧-浸出法。该工艺通过在湿法浸出前加入焙烧工艺。在除去废加氢催化剂中积碳和有机物的同时,不同的焙烧方法也可将以复杂形式存在的有价金属转化成氧化物或者盐等易于浸出的形式,然后通过后续的浸出实现对有价金属的高效回收。
| 表 2 火法湿法联合工艺回收废加氢脱硫催化剂中有价金属的主要方法 Table 2 Main method for the recovery of valuable metals from spent hydrodesulfurization catalyst by pyro-hydrometallurgical process |
 |
| 点击放大 |
1.3.1 氧化焙烧-碱性浸出法
王尔勤等利用氧化焙烧-NaOH浸出处理废催化剂,在焙烧温度为480 ℃, 焙烧时间为2 h条件下焙烧后,废加氢催化剂用NaOH溶液搅拌浸出,溶液升温至沸腾,pH值控制在11~12左右,此方法可浸出95%的Mo[55]。Parkinson等考察了不同氢氧化钠浓度对Mo浸出率的影响[70]。结果表明,随着氢氧化钠浓度从0.25 mol/L增加到2 mol/L,Mo和V的浸出率均会升高,其中氢氧化钠浓度的变化对Mo的浸出率影响更大。虽然通过提高氢氧化钠浓度可以提高Mo的浸出率,但随之出现的问题是Al的大量浸出。张智等在氧化焙烧后采用碳酸钠代替氢氧化钠作为浸出剂处理Mo-Ni/Al2O3催化剂,在焙烧温度为500 ℃、焙烧时间为6 h、浸出温度为95 ℃、浸出时间2 h、碳酸钠用量为理论用量4倍、固液比为250的较优条件下可浸出96%的Mo[57]。
在焙烧后的常压NaOH浸出过程中,当NaOH浓度较低时,有价金属不能被有效浸出;将NaOH浓度提高后,Al和Si则会在浸出过程中大量浸出。为解决这一问题,Kar B B等在采用氧化焙烧-NaOH浸出时,用加压碱浸代替常压碱浸[59]。该研究在保持低NaOH/Mo比的条件下加压浸出,可以在有效浸出废加氢催化剂中Mo的同时使Al2O3进入渣中。在较优实验条件(160℃、NaOH的用量为化学计量的1.2倍、固液比为250、反应时间2 h、搅拌速度为300 r/min)下,浸出了96%以上的Mo,同时Al的浸出率低于0.2%。固液分离后采用二次加压碱浸浸出Al2O3,最后将浸出液中的Al以Al(OH)3的形式沉淀下来,用于制备新催化剂的载体。胡建峰等在氧化焙烧后同样采用了加压浸出,不同的是该方法采用了Na2CO3作为浸出剂,在较优条件下可一次性浸出90%以上的V和Mo[61]。
在加氢脱硫催化剂的制备中,载体使用的为高反应性的γ-Al2O3,含量一般占催化剂成分的40%左右,无论采用酸浸还是碱浸均会大量浸出。Zhang等通过采用微波焙烧将γ-Al2O3转变为更稳定的α-Al2O3,以减少Al的浸出[71]。结果表明,与传统的焙烧方法相比,微波焙烧可以在更低的温度(1 000 ℃)和更短的时间(1 h)内实现γ-Al2O3向α-Al2O3的转变。在利用微波焙烧处理废催化剂之后,Al在碱浸和酸浸中的浸出率均显著降低,同时采用微波焙烧处理后,Co、Ni等有价金属的浸出率也有不同程度的上升。
氧化焙烧浸出法回收废加氢催化剂中有价金属的典型工艺流程见图 1。
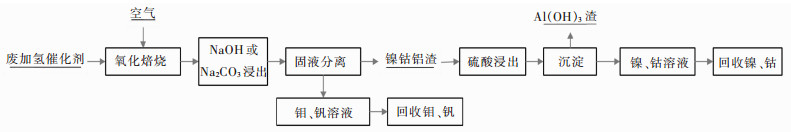 |
| 图 1 氧化焙烧-浸出法回收废加氢催化剂中有价金属的典型工艺流程 Fig. 1 Typical process flow chart of recovery of valuable metals from spent hydrogenation catalyst by oxidation roasting-leaching method |
1.3.2 氧化焙烧-酸浸法
Mihashi等提出了一种利用氧化焙烧-酸浸处理废加氢催化剂的新方法,废加氢催化剂首先在空气中焙烧2 h,焙烧温度为450~500 ℃[62]。然后使用稀硫酸和氧化剂(如过氧化氢)浸出Ni和Co,但该过程也会浸出10%的Mo和35%的V。将含有Mo和V的残留物与NaOH溶液一起搅拌,Mo和V浸出至碱液中。该方法可回收95%以上的Ni和Co,但Mo和V因在酸浸中也会部分浸出,导致碱浸过程回收率不高。Ho等采用了类似的方法处理废加氢催化剂,所不同的是此方法用高压酸浸代替了常压酸浸[63]。将焙烧后的废催化剂在高压釜中于180~220 ℃的条件下浸出,使用的浸出剂除了硫酸还加入了硫酸盐,例如硫酸钾,硫酸铵或硫酸铝。该方法在Mo、V、Ni和Co进入浸出液的同时,可以使溶液中的Al以铝矾石的形式沉淀出来。氧化焙烧-酸浸法在浸出时对有价金属没有选择性,后续的分离提纯过程较为繁琐,过程中会损失掉部分有价金属,有价金属回收率不高。
1.3.3 碳酸钠焙烧-浸出法碳酸钠焙烧-浸出法通过碳酸钠焙烧使Mo、V等有价金属的氧化物转变为相对应的钠盐,再通过水浸出将Mo、V提取。水浸出过程中,Al、Ni和Co的氧化物会进入渣中。刘润静等利用碳酸钠焙烧-水浸法处理Co-Mo废催化剂[66]。较优工艺条件为焙烧温度600 ℃、Na2CO3∶废加氢催化剂的质量比为0.15∶1、焙烧时间4 h、浸出温度80 ℃、浸出时间4 h,在此条件下可浸出97%的Mo,同时Co和Al的氧化物进入渣中进一步回收。为缩短该方法的焙烧和浸出时间,陈兴龙等提高了焙烧时的温度,在Na2CO3与(V+Mo)的摩尔比为1.5、焙烧温度为800 ℃、焙烧时间为1 h、水浸温度为80 ℃、水浸时间为1 h的条件下,V和Mo的浸取率分别达到97.4%和98.5%[67]。
为在相对短的时间和相对低的焙烧温度条件下有效浸出有价金属,有研究者利用一些强化手段来提高有价金属回收效果。Ye X. L等在利用此方法处理废催化剂时,为了有更好的氧化效果,在焙烧时用富氧空气代替了普通空气[68]。该研究在焙烧(焙烧温度为650 ℃,碳酸钠用量为Na2CO3与(Mo+V)摩尔比为2:1,焙烧时间为2 h)和浸出(水浸温度为60 ℃,浸出时间为2 h)的较优条件下,可从废催化剂中回收96%~98%的Mo和V。Yaras等利用微波强化Na2CO3焙烧处理废催化剂,目的是在提高Mo浸出率的同时缩短焙烧时间和有更好的原位固硫效果[69]。由于微波的特殊加热方法,焙烧后的废催化剂具有适合浸出的微观结构,并且S可原位转化为Na2SO4,减少SOx气体的排放。该研究在热力学分析的基础上,深入研究了微波加热温度,保温时间和Na2CO3添加量对Mo回收率的影响。此方法在焙烧温度600℃、45 min、Na2CO3与(Mo+V+S)摩尔比为1.25的条件下可浸出99%的Mo,同时Al的浸出率小于8%。
图 2所示为碳酸钠焙烧—水浸出法回收废加氢催化剂中有价金属的典型工艺流程。
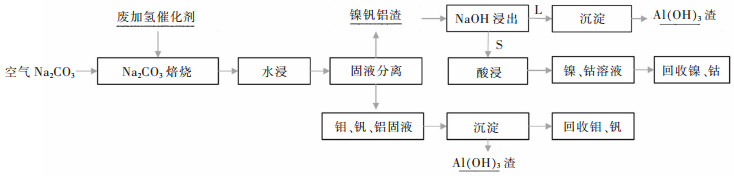 |
| 图 2 碳酸钠焙烧-水浸出法回收废加氢催化剂中有价金属的典型工艺流程 Fig. 2 Typical process flow chart of recovery of valuable metals from spent hydrogenation catalyst by Na2CO3 roasting-water leaching method |
火法湿法联合工艺是目前处理废加氢催化剂的主流方法。该工艺在焙烧过程中可将废催化剂中的油和有机物脱除,同时使有价金属转变为易于后续浸出的形态,后续通过合适的浸出剂实现有价金属的浸出。但由于废加氢催化剂中高含量的碳和有机物,焙烧过程中容易爆燃,产出大量有害气体。在焙烧后,部分有价金属会以难于浸出的复合氧化物形式存在。在后续浸出过程中,Al、Si等杂质也会同步浸出,增大了净化过程的难度。铝硅渣会夹带部分有价金属,并产出危废净化渣。
1.4 火法还原熔炼富集-合金湿法回收工艺的提出针对当前废加氢催化剂回收过程中的问题,提出了一种从废加氢催化剂中回收有价金属的新工艺。该工艺首先采用火法还原熔炼处理废加氢催化剂,通过配以各种助熔剂和辅料的方法,降低熔炼的反应温度。在1 500 ℃的熔炼温度下通过还原熔炼将废催化剂中的有价金属富集到合金中,而Al、Si等杂质以及造渣剂则形成稳定渣。该过程生产的合金成分简单,有利于后续的湿法提取。火法还原熔炼过程产出的废气经二次燃烧、冷却收尘、喷淋吸收处理后可达标排放。合金通过湿法分步选择性浸出其中的有价金属。
本研究团队通过联合相关企业展开了该技术的工业放大实验,得到如下数据。熔炼过程中,W、Mo、Co、Ni的回收率在98%以上,V的回收率在90%以上;合金湿法回收过程中,较优条件下Mo、W、V的浸出率在97%以上,Ni、Co的浸出率在95%以上。上述工艺具有金属回收率高、溶液净化工序简单、废气易处理、含盐废水量低、没有危废渣产生等显著优势,是一种具有较好经济效益并且环境友好的工艺。
2 结语与展望随着石油化工产业对加氢催化剂需求量的快速增长,每年报废的加氢催化剂量也与日俱增。废加氢催化剂中含大量有价金属,其循环利用对于环境保护和资源的高效利用意义重大。针对近年来废加氢催化剂回收的研究进展,重点分析了不同技术的主要过程、原理及其优缺点,得出了以下结论:
1) 废催化剂中组分极其复杂,含有10%~30%的有机物、积碳以及大量的Al2O3和一定量的SiO2,有价元素以氧化物、硫化物、盐、多金属复合物等多种形式存在,导致有价金属回收困难。目前废加氢催化剂的回收技术主要分为湿法工艺、火法工艺以及火法湿法联合工艺。
2) 废加氢催化剂的湿法工艺中有价金属总体浸出率不高,且载体溶解率较高,浸出过程会产生部分有毒气体,金属提取后液含有机物也较难处理;传统火法工艺温度过高,能耗大,目前只能产出合金中间产品;火法-湿法联合工艺在火法焙烧过程会产出大量有害气体,同时部分有价金属以难于浸出的复合氧化物形式存在。在后续浸出过程中,Al、Si等杂质也会同步浸出,增大了净化过程的难度,铝硅渣会夹带部分有价金属,并产出危废净化渣。
3) 提出了一种从废加氢催化剂中回收有价金属的新工艺。采用火法还原熔炼在1 500 ℃的熔炼温度下将废催化剂中的有价金属富集到合金中,而Al、Si等杂质以及造渣剂则形成稳定渣。合金通过湿法分步选择性浸出其中的有价金属。上述工艺具有金属回收率高、溶液净化工序简单、废气易处理、含盐废水量低、没有危废渣产生等显著优势,是一种具有较好经济效益并且环境友好的工艺。
| [1] |
AKCIL A, VEGLIO F, FERELLA F, et al. A review of metal recovery from spent petroleum catalysts and ash[J].
Waste Management, 2015, 45: 420–433. DOI: 10.1016/j.wasman.2015.07.007. |
| [2] |
孙晓雪, 刘仲能, 杨为民. 废弃负载型加氢处理催化剂金属回收技术进展[J].
化工进展, 2016, 35(6): 1894–1904.
|
| [3] |
YANG Q Z, QI G J, LOW H C, et al. Sustainable recovery of nickel from spent hydrogenation catalyst: economics, emissions and wastes assessment[J].
Journal of Cleaner Production, 2011, 19(4): 365–375. DOI: 10.1016/j.jclepro.2010.11.007. |
| [4] |
孙毓韬, 李雪莲. 镍基废催化剂回收及再利用的科学研究[J].
硅谷, 2014, 7(18): 188–205.
|
| [5] |
邬建辉, 王刚, 张文宏, 等. 含钨钼废催化剂回收工艺研究进展[J].
中国资源综合利用, 2013, 31(8): 42–45.
|
| [6] |
谢美求, 陈坚, 熊学良, 等. 废钨-镍型加氢催化剂中综合回收有价金属的研究[J].
金属材料与冶金工程, 2007, 35(5): 10–14.
|
| [7] |
PINTO I S S, SASEGHI S M, IZATT N E, et al. Recovery of metals from an acid leachate of spent hydrodesulphurization catalyst using molecular recognition technology[J].
Chemical Engineering Science, 2015, 138: 353–362. DOI: 10.1016/j.ces.2015.08.018. |
| [8] |
ZENG L, CHENG C Y. A literature review of the recovery of molybdenum and vanadium from spent hydrodesulphurisation catalysts: Part I: Metallurgical processes[J].
Hydrometallurgy, 2009, 98(1): 1–9. |
| [9] |
ERUST C, AKCIL A, BEDELOVA Z, et al. Recovery of vanadium from spent catalysts of sulfuric acid plant by usinginorganic and organic acids: laboratory and semi-pilot tests[J].
Waste Manag, 2016, 49: 455–461. DOI: 10.1016/j.wasman.2015.12.002. |
| [10] |
FERELLA F, OGNYANOVA A, MICHELIS I D, et al. Extraction of metals from spent hydrotreating catalysts: physico-mechanical pre-treatments and leaching stage[J].
Journal of Hazardous Materials, 2011, 192: 176–185. |
| [11] |
SRIVASTAVA R R, MITTAL N K, PADH B, et al. Removal of tungsten and other impurities from spent HDS catalyst leach liquor by an adsorption route[J].
Hydrometallurgy, 2012, 127/128: 77–83. DOI: 10.1016/j.hydromet.2012.07.004. |
| [12] |
丁云集, 张深根. 废催化剂中铂族金属回收现状与研究进展[J].
工程科学学报, 2020, 42(3): 257–269.
|
| [13] |
MOOSAKAZEMI F, TAVAKOLI M M R, ZAKERI M, et al. Development of an environmentally friendly flowsheet for the hydrometallurgical recovery of nickel and aluminum from spent methanation catalyst[J].
Journal of Cleaner Production, 2020, 244: 118731–118733. DOI: 10.1016/j.jclepro.2019.118731. |
| [14] |
IDRIS J, MUSA M, YIN C Y, et al. Recovery of nickel from spent catalyst from palm oil hydrogenation process using acidic solutions[J].
Journal of Industrial and Engineering Chemistry, 2010, 16(2): 251–255. |
| [15] |
许礼刚. 废钨回收产业的价值和发展模式探析[J].
有色金属科学与工程, 2013, 4(5): 113–116.
|
| [16] |
赵檀, 董春明. 炼油加氢废催化剂中金属分离回收工艺分析[J].
科技展望, 2016, 26(31): 48.
|
| [17] |
GAROLE D J, SAWANT A D. Recovery of nickel from spent catalyst from palm oil hydrogenation process using acidic solutions[J].
Research Journal of Chemical Sciences, 2012, 2(12): 27–30. |
| [18] |
XU A Y, YE T, ZHAO S H. Recovery of valuable metals from spent hydrogenation catalysts[J].
Applied Mechanics and Materials, 2013, 440: 97–103. DOI: 10.4028/www.scientific.net/AMM.440.97. |
| [19] |
肖连生. 中国钨提取冶金技术的进步与展望[J].
有色金属科学与工程, 2013, 4(5): 6–10.
|
| [20] |
林世雄.
石油炼制工程(下)[M]. 北京: 北京石油工业出版社, 1988: 661-665.
|
| [21] |
MARAFI M, STANISLAUS A. Spent hydroprocessing catalyst management: A review. Part Ⅱ. Advances in metal recovery and safe disposal methods[J].
Resources, Conservation and Recycling, 2008, 53: 1–26. DOI: 10.1016/j.resconrec.2008.08.005. |
| [22] |
BEOLCHINI F V, FONTI F, FERELLA, et al. Metal recovery from spent refinery catalysts by means of biotechnological strategies[J].
Journal of Hazardous Materials, 2010, 178: 529–534. DOI: 10.1016/j.jhazmat.2010.01.114. |
| [23] |
SIEMENS R E, JONG B W, RUSSELL J H. Potential of spent catalysts as a source of critical metals[J].
Conservation and Recycling, 1986, 9(2): 89–96. |
| [24] |
RUIZ V, MEUX E, SCHNEIDER M, et al. Hydrometallurgical treatment for valuable metals recovery from spent CoMo/Al2O3 Catalyst. 2. Oxidative leaching of an unroasted catalyst using H2O2[J].
Industrial & Engineering Chemistry Research, 2011, 50: 5307–5315. |
| [25] |
ROCCHETTI L, FONTI V F, VEGLIO, et al. An environ-mentally friendly process for the recovery of valuable metals from spent refinery catalysts[J].
Waste Management and Research, 2013, 31: 568–576. DOI: 10.1177/0734242X13476364. |
| [26] |
VEAL J T, ANDERSEN K A, KOWALESKI R M. Process to recover metals from spent catalyst. US: 6180072[P]. 2001.
|
| [27] |
LAI Y C, LEE W J, HUANG K L, et al. Metal recovery from spent hydrodesulfurization catalysts using a combined acid-leaching and electrolysis process[J].
Journal of Hazardous Materials, 2008, 154: 1–3. DOI: 10.1016/j.jhazmat.2007.09.093. |
| [28] |
RABAH M A, HEWAIDY I F, FARGHALY F E. Recovery of molybdenum and cobalt powders from spent hydrogenation catalyst[J].
Powder Metallurgy, 1997, 40: 283–288. DOI: 10.1179/pom.1997.40.4.283. |
| [29] |
BEUTHER H, FLINN R A. Technique for removing metal contaminants from catalysts[J].
Industrial & Engineering Chemistry Product Research and Development, 1963(2): 53–57. |
| [30] |
MULAK W, SZYMCZYCHA A, LESNIEWICZ A, et al. Preliminaryresults of metals leaching from a spent hydrodesulphurization (HDS) catalyst[J].
Physicochemical Problems of Mineral Processing, 2006, 40: 69–76. |
| [31] |
ROJAS-RODRIGUEZ A D, FLORES-FAJARDO O, GONZALEZ F S A, et al. Chemical treatment to recover molybdenum and vanadium from spent heavy gasoil hydro-desulfurization catalyst[J].
Advances in Chemical Engineering and Science, 2012(2): 408–412. |
| [32] |
VILLARREAL S M, KHARISOV B I, TORRES M L M, et al. Recovery of vanadium and molybdenum from spent petroleum catalyst of PEMEX[J].
Industrial Engineering Chemistry Research, 1999, 38: 4624–4628. DOI: 10.1021/ie980717j. |
| [33] |
ISABEL S S, PINTO H, SOARES M V M. Selective leaching of molybdenum from spent hydrodesulphurisation catalysts using ultrasound and microwave methods[J].
Hydrometallurgy, 2012, 129/130: 19–25. DOI: 10.1016/j.hydromet.2012.08.008. |
| [34] |
ZHAO Z, GUO M, ZHANG M. Extraction of molybdenum and vanadium from the spent diesel exhaust catalyst by ammonia leaching method[J].
Journal of Hazardous Materials, 2015, 286: 402–409. DOI: 10.1016/j.jhazmat.2014.12.063. |
| [35] |
PARK K H, MOHAPATRA D, REDDY B R. Selective recovery of molybdenum from spent HDS catalyst using oxidative soda ash leach/carbon adsorption method[J].
Journal of Hazardous Materials, 2006, 138: 311–316. DOI: 10.1016/j.jhazmat.2006.05.115. |
| [36] |
WANG L, CHAO L, QU W W, et al. Ultrasound-assisted oil removal of γ-Al2O3-based spent hydrodesulfurization catalyst and microwave roasting recovery of metal Mo[J].
Ultrasonics Sonochemistey, 2018, 49: 24–32. DOI: 10.1016/j.ultsonch.2018.05.023. |
| [37] |
MARAFI M, STANISLAUS A, ABSI-HALABI M. Heavy oil hydro-treating catalyst rejuvenation by leaching of foulant metals with ferric nitrate-organic acid mixed reagents[J].
Applied Catalysis B:Environmental, 1994(4): 19–27. |
| [38] |
VALVERDE I M, PAULINO J F J, AFONSO J C. Hydrometallurgical route to recover molybdenum, nickel, cobalt and aluminum from spent hydrotreating catalysts in sulphuric acid medium[J].
Journal of Hazardous Materials, 2008, 160: 310–317. DOI: 10.1016/j.jhazmat.2008.03.003. |
| [39] |
彭人勇, 魏继宽. 从废镍催化剂中酸浸镍试验研究[J].
湿法冶金, 2019, 38(4): 287–290.
|
| [40] |
MARAFI M, RANA M S. Metal leaching from refinery waste hydroprocessing catalyst[J].
Journal of Environmental Science and Health-Part A Toxic/Hazardous Substances and Environmental Engineering, 2018, 53: 951–959. |
| [41] |
GUTNIKOV G. Method of recovering metals from spent hydrore-fining catalysts. US: 3567433[P]. 1971.
|
| [42] |
ROKUKAWA N. Method for selective recovery of molybdenum and vanadium values from spent catalysts. US: 4382068[P]. 1983.
|
| [43] |
ASGHARI I, MOUSAVI S M, AMIRI F, et al. Bioleaching of spent refinery catalysts: A review[J].
Journal of Industrial and Engineering Chemistry, 2013, 19: 1069–1081. DOI: 10.1016/j.jiec.2012.12.005. |
| [44] |
SUZUKI I. Microbial leaching of metals from sulfide minerals[J].
Biotechnology Advances, 2001, 19: 119–132. DOI: 10.1016/S0734-9750(01)00053-2. |
| [45] |
MISHRA D, KIM D J, RALPH D E, et al. Bioleaching of spent hydro-processing catalyst using acidophilic bac-teria and its kinetics aspect[J].
Journal of Hazardous Materials, 2008, 152: 1082–1091. DOI: 10.1016/j.jhazmat.2007.07.083. |
| [46] |
TANG K, BASKARAN V, NEMATI M. Bacteria of the sulphur cycle: An overview of microbiology, biokinetics and their role in petroleum and mining industries[J].
Biochemical Engineering Journal, 2009, 44: 73–94. DOI: 10.1016/j.bej.2008.12.011. |
| [47] |
MISHRA D, KIM D J, RALPH D E, et al. Bioleaching of vanadium rich spent refinery catalysts using sulfur oxidizing lithotrophs[J].
Hydrometallurgy, 2007, 88: 202–209. DOI: 10.1016/j.hydromet.2007.05.007. |
| [48] |
KIM D J, SRICHANDAN H, GAHAN C S, et al. Thermophilic bioleaching of spent petroleum refinery catalyst using sulfolobus metallicus[J].
Canadian Metallurgical Quarterly, 2012, 51: 403–412. DOI: 10.1179/1879139512Y.0000000031. |
| [49] |
MISHRA D, AHN J G, KIM D J, et al. Dissolution kinetics of spent petroleum catalyst using sulfur oxidizing acidophilic microorganisms[J].
Journal of Hazardous Materials, 2009, 167: 1231–1236. DOI: 10.1016/j.jhazmat.2009.01.056. |
| [50] |
PRADHAN D, MISHRA D, KIM D J, et al. Bioleaching kinetics and multivariate analysis of spent petroleum catalyst dissolution using two acidophiles[J].
Journal of Hazardous Materials, 2010, 175: 267–273. DOI: 10.1016/j.jhazmat.2009.09.159. |
| [51] |
朱兆鹏, 杨夫清, 梁宗跃, 等. 用等离子炉处理含钼废催化剂回收有价金属的研究[J].
中国钼业, 2003(3): 14–16.
|
| [52] |
CANHAM D L, AURICH V G. Recovery of metals from spent catalysts in a DC plasma furnace[J].
Institution of Mining and Metallurgy, 1991: 241–247. |
| [53] |
PAK J J, KIM D H, PAEK M K, et al. Ferroalloy production from spent petroleum catalysts by reductive smelting and selective oxidation processes[J].
REWAS, 2019: 167–175. |
| [54] |
HOWARD R A, BARNES, W R. Smelting process for recovery of valuable metals from spent catalysts on an oxide support. US: 5013533[P]. 1991.
|
| [55] |
王尔勤, 杨国安, 华启峰. 含钼废料回收钼的化学方法和实践[J].
中国钼业, 1998(3): 32–33.
|
| [56] |
VINCENT R, ERIC MEUX, SEBASTIEN D, et al. Hydrometallurgical treatment for valuable metals recovery from spent CoMo/Al2O3 catalyst. 1. improvement of soda leaching of an industrially roasted catalyst[J].
Industrial & Engineering Chemistry Research, 2011, 50(9): 5295–5306. |
| [57] |
张智, 高严, 刘玉珍. 含钼加氢精制废催化剂中金属钼的回收工艺研究[J].
辽宁化工, 1998, 4: 58–60.
|
| [58] |
CHOI I H, KIM H R, MOON G, et al. Spent V2O5-WO3/TiO2 catalyst processing for valuable metals by soda roasting-water leaching[J].
Hydrometallurgy, 2018, 175: 292–299. DOI: 10.1016/j.hydromet.2017.12.010. |
| [59] |
KAR B B, DATTA P, MISRA V N. Spent catalyst: secondary source for molybdenum recovery[J].
Hydrometallurgy, 2004, 72: 87–92. DOI: 10.1016/S0304-386X(03)00122-1. |
| [60] |
HUANG S B, ZHAO Z W, CHEN X Y, et al. Alkali extraction of valuable metals from spent Mo-Ni/Al2O3 catalyst[J].
International Journal of Refractory Metals and Hard Materials, 2014, 46: 109–116. DOI: 10.1016/j.ijrmhm.2014.06.005. |
| [61] |
胡建锋, 朱云, 胡汉. 从废催化剂中综合提取钒和钼[J].
稀有金属, 2006(5): 711–714.
|
| [62] |
MIHASHI T, MOTOMURA H, TAKEUCHI H. Recovering processes of valuable metals from spent petroleum hydrodesulphurisation catalysts. Japan: 57022119[P]. 1982.
|
| [63] |
HO E M. Recovery of metals from spent catalysts[D]. Honours Thesis, Murdoch University, Perth, Australia, 1992.
|
| [64] |
HONG I K, KYUNG H P, DEVABRATA M. Influence of sulfuric acid baking on leaching of spent Ni-Mo/Al2O3 hydro-processing catalyst[J].
Hydrometallurgy, 2009, 98: 192–195. DOI: 10.1016/j.hydromet.2009.04.002. |
| [65] |
ILHAN S. Extraction of molybdenum, nickel and aluminium from spent Ni-Mo hydrodesulphurization (HDS) catalyst in oxalic acid solutions[J].
Canadian Metallurgical Quarterly, 2020, 59: 26–35. DOI: 10.1080/00084433.2020.1715691. |
| [66] |
刘润静, 李小云, 郭春. 从钴—钼废催化剂中回收钼的研究[J].
无机盐工业, 1996(2): 34–36.
|
| [67] |
陈兴龙, 肖连生, 徐劼, 等. 从废石油催化剂中回收钒和钼的试验研究[J].
矿冶工程, 2004(3): 47–49.
|
| [68] |
YE X L, GUO S H, QU W W, et al. Microwave sodium roasting (MWSR) spent HDS catalysts for recovery Mo and in situ sulfur fixation[J].
Journal of the Taiwan Institute of Chemical Engineers, 2019, 97: 146–157. DOI: 10.1016/j.jtice.2019.01.009. |
| [69] |
YARAS A, ARSLANOGLU H. Extraction of selected metals from spent hydrodesulfurization catalyst using alkali leaching agent[J].
Separation Science and Technology, 2019: 1–12. |
| [70] |
PARKINSON G, ISHIO S. Recyclers try new ways to process spent catalysts[J].
Chemical Engineering, 1987, 94: 25–31. |
| [71] |
ZHANG J L, YANG C, CHEN Y Q, et al. Encient phase transformation of γAl2O3 to αAl2O3 in spent hydrodesulphurization catalyst by microwave roasting method[J].
Industrial & Engineering Chemistry Research, 2019, 58: 1495–1501. |
 2020, Vol. 11
2020, Vol. 11


