| 树脂法提取茶多酚的工艺研究 |
茶多酚(Tea polyphenols, 简称TP),纯净物为白色无定形结晶,提取过程中易被氧化呈淡黄至淡褐色.易溶解在水中, 能溶解于有机溶剂,不溶解于氯仿[1, 2].通常由茶叶中提取得到,是茶叶中的主要有效成分[3].研究表明茶多酚在降血脂[4, 5]、抗氧化[6-8]、消炎杀菌[9, 10]、防癌防辐射[11, 12]等方面有显著功效,在食品、饮品、冷藏等方面的研究前景广阔[13].国内外,关于茶多酚的提取技术主要有:溶剂萃取法、沉淀提取法、层析法和超临界流体萃取法[14, 15].近两年有一种双水相的方法用于茶多酚的提取,该法是利用两相间的选择性分配来得到目标成分,李洋等[16]利用此法使茶多酚提取率达到17.43%.
实验选用树脂法提取茶汤中的茶多酚,树脂的价格虽然较高,但比超临界萃取法更为经济,且该法吸附分离简便,操作工艺简单,不像有机溶剂法需要一再地提取除杂,牛志平等[17]分别用8种树脂作为吸附剂,用2 BV水作清洗液, 70%乙醇(2.5 BV)作解吸剂进行解吸.结果发现可使解吸率达到98.2%, 产品得率为85.8%.曹雪文等[18].利用XDL-1树脂对茶多酚进行纯化,并利用Design-Expert软件进行单因素条件优化,在较优实验条件下可得到纯度为67.09%的茶多酚.树脂法耗能低,生产条件温和,能够有效避免产品失活,树脂也可循环再生,整个分离过程以乙醇作为洗脱剂,乙醇回收较为容易,无毒、无污染,此法提取茶多酚十分有意义[19, 20].
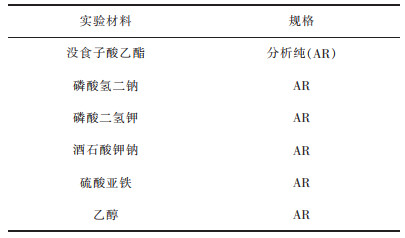
1 材料与方法 1.1 材料实验采用的12种树脂包括DM-8、DM-131、DM-16X、DM-130、NKA-9、HPD-600、聚酰胺、NKA-2、LSA-21、X-5、DM-301、HZ-802均来自艾美康健树脂公司,绿茶茶叶来自江西某茶厂,其他实验药品见表 1.
| 表 1 实验所需材料 Table 1 Materials required for the experiment |
 |
| 点击放大 |
1.2 仪器
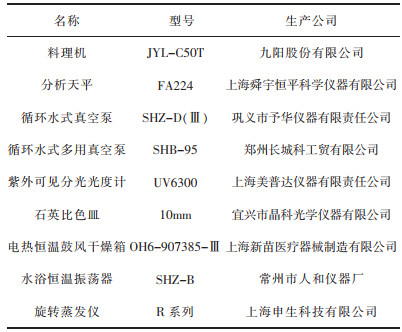
实验仪器主要有:料理机将茶叶打碎成粉末状;分光光度计、比色皿测定溶液中茶多酚含量;恒温振荡器控制多个样品处于同一吸附温度与振荡频率;旋转蒸发仪除去脱附液中的有机溶剂.实验中具体仪器设备见表 2.
| 表 2 实验用仪器设备 Table 2 Experimental equipment |
 |
| 点击放大 |
2 实验 2.1 树脂的筛选 2.1.1 树脂的预处理
树脂的预处理:将12种大孔树脂洗净,用95%的乙醇溶液浸泡24 h,使其充分激活,之后用蒸馏水洗涤至无明显醇味,用水浸泡备用.
2.1.2 茶叶浸提液的制备茶汤的制备:将5 g茶叶用料理机打碎,并用孔径为450?滋m的筛子筛下茶叶粉末,使茶叶粉末与蒸馏水以料液比为1:20在80 ℃下浸提3次,第1次浸提1 h,过滤,留下滤液,将滤渣进行第2次和第3次浸提,均浸提30 min.之后将滤液合并,定容至500 mL.
2.1.3 茶多酚含量的测定方法酒石酸亚铁法(GB/8313—2002)测定、超高液相色谱法.
酒石酸亚铁法比色液的配制:取2 mL的待测液、10 mL酒石酸铁溶液(硫酸亚铁1.0 g,酒石酸钾钠5.0 g加水溶解并定容至1 L)于50 mL容量瓶,用pH=7.5的磷酸盐缓冲液(a液(1/15 moL的磷酸氢二钠溶液):b液(1/15 moL的磷酸二氢钾溶液)=85:15)定容至刻度线.
2.1.4 实验过程及计算筛选出较优吸附量与脱附率的树脂之后,再利用单因素实验对动态吸附的吸附速度、脱附速度、脱附体积进行研究,并且通过吸附特性曲线的描绘得出合理的吸附体积以防吸附过程中发生穿透现象,浪费原料.

|
(1) |

|
(2) |

|
(3) |
吸取待测液2 mL,注入50 mL容量瓶中,加酒石酸亚铁溶液10 mL,充分混合,再加pH为7.5的缓冲液至刻度,用10 mm比色杯,在波长540 nm处以空白溶液作参比.
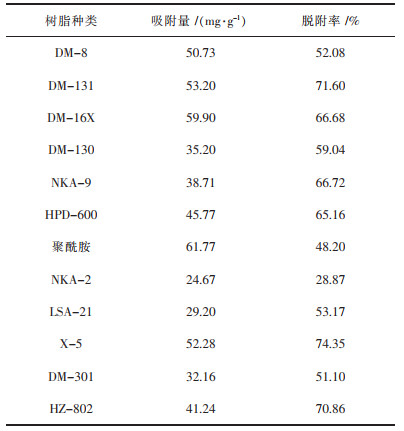
3 结果与讨论 3.1 吸附树脂的选择结果精确称量树脂2 g,预处理后转移至锥形瓶中,加入50 mL的10 mg/mL的茶汤,每隔10 min用恒温振荡器在30 ℃下振摇10 s,持续1.5 h.之后取出锥形瓶,静置24 h,使其吸附饱和.吸取上层液,测定茶多酚含量,计算静态饱和吸附量和脱附率.除去上层的吸附液,用滤纸吸干12种吸附饱和树脂上的水分,再用30 mL 70%的乙醇将这12种树脂分别转移到另12个锥形瓶中,放入30 ℃的恒温振荡器中震摇1.5 h,将解析液过滤,测解吸率.结果见表 3.
| 表 3 不同树脂茶汤吸附量 Table 3 Adsorption capacity of different resin tea soup |
 |
| 点击放大 |
根据实验测得的各种树脂的性能参数:聚酰胺的吸附量最大,其次是DM-16X,之后是DM-131、X-5树脂.而脱附率从大到小的顺序则是X-5 > DM-131 > DM-16X, 综合考虑这几种树脂的吸附量和脱附率的差值,本实验选取DM-16X作为实验树脂.
3.2 动态吸附实验 3.2.1 上样速度对吸附性能的影响取10 mL预处理好的DM-16X树脂湿法装柱,导入一定体积的茶汤于柱中.上柱流速分别为2 BV/h、4 BV/h、6 BV/h、8 BV/h、10 BV/h、12 BV/h.检测各个速度下每2.5 BV流出液中茶多酚的含量,考察上柱液流速对树脂吸附茶多酚的影响,绘制动态吸附曲线,结果如图 1所示.
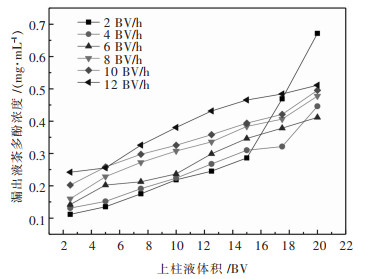 |
| 图 1 吸附速度对吸附特性的影响 Fig. 1 Effect of adsorption rate on adsorption characteristics |
根据图 1可以看出,流速是通过影响溶质在树脂表面的扩散从而影响吸附效果.各曲线均为增长型,且在第6组样品开始,茶多酚漏出液浓度增长明显,其中2 BV/h曲线该现象最为突出,这是因为在最后几组样品中茶多酚已经发生穿透,而2 BV/h速度实验由于流速慢使得前几组体积的茶汤吸附得较为完全,在收集第7个和第8个样品时已达到树脂吸附饱和状态,故之后穿透更为明显.其他速度实验由于流速更快吸附不够饱和,因此在最后几个样品中均未发生像2 BV/h速度实验那样增长太过明显的现象.从实验结果可知6 BV/h比起2 BV/h、4 BV/h更快,但是其漏出茶多酚的现象比起8 BV/h、10 BV/h更不明显,其曲线的增长幅度又更均匀,较易控制.因此上柱流速选择6 BV/h.
3.2.2 吸附特性曲线以6 BV/h的流速、茶多酚浓度为1.51 mg/mL、体积为200 mL的茶汤上柱,每隔2.5 BV分步收集流出液,测定其茶多酚的含量以绘制该曲线.结果如图 2所示.
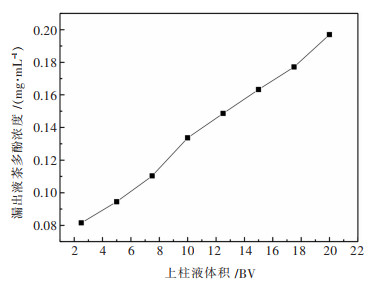 |
| 图 2 吸附特性曲线 Fig. 2 Adsorption characteristics |
由吸附特性曲线图(图 2)可见,漏出液中茶多酚量增加得较为稳定,直到第5个样品,茶多酚的漏出浓度约为0.15 mg/mL达到原液浓度的9.87%,第6个样品茶多酚浓度为0.16 mg/mL,占原液浓度的10.84%.因此可以确定在第5个和第6个样品之间发生穿透现象(当漏出液茶多酚浓度达到原液浓度的10%时即发生穿透现象),因此本实验的原液体积宜控制在12.5 BV.
3.2.3 脱附剂体积对脱附率的影响按确定好的较优吸附条件进行上柱,吸附平衡后用等量蒸馏水淋洗树脂,洗脱流速选择8 BV/h,并且以70%的乙醇作为洗脱剂,洗脱液体积20 mL、40 mL、60 mL、80 mL和100 mL.分别测定各个体积的乙醇的脱附率见图 3,并选择出较优洗脱体积.
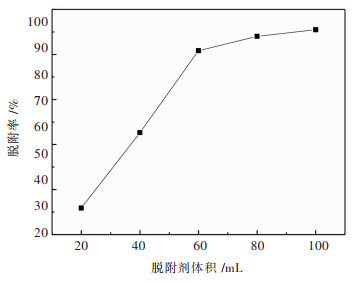 |
| 图 3 脱附体积对脱附率的影响 Fig. 3 Effect of desorption volume on desorption rate |
由图 3可知:洗脱剂用量越大,洗脱率越大,当洗脱剂体积为100 mL时,茶多酚几乎完全被洗下,而80 mL时洗脱率也超过95%,与100 mL的洗脱率相差不大,为节省乙醇,选择80 mL脱附.
3.2.4 脱附速度对脱附率的影响按确定好的较优吸附条件进行上柱,吸附平衡后用等量蒸馏水淋洗树脂,以80 mL,70%的乙醇作为洗脱剂,测量洗脱速度为2 BV/h、4 BV/h、6 BV/h、8 BV/h、10 BV/h下的洗脱率,选择出较优的脱附速度.脱附速度对脱附率的影响如图 4所示.
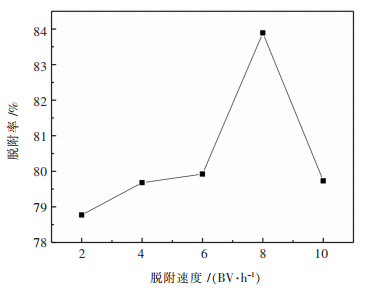 |
| 图 4 脱附速度对脱附率的影响 Fig. 4 Effect of desorption rate on desorption rate |
由图 4可知:流速为8 BV/h时,脱附率最大,小于8 BV/h时,由于流速过慢,洗脱过程中扩散速率较慢,外扩散阻力较大,影响了脱附率,导致脱附率较小.因此,本实验将动态洗脱流速控制在8 BV/h.
按较佳条件处理所得最终产品的UPLC(超高液相色谱)检测色谱图如图 5所示.
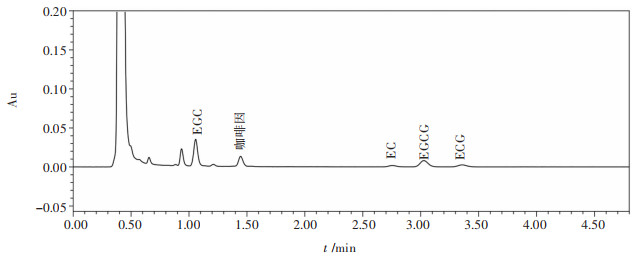 |
| 图 5 最终茶汤样品UPLU色谱 Fig. 5 Final tea soup sample UPLU chromatography |
| 表 4 茶汤中4种儿茶素及咖啡碱的回归方程 Table 4 Regression equation of four catechins and caffeine in tea soup |
 |
| 点击放大 |
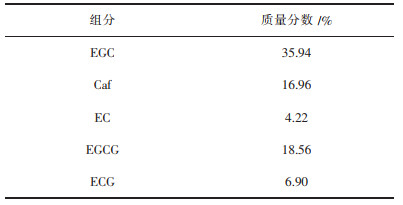
| 表 5 4种儿茶素及咖啡碱的含量 Table 5 Content of four catechins and caffeine |
 |
| 点击放大 |
由酒石酸亚铁法测出产品茶多酚含量(质量分数,下同)为76.57%,根据UPLC检测:EGC含量为35.94%;EC含量为4.22%,EGCG含量为18.56%,ECG含量为6.9%;最终计算得4种儿茶素的含量达到65.62%,咖啡碱含量为16.96%.
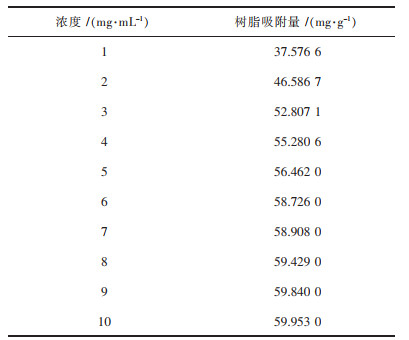
4 吸附热力学、吸附动力学研究 4.1 吸附热力学研究 4.1.1 DM-16X树脂吸附等温线的绘制准确称取5.0 g经过预处理的DM-16X树脂,放入100 mL的锥形瓶中,然后分别加入茶多酚浓度为1 mg/mL、2 mg/mL、3 mg/mL、4 mg/mL、5 mg/mL的溶液, 25 ℃下震荡至吸附平衡,分析上清液茶多酚浓度.以茶多酚的浓度作为横坐标,把树脂的吸附量作为纵坐标,具体数据见表 6,绘制吸附等温线,如图 6所示.
| 表 6 吸附热力学实验数据 Table 6 Adsorption thermodynamic experimental data |
 |
| 点击放大 |
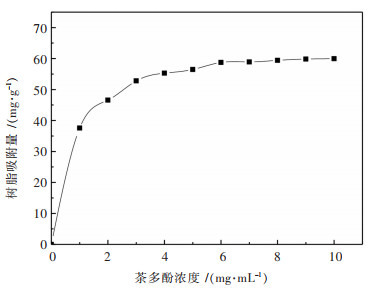 |
| 图 6 DM-16X树脂吸附等温线(25℃) Fig. 6 DM-16X resin adsorption isotherm (25℃) |
由图 6可见,DM-16X树脂对茶多酚符合单分子层吸附体系,其吸附等温线可用Langmuir方程描述,图 6中吸附等温线的斜率随着茶多酚浓度的增加而逐渐降低.说明随着茶多酚浓度的升高,茶多酚分子和树脂之间的亲和力降低.
4.1.2 吸附热力学方程的求解Langmuir建立了单分子层的吸附等温线,该吸附等温线有以下几个假设:吸附运动是在活性中心上进行的,每个活性中心有比较远的距离,且有相同的能量,各个分子之间没有相互作用,吸附呈现单分子吸附.
吸附速度与吸附质的浓度成正比关系,同时也和吸附剂表面上还没被吸附质占有的活性中心的数目成正比,脱附速度会和已经被吸附质占有了的活性中心的数目成正比.即
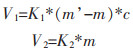
|
V1为吸附速度;V2为脱附速度;m为每克吸附剂的吸附量;m′为每克吸附剂的最大吸附量;c为吸附质溶液浓度;K1为吸附速度;K2为脱附速度.
吸附平衡时有
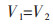
|
推导出方程
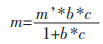
|
令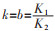
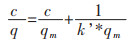
|
qm为吸附剂的最大吸附量;q为吸附剂的吸附量;k’为Langmuir吸附常数.
根据以上所得数据,DM-16X树脂的吸附等温线方程为:
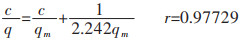
|
向5 g已经处理好的DM-16X树脂中加入已知浓度的茶汤,每隔30 min测定茶多酚含量,结果如图 7所示.
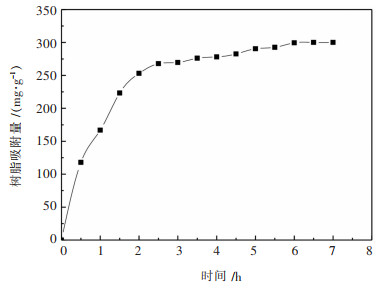 |
| 图 7 吸附动力学曲线 Fig. 7 Adsorption kinetics curve |
由图 7可以看出5 g的DM-16X树脂对茶多酚的吸附量随着时间的增大而增大,最后在时间为6 h时趋于平衡,实验过程中,不仅要考虑树脂的吸附性能,还要考虑吸附时间,时间不够,树脂的吸附量达不到最大,时间太长,不利于实验的进行.
4.2.2 平衡常数k的求解根据以上吸附动力学实验所得数据,结合Langmuir吸附速率方程,该直线斜率即为该吸附剂的平衡速率常数k,经计算可得k=0.82 h-1.以时间t为横轴,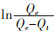
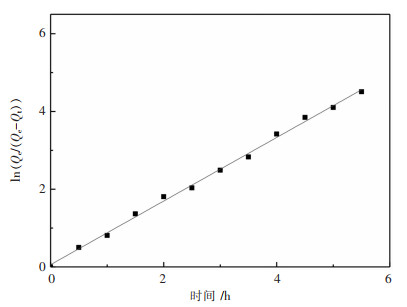 |
| 图 8 吸附速率图示 Fig. 8 Adsorption rate map |
由图 8可求得k值大小,k值越大,吸附速率越大,反之则越小.计算得吸附动力学方程如下:
Langmuir吸附速率方程:
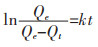
|
其中:Qt为t时刻树脂吸附量(mg/g);Qe为吸附平衡时树脂吸附量(mg/g);k为平衡速率常数.
最终得到吸附动力学方程为:
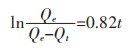
|
1)通过对12种树脂的选型实验,得出DM-16X为实验较优树脂.
2)动态吸附实验中,流速对于树脂吸附茶多酚量的研究表明,流速为6 BV/h速度适宜,茶多酚的漏出浓度均匀,速度调控更加方便.
3)吸附特性曲线表明吸附流速6 BV/h时,用10 mL树脂吸附含茶多酚1.51 mg/mL的茶汤,吸附体积最好控制在12.5 BV及之前,否则发生穿透现象.
4)通过研究不同体积和脱附速度脱附液对树脂中茶多酚的脱附率可知,80 mL、8 BV/h的乙醇溶液脱附效果不仅好而且经济.
5)本实验得出的DM-16X对茶多酚的吸附—脱附工艺条件得到的成品茶多酚最终测定纯度可达76.57%,其中计算得4种儿茶素的含量达到65.62%,咖啡碱含量为16.96%.
6)通过DM-16X吸附等温线图可发现:该树脂对于茶多酚的吸附过程属于单分子层吸附,可用Langmuir方程进行描述.结合试验所得数据,利用orign软件对图形进行曲线拟合,可得吸附等温线方程为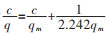
7)由吸附动力学曲线,DM-16X树脂吸附性能较好,吸附平衡常数k=0.82 h-1.
| [1] |
陈继英, 郭嘉林, 张存彦, 等. 茶多酚的研究进展[J].
中草药, 2004, 35(10): 011–013.
|
| [2] |
茶多酚的药理作用研究进展[J].药物评价研究, 2013, 36(2): 157-160.
|
| [3] |
汪多仁. 茶多酚的开发与应用进展[J].
饮料工业, 2011, 14(1): 11–14.
DOI: 10.3969/j.issn.1007-7871.2011.01.001.
|
| [4] |
GUO X, CHENG M, ZHANG X, et al. Green tea polyphenols reduce obesity in high- fat diet-induced mice by modulating intestinal microbiota composition[J].
International Journal of Food Science & Technology, 2017, 52(8): 1723–1730. |
| [5] |
AHMADI A, KHALILI M, MASHAEE F, et al. The effects of solvent polarity on hypoglycemic and hypolipidemic activities of vaccinium arctostaphylos l. unripe fruits[J].
Pharmaceutical Chemistry Journal, 2017, 50(11): 746–752. DOI: 10.1007/s11094-017-1524-4. |
| [6] |
ALI B, LEE L H, LASKAR N, et al. Modified green tea polyphenols EGCG-S and LTP inhibit endospore in three bacillus spp[J].
Advances in Microbiology, 2017, 7(3): 175–187. DOI: 10.4236/aim.2017.73014. |
| [7] |
GAO Y. The Research of the relationship between antioxidation of tea extractive and tea polyphenols as well as catechins[J].
Journal of Chinese Institute of Food Science & Technology, 2013, 13(6): 40–47. |
| [8] |
TIPOE G, LEUNG T M, HUNG M W, et al. Green tea polyphenols as an anti-oxidant and anti-inflammatory agent for cardiovascular protection[J].
Cardiovascular & Hematological Disorders-Drug Targets, 2007, 7(2): 135–144. |
| [9] |
WANG X, HAO L, ZHANG C, et al. High efficient anti-cancer drug delivery systems using tea polyphenols reduced and functionalized graphene oxide[J].
Journal of Biomaterials Applications, 2017, 31(8): 1108–1122. DOI: 10.1177/0885328216689364. |
| [10] |
OZ H S, CHEN T S, VILLIERS W J S D. Tu1644 green tea polyphenols and sulfasalazine have parallel anti-Inflammatory properties in colitis models[J].
Frontiers in Immunology, 2013, 4(5): 132. DOI: 10.1016/S0016-5085(13)63013-9. |
| [11] |
ZHANG L, LI S, DONG Y, et al. Tea polyphenols incorporated into alginate-based edible coating for quality maintenance of Chinese winter jujube under ambient temperature[J].
LWT - Food Science and Technology, 2016, 70: 155–161. DOI: 10.1016/j.lwt.2016.02.046. |
| [12] |
WANG J, PAN Y, HU J, et al. Tea polyphenols induce s phase arrest and apoptosis in gallbladder cancer cells[J].
Brazilian Journal of Medical & Biological Research, 2018, 51(4): 82–86. DOI: 10.1590/1414-431x20176891. |
| [13] |
马梦君, 罗理勇, 李双, 等. 茶多酚和咖啡碱对茶乳酪形成的影响[J].
食品科学, 2014, 35(13): 15–19.
DOI: 10.7506/spkx1002-6630-201413003.
|
| [14] |
王玉春, WANG Yu-chun. 茶多酚的提取方法及应用研究进展[J].
兰州文理学院学报(自然科学版), 2008, 22(3): 51–55.
DOI: 10.3969/j.issn.1672-691X.2008.03.016.
|
| [15] |
杨世军, 张会香. 茶多酚的提取工艺研究[J].
食品工业, 2004(6): 34–35.
|
| [16] |
李洋, 熊道陵, 张建平, 等. 响应面法优化微波-超声耦合双水相提取茶多酚工艺[J].
江西理工大学学报, 2018, 39(1): 52–59.
|
| [17] |
牛志平, 高伟, 王红霞, 等. 树脂法制备高含量茶多酚工艺研究[J].
中国食品添加剂, 2017(1): 100–104.
DOI: 10.3969/j.issn.1006-2513.2017.01.008.
|
| [18] |
曹雪文, 熊道陵, 李洋, 等. 响应面法优化树脂纯化茶多酚工艺研究[J].
江西理工大学学报, 2018, 39(5): 58–65.
|
| [19] |
孙健.茶多酚的定性定量分析方法及大孔吸附树脂纯化工艺条件优化的研究[D].大连: 大连理工大学, 2002.
|
| [20] |
叶俭慧, 梁月荣. 大孔吸附树脂分离茶多酚的研究[J].
茶叶, 2006, 32(3): 128–132.
DOI: 10.3969/j.issn.0577-8921.2006.03.002.
|
 2019, Vol. 10
2019, Vol. 10


