| Mg-Al-Pb-Ga-Y海水电池用镁阳极的成分优化和电化学性能 |
2. 中南大学材料科学与工程学院,长沙 410083
2. School of Materials Science and Engineering, Central South University, Changsha 410083, China
镁合金电化学性能优异, 能量比容量大、标准电极电位较负(-2.375 V)、电化学当量高(2 200 Ah/kg), 是一种理想的牺牲阳极材料、电池负极材料[1-2], 可应用于海上浮标、水下推进器[3]和生物微系统[4]等方面.
目前常用的镁合金用阳极材料有AZ系列、英国镁电子公司研发的AP65, 以及俄罗斯研发的Mg-Hg阳极材料[5]等.常见的AZ系列合金有AZ31、AZ61和AZ91, 其特点是耐蚀性强, 自腐蚀速率低[6-7], 利用率高, 适合于小电流密度和功率低的一次性电池中使用[8].但AZ系列镁阳极仍存在许多缺点,这也限制了其进一步发展和应用. AZ系列镁阳极的放电活性低、放电电压小, 难以满足电池所需要的比能量和比功率[9],增加了一次性电池的更换次数和成本.研究表明,添加活性元素是目前提高镁海水电池阳极化学活性和工作电压的常见方法.
Al、Hg、Sn、Pb、Ga、Zn、Mn、稀土元素等是镁合金阳极中常用的活性元素[10]. Beldjoudi T等[11]发现Al能固溶在基体中, 提高镁合金表面膜的稳定性.但是Al含量过多时, 过量的Al容易与Mg结合生成Mg2Al3第2相, 导致晶间腐蚀, 降低合金的耐蚀性能[12].稀土元素可细化镁合金晶粒[13-14], 或与其他元素形成表面膜[15]的方式, 这是因为稀土元素易氧化, 形成钝化膜, 提高合金耐蚀性的作用.研究表明[16],当合金中存在Al元素时, Pb加入后, 在放电过程中, Pb2+以PbO2的形式沉积在电极表面, 并在于Al的共同作用下剥落放电产物, 维持放电活性和放电电压. Shaoqian Yuan[17]认为In和Ga的加入使合金电位负移, 增加了合金的电容密度和功率密度.这是由于Hg、Ga和In元素之间的溶解沉积作用[18]或与Pb、Sn元素形成低熔点共熔物来破坏合金表面钝化膜, 保持了镁阳极持续地活化溶解, 提高合金放电电压.
很多文章研究了Pb和Ga元素的单一添加对镁阳极性能的影响, 结果表明,Pb、Ga对合金起到重要的活化作用,可提高合金的化学活性和放电电压. HamedMoghanni等[19]研究了Pb、Ga的混合添加对Al阳极的影响,发现在铝中添加Pb和Ga后,合金表面点蚀更严重,产生了明显的铝活化且活化程度与合金元素的含量直接相关.但Pb、Ga和稀土元素的混合添加以及不同配比对镁合金组织和电化学性能影响的研究却较少.研制添加提高镁阳极放电电压、化学活性的合金元素的镁合金材料, 探究其放电行为和电化学性能, 具有重要的理论和工程实际意义.文中基于AZ31镁阳极,以Mg-Al-Pb-Ga为合金体系, 改变添加元素的含量, 研究Pb、Ga元素对合金电化学性能的作用.
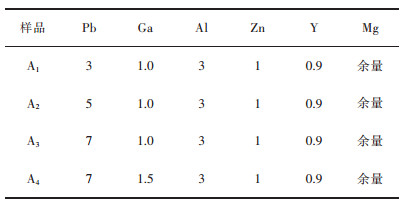
1 实验拟定合金元素的添加量,如表 1所列.
| 表 1 4组合金的化学成分/% Table 1 Chemical composition of four alloy /% |
 |
| 点击放大 |
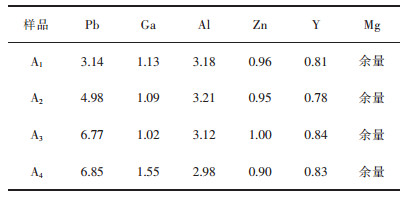
实验用的镁合金由熔炼铸造的方法制得.添加的合金元素分别是纯度均为99.99%的Mg、Al、Pb、Zn、Ga, 稀土元素Y以Mg-25%Y中间合金的形式加入.将实验原料按设计方案进行配料, 在氩气保护下在电阻炉中熔炼.熔炼温度为750 ℃, 待金属熔融之后, 搅拌除渣, 并在720 ℃下静置10 min.在硫粉的保护下将熔融金属液浇铸于铸铁模中, 冷却得到铸锭.铸态镁锭在400 ℃保温24 h,得到均匀化态镁锭.对均匀化态镁合金进行成分测试,结果如表 2所列.
| 表 2 4组合金的实际化学成分/% Table 2 Actual chemical composition of four alloy /% |
 |
| 点击放大 |
用金相砂纸将样品打磨, 金刚石研磨膏抛光, 再用3 g苦味酸, 2.5 mL醋酸, 50 mL无水乙醇和5 mL去离子水进行腐蚀.采用LEICA MC120 HD金相显微镜进行显微组织观察.采用扫描电子显微镜和能谱分析仪对合金铸态和均匀化态组织以及放电后形貌进行观察分析.
采用D/Max2500型号X射线衍射仪对合金铸态和均匀化态组织进行相组成分析.取测试样品, 用由粗到细的金相砂纸连续打磨, 最后用1 200#砂纸磨光表面.扫描速度为8 °/min, 扫描范围为10°~80°.
9组样品的电化学实验包括恒电流极化测试和动电位极化测试.所有样品的测试尺寸均为10 mm×10 mm.样品用金相砂纸后用去离子水清洗, 冷风吹干.测试仪器为CS310电化学工作站, 采用的体系为三电极体系.所有测试均在(25±1)℃下的3.5%NaCl溶液中进行.为了确保重复性, 所有电化学均测试3次以上.
恒电流极化曲线测试分别是在20 mA/cm2和100 mA/cm2的电流密度下进行的, 测试时间为600 s.动电位极化曲线的测试在OCP稳定之后进行的, 扫描范围为OCP上下0.2 V, 扫描速率为1 mV/s.
2 结果与分析 2.1 显微组织分析图 1所示分别为4组合金A1、A2、A3、A4的铸态金相图, 铸态组织主要由α-Mg基体和第2相组成.晶内第2相较少, 在晶界上分布着大量连续的第2相. 4个样品的铸态组织中的晶粒呈等轴晶分布, 平均晶粒尺寸相近, 为30~40 μm之间.
 |
| 图 1 4组合金的铸态金相图 Fig. 1 Optical microstructure of the prepared samples |
图 2所示为4组合金均匀化后的样品的金相组织图.经过均匀化处理后, 晶粒长大, 最大尺寸达到200 μm.与铸态组织相比,第2相的数量减少, 晶界上无明显第2相存在,说明第2相回溶到基体, 只有少数较为稳定的第2相保存下来.
 |
| 图 2 4组合金的均匀化态态金相图 Fig. 2 Homogeneous microstructure of all alloys |
图 3所示为A1样品和A4样品铸态和均匀化态的XRD图谱.合金中主要为α-Mg相.同时, 还存在一定的Al2Y、Ga5Mg2和MgZn相.这些相是熔融金属凝固过程中生成的初生相,大量分布在晶界,这与先前的文献[20-22]研究结果相符合.对于Al2Y、Ga5Mg2和MgZn相,在400 ℃均匀化退火时,温度没有达到其物相转变的温度,没有发生变化.尤其是Al2Y相,该相具有高温稳定性,一般在镁合金的均匀化温度下不会回溶进基体.在铸态下还含有一定的Al12Mg17相,根据Mg-Al相图可知,Al含量为13%时才出现共晶Al12Mg17相,而实验中Al含量仅为3%便有Al12Mg17相,说明液态金属冷却时发生了非平衡凝固.经过均匀化退火后, 该相消失, 说明经过均匀化后Al12Mg17相溶进基体里[23].
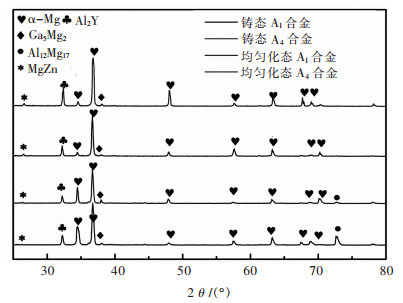 |
| 图 3 A1和A4样品铸态和均匀化态的XRD图谱 Fig. 3 XRD patterns of as-cast and homogenized samples of A1 and A4 |
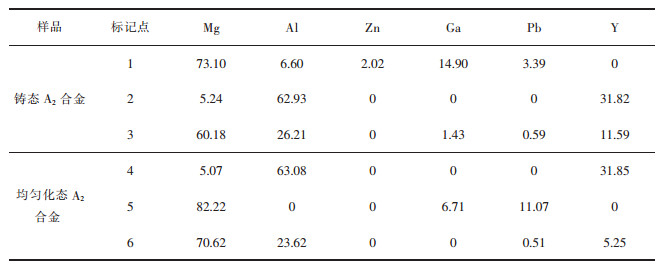
图 4所示为A2号样品在铸态和均匀化态下的扫描电镜图,表 3所列为图 4中各点的原子百分比.结合两者分析, 如图 4(a)和图 4(b)所示, 铸态合金中含有连续分布在晶界的第2相(主要为Ga5Mg2和MgZn2的混合相)和一些Al2Y稀土相.同时, Al17Mg21相以细长的形状分布在晶界上(图 4(c)中的点3).由于Pb元素在镁中的固溶度较高,因此主要固溶在基体里.从图 4(d)、图 4(e)、图 4(f)中可以看出, 均匀化退火后样品中的大部分第2相溶于基体, 晶间粗大的相减少, 组织更加均匀.由于稀土相具有高温稳定性[19], 经过400 ℃的均匀化处理后组织中仍有稀土相存在.
 |
| 图 4 A2号样品的扫描电镜像 Fig. 4 Scanning electron microscope graph of sample A2 |
| 表 3 铸态和均匀化态A2合金中各点的原子百分比/% Table 3 Mass percentage of points in As-cast and homogeneous A2 Alloys /(atom, %) |
 |
| 点击放大 |
2.2 合金元素对合金的电化学和腐蚀性能的影响
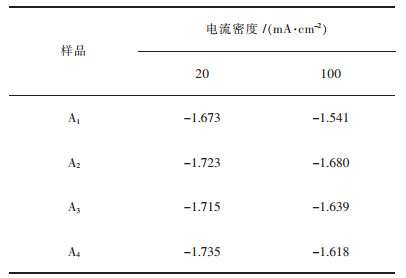
图 5所示为4组合金在20 mA/cm2和100 mA/cm2下的恒电流放电曲线.从图 5中可以看出,放电过程中,A1、A3和A4均出现一定程度的极化, 电位正移. A2合金不仅放电电位负, 放电平稳极化小, 而且激活时间短. 表 4为合金的放电电位. 图 5(a)中, 电流密度为20 mA/cm2时, A3号样品具有最负的电位, 达到-1.735 V, 其次为A2合金,为-1.723 V. A1样品具有最正的电位, 为-1.673 V.如图 5(b)所示, 电流密度为100 mA/cm2时, A2号样则具有最负的放电电位, 达到了-1.680 V, 其次为A4号样品, 电位为-1.639 V, A1号样品的电位只有-1.541 V.
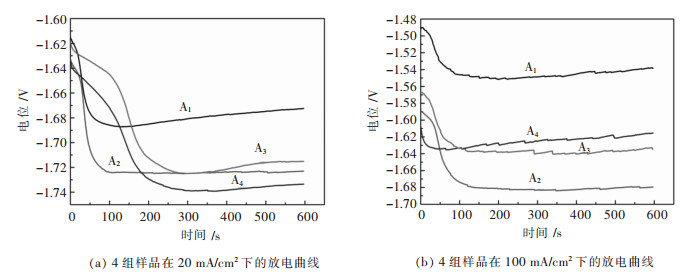 |
| 图 5 样品的恒电流放电曲线 Fig. 5 Constant current discharge curves of A1, A2, A3 and A4 alloy at current densities of 20 mA/cm2 and 100 mA/cm2 |
| 表 4 4组合金在不同电流密度下的放电电位 Table 4 Discharge potential of four samples |
 |
| 点击放大 |
在小电流密度(20 mA/cm2)下放电, Pb含量为5%和7%(A2、A3)时的合金放电电压明显比含量为3%(A1)时更大,这可能与Pb2+的浓度有关, 研究[16]发现Pb和Al元素间存在协同作用, Pb2+以化合物的形式在合金表面沉积,促进Al3+以Al(OH)3的形式沉积在电极表面,并以2Mg(OH)2 Al(OH)3的形式剥落放电产物,带动其他放电产物的脱落对镁阳极起到活化作用.因此A2、A3中Pb2+浓度的增加促使放电产物快速脱落,提高了合金放电活性. A4的放电电压比A3大0.2 V, 这是因为Ga含量的增加(多0.5%)有效提升了合金的放电电压. Pb和Ga元素间有沉积-溶解作用, 两者容易生成可黏附在基体表面的, 易脱落的低熔点物质,如Ga(OH)3, 维持后续反应的进行[20].Ga(OH)3的生成与元素Ga的添加量有直接关系,因此Ga含量的增加有利于合金的放电电压.
在大电流密度下(100 mA/cm2)放电时, 如图 5(b), A2合金具有最大的放电电位, A1则具有最小的电位, A2比A1的电位大0.139 V, A3、A4电位相差不大.该电流密度下, Pb含量为5%(A2)时合金具有最大的放电电压. Ga含量由1%(A3)增加至1.5%(A4)时, 合金的放电电压反而减小.导致这个现象的原因可能有2个:①在大电流密度下, 第2相加快了自腐蚀, A4合金中Ga5Mg2相含量更大,造成电流效率降低;②放电反应剧烈, 放电过程中Pb和Ga元素生成的低熔点物质附着在合金表面, 阻碍合金新鲜表面与电解液的接触, 降低了合金活性和电流效率.对比AZ31的恒电流极化曲线[16, 21], 可以发现A2合金有更负且稳定的放电电位, 说明A2合金具有更优异的放电性能.
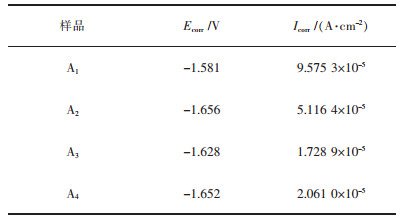
图 6所示为4组样品A1、A2、A3、A4的动电位极化曲线图, 表 5为拟合出的极化曲线数据. A2合金具有最负的腐蚀电位, 为-1.656 V, 其次为A4、A3和A1, 说明Pb和Ga元素都能有效提高A2合金的化学活性. A1样品的腐蚀电流密度最大, 达到9.4019×10-5A/cm2, 其次为A2样品的5.1164×10-5A/cm2, A4的腐蚀电流密度最小, 为1.7289×10-5A/cm2.由于Pb具有高析氢过电位, 对于A3和A4合金,Pb含量最高(达到7%), 合金的腐蚀电流密度会减小. A3样品相比A4样品Ga含量多0.5%, Ga元素提高合金的化学活性的同时, 腐蚀电流密度也更大.
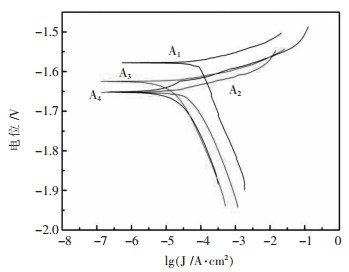 |
| 图 6 4组样品的动电位极化曲线 Fig. 6 Potentiodynamic polarization curves of A1, A2, A3 and A4 alloys |
| 表 5 4组合金的极化曲线参数 Table 5 Polarization curve parameters of four samples |
 |
| 点击放大 |
2.3 放电后形貌观察
图 7所示为AZ31和A2样品在20 mA/cm2和100 mA/cm2电流密度放电后的样品形貌图.在20 mA/cm2电流密度放电后, AZ31出现明显的局部放电现象, 基体上只有少数裂纹存在(图 7(a)),部分基体维持原貌;而A2样品放电后呈现一个均匀的放电形貌, 放电产物和裂纹遍布整个合金表面,如图 7(b)所示,表明A2合金具有更高的放电活性.从图 7(c)和图 7(d)可以看到, 在100 mA/cm2电流密度下放电后, 两者均出现严重的放电产物覆盖现象, 存在大量裂纹, 而在图 7(d)圆圈部分可以看到放电产物出现脱落后的痕迹.放电产物脱落后, 合金不断暴露在电解液中, 维持了阳极的电化学活性, 使合金保持平稳的放电过程而不出现严重的极化现象.
 |
| 图 7 AZ31和A2合金在20 mA/cm2和100 mA/cm2电流密度放电后的形貌 Fig. 7 Morphology of AZ31 and A2 alloys after discharge at 20 mA/cm2 current density and 100 mA/cm2 |
结合A2合金组织以及放电形貌,可推测A2和AZ31在放电过程表面发生的反应. A2和AZ31合金的均匀化退火后,A2组织中晶粒内和晶界上分布着第2相,AZ31合金组织中几乎没有第2相存在.放电反应发生时(特别是小电流密度),对于A2合金,Pb和Ga元素可固溶在基体中提高镁阳极的电化学活性.同时,合金元素间某些相互反应生成的第2相,如Mg5Ga2和Al2Y,组织中的第2相作为阴极相,与镁基体组成原电池,放电反应发生时,这些区域作为反应活性点,促进合金的活化溶解.由于第2相弥散分布,放电反应发生的区域较多,宏观上显示为均匀的放电现象.而对于AZ31合金,基体中几乎没有第2相存在,并且合金化学活性较低,放电反应优先在一些高能量的晶界处发生,宏观上显示为局部放电现象.由此可见,活化元素可以通过形成第二相改善合金的放电性能.
3 结论1)设计了一种成分为Mg-3Al-5Pb-1Ga-1Zn-0.9Y的海水电池用镁合金阳极材料, 该合金在电流密度为20 mA/cm2和100 mA/cm2下工作电位分别为-1.723 V和-1.680 V, 腐蚀电流密度为5.1164×10-5 A/cm2.
2)一定范围内, Pb和Ga元素含量增加能提高合金放电电压, 随着含量增加,Pb还能提高合金的耐腐蚀性能, 而Ga则降低了耐腐蚀性. Pb和Ga的溶解-沉积作用有效提高了合金的化学活性和放电电压.这与添加元素Ga、Y形成的第2相有关, 这些第2相作为阴极相, 促进了合金的活性溶解, 有效提高了合金化学活性和放电电压.
| [1] |
CAO D X, WU L, WANG G, et al. Electrochemical oxidation behaviour of Mg–Li–Al–Ce–Zn and Mg–Li–Al–Ce–Zn–Mn in sodium chloride solution[J].
Power Sources, 2008, 183(2): 799–804. DOI: 10.1016/j.jpowsour.2008.06.005. |
| [2] |
张俊昌, 冯艳, 王乃光, 等. 挤压比对海水激活电池用AP65镁合金阳极材料放电性能的影响[J].
有色金属科学与工程, 2017, 8(3): 54–63.
|
| [3] |
马洪斌. 阀控铅酸蓄电池发展现状[J].
蓄电池, 2004, 41(3): 137–140.
DOI: 10.3969/j.issn.1006-0847.2004.03.012.
|
| [4] |
马永刚. 2005年我国铅酸蓄电池市场需求量预测[J].
中国有色金属, 2005(3): 56–57.
|
| [5] |
FENG Y, WANG R C, PENG C Q, et al. Aging behaviour and electrochemical properties in Mg-4.8Hg-8Ga (wt.%) alloy[J].
Corrosion Science, 2010, 52(10): 3474–3480. DOI: 10.1016/j.corsci.2010.06.024. |
| [6] |
ANDREI M, GABRIELE F D, BONORA P L, et al. Corrosion behaviour of magnesium sacrificial anodes in tap water[J].
Materials & Corrosion, 2015, 54(1): 5–11. |
| [7] |
BALASUBRAMANIAN R, VELUCHAMY A, VENKATAKRISHNAN N, et al. Electrochemical characterization of magnesium/silver chloride battery[J].
Journal of Power Sources, 1995, 56(2): 197–199. DOI: 10.1016/0378-7753(95)80034-E. |
| [8] |
王乃光, 王日初, 彭超群, 等. 镁阳极在海水激活电池中的应用[J].
中国有色金属学报, 2016, 26(5): 1034–1044.
|
| [9] |
THIRUNAKARAN R, VASUDEVAN S, SIVASHANMUGAM A, et al. 1-Nitronaphthalene as a cathode material for magnesium reserve batteries[J].
Power Sources, 1996, 58(2): 213–215. DOI: 10.1016/S0378-7753(96)02376-2. |
| [10] |
张嘉佩.合金元素及热加工工艺对镁阳极组织和性能的影响[D].长沙: 中南大学, 2011.
http://cdmd.cnki.com.cn/Article/CDMD-10533-1011183132.htm |
| [11] |
BELDJOUDI T, FIAUD C, ROBBIOLA L. Influence of homogenization and artificial aging heat treatments on corrosion behavior of Mg-Al Alloys[J].
Corrosion -Houston Tx-, 1993, 49(9): 738–745. DOI: 10.5006/1.3316126. |
| [12] |
腾昭阳.合金元素对镁阳极腐蚀和电化学性能的影响[D].长沙: 中南大学, 2014.
http://cdmd.cnki.com.cn/Article/CDMD-10533-1014407910.htm |
| [13] |
LIU X G, PENG X D, XIE W D, et al. Preparation technologies and applications of strontium-magnesium master alloys[J].
Materials Science Forum, 2005, 488/489: 31–34. |
| [14] |
李高林.稀土(Y、Nd)对AZ80镁合金耐腐蚀性能影响的研究[D].洛阳: 河南科技大学, 2012.
http://cdmd.cnki.com.cn/Article/CDMD-10464-1012042798.htm |
| [15] |
钟丽应.稀土元素对AZ91镁合金组织结构和腐蚀行为的影响[D].杭州: 浙江大学, 2008.
http://cdmd.cnki.com.cn/Article/CDMD-10335-2008148684.htm |
| [16] |
王乃光. AP65镁合金在氯化钠溶液中电化学行为研究[D].长沙: 中南大学, 2013.
http://cdmd.cnki.com.cn/Article/CDMD-10533-1013358689.htm |
| [17] |
ZHANG J P, WANG R C, FENG Y, et al. Effects of Hg and Ga on microstructures and electrochemical corrosion behaviors of Mg anode alloys[J].
Transactions of Nonferrous Metals Society of China, 2012, 22(12): 3039–3045. DOI: 10.1016/S1003-6326(11)61568-9. |
| [18] |
YUAN S, LU H, SUN Z, et al. Electrochemical Performance of Mg-3Al Modified with Ga, In and Sn as Anodes for Mg-Air Battery[J].
Journal of the Electrochemical Society, 2016, 163(7): 1181–1187. DOI: 10.1149/2.0371607jes. |
| [19] |
HAMEDMOGHANN B O, JALAL A, MOSTAFA H. Effects of gallium and lead on the electrochemical behavior of Al-Mg-Sn-Ga-Pb as anode of high rate discharge battery[J].
Journal of Alloys and Compounds, 2017, 695: 2637–2644. DOI: 10.1016/j.jallcom.2016.11.176. |
| [20] |
WANG N, WANG R, FENG Y, et al. Discharge and corrosion behaviour of Mg-Li-Al-Ce-Y-Zn alloy as the anode for Mg-air battery[J].
Corrosion Science, 2016, 112: 13–24. DOI: 10.1016/j.corsci.2016.07.002. |
| [21] |
邓姝皓, 易丹青, 赵丽红, 等. 一种新型海水电池用镁负极材料的研究[J].
电源技术, 2007, 31(5): 402–405.
DOI: 10.3969/j.issn.1002-087X.2007.05.016.
|
| [22] |
MASSALSKI T B, OKAMOTO H, SUBRAMANIAN P, et al.
Binary alloy phasediagrams[M]. Geauga: ASM Int, 1990.
|
| [23] |
MERINO M C, PARDO A, ARRABAL R, et al. Influence of chloride ion concentration and temperature on the corrosion of Mg-Al alloys in salt fog[J].
Corrosion Science, 2010, 52(5): 1696–1704. DOI: 10.1016/j.corsci.2010.01.020. |
 2019, Vol. 10
2019, Vol. 10


