| 新型层状多阴离子化合物Bi3O3SeBr的晶体结构和物理性质 |
近年来, 具有层状特点的双阴离子化合物由于独特的电子结构和物理性能引起材料化学和功能材料领域的广泛关注.例如在LaOFeAs[1]材料体系发现超导电性, 在BiOCuSe[2]材料体系发现良好的热电性能, LaOCuS[3]材料体系是很好的P型透明半导体等.这类双阴离子化合物具有O离子和另外一种非金属元素阴离子(如As3-, S2-和Se2-等).由于化学性质(如离子半径和离子极化)差异较大, 这2种阴离子在材料中与不同的金属阳离子结合, 出现层状排列:O离子与高价阳离子如La3+或Bi3O3+形成离子键作用的正电荷层; 而另外一种非金属元素阴离子与低价过渡金属阳离子如Fe2+或Cu+形成共价键主导的负电荷层.不同的层状结构以及排列方式显著影响化合物的电子性质.比如对于具有FeAs层状结构的超导化合物, LaOFeAs的最高超导温度是26 K[1], 而Sr2VO3FeAs的最高超导温度是37 K[4].
鉴于双阴离子化合物的结构和性能多样性, 探索三阴离子的层状化合物可以进一步丰富其结构化学和物理性能.然而截至目前, 这方面的研究非常少:仅有少数三阴离子层状材料被文献报导, 其大部分具有与双阴离子化合物类似的晶体结构, 如(SrF)2Ti2OSb2[5]是(SmO)2Ti2OSb2的同构化合物, 而(SrF)2Fe2OSe2[6]和(LaO)2Fe2OSe2[7]具有相同的结构.最近, 文献[8]报导了具有不同特点的层状多阴离子化合物, 其中La5O4Cu4As4Cl2由La2O2, Cl, Cu2As2和La离子层有序排列而成, 而Bi4O4Cu1.7Se2.7Cl0.3由Bi2O2, 含有Cu缺陷的Cu1.7Se2层和Cl离子掺杂的Se0.7Cl0.3离子层所组成[9].
文中使用真空固相烧结法制备了一种新型层状三阴离子化合物Bi3O3O3SeBr, 并通过衍射技术确定了其晶体结构, 发现该化合物由Bi2O2层、Br离子双层和Se离子层有序排列而成.初步的性质研究表明该化合物为具有间接带隙的窄带隙n型半导体, 可见光照射下具有稳定的光电响应.
1 实验 1.1 样品制备实验所用试剂:Bi2O3(99 %, 麦克林试剂), Bi粉(99.99 %, 麦克林试剂), Se粉(99.9 %, 麦克林试剂), Bi(NO3)3·5H2O(99.5 %, 西亚化工)和NaBr(99 %, 西陇化工).
BiOBr前驱体的合成[10]:向50 mL烧杯中加入等体积的0.4 mol/L的Bi(NO3)3溶液和NaBr溶液并快速搅拌.后将混合悬浊液转移至50 mL水热反应釜中, 在160 ℃恒温烘箱中反应16 h.取出产物并先后使用去离子水和无水乙醇洗涤, 后置于烘箱中100 ℃充分干燥, 取出少量产物进行XRD以确证其纯度.
按照2:2:3:3的摩尔比称取Bi2O3, Bi粉, Se粉和BiOBr, 充分研磨并压制成片, 置于刚玉坩埚中并移至一端封闭的石英管内, 在保持真空度小于1 Pa的条件下, 使用氢氧焰密封石英管.密封石英管转移至高温马弗炉, 以100 ℃/h的速率升温至700 ℃并保温24 h, 而后自然冷却至室温.将所得样品重新研磨压片并置于刚玉坩埚中, 重复上述加热步骤, 即得亮灰色Bi3O3O3SeBr样品.
1.2 样品表征用PANalytiacl H’Pert PRO型X射线粉末衍射仪来检测实验样品的物相组成和晶体结构, 所用X射线为Cu Kα射线, X射线波长为0.154 2 nm.采用GSAS-II软件来进行XRD数据的精修分析[11].在结构精修中, 衍射背景采用Chebyshev函数来描述, 衍射峰形采用洛伦茨函数和pseudo-Voigt函数来描述.
使用K-Alpha+型X射线光电子能谱仪(美国Thermo fisher公司)来检测样品的元素组成和价态, 所用X射线为单色化Al Kα线, 能量为1 486.6 eV, 束斑大小为400 μm, 样品腔的真空度为2×10-5 Pa.使用Lambda 750型分光光度计(美国Perkin Elmer公司)测量样品在280~2 500 nm波长范围的漫反射谱, 以BaSO4参比物质.
1.3 光电化学性能测试负载样品的ITO玻璃工作电极的制备如下:将5 % (指百分含量, 下同)Nafion溶液用1:1的乙醇溶液稀释100倍, 取10 mg样品超声分散于100 μL该溶液中, 移取少量溶液滴涂在ITO导电玻璃上, 室温干燥后置于100 ℃烘箱中.
使用CHI 760E电化学工作站, 采用三电极系统, Ag/AgCl电极为参比电极, Pt丝为对电极, 样品-ITO玻璃为工作电极, 在0.1 mol/L Na2SO4水溶液(pH=6.8)中, 进行测量样品的电化学性能.使用带紫外滤光片的氙光光源(普林塞斯PL-HD 500型)模拟可见光源, 测试样品在可见光以及无辐射下的电流-时间曲线, 对阳极施加1 V偏置电压, 采样间隔为0.1 s.在无辐射条件下采集样品的电化学阻抗谱和莫特-肖特基图谱:前者测试电压为0 V, 频率范围为106~10-1 Hz, 振幅为5 mV; 后者电压步长为10 mV, 测试频率为1 kHz, 振幅为5 mV.
2 结果与讨论 2.1 晶体结构的确定Bi3O3O3SeBr的晶体结构是对X射线粉末衍射数据使用从头计算法得出的, 其纯相样品的粉末衍射数据如图 1所示.使用PowderX程序可以将其指标化成一个四方单胞[12], 其晶胞参数为a=3.922 8(1) Ǻ和c=20.2381(1)Ǻ.根据指标化结果, 得出其衍射消光条件为(0 k 0)k=2n+1和(h k 0)h+k=2n+1.满足这个消光条件的四方空间群只有P 4/nmm和P 4/n两种情况.进一步确定样品的对称性需要使用选区电子衍射和汇聚束电子衍射.选择高对称性的P 4/nmm以减少晶体结构的变量数目.
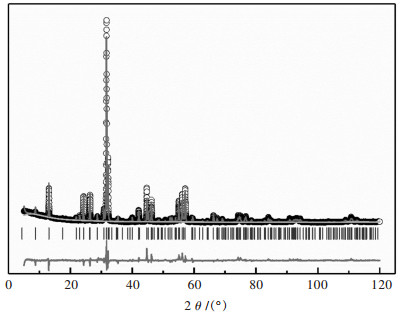 |
| 图 1 Bi3O3O3SeBr样品的实验(空心球)、计算(竖向曲线)以及差值(底部实线)X射线粉末衍射图谱(在谱图下部用垂直线段标示出Bi3O3O3SeBr的衍射峰位) Fig. 1 Experimental (hollow sphere), calculated (in vertical solid curve) and differential(in gray line) XRD plots of Bi3O3O3SeBr. The peak is marked with vertical bar on bottom |
在确定了空间群和晶胞参数的情况下, 使用EXTRA程序来得出Bi3O3O3SeBr的结构因子振幅[13].结合已知的化学组成, 使用直接法可以直接确定Bi, Se, Br和部分氧原子的分数坐标, 并在此基础上通过差分傅里叶变换, 可以确定剩余的氧原子位置[14].
使用该初始结构模型, 对XRD粉末衍射数据进行Rietveld全谱拟合[15-16].由于Br离子和Se离子具有相同的电子云密度和X射线散射能力, XRD无法区分两者; 而且Bi3O3O3SeBr中O离子对于X射线强度的贡献最小, 其准确位置也不能确定.参考Bi2O2Se和BiOBr的晶体结构特点[10, 17], 做出如下合理假定:①Br离子和Se离子分别在Bi2O2层间形成双原子插层和单原子插层, 并且完全有序分布; ②O2位于在Bi2O2层的正中间, 即2zO2=zBi1+zBi2.在此基础上, 固定氧原子的温度因子为0.012 7 Ǻ2, 设定不同Bi原子具有相同的温度因子, 以晶胞参数和其他原子的分数坐标和温度因子为可变量, 对XRD数据进行Rietveld全谱拟合.最终拟合图谱如图 1所示, 具有很高的可信度, 其权重全谱拟合因子Rwp为7.3 %.所得结构的重要参数如表 1所列, 其部分键长如表 2所列.
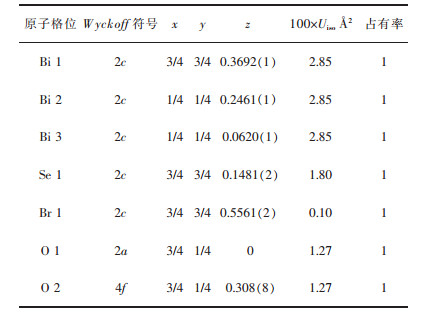
| 表 1 结构精修得出的Bi3O3O3SeBr晶体结构参数(空间群P 4/nmm, a=3.92284(6)Ǻ, c=20.23814(3)Ǻ) Table 1 Lattice parameters and atomic coordinates from the refined XRD data(Space group P 4/nmm, a=3.922 84(6)Ǻ and c=20.238 14(3)Ǻ) |
 |
| 点击放大 |
| 表 2 Bi3O3O3SeBr部分键长 Table 2 Selected bond distance of Bi3O3O3SeBr |
 |
| 点击放大 |
2.2 晶体结构
Bi3O3O3SeBr的晶体结构示意图如图 2所示, 为层状结构, 由Bi2O2层、Se离子单层和Br离子双层所组成.Br离子双层和Se离子单层位于B2O2层中间, 形成BiOBr和Bi2O2Se层状结构单元, 并沿c轴共用Bi2O2层形成Bi3O3O3SeBr结构, 如图 2(a)和图 2(b)所示.
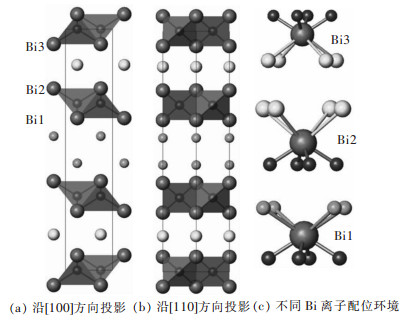 |
| 图 2 Bi3O3O3SeBr的晶体结构示意图(深色大球、浅色大球、浅色小球和深色小球分别表示Bi、Se、Br和O原子) Fig. 2 Crystal structure of Bi3O3O3SeBr (The bismuth, selenium, bromine and oxygen ions are marked in dark big sphere, light big sphere, light small sphere and dark small sphere respectively) |
结构中有3种Bi位点和2种Bi2O2层.其中Bi3O3-O1-Bi3O3层为对称层, 两侧均为Se离子层; 而Bi1-O2-Bi2层为不对称, 两侧分别为Se离子层和Br离子层.3种Bi离子均为八配位, 形成4个Bi-O键和4个Bi-Se或Bi-Br键, 其配位多面体为一组相对面旋转45 °的近似立方体, 如图 2(c)所示. 3种Bi离子具有基本相同的Bi-O键长, 为2.33(1)Ǻ-2.32(1)Ǻ.Bi1离子与4个Br离子成键, 其Bi-Br键与BiOBr中的Bi-Br键长相同.而Bi2和Bi3O3离子均与4个Se离子成键, 但Bi3O3位点具有较长的Bi-Se键, 这表明Se离子偏离Bi2和Bi3O3原子层的中间, 偏向Bi2原子层.而在Bi2O2Se晶体结构中, Se离子位于Bi2O2层的正中间.
2.3 XPS分析Bi3O3O3SeBr样品的XPS谱图如图 3所示.图 3(a)~图 3(d)分别显示了Bi 4f、Br 3d、O 1s和Se 3d吸收峰及其高斯拟合图谱.拟合结果表明Bi 4f5/2和Bi 4f7/2均为单峰, 其电子结合能分别为164.7 eV和159.4 eV, 与文献[18]中Bi3+的结合能相同, 说明Bi元素以Bi3+的形态存在. Br 3d3/2和Br 3d5/2均为单峰, 其结合能为70.0 eV和68.9 eV, 与KBr晶体中Br离子的结合能相同, 表明材料Br元素以Br-的形态存在[19]. O 1s窄谱中位于530.1 eV的单峰对应Bi-O键.在Se 3d窄谱中, Se 3d3/2和Se 3d5/2单峰分别位于54.5 eV和53.7 eV, 与CuInSe2样品中Se2-的结合能相同, 揭示了样品中Se元素为-2价[20], 另外位于55.1 eV的小峰与Se单质结合能匹配, 这种情况在Bi2Se3中出现过[21], 可能是材料表面发生氧化的结果.
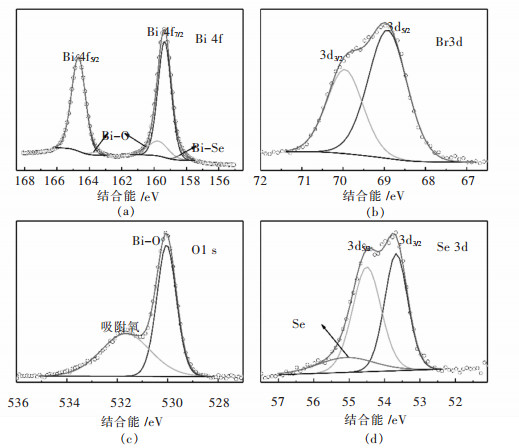 |
| 图 3 Bi3O3O3SeBr的X射线光电子能谱 Fig. 3 Fitted XPS spectra of Bi3O3O3SeBr |
2.4 电子能带结构
使用Castep程序包对Bi3O3O3SeBr的电子结构进行计算.使用基于广义梯度近似(GGA)的PBE方程来描述其进行电子交换关联函数; 使用缀加平面波法(PAW)来描述其外层电子, 能量截断值为380 eV, 内层电子则用超软赝势法(USPP)来描述.首先要对Bi3O3O3SeBr的原始单胞进行结构优化, 确定了最优化的原子位置和晶胞参数之后, 再计算其电子结构, 其k值设定为6×6×1.
Bi3O3O3SeBr的能带结构如图 4(a)和4(b)所示:价带顶有多个近简并态的极大值, 其最大值处于R点, 与Bi2O2Se类似[15].导带底位于Z点, 其间接带隙(R→Z)为0.66 eV, 位于Z点的直接带隙为1.24 eV.导带底部主要是由Bi 6p能带所贡献.价带顶部主要由Se元素的4p能带所贡献, 价带中部主要由Br元素的4p能带所贡献, 价带底部主要由O元素的2p能带所组成.Bi元素的6s能带主要位于低于费米能级10 eV下方.
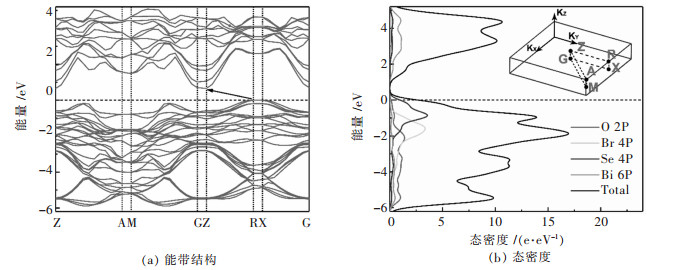 |
| 图 4 Bi3O3SeBr的电子能带结构图(b)插图为k空间示意图, 虚线显示不可约布里渊区 Fig. 4 Electronic structure of Bi3O3SeBr computed with PBE+PAW level DFT. The band structure is plotted on the left along high symmetry paths in the Brillouin zone show in figure (b) inset |
对于晶态半导体, 其能带宽度可以通过近吸收边的光吸收数据来测定.其定量关系为:
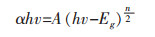
|
其中, α为吸光系数; h为普朗克常数; v为频率; A为常数; Eg样品禁带宽度.其中n与半导体类型有关, 直接带隙半导体n=1, 间接带隙半导体n=4.图 5(a)是Bi3O3O3SeBr的漫反射光谱, 样品在400~1 000 nm波长范围内有较强吸收, 其吸收边可以外推至λ=1 451 nm, 位于近红外光区, 略小于Bi2O2Se.而波长2 000 nm附近的吸收峰与Bi-Se振动有关.
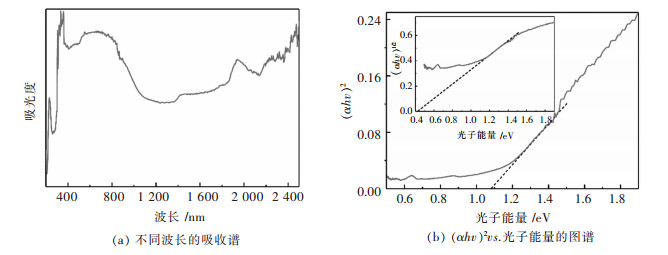 |
| 图 5 Bi3O3O3SeBr的漫反射光谱(虚线是临界光吸收数据的拟合结果) Fig. 5 Diffused reflectance spectroscopy of Bi3O3O3SeBr (The fitted results are shown in dotted lines) |
采用n=1和n=4对Bi3O3O3SeBr的临界光吸收数据(波长范围800~1 200 nm)进行拟合, 得出直接带隙和间接带隙分别为1.08 eV和0.42 eV.拟合图谱见图 5(b)和内插图.其实验带隙数值比理论计算的带隙数值小0.2 eV, 主要原因是定量能带计算对计算量要求较高, 文中采用的理论计算方法只能达到半定量的要求.
2.5 光电性能在可见光照射下, Bi3O3O3SeBr样品表现出稳定的光电响应, 如图 6(a)所示.其光生电流密度间为0.70 μA/cm2, 高于Bi2O2Se(0.55 μA/cm2), 具有更好的光电性能.
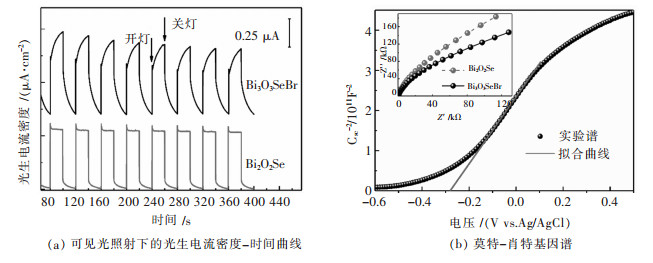 |
| 图 6 Bi3O3O3SeBr和Bi2O2Se样品的光电化学性能测试(插图为电化学阻抗普) Fig. 6 Photoelectrochemical measurements of Bi3O3O3SeBr and Bi2O2Se samples (The inset shows the electrochemical impedance spectroscopy) |
使用电化学阻抗谱(EIS)和Mott-Schottky测试理解材料的载流子输运性能.与Bi2O2Se相比, Bi3O3O3SeBr的阻抗弧较小表明其具有较小的载流子迁移阻力.由于Bi2O2Se和Bi3O3O3SeBr的载流子传输层均为Bi2O2层, 其载流子迁移率比较接近.与Bi2O2Se相比, Bi3O3O3SeBr的能带宽度较小, 其载流子浓度较高, 这是其低电阻的主要原因.通常, Mott-Schottky曲线可以反映半导体中移动载流子的主导类型, Bi3O3O3SeBr斜率为正, 说明它是典型的n型半导体, 主要载流子为导带中的电子.
3 结论文中采用传统固相法制备了新型的三阴离子层状化合物Bi3O3O3SeBr.使用X射线粉末衍射技术、X射线光电子能谱、第一性原理计算、漫反射光谱和光电性能测试研究了其晶体结构和物理性质.结果如下:
1) Bi3O3O3SeBr化合物为四方晶系, 其空间群为P 4/nmm, 晶胞参数a=3.922 84(6) Ǻ, c=20.238 14(3) Ǻ, Se离子层和Br离子双层位于Bi2O2层中间, 形成Bi2O2Se和BiOBr结构单元, 沿着c方向共用Bi2O2层交替堆叠而成的层状化合物.
2) 能带结构计算揭示Bi3O3O3SeBr的价带顶(VBM)主要是由Se 4p能带构成, 而Bi 6p能带主要形成导带底(CBM), 漫反射结果表明其间接带隙为0.42 eV, 直接带隙为1.08 eV, 结合Mott-Schottky分析说明Bi3O3O3SeBr是具有间接跃迁的n型半导体.
3) 在可见光照射下Bi3O3O3SeBr表现出稳定的光电性能, 其光生电流密度为0.70 μA/cm2, 高于Bi2O2Se, 证明Bi3O3O3SeBr在光电探测领域具备潜在的应用前景.
| [1] |
KAMIHARA Y, WATANABE T, HIRANO M, et al. Iron-based layered superconductor La[O1-xFx]FeAs (x=0.05-0.12) with Tc=26 K[J].
Journal the American Chemical Society, 2008, 130(11): 3296–3297. DOI: 10.1021/ja800073m. |
| [2] |
ZHAO L D, HE J, BERARDAN D, et al. BiCuSeO oxyselenides: new promising thermoelectric materials[J].
Energy & Environmental Science, 2014, 7(9): 2900–2924. |
| [3] |
DOUSSIER-BROCHARD C, CHAVILLON B, CARIO L., et al. Synthesis of p-type transparent LaOCuS nanoparticles via soft chemistry[J].
Inorganic Chemistry, 2010, 49(7): 3074–3076. DOI: 10.1021/ic902521r. |
| [4] |
ZHU X, HAN F, MU G, et al. Transition of stoichiometric Sr2VO3FeAs to a superconducting state at 37.2 K[J].
Physical Review B, 2009, 79(22): 2205121–2205124. |
| [5] |
LIU R, SONG Y, LI Q, et al. Structure and Physical Properties of the Layered Pnictide-Oxides: (SrF)2Ti2Pn2O (Pn = As, Sb) and (SmO)2Ti2Sb2O[J].
Chemistry of Material, 2010, 22(4): 1503–1508. DOI: 10.1021/cm9027258. |
| [6] |
KABBOUR H, JANOD E, CORRAZE B, et al. Structure and magnetic properties of oxychalcogenides A2F2Fe2OQ2(A=Sr, Ba; Q=S, Se) with Fe2O square planar layers representing an antiferromagnetic checkerboard spin lattice[J].
Journal of the American Chemical Society, 2008, 130(26): 8261–8270. DOI: 10.1021/ja711139g. |
| [7] |
FREE D G, EVANS J S, Low-temperature nuclear and magnetic structures of La2O2Fe2OSe2 from x-ray and neutron diffraction measurements[J]. Physical Review B 2010, 81(21): 2144331-2144337.
|
| [8] |
EUL M, JOHRENDT D, PöTTGENA R, An extension of pnictide oxide chemistry-salt flux synthesis and structure of La5Cu4As4O4Cl2[J]. Zeitschrift fur Naturforschung Section B-a journal of Chemical Sciences, 2009, 64(11): 1353-1359.
|
| [9] |
GIBSON Q D, DYER M S, WHITEHEAD G F S et al. Bi4O4Cu1.7Se2.7Cl0.3: intergrowth of BiOCuSe and Bi2O2Se stabilized by the addition of a third anion[J]. Journal of the American Chemical Society 2017, 139(44): 15568-15571.
|
| [10] |
LI H, HU T, DU N, et al. Wavelength-dependent differences in photocatalytic performance between BiOBr nanosheets with dominant exposed (001) and (010) facets[J].
Applied Catalysis B: Environmental, 2016, 187(15): 342–349. |
| [11] |
TOBY B H, VON DREELE R B. GSAS-II: the genesis of a modern open-source all purpose crystallography software package[J].
Journal of Applied Crystallography, 2013, 46(2): 544–549. |
| [12] |
DONG C. PowderX: Windows-95-based program for powder X-ray diffraction data processing[J].
Journal of Applied Crystallography, 1999, 32(4): 838. |
| [13] |
ALTOMARE A, BURLA M C, CASCARANO G, et al. EXTRA: Aprogram for extracting structure-factor amplitudes from powder diffraction data[J].
Journal of Applied Crystallography, 1995, 28(6): 842–846. DOI: 10.1107/S0021889895005619. |
| [14] |
YIN C L, LI G B, JIN T N, et al. Synthesis, structure, and characterization of the hexagonal provskite Ba5In0.93Mn4O14.40[J].
Chemistry of Materials, 2008, 20(6): 2110–2116. DOI: 10.1021/cm7025152. |
| [15] |
孙鹏, 尹从岭, 雷秀云. Pb3Mn7O15:合成、相变、转换和分解[J].
有色金属科学与工程, 2017, 8(1): 75–79.
|
| [16] |
吕庆文, 尹从岭, 钟盛文, 等. LiNi0.6Co0.1Mn0.3O2正极材料的合成与性能[J].
有色金属科学与工程, 2016, 7(4): 50–54.
|
| [17] |
WU J X, YUAN H T, MENG M M, et al. High electron mobility and quantum oscillations in non-encapsulated ultrathin semiconducting Bi2O2Se[J].
Nature Nanotechnology, 2017, 12(6): 530–534. DOI: 10.1038/nnano.2017.43. |
| [18] |
ZHAO L Z, ZHANG J B, Bi and O valences in Ba-K-Bi-O, Ba-K-M-Bi-O (M = Rb, La, Eu, In, Tl and Pb) and the related compounds[J]. Solid State Communications, 1994, 90(11): 709-712.
|
| [19] |
MORGAN W E, VAN WAZER J R, STEC W J. Inner-orbital photoelectron spectroscopy of the alkali metal halides, perchlorates, phosphates, and pyrophosphates[J].
Journal of the American Chemical Society, 1973, 95(3): 751–755. DOI: 10.1021/ja00784a018. |
| [20] |
CAHEN D, IRELAND P J, KAZMERSKI L L, et al. X-ray photoelectron and Auger electron spectroscopic analysis of surface treatments and electrochemical decomposition of CuInSe2 photoelectrodes[J].
Journal of Applied Physics, 1985, 57(10): 4761–4771. DOI: 10.1063/1.335341. |
| [21] |
KONG D S, CHA J J, LAI K J, et al. Rapid surface oxidation as a source of surface degradation factor for Bi2Se3[J].
ACS nano, 2011, 5(6): 4698–4703. DOI: 10.1021/nn200556h. |
 2019, Vol. 10
2019, Vol. 10


