| 铜渣直接还原动力学 |
我国铜矿资源大多是贫矿、共伴生矿,品位较低[1],因此铜矿冶炼过程产生了大量的铜渣.文献[2]研究表明,生产1 t铜约产生2.2 t的铜渣.在现有的炼铜工艺规模中,我国铜渣增量约为1 000万t/a.然而产生的铜渣除少部分用作水泥混凝土原料、防锈磨料外[3-6],大部分采用堆积方式处理,会污染水体和土壤,累计堆存量已经达到1.2亿t[7-8].另外,铜渣中含有多种有价金属和贵金属(Fe、Zn、Cu、Pb、Co、Ni、Au、Ag等),可提炼回收加以利用.其中Fe含量可达到40 %,而我国铁矿石的可采品位为>27 %[9].因此,加强铜渣的资源无害化处理意义重大且势在必行, 尤其铜渣中铁资源的回收利用具有一定的经济效益.
然而铜渣中的Fe大多以铁橄榄石(Fe2SiO4)和磁铁矿(Fe3O4)的形式存在,对其用传统工艺提取很难有效回收利用.而铜渣中铁资源的回收,目前现有的研究方法主要有3种[1]:高温熔融氧化法、直接还原法和磨矿选别法.其中采用直接还原提取金属铁的方法,近几年已有不少学者研究[10-13],但对于铜渣直接还原的动力学方面未见报道.而铜渣直接还原提取金属铁的方法,即是在高温惰性气氛下铜渣中的含铁组分受外加还原剂作用还原成金属铁回收利用的方法.因此,对其动力学方面的研究主要集中在铜渣中含铁组分还原生成单质铁反应的动力学研究.文中以铜渣和无烟煤为原料,进行氩气下的等温还原,并对其进行动力学分析,进而确定铜渣直接还原过程中的限速环节,以期能够优化实验参数,为铜渣中含铁组分的资源化利用提供参考.
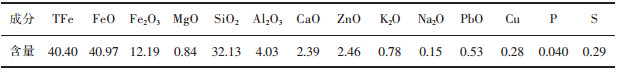
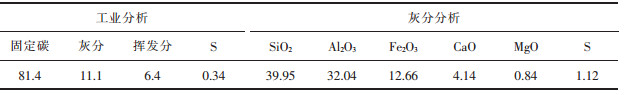
1 实验 1.1 实验原料实验所用铜渣主要成分如表 1所列.可以看出,铜渣中TFe、SiO2、Fe2O3和Al2O3的含量较高.通过表 1可得铜渣碱度为0.09,为酸性渣,即m(CaO+MgO)/m(SiO2+Al2O3)=0.09. 图 1所示为铜渣的XRD图谱.由图 1可以看出,铜渣中含铁矿物主要为铁橄榄石(Fe2SiO4)和磁铁矿(Fe3O4),属于较难还原的矿物.实验所用还原剂为无烟煤,其工业分析结果如表 2所列.为确保反应充分,将实验所用铜渣研磨至粒度 < 0.27 mm的球形颗粒,无烟煤的粒度为 < 0.18 mm.
| 表 1 铜渣所含成分/(质量分数,%) Table 1 Chemical composition of received copper slag /(massfraction, %) |
 |
| 点击放大 |
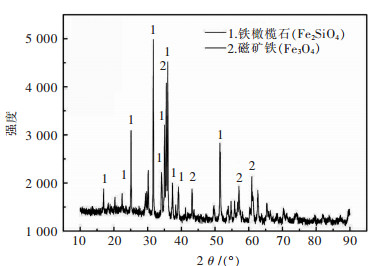 |
| 图 1 原铜渣样XRD谱 Fig. 1 XRD pattern of received copper slag |
| 表 2 无烟煤主要成分/(质量分数,%) Table 2 Main composition of anthracite /(massfraction, %) |
 |
| 点击放大 |
1.2 实验方法
文中采用含碳球团等温还原实验,具体实验步骤如下所示:
1)将100 g铜渣、11.76 g煤粉(nc/no=1.0)、9gH2O充分混匀.
2)取混合样10 g装入特制的柱形模具中,用手板式千斤顶以20 MPa的压力压制成直径为20 mm的圆柱体(球团).将球团在105 ℃的烘干箱中烘干24 h后取出称重,然后放置在刚玉坩埚中.将坩埚悬吊在竖式管炉的恒温区内,上方挂在梅特勒电子天平的挂钩上.悬挂坩埚所用吊丝为Fe-Cr-Al-Mo丝.该实验温度分别为1 000 ℃、1 050 ℃、1 100 ℃、1 150 ℃、1 200 ℃,反应时间为30 min,所通气体为高纯氩气,流量为4 L/min,具体的实验装置如图 2所示.
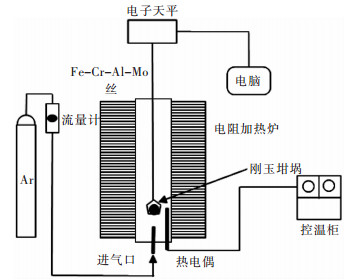 |
| 图 2 等温还原实验装置示意 Fig. 2 Schematic diagram of isothermal reduction experimental device |
1.3 实验原理
铜渣中的主要化合物Fe2SiO4和Fe3O4的直接还原行为不同,Fe3O4不能被直接还原成单质Fe,在温度高于843 K时,先被还原成FeO,然后FeO再被还原成单质Fe. Fe2SiO4和Fe3O4直接还原的主要反应[14]如下:
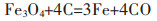
|
(1) |
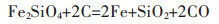
|
(2) |
通过对反应式(1)和式(2)的△Gθ与温度关系进行热力学分析,可知在合适的温度下可以实现Fe2SiO4和Fe3O4的直接还原,因此铜渣采用直接还原的工艺提取有价金属可以实现.
而对铜渣还原反应的动力学研究,可参考含碳球团还原铁氧化物的动力学.目前对于含碳球团的自还原机理已基本得到共识[15],公认为由式(3)间接还原和式(4)碳气化反应组成.而刚开始反应时,紧密接触的铁氧化物与碳发生直接还原反应产生CO气体,如式(5).随着反应的进行,与铁氧化物紧密接触的碳消耗完全,则还原由式(3)、式(4)所组成.
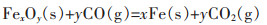
|
(3) |
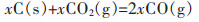
|
(4) |
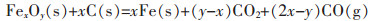
|
(5) |
为方便计算,对上述反应进行理想化处理,即认为还原过程中无CO2逸出,气体产物只有CO,则铜渣含碳球团的还原度α可按如下公式计算:

|
(6) |
式(6)中:△m为从反应开始到t时刻球团失去的质量,g;mo为原铜渣所含铁氧化物中氧原子的质量,g;mc为原无烟煤中固定碳的质量,g;mv为原无烟煤中挥发分的质量,g.
2 实验结果无烟煤+铜渣球团的还原度在不同温度下的变化曲线如图 3所示.可以看出,温度对反应速率有显著影响,且温度越高,还原速率越大;对于同一温度而言,反应速率随着反应的进行先增大后减小;反应温度的改变会影响反应终点还原度的大小,温度越高反应越彻底.终点还原度相对较低,反应均未到达平衡,可能是由于该铜渣碱度呈酸性,在还原过程中SiO2和Al2O3与部分FeO结合形成复杂的难还原物相,阻碍进一步还原.
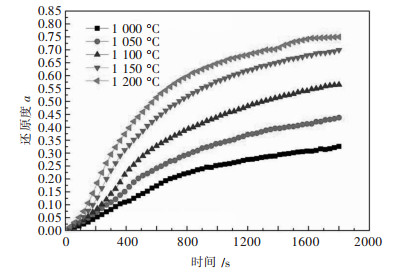 |
| 图 3 球团还原度变化曲线 Fig. 3 Reduction degree curve of pellets |
3 反应动力学分析
通过前文对铜渣直接还原反应与含碳球团还原提铁类比分析,可知该反应的限速环节可能为以下3种:①界面化学反应;②碳气化反应;③球团内部的气体扩散.为了弄清楚该反应的主要限速环节,作者借鉴前人的研究工作[16-19],对这3种限速环节分别采用不同的动力学模型进行处理.
若认为界面化学反应为铜渣含碳球团等温还原反应的限速环节时,则还原度α与反应速率常数k的关系式为:
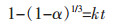
|
(7) |
若认为碳气化反应为该反应的限速环节时,则α与k的关系式为:
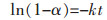
|
(8) |
若认为球团内部的气体扩散为限速环节,则α与k的关系式为:
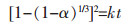
|
(9) |
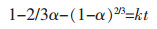
|
(10) |
处理实验数据,分别取y1=1-(1-α)1/3、y2=-ln(1-α)、y3=[1-(1-α)1/3]2、y4=1-2/3α-(1-α)2/3建立y与t的关系图,如图 4所示.若某一模型所得图形线性拟合度最高,即可认为该模型所对应的项为反应的限速环节,则可通过直线斜率求解相关的动力学参数.
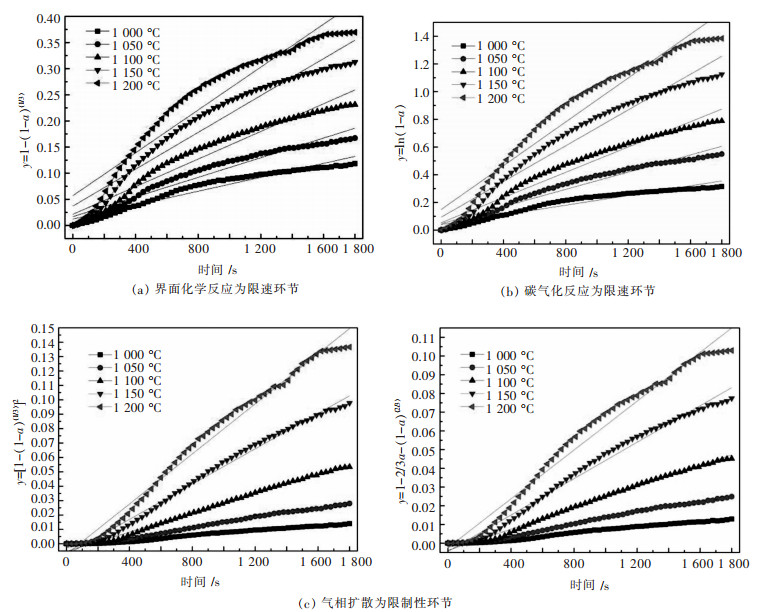 |
| 图 4 不同限制性环节的动力学分析 Fig. 4 Dynamic analysis of different restrictive links |
显而易见,以界面化学反应与碳气化反应为限速环节所拟合出来的直线其拟合度较差,而以球团内气相扩散为限速环节时,直线拟合度较高,从而可知气相扩散可能为铜渣直接还原的限速环节.原因可能为铜渣中的铁橄榄石在高温下熔融呈现液相状态,使得气体扩散受阻. 图 5所示为Fe2SiO4相图,可以看出纯Fe2SiO4熔点为1 205 ℃,但Al2O3及CaO的存在,形成了低熔点矿物,致使球团孔隙度降低,阻碍了气相的扩散.而且还原实验后样品的形态也验证了低熔点物质的存在,如图 6所示.
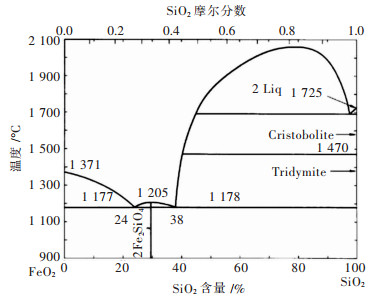 |
| 图 5 Fe2SiO4相图 Fig. 5 Phase diagram of Fe2SiO4 |
 |
| 图 6 1 100 ℃ 30 min样品形貌 Fig. 6 Sample morphology at 1 100 ℃ for 30 min |
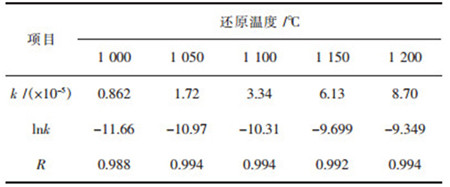
图 4(c)中各直线的斜率即为不同温度下反应的速率常数k值,将其绘制成表格,如表 3所列.
| 表 3 不同温度下铜渣含碳球团反应的速率常数 Table 3 Rate constant of carbonaceous pellets included copper slag at different temperatures |
 |
| 点击放大 |
由Arrhenius公式:
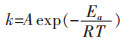
|
(11) |
式(11)中: A为指前因子,s-1;Ea为反应活化能,J/mol;R为理想气体常数,值为8.314 J/(mol·K);T为热力学温度,K.
得:
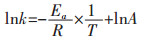
|
(12) |
将数据代入上式,可做出lnk与1/T的线性回归曲线,其线性拟合结果如图 7所示.可求出反应活化能,如表 4所列.因此,铜渣含碳球团直接还原反应是以球团内部气相扩散为限速环节,其活化能数值为118.059 kJ/mol.
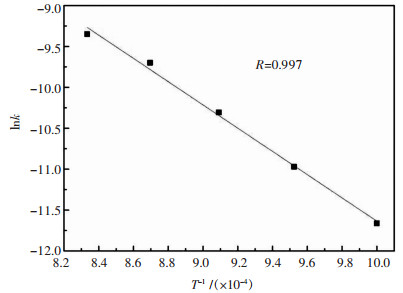 |
| 图 7 lnk与1/T的线性回归曲线 Fig. 7 Linear regression curve of lnk and 1/T |
| 表 4 铜渣含碳球团的活化能 Table 4 Activation energy of copper smelting slag/carbon composite pellets |
 |
| 点击放大 |
上述方法对铜渣直接还原反应的动力学分析,是对全过程反应理想化处理的结果,即只有一个限制性环节.为弄清该反应不同阶段的限速环节,现对其采用积分法进行动力学分析[20].该方法较上面模型分析处理的好处是,可以求得不同还原度下反应的活化能,即可知反应不同阶段对应的控速环节[21],具体步骤如下:
k与α的关系可以由如下公式表示:
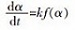
|
(13) |
式(13)中: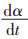
将式(11)代入式(13)进行积分处理,可得
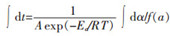
|
(14) |
对式(14)进一步处理,可以得到对于确定的还原度数值α,其
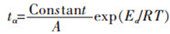
|
(15) |
式(15)中:tα为还原度为α时对应的还原时间.
对式(15)两边取对数,可得
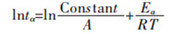
|
(16) |
可以看出上式形如y=a+bx,即lntα与1/T呈直线关系.将T和tα带入式(16),得lntα与1/T的关系图,即可根据斜率求得Ea的数值,lntα与1/T的拟合结果如图 8所示.
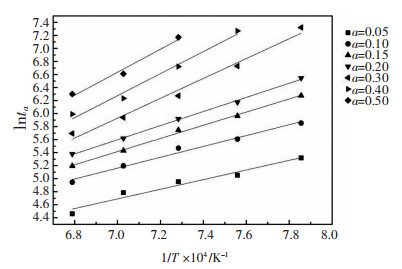 |
| 图 8 lntα与1/T间的线性拟合 Fig. 8 Linear fit between lntα and 1/T |
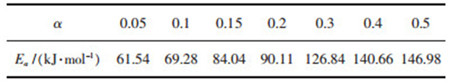
从图(8)可以很容易地看出,还原度一定时,lntα与1/T在全温度范围内几乎呈直线关系.将所求得的Ea列成表 5,可以看出:铜渣含碳球团等温还原反应的活化能随着还原度的增大而增大,其变化范围为61.54~146.98 kJ/mol,这与上文气相扩散为限速环节所求得的活化能数值相近.因此,可以将还原过程分为2个阶段,即①α≤0.2,此阶段为还原反应初始阶段;②0.2 < α < 0.5,此阶段为快速反应阶段.
| 表 5 表观活化能拟合计算结果 Table 5 Apparent activation energy fitting calculation results |
 |
| 点击放大 |
第1阶段反应活化能数值较小,原因可能是该阶段反应刚开始,原铜渣中含有一些铁氧化物(Fe3O4)先参与了反应;第2阶段反应活化能较高,此时原铜渣中的铁氧化物已基本反应,铁以橄榄石的状态存在,且橄榄石呈液态,致使球团孔隙度降低,气体在球团内的扩散受阻.
4 结论文中通过对铜渣含碳球团等温还原反应的动力学分析,可得到以下结论:
1)温度对铜渣含碳球团的还原速率有显著影响,温度越高,还原速率越大;反应温度的改变会影响反应终点还原度的大小,温度越高反应越彻底.
2)铜渣含碳球团的等温还原反应主要限速环节为气相扩散,活化能数值为118.059 kJ/mol;对其进行阶段性动力学分析,其活化能在61.54~146.98 kJ/mol范围内,且活化能的数值随着还原度的变化而变化,具体表现为:第1阶段反应活化能数值较小,原因可能是该阶段反应刚开始,原铜渣中含有一些铁氧化物(Fe3O4)先参与了反应;第2阶段反应活化能较高,此时原铜渣中的铁氧化物已基本反应,铁以橄榄石的状态存在,且橄榄石呈液态,致使球团孔隙度降低,气体在球团内的扩散受阻.
| [1] |
王华, 李磊.
铜渣中有价金属回收的应用基础研究[M]. 北京: 科学出版社, 2013.
|
| [2] |
SHEN H T, FORSSBERG E. An overview of recovery of metals from slags[J].
Waste Management, 2003, 23(10): 933–949. DOI: 10.1016/S0956-053X(02)00164-2. |
| [3] |
SHI C J, MEYER C, BEHNOOD A. Utilization of copper slag in cement and concrete[J].
Resources, Conservation and Recycling, 2008, 52(10): 1115–1120. DOI: 10.1016/j.resconrec.2008.06.008. |
| [4] |
KAMBHAM K, SANGAMESWARAN S, DATAR S R, et al. Copper slag:optimization of productivity and consumption for cleaner production in dry abrasive blasting[J].
Journal of Cleaner Production, 2007, 15(5): 465–473. DOI: 10.1016/j.jclepro.2005.11.024. |
| [5] |
赵凯, 程相利, 齐渊洪, 等. 铜渣处理技术分析及综合利用新工艺[J].
中国有色冶金, 2012, 41(1): 56–60.
DOI: 10.3969/j.issn.1672-6103.2012.01.016.
|
| [6] |
张林楠, 张力, 王明玉, 等. 铜渣的处理与资源化[J].
矿产综合利用, 2005(5): 22–27.
|
| [7] |
ALTER H. The composition and environmental hazard of copper slags in the context of the Basel Convention[J].
Resources, Conservation and Recycling, 2005, 43(4): 353–360. DOI: 10.1016/j.resconrec.2004.05.005. |
| [8] |
CARRANZA F, ROMERO R, MAZUELOS A, et al. Biorecovery of copper from converter slags:slags characterization and exploratory ferric leaching tests[J].
Hydrrometallurgy, 2009, 97(1/2): 39–45. |
| [9] |
CAO H Y, FU N X, WANG C G, et al. Selective precipitation and separation of Fe components from copper smelting slags[J].
Multipurpose Utilization of Mineral Resources, 2009(2): 8–11. |
| [10] |
李镇坤, 文衍宣, 苏静. 无烟煤直接还原铜渣中铁矿无工艺研究[J].
无机盐工业, 2014, 46(6): 51–55.
DOI: 10.3969/j.issn.1006-4990.2014.06.014.
|
| [11] |
曹志成, 孙体昌, 薛逊, 等. 无烟煤转底炉直接还原铜渣回收铁、锌研究[J].
矿冶工程, 2017, 37(2): 74–78.
DOI: 10.3969/j.issn.0253-6099.2017.02.019.
|
| [12] |
赵凯, 宫晓燕, 李杰, 等. 直接还原法回收铜渣中铁、铜和锌的热力学[J].
环境工程学报, 2016, 10(5): 2638–2646.
|
| [13] |
王云, 朱荣, 郭亚光, 等. 铜渣还原磁选工艺实验研究[J].
有色金属科学与工程, 2014, 5(5): 61–67.
|
| [14] |
杨慧芬, 景丽丽, 党春阁. 铜渣中铁组分的直接还原与磁选回收[J].
中国有色金属学报, 2011, 21(5): 1165–1170.
|
| [15] |
杨学民, 郭占成, 王大光, 等. 含碳球团还原机理研究[J].
化工冶金, 1995, 16(2): 118–127.
DOI: 10.3321/j.issn:1009-606X.1995.02.006.
|
| [16] |
SEATON C E, FOSTER J S, VELASCO J. Redution kinetics of hematite and magnetite pellets containing coal char[J].
Transactions of the Iron and Steel Institute of Japan, 1983, 23(6): 490–496. DOI: 10.2355/isijinternational1966.23.490. |
| [17] |
RAO Y K. The kinetics of reduction of hematite by carbon[J].
Metallurgical and Materials Transactions B, 1971, 2(5): 1439–1447. |
| [18] |
JANDER W. Reactions in the sofid state at high temperatures[J].
Z. Anorg. Ailgem. Chem., 1927, 163(1/2): 1–30. |
| [19] |
GINSTLING A M, BROUNSHTEIN B I. Concerning the diffusion kinetics of reactions in spherical particles[J].
J Appl. Chem. USSR, 1950, 23(12): 1327. |
| [20] |
DEY S K, JANA B, BASUMALLICK A. Kinetics and reduction characteristics of hematite-noncoking coal mixed pellets under nitrogen gas atmosphere[J].
ISIJ Int, 1993, 33(7): 735. DOI: 10.2355/isijinternational.33.735. |
| [21] |
王广, 薛庆国, 沈颖峰, 等. 硼铁精矿的碳热还原热力学[J].
工程科学学报, 2016, 38(5): 623–629.
|
 2019, Vol. 10
2019, Vol. 10


