| 基于非等温热重法的氟化石墨热分解动力学研究 |
氟化石墨是氟与碳反应生成的一种氟化碳聚合物,化学通式为(CFx)n(0.5≤x < 1.2),有聚单氟二碳(C2F)n(0.5≤x < 1)和聚单氟碳(CF)n(1≤x < 1.2)2种结构[1].(CFx)n继承了石墨层状结构的特征,氟原子置入碳原子层间使层间距由3.35 Å增大到5.8~8.9 Å[2, 3],并且氟强的吸电子特性使其具有优良的物理化学性质,在固体润滑剂、高能电池、表面涂层、氟化石墨烯等领域得到广泛的应用研究[4-8].然而,在氟化物熔盐电解中,氟离子在碳阳极表面放电也会生成(CFx)n,使阳极电阻率增大、润湿性变差,导致槽电压升高,甚至发生阳极效应[9, 10].碳阳极上生成(CFx)n的电极过程耦合反应产物分解的化学反应[10-12],(CFx)n的分解速率和电化学生成速率关系到电极表面反应产物(CFx)n的净生成量,决定着电极表面状态,因而明确(CFx)n热分解动力学对进一步研究碳阳极电化学氟化钝化机理具有重要的理论指导意义.
(CFx)n热分解生成无定型碳C*和气态碳氟化合物,可由式(1)描述[13-15]:
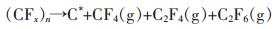
|
(1) |
针对(CFx)n的热分解反应,Kamarchik等[16]采用热重法研究不同F/C比的(CFx)n(x=0.61,0.96,1.08,1.12)在等温条件下的分解反应动力学,提出二维的碳成核生长动力学机理,机理函数为n=2的Avrami-Erofeyev方程g(α)=[-ln(1-α)]1/2,并指出分解发生在(CFx)n微晶边缘.随后,Watanabe等[17]基于碳成核生长机理分析(CFx)n等温分解过程的动力学,发现(CFx)n分解反应动力学机理函数随转化率而改变,认为反应动力学包含多个连续的动力学机理步骤,同时也强调晶界对成核位点形成的重要性.近年来,Chen等[15]采用非等温差示扫描量热法研究(CF)n热分解的动力学,指出(CF)n热分解反应为一步放热反应,并且也发现动力学机理函数随转化率而改变,这与Watanabe等[17]的研究结果相近,但二者报道的动力学机理函数存在差别.目前,(CFx)n热分解反应动力学机理的研究结论并不一致,而且有关研究未提供明确的动力学预测信息.为此,文中基于多组(CF)n非等温分解过程的热重曲线,利用无动力学模型法(Model-free kinetics method,MFK法)和y(α)标准曲线法分析(CF)n分解反应动力学,明确分解过程动力学特征及反应动力学机理函数,提供(CFx)n热分解动力学预测的基本参数,以期为相关研究提供依据.
1 实验测试使用的氟化石墨来源于上海富邦化工有限公司研究中心,纯度(碳、氟组分) > 99.5 %,氟含量(质量分数)为56 %,平均粒径4~6 μm.实验样品的物相及特征分别利用X射线衍射(Empyrean X射线粉末衍射仪,帕纳科公司,荷兰)和Raman光谱(inVia显微Raman光谱仪,雷尼绍公司,英国)进行表征.
热重测量采用STA 449 C同步热分析仪(耐驰仪器制造有限公司,德国),使用无盖的氧化铝坩埚作为试样坩埚和参比坩埚,测试样品量为4~6 mg.非等温测量分别以10 K/min、15 K/min、20 K/min和25 K/min的升温速率由室温加热至1 050 K,测量过程通入高纯氮气(纯度99.999 %),气体流速为20 mL/min.每次测量前均进行基线校正.
2 结果与讨论 2.1 (CFx)n样品物相及拉曼特征XRD物相分析结果如图 1所示.由图 1可知,实验使用的(CFx)n样品的(001)、(002)、(100)、(110)和(200)晶面间距分别为5.87 Å、2.90 Å、2.21 Å、1.29 Å和1.11 Å,属于聚氟化碳(CF)n[2, 3];另外,样品中还含有未完全氟化的石墨组分,其(002)和(004)晶面间距分别为3.37 Å和1.68 Å.
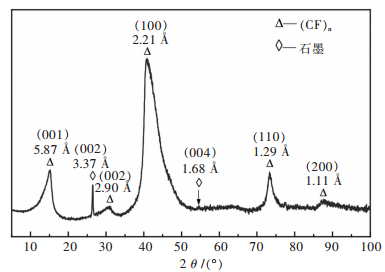 |
| 图 1 (CFx)n样品的XRD衍射谱 Fig. 1 XRD diffraction spectrum of (CFx)n sample |
图 2所示的拉曼光谱表明(CF)n原子振动模式E2g振动模(G峰)的拉曼频移位于1 574 cm-1处,A1g振动模(D峰)的拉曼频移位于1 315 cm-1处,与石墨相比,G峰和D峰的拉曼频移向左偏移.无序引起的D峰与面内振动E2g振动模引起的G峰的强度比ID/IG表征试样的无序性敏感[18].由图 2可知,(CF)n的ID/IG为1.56,远大于石墨的ID/IG值0.24,表明氟化的碳原子层长程周期性被破坏,(CF)n结构长程无序.
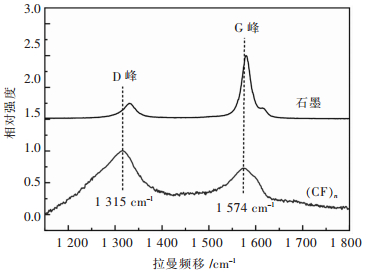 |
| 图 2 (CF)n的拉曼光谱激光波长633 nm;激光功率18 mW;狭缝宽度200 μm Fig. 2 Raman spectra of (CF)n Laser wave length 633 nm; laser power 18 mW; slit width 200 μm |
2.2 反应表观活化能
图 3(a)所示为(CF)n热分解的非等温TG曲线.从图 3(a)中可以看到,升温过程中出现一个失重步骤,分解反应温度起始于803 K,至963 K分解完全,反应物失重率68 %.按氟含量56 %计算,失重部分平均气相成分为CF2.95,与Bettinger等[14]报道的平均气相成分CF2.9接近.这意味着反应产生大量的中间体CF3原子团,中间体CF3通过继续吸收F原子生成CF4,或聚合生成C2F6[14].(CF)n分解反应的转化率α=(m0-m)/Δm,各升温速率条件对应的α-T关系曲线如图 3(b)所示.
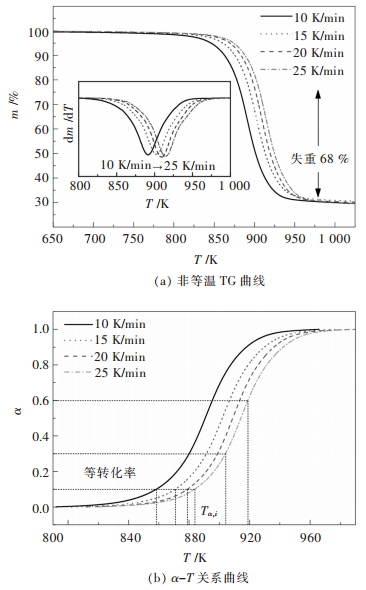 |
| 图 3 (CF)n热分解的非等温TG曲线和对应的α-T关系曲线 Fig. 3 Non-isothermal TG curves of(CF)n thermal decomposition and corresponding α-T curves |
对于多组升温速率的热分析曲线,在恒定的转化率下,反应速率仅是温度的函数[19].因此,基于等转化率规则,在不考虑任何特定形式的反应模型的情况下,能够计算各恒定转化率下的有效活化能,即MFK法,并且能通过有效活化能随转化率的变化判断反应过程的动力学特征[19-21].根据第Ⅰ类动力学方程的微分式:
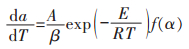
|
(2) |
式(2)中,α为转化率;T为温度,K;β为升温速率,K/min;A为指前因子,s-1;E为反应活化能,kJ/mol;R为理想气体常数,8.314 J/(mol·K);f(α)为动力学机理函数.
式(2)两边取对数并整理得:
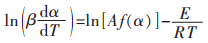
|
(3) |
由式(3)可知,不同升温速率条件下反应达到相同转化率时,ln(βdα/dT)i与1/Ti具有线性关系,斜率为-E/R,通过斜率可以计算出等转化率活化能Eα.
利用图 3(b)中α、T数值,取Δα为0.05,作各转化率时的ln(βdα/dT)i-1/Ti关系,并进行线性拟合,结果如图 4所示.各组数据的线性相关系数r2分布于0.982 2~0.999 9之间,线性拟合参数及计算的Eα值列于表 1.
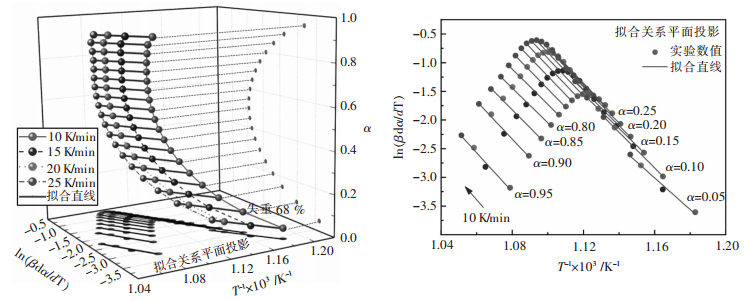 |
| 图 4 各转化率α下ln(βdα/dT)i-1/Ti的线性关系 Fig. 4 Linear relation of ln(βdα/dT)i-1/Ti for each extent of conversion α |
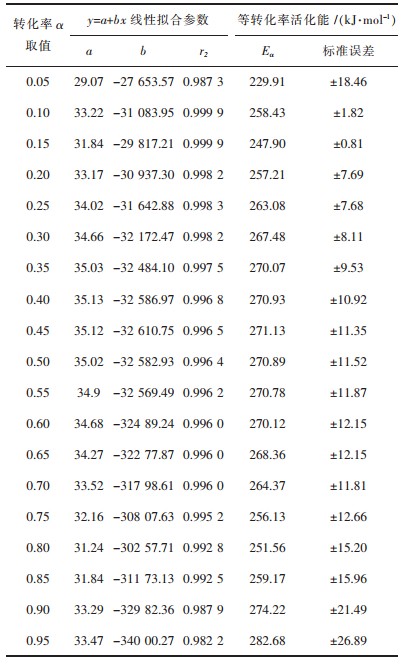
| 表 1 ln(βdα/dT)i-1/Ti线性关系的拟合结果及计算的Eα值 Table 1 Linear fitting results of ln(βdα/dT)i-1/Ti relationships and calculated Eα values |
 |
| 点击放大 |
表 1中Eα值及其标准误差随转化率α的变化关系如图 5所示.由图 5可知,在整个转化率范围内,Eα随α发生变化,并且出现两个“谷”,意味着(CF)n分解反应涉及复杂的动力学机理[19].另外,Eα值介于229.91 kJ/mol和282.68 kJ/mol之间,相对误差均小于10 %,而且在0.1 < α < 0.9范围内,Eα值变化不大,通过数值统计分析,其平均值E0为264.23±7.82 kJ/mol,均值95 %置信区间下、上限分别为260.21 kJ/mol和268.25 kJ/mol.
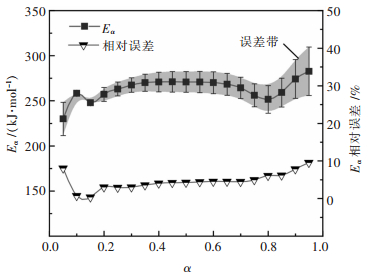 |
| 图 5 等转化率活化能Eα与转化率α的关系 Fig. 5 Dependence of isoconversion activation energy (Eα) on the extent of conversion (α) |
此外,从图 5中还可以看出Eα值的误差带随着转化率增加而逐渐变宽,其原因是测量过程中气态产物浓度的增加或体系温度的升高使某些气态产物的歧化反应加剧,进而对反应体系热效应的扰动增大.体系可能发生的歧化反应如反应式(4)~式(6)所描述,相应的反应吉布斯自由能ΔG与温度T的关系见图 6.由图 6可知,在室温至1 050 K温度范围内各反应的ΔG均小于0,反应能够自发进行;特别是反应式(6)的ΔG随温度T升高而显著降低,表明高温下C2F6转化为CF4的反应趋势更大.
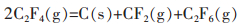
|
(4) |
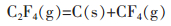
|
(5) |
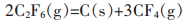
|
(6) |
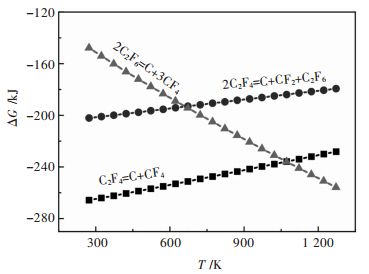 |
| 图 6 体系中可能发生的气态产物转化反应的ΔG-T关系 Fig. 6 ΔG-T relationships of the possible gaseous product reactions in the system |
2.3 动力学机理函数及指前因子
在Eα变化不大的情况下,可采用y(α)主曲线法判明动力学机理函数[19, 22].取Eα的平均值E0替代活化能,y(α)主曲线方程可表达为:
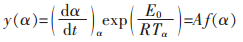
|
(7) |
由式(7)可知,指前因子A是常数,所以y(α)的形状与动力学机理函数f(α)的形状保持一致,因而可以由实验数据计算y(α)=(dα/dt)αexp[E0/(RTα)],并与理论的f(α)比较,通过曲线形状匹配确定动力学机理函数.由于指前因子A值未知,因此y(α)需要在0到1范围归一化.
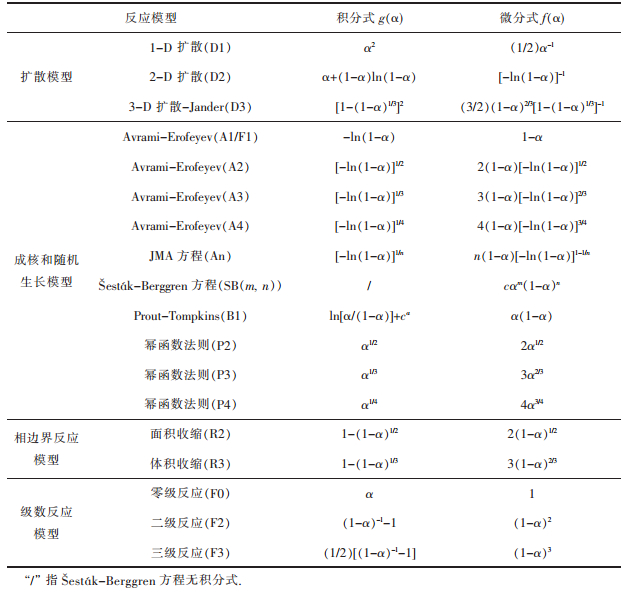
热分析动力学常见的固相反应动力学机理模型有扩散模型、成核和随机生长模型、相边界反应(几何收缩)模型和级数反应模型,相应动力学机理函数的积分式和微分式见表 2[23].
| 表 2 常见的固相反应机理模型 Table 2 Common solid state reaction mechanism models |
 |
| 点击放大 |
利用式(7)的曲线关系,通过匹配表 2中各反应模型机理函数和实验测量数据,确定的动力学机理函数如图 7所示.结果表明(CF)n热分解反应依次由4种动力学机理控制:α < 0.1,为随机成核和随后的一维核生长机理,该阶段成核频率随反应时间逐渐减少[22, 23],机理函数为n=1.5的JMA方程f(α)=1.5(1-α)[-ln(1-α)]1/3;0.15 < α < 0.3,为随机成核和随后的二维核生长机理,机理函数为n=2的Avrami-Erofeyev方程f(α)=2(1-α)[-ln(1-α)]1/2;0.3≤α < 0.8,为核的链生长机理,链生长过程存在复杂的分支链相互作用[24, 25],机理函数为m=1.2、n=2的Šesták-Berggren方程f(α)=cα1.2(1-α)2;0.85 < α,单个粒子上有一个核的随机成核和随后的一维核生长机理,机理函数为n=1的Avrami-Erofeyev方程f(α)=(1-α).
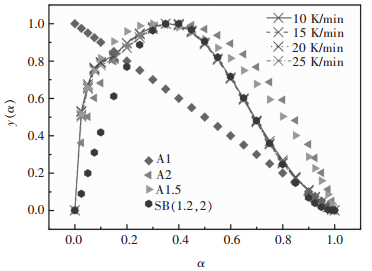 |
| 图 7 动力学机理函数匹配结果 Fig. 7 Matching results of the kinetics mechanism functions |
Šesták-Berggren方程的参数m、n由式(7)的一阶导数特征y′(αmax)=A f ′(αmax)=0确定[26].图 7中实验测量数据的y(α)-α曲线极值点αmax约为0.375,所以有,fSB′(αmax)=cmαmaxm-1(1-αmax)n-cnαmaxm(1-αmax)n-1=0,解得m/n=0.6.另外,将SB(m, n)机理函数代入动力学方程式(2)中,整理可得:
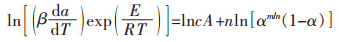
|
(8) |
式(8)表明ln[(βdα/dT)exp(E/RT)]与ln[αm/n(1-α)]具有线性关系,斜率即为n.利用升温速率为20 K/min的实验数据,作ln[(βdα/dT)exp(E/RT)]-ln[αm/n(1-α)]关系图,并进行线性拟合,结果如图 8所示.线性斜率n值约为2,进而计算m值约为1.2.
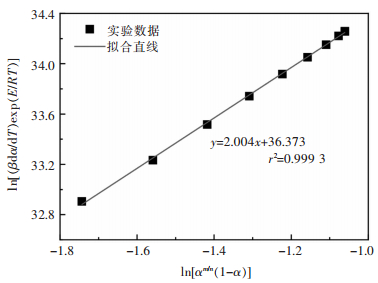 |
| 图 8 ln[(βdα/dT)exp(E/RT)]-ln[αm/n(1-α)]线性关系 Fig. 8 Linear relationship of ln[(βdα/dT)exp(E/RT)]-ln[αm/n(1-α)] |
由动力学方程式(2)可得指前因子表达式:
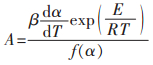
|
(9) |
分别代入10 K/min、15 K/min、20 K/min和25 K/min升温速率的实验测量数值,以及前述的平均活化能E0和动力学机理函数,计算对应条件下的Aα, i值,然后通过计算多条Aα, i-α曲线的均值获取平均指前因子A0.计算Aα, i时SB方程的参数c取值为1,结果如图 9所示.通过计算多条曲线均值,在0 < α < 0.9范围内A0值为(8.70±0.21)×1014/s,而代入SB方程计算的A0′值为(6.50±0.17)×1015/s,由此可得SB方程的参数c为A0′/A0≈7.5.所以,最终确定SB方程为f(α)=7.5α1.2(1-α)2.
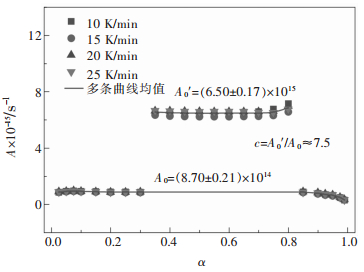 |
| 图 9 指前因子A0计算结果 Fig. 9 Calculated result of the pre-exponential factor A0 |
2.4 动力学模拟验证
研究结果表明(CF)n热分解为一步分解反应,平均表观活化能为264.23±7.82 kJ/mol,指前因子为(8.70±0.21)×1014/s,动力学机理函数f(α)随转化率而变化:
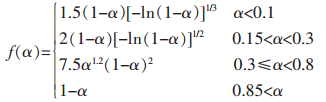
|
(10) |
利用上述动力学三因子分别模拟计算10 K/min、15 K/min、20 K/min和25 K/min升温速率条件下(CF)n分解过程的动力学数值,并与实验测量值进行比较,以验证动力学三因子的可靠性,结果如图 10所示.从图 10中可以看到模拟的数值基本完全落于实验测量曲线上,表明所确定的动力学三因子能够较好地反映(CF)n分解反应动力学的表观特征.
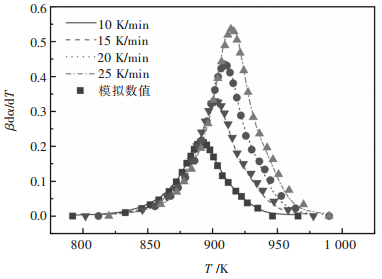 |
| 图 10 (CF)n热分解的非等温动力学模拟验证 Fig. 10 Simulation and verification for the non-isothermal kinetics of (CF)n thermal decomposition |
另外,对于等温动力学过程,微分动力学方程:
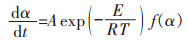
|
(11) |
分离变量并积分,可得:
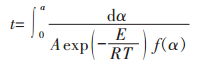
|
(12) |
式(12)可用于等温过程的动力学预测[18].
在853 K温度下(CF)n分解的TG曲线如图 11(a)所示,分解过程经历一个失重步骤,测量结束时反应物失重约65 %,分解率约为95 %,其中等温阶段从时间t=14.5 min开始.利用所确定的动力学三因子,通过式(12)预测853 K温度下(CF)n的分解反应,并与实验测量结果进行比较,如图 11(b)所示.从图 11(b)中可以看出,预测数值轨迹与实验测量曲线基本完全一致,表明所确定的动力学三因子能够用于预测等温条件下(CF)n的热分解过程.
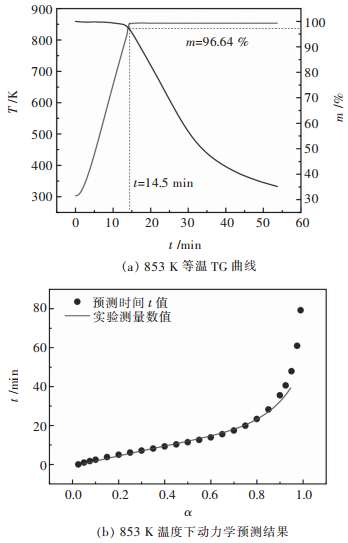 |
| 图 11 853 K温度下(CF)n分解的TG曲线及等温动力学预测结果 Fig. 11 TG curve of (CF)n decomposition and the result of isothermal kinetic prediction at 853 K |
2.5 (CFx)n热分解过程特征
(CFx)n分解的本质是C-F键的断裂和C-C键的重组,分解过程碳成核生长机理随转化率而变化,取决于(CFx)n的链聚合结构性质.根据各动力学机理函数的物理意义,可对(CFx)n热分解反应特征作如下描述:分解初始阶段(α < 0.1)为碳形核诱导期,高反应活性位点的C-C*键(C*:边界位置CF2、CF3基团)及C-F键(聚合体中缺陷位置)发生断裂和重组,形成碳核胚.碳核胚在聚合体中会引起应变而不稳定,重新恢复到反应物(CFx′)n(x′ < x);在晶界位置的碳核胚更容易达到临界数而成长为生长核,通过摄取或合并潜在的成核位点随机生长.并且,随时间持续,高活性位点减少,形核频率会逐渐减小.分解中间阶段(0.15 < α < 0.8),稳定的碳核进行面向同性生长,即二维的核生长.由于(CFx)n的链聚合结构和碳原子层的环结构性质,碳核趋向链生长,并且与形成的分支链发生相互作用,使产物碳形成非晶态结构(0.3≤α < 0.8).分解后期(0.85 < α),剩余物为形体结构简单的碳氟化合物,单个反应粒子上随机形成一个碳核.而且此类碳氟化合物的热稳定性更高,分解反应活化能也较高.
3 结论1)(CF)n的E2g、A1g拉曼振动模频移分别位于1 574 cm-1和1 315 cm-1处,其拉曼无序性敏感参量ID/IG为1.56,远大于石墨的ID/IG值0.24,表明(CF)n微观结构长程无序.
2)(CF)n热分解历程为一步分解反应,反应起始温度为803 K,分解产生的碳氟化合物气体平均气相成分为CF2.95.分解反应的动力学机理函数随转化率而变化,其复杂的动力学机理取决于(CF)n的链聚合结构性质.
3)基于非等温热重分析确定的(CF)n热分解反应动力学三因子:表观活化能为264.23±7.82 kJ/mol,指前因子为(8.70±0.21)×1014/s,动力学机理函数按转化率α的分段函数表示为:
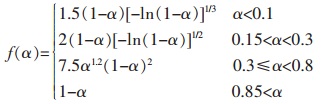
|
利用上述动力学三因子可以进行等温条件下(CF)n热分解的动力学预测.
| [1] |
NAKAJIMA T.
Fluorine-carbon and fluoride-carbon materials: chemistry, physics and applications[M]. New York: Marcel Dekker, 1995: 1-31.
|
| [2] |
SATO Y, ITOH K, HAGIWARA R, et al. Short-range structures of poly (dicarbon monofluoride) (C2F)n and poly (carbon monofluoride) (CF)n[J].
Carbon, 2004, 42(14): 2897–2903. DOI: 10.1016/j.carbon.2004.06.042. |
| [3] |
LAZAR P, OTYEPKOVÁ E, KARLICKY F, et al. The surface and structural properties of graphite fluoride[J].
Carbon, 2015, 94: 804–809. DOI: 10.1016/j.carbon.2015.07.064. |
| [4] |
THOMAS P, DELBÉ K, HIMMEL D, et al. Tribological properties of low-temperature graphite fluorides. Influence of the structure on the lubricating performances[J].
Journal of Physics & Chemistry of Solids, 2006, 67(5/6): 1095–1099. |
| [5] |
MIAO X, YANG J, PAN W, et al. Graphite fluoride as a cathode material for primary magnesium batteries with high energy density[J].
Electrochimica Acta, 2016, 210: 704–711. |
| [6] |
房亚楠, 刘栓, 赵文杰, 等. 石墨/氟碳涂层与氟化石墨/氟碳涂层腐蚀行为的研究[J].
电镀与涂饰, 2016, 35(14): 747–754.
|
| [7] |
康文泽, 李尚益. 氟化石墨烯制备与研究进展[J].
炭素, 2016(3): 12–16.
|
| [8] |
黄海平, 徐亮, 岳亚锋, 等. 基于石墨烯量子点修饰电极的亚硝酸根电化学传感器[J].
有色金属科学与工程, 2017, 8(2): 47–51.
|
| [9] |
CRASSOUS I, GROULT H, LANTELME F, et al. Study of the fluorination of carbon anode in molten KF-2HF by XPS and NMR investigations[J].
Journal of Fluorine Chemistry, 2009, 130(12): 1080–1085. DOI: 10.1016/j.jfluchem.2009.07.022. |
| [10] |
ZHU H M, SADOWAY D R. Anode reaction in aluminium electrolysis prior to and during anode effect[C]//ANJIER J L. Light Metals 2003. New York: John Wiley & Sons, Inc., 2003: 343-349.
|
| [11] |
HAVERKAMP R G. An XPS study of the fluorination of carbon anodes in molten NaF-AlF3-CaF2[J].
Journal of Materials Science, 2012, 47(3): 1262–1267. DOI: 10.1007/s10853-011-5772-5. |
| [12] |
CHEN G, SHI Z N, WANG Z W, et al. Mechanism of graphite electrode fluorinated in 2.4 NaF/AlF3-Al2O3 melt at 1 373 K[J].
Journal of the Electrochemical Society, 2014, 161(14): C587–C593. DOI: 10.1149/2.0781414jes. |
| [13] |
WATANABE N, KOYAMA S, IMOTO H. Thermal decomposition of graphite fluoride. Ⅰ. Decomposition products of graphite fluoride, (CF)n in a vacuum[J].
Bulletin of the Chemical Society of Japan, 1980, 53(10): 2731–2734. DOI: 10.1246/bcsj.53.2731. |
| [14] |
BETTINGER H F, PENG H. Thermolysis of fluorinated single-walled carbon nanotubes: Identification of gaseous decomposition products by matrix isolation infrared spectroscopy[J].
Journal of Physical Chemistry B, 2005, 109(49): 23218–23224. DOI: 10.1021/jp054370r. |
| [15] |
CHEN G, SHI Z, YU J, et al. Kinetic analysis of the non-isothermal decomposition of carbon monofluoride[J].
Thermochimica Acta, 2014, 589(10): 63–69. |
| [16] |
KAMARCHIK P, MARGRAVE J L. A study of thermal decomposition of the solid-layered fluorocarbon, poly (carbon monofluoride)[J].
Journal of Thermal Analysis, 1977, 11(2): 259–270. DOI: 10.1007/BF01909964. |
| [17] |
WATANABE N, KOYAMA S. Thermal decomposition of graphite fluoride. Ⅱ. Kinetics of thermal decomposition of (CF)n in a vacuum[J].
Bulletin of the Chemical Society of Japan, 1980, 53(11): 3093–3099. DOI: 10.1246/bcsj.53.3093. |
| [18] |
杨序纲, 吴琪琳.
拉曼光谱的分析与应用[M]. 北京: 国防工业出版社, 2008: 158-163.
|
| [19] |
VYAZOVKIN S, BURNHAM A K, CRIADO J M, et al. ICTAC kinetics committee recommendations for performing kinetic computations on thermal analysis data[J].
Thermochimica Acta, 2011, 520(1): 1–19. |
| [20] |
VYAZOVKIN S. Model-free kinetics: staying free of multiplying entities without necessity[J].
Journal of Thermal Analysis & Calorimetry, 2006, 83(1): 45–51. |
| [21] |
吴易燃, 姜恒, 宫红, 等. 氢氧化镧的热分解动力学[J].
稀土, 2015, 36(4): 116–119.
|
| [22] |
MÁLEK J. The kinetic-analysis of nonisothermal data[J].
Thermochimica Acta, 1992, 200(8): 257–269. |
| [23] |
KHAWAM A, FLANAGAN D R. Solid-state kinetic models: basics and mathematical fundamentals[J].
Journal of Physical Chemistry B, 2006, 110(35): 17315–17328. DOI: 10.1021/jp062746a. |
| [24] |
ŠESTÁK J, BERGGREN G. Study of the kinetics of the mechanism of solid-state reactions at increasing temperature[J].
Thermochimica Acta, 1971, 3(1): 1–12. DOI: 10.1016/0040-6031(71)85051-7. |
| [25] |
ŠIMON P. Fourty years of the Šesták-Berggren equation[J].
Thermochimica Acta, 2011, 520(1): 156–157. |
| [26] |
胡荣祖.
热分析动力学[M]. 2版. 北京: 科学出版社, 2008: 163-164.
|
 2018, Vol. 9
2018, Vol. 9


