| Cu掺杂LiNi0.6Co0.2Mn0.2O2的电化学性能 |
b. 江西理工大学,江西省动力电池及其材料重点实验室,江西 赣州 341000
b. Jiangxi Key Laboratory of Power Battery and Materials, Jiangxi University of Science and Technology, Ganzhou 341000, China
随着社会的快速发展,能源的需求和消耗越来越大,煤炭石油等化石燃料不可再生资源含量非常有限,并且使用过程中会造成大气污染,破坏环境.锂离子电池具有工作电压高、能量密度大、安全性能好、循环寿命长、自放电率低等众多优点[1-2],已广泛应用.三元正极材料LiNi1-x-yCoxMnyO2具有较好的层状结构,它综合了LiCoO2,LiNiO2和LiMnO2的优点,钴元素减少材料的阳离子混排度,镍元素增加材料的比容量,锰元素稳定了材料的晶体结构,三者具有很强的协同作用[3-4].当1-x-y≥0.5时认为是高镍,材料随镍含量的增加放电比容量增加,同样其合成条件更加严格.镍含量增加不仅加剧锂镍混排[5],引起锂的析出,造成阻抗上升及稳定性变差等问题,而且容易与空气反应,在表面生成Li2CO3和LiOH,LiOH又会与电解液中的LiPF6反应生成HF,腐蚀电极和集流体,降低安全性能[6-7].虽然NCM333、NCM523材料已经成熟的应用于生产,但其实际容量还不能满足于社会的需求,必须着力于容量更高、循环稳定性更好、安全性能更优越的电池材料研究.
Peng等[8]采用喷雾干燥法制备了LiNi0.6Co0.2Mn0.2O2材料,在850 ℃烧结的材料具有优异的电化学性能,在16 mA /g的电流密度下,在2.8~4.3 V之间173.1 mAh /g的初始放电容量并表现出良好的循环性能. Cheng等[9]研究了900 ℃烧结的LiNi0.6Co0.2Mn0.2O2材料在不同截止电压下的电化学性能,在2.7~4.3 V, 4.4 V和4.5 V的截止电压范围内,煅烧样品的初始放电容量分别为170.7 mAh/g, 180.9 mAh/g和192.8 mAh/g,速率为1C.200次循环后相应的保留率分别为86.8 %,80.3 %和74.4 %.Yuan等[10]研究煅烧气氛对LiNi0.6Co0.2Mn0.2O2材料结构和电化学性能的影响,氧气烧结的样品具有更好的层状结构和更小的初级粒度,有效减小Li+/Ni2+混排,在0.1 C时为184.6 mAh/g,0.5 C下100次循环保持率为91.4 %,并且提高了倍率性能.Lei等[11]研究了一种新的表面改性方法,在LiNi0.6Co0.2Mn0.2O2表面掺杂Li2SiO3涂层, 涂层Li2SiO3未掺入LiNi0.6Co0.2Mn0.2O2主体结构中,并且很好地涂覆在活性材料的表面上,样品涂有3 mol Li2SiO3在100次循环后在0.2 C下提供168 mAh/g的容量,并且仍然是第1次放电容量的85.5 %. 100次循环后1 C的容量保持率为73.6 %,因为涂层抑制电极/电解质界面的副反应并提高结构稳定性的涂层,同时,它可以减少电极极化.
随着锂电池的兴起和应用,废旧锂电池材料的回收问题也迎来了新的挑战,若先将电池进行拆分,再将正负极中的集流体和活性物质分离,则效率低,回收成本高,不宜推广.而大部分锂电池以铜箔为负极集流体,采用湿法回收锂离子电池正极材料中的有价元素Ni、Co、Mn时,溶液中同时存在Cu2+,普遍采用的方法是先将Cu2+分离去除,再行回收Ni、Co、Mn,但是并不能完全除去Cu2+[12-13], 对此,研究Cu对正极材料性能的影响就显得很有必要.王东等[14]研究了Cu掺杂对锂离子电池正极材料Li[Ni1/3Co1/3Mn1/3]O2的影响,表明,Li[(NiCoMn)0.99Cu0.01]1/3O2与未掺杂的XRD图谱相似,过多掺杂导致杂质相CoCu2O3生成;所有样品中,Li[(NiCoMn)0.99Cu0.01]1/3O2具有较好的容量保持率和可逆性.文中采用共沉淀法制备前驱体,再将前驱体与Cu2(OH)2CO3·H2O及LiOH·H2O混合球磨,然后进行高温固相烧结,制得正极材料,探究少量Cu对材料性能的影响.
1 实验 1.1 材料合成前躯体Ni0.6Co0.2Mn0.2(OH)2的合成:以硫酸镍、硫酸钴、硫酸猛为原料,按n(Ni):n(Co):n(Mn)=6:2:2的物质的量比,用去离子水准确配成2 mol/L混合盐的溶液,4 mol/L的NaOH溶液,用NH3H2O控制溶液pH值在11.2左右,整个反应区间通入N2保护,待反应完全陈化12 h,所得的沉淀用去离子水充分洗涤后,将沉淀物置于120 ℃真空干燥,便得到前驱体Ni0.6Co0.2Mn0.2(OH)2.Li(Ni0.6Co0.2Mn0.2)1-xCuxO2样品合成:按n(Ni0.6Co0.2Mn0.2(OH)2 +Cu2(OH)2CO3·H2O):n(LiOH·H2O) =1:1.05混合并研磨均匀,其中x分别为0、0.01、0.015、0.02,锂过量是为弥补烧结过程中少量的损耗,在550 ℃预烧6 h, 然后850 ℃氧气中烧结12 h,冷却至室温经过研磨即可得到样品.
1.2 材料表征采用x射线衍射仪(XRD)和扫描电镜(SEM)分析样品的晶体结构和形貌.XRD测试采用的是日本Miniflex 600 X射线衍射仪,X射线源Cu Kα,电流15 mA,管电压40 kV,步宽0.02°,扫描速率10 °/min,衍射角扫描范围10°~90°.采用场发射扫描电子显微镜JSM-7800F, 电压5 kV.
1.3 电池组装与电化学性能测试按Li(Ni0.6Co0.2Mn0.2)1-xCuxO2:S-P:PVDF=90:4:6的质量比混合, 1-甲基-2吡咯烷酮作为溶剂,在球磨机中球磨8 h均匀后涂片,120 ℃烘干后制成正极片.以锂片为负极, 在充满氩气的干燥手套箱中装成CR2032型扣式电池, 在电压2.75~4.2 V范围内进行充放电试验,电化学工作站进行循环伏安测试.
2 结果与讨论 2.1 材料结构与形貌图 1所示为样品Li(Ni0.6Co0.2Mn0.2)1-xCuxO2(x=0, 0.01, 0.015, 0.02)在扫描范围10 °~90 °(2θ)之间以10 °/min的速度进行扫描的XRD衍射图谱,利用MDI.Jade 6.5将4个样品对照LiNiO2标准卡片进行指标化,计算晶胞参数如表 1所示.从图 1中可以看出所有样品均具有相同的晶体结构,属于α-NaFeO2型结构,空间群为R-3m,没有出现杂相,说明掺杂少量的Cu并不会改变材料的晶型.Huang等[15-16]认为在38°及65°左右出现的(006)/(102)峰以及(108)/(110)峰分裂程度越明显,预示材料的层状结构越完整,此时有序度比较高,有助于Li+脱嵌.从图 1可看出,样品(108)/(110)峰分裂明显,说明材料有着良好的层状结构,为锂离子的脱嵌提供了良好条件.
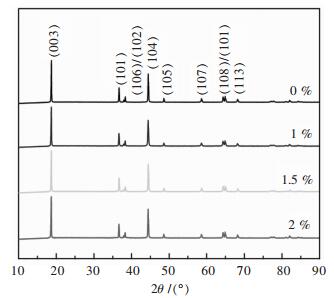 |
| 图 1 正极材料的Li(Ni0.6Co0.2Mn0.2)1-xCuxO2的XRD谱 Fig. 1 XRD pattern of cathode material Li(Ni0.6Co0.2Mn0.2)1-xCuxO2 |
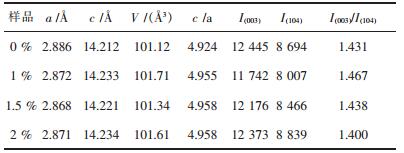
| 表 1 Li(Ni0.6Co0.2Mn0.2)1-xCuxO2的晶胞参数计算值 Table 1 Calculated Cell Parameters of Li(Ni0.6Co0.2Mn0.2)1-xCuxO2 |
 |
| 点击放大 |
表 1所列为4个样品的部分峰强和Jade软件计算的晶胞参数,一般将c及c/a值与I(003)/I(104)大小判断层状特性和阳离子混排程度的参数,c/a比值大于4.899且越大则材料的层状特性越显著,峰强I(003)/I(104)之比大于1.2,则表明了阳离子没有发生明显的混排[17-19].由表 1可知,4个样品的c/a比值都大于4.899,掺杂Cu后,a值减小,c值增大,c及c/a增大,材料的层间距增大,特性更加显著,Li在材料中的脱嵌和迁移通道增大,能够有效减小电池的阻抗,改善其导电性.不掺杂时I(003)/I(104)值为1.431,掺杂1 %和1.5 %比值分别为1.467、1.438,比值增大,说明掺杂少量Cu能够减小阳离子混排,使得结构更加有序;当掺杂量为2 %时,掺杂过量,可能有少量Cu取代晶格中的金属原子,导致晶格参数c增大,同时,I(003)/I(104)值为1.400,比不掺杂时的1.431小,加剧阳离子混排程度,破坏了材料的有序程度.综合c/a与I(003)/I(104)值,掺杂量为1.5 %时,材料的结构较优,阳离子混排程度最小,材料的层状结构更优异,更有利于Li的迁移与扩散.
图 2所示为不同Cu掺杂量合成的正极材料Li(Ni0.6Co0.2Mn0.2)1-xCuxO2的SEM,放大倍数为10 000倍,可以看出由一次颗粒团聚而成的二次颗粒具有较好的类球形结构,一次颗粒紧密结合,之间没有空隙,致密性好,结晶度较好,球形表面有更为细小的颗粒粘附.当掺杂量为2 %时,颗粒之间出现部分熔合,一次颗粒的棱角模糊,可能是掺杂过量,过量的Cu与其他金属形成固溶体[14],熔融在二次颗粒的表面,影响材料内部的容量的释放,降低容量与稳定性.
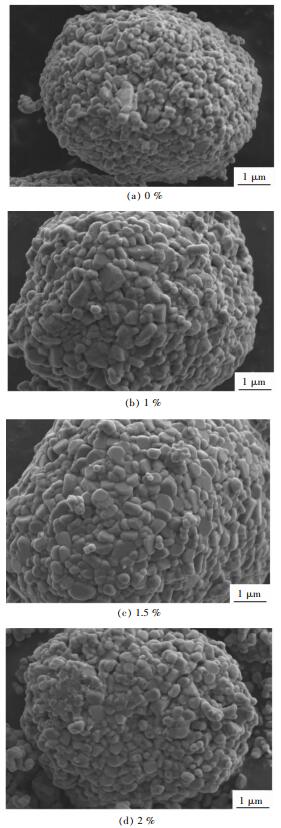 |
| 图 2 正极材料Li(Ni0.6Co0.2Mn0.2)1-xCuxO2的SEM像 Fig. 2 SEM of cathode material Li(Ni0.6Co0.2Mn0.2)1-xCuxO2 |
2.2 材料电化学性能
图 3所示为电池在2.75~4.2V首次放电曲线及0.2 C循环曲线,Li(Ni0.6Co0.2Mn0.2)1-xCuxO2(x=0, 0.01, 0.015, 0.02)样品首次放电比容量依次为170.6 mAh/g、164.1 mAh/g、163.6 mAh/g和162.4 mAh/g,随着Cu的掺杂,材料中活性物质的质量减少,所以放电比容量降低.当x=0时,首次循环放电比容量为169.7 mAh/g,经过100次循环,放电比容量为147.8 mAh/g,容量呈现逐渐递减的趋势,容量保持率为87.09 %.掺杂Cu,电池出现容量递增现象,可能是掺杂Cu,黏附在活性物质表面,锂离子需要更多的时间脱嵌出来,随着循环的进行,二次颗粒内部及附有Cu活性物质得到释放,容量增加.再者,掺杂少量的Cu,能够减小电池阻抗,降低电池内部的自放电.其中掺杂量为1.5 %时最明显,第1次放电比容量为161.8 mAh/g,经过100次循环,比容量增加到173.5 mAh/g,相对于第1次循环增加了12.3 mAh/g.掺杂量为1 %,容量递增的过程主要在前40次,随后的循环中保持平稳,总体上保持率为98.7 %.而掺杂2 %时,容量递增的过程较短,稳定性相对较差,容量保持为87.7 %,可能是Cu掺杂过量,与其他金属形成固溶体,同时加剧了阳离子混排程度,破坏了材料的球形度,使得材料稳定性下降[14].
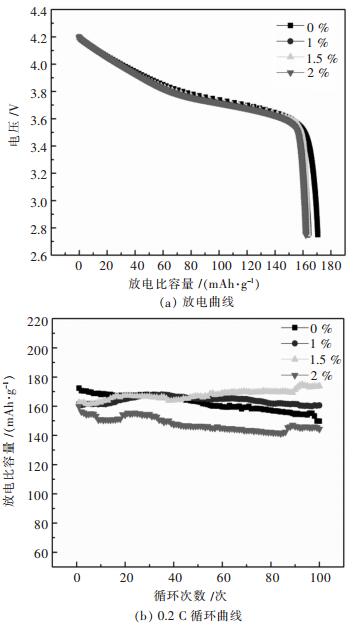 |
| 图 3 电池首次放电曲线及0.2 C循环曲线 Fig. 3 The first battery discharge (a) and 0.2 C cycle curve (b) |
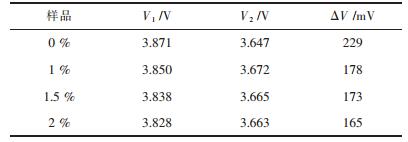
为研究不同Cu掺杂量对材料的影响,将材料制成的扣式电池以扫描电压为1.5~4.8 V,扫描速度为0.2 mV/s下进行循环伏安测试, 第3次循环伏安曲线如图 4所示,表 2为4个样品氧化、还原电位及其差值.4个电池在3.8 V左右都出现明显的氧化峰,3.6 V左右出现还原峰,是对应于Ni2+/Ni4+的氧化还原;在4.5 V附近Co3+/Co4+的氧化还原峰,峰形较弱;4个电池的循环伏安图形相似,峰形尖锐,不掺杂时曲线的面积最大,容量最高,这与上述的放电性能一致.氧化峰与还原峰的电位差参考电池极化程度,数值越小说明电池的极化程度越低[20-22],V1为氧化电位电势,V2为还原电位电势,ΔV表示电位差;不掺杂时ΔV为229 mV,掺杂少量的Cu,ΔV减小,减小了氧化还原电位差,降低了电池的极化程度,不同掺杂量所降低的电池极化程度相差不大;但在1 %,1.5 %,2 %这3个掺杂量中,掺杂1.5 %时,在4.5 V附近Co3+/Co4+的氧化还原峰最强,充放电过程中存在着价态变化,Co3+/Co4+之间的价态转换使得材料的稳定性更强;掺杂量为2 %时,可能Cu与Co形成固溶物,减少Co的含量,使得峰形更弱.综合这两个因素,可以看出掺杂1.5 %时,性能较优,这与之前的结论相一致.
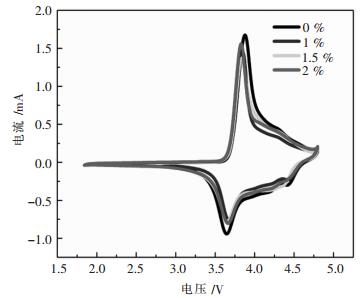 |
| 图 4 Li(Ni0.6Co0.2Mn0.2)1-xCuxO2第3次循环伏安曲线 Fig. 4 Third cyclic voltammogram of Li(Ni0.6Co0.2Mn0.2)1-xCuxO2 |
| 表 2 Li(Ni0.6Co0.2Mn0.2)1-xCuxO2氧化还原电位 Table 2 Li(Ni0.6Co0.2Mn0.2)1-xCuxO2 redox potential |
 |
| 点击放大 |
3 结论
1) 文中采用共沉淀法制备了前驱体,将前驱体与Cu2(OH)2CO3·H2O及LiOH·H2O混合球磨,然后进行高温固相烧结获得正极材料Li(Ni0.6Co0.2Mn0.2)1-xCuxO2(x=0、0.01、0.015和0.02),材料均具有α-NaFeO2型结构,没有出现杂相,样品(108)/(110)峰分裂明显,材料有着良好的层状结构;
2) x=0、0.01、0.015和0.02的样品首次放电比容量依次为170.6 mAh/g、164.1 mAh/g、163.6 mAh/g和162.4 mAh/g.当x为0,1 %,2 %经过100次循环,保持率为87.1 %、98.7 %、和87.7 %;x为1.5 %,比容量从161.8 mAh/g增加到173.9 mAh/g,性能较优,循环稳定性最强.
3) 掺杂Cu,c和c/a增大,层间距增大,Li+脱嵌通道增大,改善导电性;当掺杂1.5%时,c/a值为4.958,I(003)/I(104)比值为1.438,比不掺杂的I(003)/I(104)比值1.431大,更有效的减小了阳离子混排,材料的层状结构更加有序;根据CV测试,掺杂1.5 %时,在4.5 V附近Co3+/Co4+的氧化还原峰最强,Co3+/Co4+之间的价态转换使得材料在充放电过程中稳定性更强,并且减小了氧化还原电位差,降低电池的极化程度.
| [1] |
徐悦斌, 钟胜奎, 张倩. Ti掺杂LiNi0.6Co0.2Mn0.2O2的制备及电化学性能[C]//中国功能材料及其应用学术会议.长沙: 中南大学出版社, 2010.
http://www.wanfangdata.com.cn/details/detail.do?_type=conference&id=7340619 |
| [2] |
张芸.锂离子电池正极材料LiNi1/3Co1/3Mn1/3O2的合成及其电化学性能研究[D].南京: 南京工业大学, 2016.
http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y3107918 |
| [3] |
袁晶.锂离子电池正极材料LiNi0.6Co0.2Mn0.2O2的合成与改性[D].合肥: 合肥工业大学, 2017.
http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y3235389 |
| [4] |
吕庆文.高容量镍基正极材料LiNi0.9Mn0.1O2的合成及改性研究[D].赣州: 江西理工大学, 2017.
http://cdmd.cnki.com.cn/Article/CDMD-10407-1017223375.htm |
| [5] |
卢道焕, 胡明超, 黄瑞鸿, 等. 锂离子电池材料LiNi0.6Co0.2Mn0.2O2的制备与性能研究[J].
中国锰业, 2017, 增刊1: 47–50.
|
| [6] |
吕庆文, 尹从岭, 钟盛文, 等. LiNi0.6Co0.1Mn0.3O2正极材料的合成与性能[J].
有色金属科学与工程, 2016, 7(4): 50–54.
|
| [7] |
李龙.锂离子电池镍钴锰三元正极材料的合成与改性研究[D].北京: 清华大学, 2012.
http://cdmd.cnki.com.cn/Article/CDMD-10003-1013016902.htm |
| [8] |
PENG Y, WANG Z, PENG W, et al. Spray-drying synthesized LiNi0.6Co0.2Mn0.2O2 and its electrochemical performance as cathode materials for lithium ion batteries[J].
Powder Technology, 2011, 214(3): 279–282. DOI: 10.1016/j.powtec.2011.08.022. |
| [9] |
Cheng K L, Mu D B, Wu B R, et al. Electrochemical performance of a nickel-rich LiNi0.6Co0.2Mn0.2O2 cathode material for lithium-ion batteries under different cut-off voltages[J].
International Journal of Minerals Metallurgy and Materials, 2017, 24(3): 342–351. DOI: 10.1007/s12613-017-1413-6. |
| [10] |
YUAN J, WEN J, ZHANG J, et al. Influence of calcination atmosphere on structure and electrochemical behavior of LiNi0.6Co0.2Mn0.2O2, cathode material for lithium-ion batteries[J].
Electrochimica Acta, 2017, 230: 116–122. DOI: 10.1016/j.electacta.2017.01.102. |
| [11] |
LEI W, MU D B, WU B R, et al. Enhanced electrochemical performance of lithium metasilicate-coated LiNi0.6Co0.2Mn0.2O2, Ni-rich cathode for Li-ion batteries at high cutoff voltage[J].
Electrochimica Acta, 2016, 222: 806–813. DOI: 10.1016/j.electacta.2016.11.041. |
| [12] |
陈亮, 唐新村, 张阳, 等. 从废旧锂离子电池中分离回收钴镍锰[J].
中国有色金属学报, 2011, 21(5): 1192–1198.
|
| [13] |
陈亮.废旧锂离子电池中有色金属资源化回收利用研究[D].长沙: 中南大学, 2011.
http://cdmd.cnki.com.cn/Article/CDMD-10533-1011182062.htm |
| [14] |
王东, 吴照金. Cu掺杂对锂离子电池正极材料Li[Ni1/3Co1/3Mn1/3] O2的影响[J].
当代化工, 2015(10): 2335–2337.
DOI: 10.3969/j.issn.1671-0460.2015.10.019.
|
| [15] |
HUANG Y, WANG Z X, LI X H, et al. Synthesis of Ni0.8Co0.1Mn0.1(OH)2, precursor and electrochemical performance of LiNi0.8Co0.1Mn0.1O2, cathode material for lithium batteries[J].
Transactions of Nonferrous Metals Society of China, 2015, 25(7): 2253–2259. DOI: 10.1016/S1003-6326(15)63838-9. |
| [16] |
CHEN Y, ZHANG Y, CHEN B, et al. An approach to application for LiNi0.6Co0.2Mn0.2O2, cathode material at high cutoff voltage by TiO2, coating[J].
Journal of Power Sources, 2014, 256(12): 20–27. |
| [17] |
赖江洪, 钟盛文, 郭进康, 等. LiNi1/3Co1/3Mn1/3O2正极材料的合成与性能[J].
有色金属科学与工程, 2017, 8(4): 68–72.
|
| [18] |
陆雷, 钟伟攀, 杨晖. 高致密球形LiNi0.8Co0.1Mn0.1O2颗粒的合成及性能研究[J].
无机材料学报, 2012, 27(3): 258–264.
|
| [19] |
郑卓, 吴振国, 向伟, 等. Na+掺杂锂离子电池正极材料LiNi0.6Co0.2Mn0.2O2的制备及电化学性能[J].
高等学校化学学报, 2017, 38(8): 1458–1464.
|
| [20] |
YUAN J, WEN J, ZHANG J, et al. Influence of calcination atmosphere on structure and electrochemical behavior of LiNi0.6Co0.2Mn0.2O2, cathode material for lithium-ion batteries[J].
Electrochimica Acta, 2017, 230: 116–122. DOI: 10.1016/j.electacta.2017.01.102. |
| [21] |
夏云飞.层状三元材料LiNi0.6Co0.2Mn0.2O2的烧结工艺及其Al离子掺杂改性研究[D].哈尔滨: 哈尔滨工业大学, 2015.
http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=D754719 |
| [22] |
郝晶敏, 刘海萍, 吉元鹏, 等. 锡掺杂LiNi0.5Mn1.5O4锂离子电池高电压正极材料的制备及性能研究(英文)[J].
Science China Materials, 2017(4): 315–323.
|
 2018, Vol. 9
2018, Vol. 9


