| 真空挥发法脱除钼硫化后液中负二价硫的研究 |
钨钼分离是钨冶炼的重要工序[1-3].在众多除钼方法中,基于钼易与负价硫形成硫代钼酸根的除钼方法被研究最多,且长期应用于工业生产[4-8].钼的完全硫化是影响这类方法除钼效果的关键因素.由于钼酸根转化为四硫代钼酸根是硫化过程中最为困难的步骤[9],而在钨酸盐溶液中通过降低pH值促进硫化反应的调控空间有限,因此,往往加入数倍于理论量的硫化剂来促进钼的深度硫化[10].随着高钼的钨资源逐渐被利用,钨冶炼溶液中钼含量由以往1 g/L左右升高到5 g/L甚至更高[11-14].在此条件下,硫化剂用量随之成倍增加,势必造成更多的负价硫过剩.然而,过剩的负价硫不利于钨冶炼的正常进行.硫化后若采用溶剂萃取或离子交换除钼,部分负价硫将进入有机相或树脂相,对萃取剂或交换树脂的再生造成不利影响.除钼后残留在钨酸钠溶液的负价硫影响后续的转型工艺;而残留在钨酸铵溶液中的负价硫则在蒸发结晶制取仲钨酸铵过程中随氨和水蒸气挥发,不利于氨的回收.因此,采用硫化的方法处理含钼高的钨酸盐溶液,脱除并回收除钼后液中过剩的负价硫势在必行.文中拟通过真空挥发的方式将过剩的负二价硫从钼的硫化后液中脱除,以期为硫化除钼法负二价硫的回收利用提供参考.
1 原理如反应(1),H+参与MoO42-的逐级硫化反应,碱度高不利于钼的硫化.因此,钼酸钠溶液与硫化钠溶液直接混合无硫化反应发生,溶液亦无颜色变化.氯化铵是一种强酸弱碱盐,可使溶液pH值降低,在促进硫化反应进行的同时,又不会在常压条件下引起硫化氢的显著挥发.当在真空条件下,氨的挥发得以强化,从而促进NH4+不断解离释放H+,如反应(2).由NH4+解离释放的H+对W-Mo-S-H2O系溶液存在3方面的影响:①可促进钼的硫化反应;②促成硫化氢的挥发,使游离的负二价硫挥发至气相,如反应(3);③促进钨酸根转换为仲钨酸根,如反应式(4).对于含铵的溶液,如果仲钨酸根生成量较大,且含有一定量游离铵,则可能生成仲钨酸铵或铵钠复盐沉淀,不利于后续除钼操作.因此,在真空挥发过程中,尽可能促成反应(1)、反应(2)和反应(3)的进行,避免仲钨酸盐沉淀的形成.
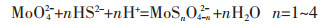
|
(1) |
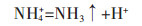
|
(2) |
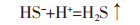
|
(3) |
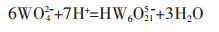
|
(4) |
如图 1所示,采用硫化钠和氯化铵的混合溶液为硫化剂.将一定量硫化剂与含钼溶液混合并在60 ℃水浴中静置一定时间使其发生硫化反应.硫化反应后,将硫化后液置入有一定真空度的三角烧瓶中,并在恒温水浴中搅拌.挥发的气体依次采用钼酸钠和氢氧化钠溶液吸收.硫化溶液经真空挥发后定容,并测定其中钼和负价硫的含量.进一步,可采用季铵盐萃取的方法,考察真空挥发过程对除钼的影响.萃取有机相配比为:5% N263+10%多元醇+85%磺化煤油.
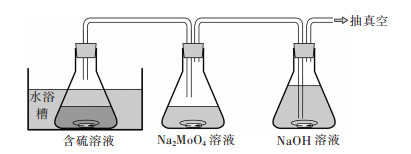 |
| 图 1 真空挥发实验示意 Fig. 1 Schematic diagram of vacuum volatilization experiment |
2.2 分析检测方法
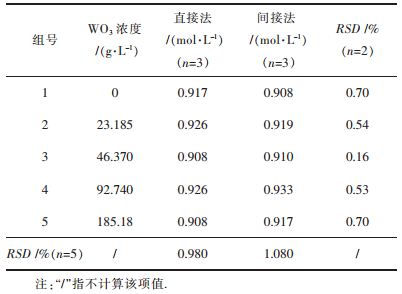
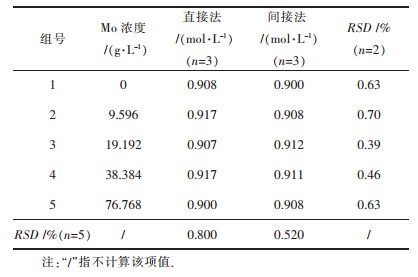
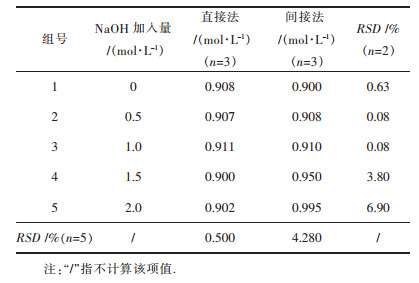
采用双氧水和氢氧化钠混合溶液将待测液中的负价硫完全氧化后,通过硫氰酸盐比色法分析其中的钼含量[15].文中比较了直接碘量法和间接碘量法运用于W-Mo-S-H2O系中负价硫测定的效果[16-18],数据如表 1至表 3所示.结果表明:①钨对负价硫的测定无影响;②虽然负价硫与钼酸根反应生成各种形态的硫代钼酸根,但钼对负价硫的测定无影响,说明无论是游离态的还是与硫代钼酸根当中的负价硫,在碘量法中都可以被碘氧化;③氢氧化钠浓度对直接法测定负价硫的影响较小,其测定值的相对标准偏差RSD在1%以下.但是间接法测定负价硫含量时,当试样中的氢氧化钠浓度超过1.5 mol/L时,硫的测定值会明显偏大,RSD超过3%,超出了误差允许的范围.究其原因,可能是由于碱度较高,氢氧根参与间接法滴定过程中单质碘的歧化反应,生成不可使淀粉变蓝的IO3-和I-,从而增加碘的消耗,使硫的测定值偏高[19, 20].因此,文中采用直接碘量法测定负价硫的含量.
| 表 1 钨对硫化钠氯化铵混合溶液硫测定的影响(pH=9.5) Table 1 Effect of tungsten on sulfur determination in mixed solution of sodium sulfide and ammonium chloride (pH=9.5) |
 |
| 点击放大 |
| 表 2 钼对硫化钠氯化铵混合溶液硫测定的影响(pH=9.5) Table 2 Effect of molybdenum on sulfur determination in mixed solution of sodium sulfide and ammonium chloride (pH=9.5) |
 |
| 点击放大 |
| 表 3 氢氧化钠对硫化钠氯化铵混合溶液硫测定的影响 Table 3 Effect of sodium hydroxide on sulfur determination in mixed solution of sodium sulfide and ammonium chloride |
 |
| 点击放大 |
3 结果与讨论 3.1 铵硫比对硫化钠溶液中硫挥发的影响
向硫化钠溶液中加入不同量的氯化铵后定容,使硫的浓度为0.4 mol/L.在真空度-80 kPa、温度60 ℃的条件下挥发2 h后,测定溶液中负价硫含量.铵硫物质的量比n(NH4+/S2-)对硫挥发率的影响如图 2所示.由图 2可见,硫挥发率随着铵硫比增大而增加,并在n(NH4+/S2-)超过3后趋于不变.表明,铵分解产生的H+对硫化氢生成的影响较大,是影响硫挥发率的重要因素.实验中还发现,真空挥发的气体可与钼酸根发生硫化反应,使吸收瓶中钼酸钠溶液变黄,且颜色逐渐加深.这表明即便是在负压条件下,钼发生硫化反应的趋势仍然较大,因此,真空挥发出来的负二价硫后可被含钼料液吸收利用,从而节省硫化剂的消耗量.
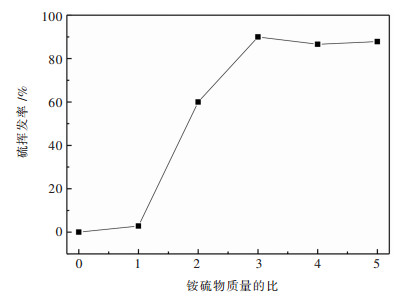 |
| 图 2 铵硫比对硫挥发率的影响 Fig. 2 Effect of ammonium-sulfur ratio on sulfur volatilization rate |
3.2 温度对硫挥发的影响
配制硫浓度为0.4 mol/L、n(NH4+/S2-)为3的硫化钠氯化铵的混合溶液.在真空度-80 kPa、挥发2 h的条件下,考察温度对该溶液硫挥发率的影响,如图 3所示.由图 3可见,温度低于50 ℃,硫的挥发率稳定在20%左右;当温度超过60 ℃,硫的挥发率跃居到90%左右.造成该现象的原因在于氨和硫化氢在溶液中的溶解度随温度升高而降低;并且,氨的挥发促成铵分解释放质子,进而又促成硫化氢的生成.考虑到降低能耗,挥发温度选择60 ℃为优.
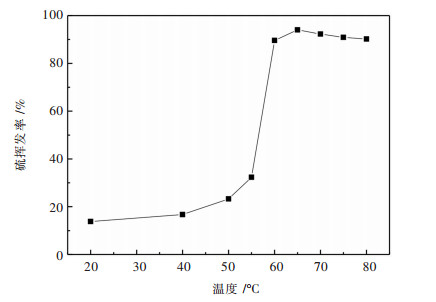 |
| 图 3 温度对硫挥发率的影响 Fig. 3 Effect of temperature on sulfur volatilization rate |
3.3 时间对硫挥发的影响
对于硫浓度为0.4 mol/L、n(NH4+/S2-)为3的硫化钠氯化铵的混合溶液,在真空度-80 kPa,考察不同温度下硫挥发率与挥发时间的关系,如图 4所示.结果表明,温度是影响硫挥发速率的重要因素,在60 ℃挥发0.5 h后,硫的挥发率接近90%,且随着时间延长变化较小;在20 ℃和40 ℃时,硫的挥发率随时间延长呈直线上升,并在2 h后趋缓,4 h后挥发率分别为42.4%和57.6%.此结果亦表明,较高温度对硫化氢的生成和挥发是有利的,使其挥发速度和程度都有提升.
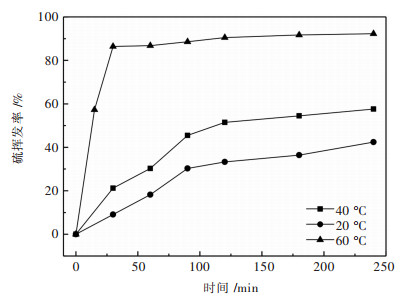 |
| 图 4 不同温度下反应时间对硫挥发率的影响 Fig. 4 Effect of reaction time on sulfur volatilization rate at different temperature |
3.4 钼含量对硫挥发的影响
将硫化钠、氯化铵和钼酸钠溶液混合,混合溶液硫浓度为0.4 mol/L、n(NH4+/S2-)为3,在60 ℃条件下硫化反应2 h,使钼转化为硫代钼酸根.然后在真空度-80 kPa、60 ℃挥发1 h后,测定溶液中负价硫,结果如图 5所示.由图 5可知,随着溶液中钼浓度的增加,硫挥发率呈直线下降,由90%降至20%左右,继续增大溶液中的钼含量,硫的挥发率基本不变.表明,负压条件下钼酸根与负二价硫生成硫代钼酸根的反应能力仍然较大,负二价硫一旦进入硫代钼酸根后便难以挥发,从而使硫的挥发率随钼含量增大而下降.
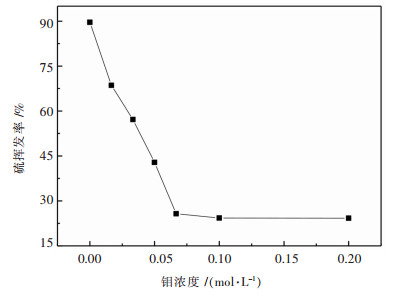 |
| 图 5 钼浓度对硫挥发率的影响 Fig. 5 Effect of molybdenum concentration on sulfur volatilization rate |
3.5 钨含量对硫挥发和萃取除钼的影响
将硫化钠、氯化铵、钼酸钠和钨酸钠溶液混合,混合溶液钼浓度为0.05 mol/L、n(S2-/Mo)为12、n(NH4+/S2-)为3,在60 ℃条件下硫化反应2 h,然后在真空度-80 kPa、60 ℃挥发1 h后,测定溶液中负价硫含量.真空挥发后的溶液通过季铵盐萃取,检验除钼效果.结果如图 6所示.随着溶液中钨含量增大,硫的挥发率和钼的萃取率均呈现下降的趋势.表明,铵分解释放的H+会与钨酸根结合生成仲钨酸根,进而减少了参与硫化氢生成和钼硫化反应的H+,导致硫的挥发率和钼的萃取率随着钨浓度增加而下降.
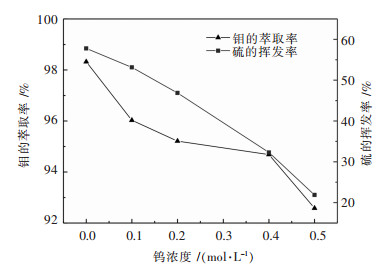 |
| 图 6 钨浓度对硫挥发率和钼萃取率的影响 Fig. 6 Effect of tungsten concentration on sulfur volatilization rate and molybdenum extraction rate |
3.6 铵硫比对硫挥发及钨钼结晶的影响
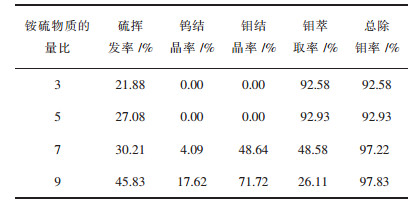
将硫化钠、氯化铵、钼酸钠和钨酸钠溶液混合,使钨浓度为0.5 mol/L、钼浓度为0.05 mol/L、n(S2-/Mo)为12.溶液在60 ℃条件下硫化反应2 h,然后在真空度-80 kPa、60 ℃挥发1 h后,测定溶液中负价硫含量.当溶液中氯化铵浓度较高时,硫代钼酸根和仲钨酸根会与铵结合形成晶体沉淀,因此,将溶液过滤后,测定滤液的钨和钼含量,计算其结晶率.滤液经季铵盐萃取,测定萃余液的钼含量,计算钼的萃取率,如表 4所列.结果表明,硫挥发率和总除钼率随着铵硫比增大而增大,但氯化铵浓度较高时,部分钨和钼在真空挥发后以结晶析出,需要增加一道过滤工序方可进行萃取.因此,对于含钨溶液,应当控制铵硫比,或者控制真空挥发的程度,保证溶液的稳定性.
| 表 4 铵硫比对硫挥发率、钨钼结晶率及钼萃取率的影响 Table 4 Effect of ammonium-sulfur ratio on sulfur volatilization rate, molybdenum extraction rate and the crystallization rate of tungsten and molybdenum |
 |
| 点击放大 |
3.7 真空挥发对硫化萃取除钼的影响
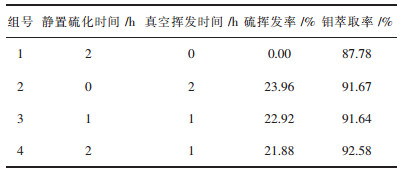
将硫化钠、氯化铵、钼酸钠和钨酸钠溶液混合,使钨浓度为0.5 mol/L、钼浓度为0.05 mol/L、n(S2-/Mo)为12、n(NH4+/S2-)为3.硫化温度为60 ℃、真空挥发温度为60 ℃、真空度为-80 kPa.在不同的静置硫化时间和真空挥发时间下获得硫化后液,再经季铵盐萃取,所测数据如表 5所列.由表 5可知,混合溶液不经静置硫化,直接真空挥发也可获得较好除钼率,说明真空挥发过程氨生成释放出来的H+也会促进钼的硫化反应,进而提升钼的萃取率;含钼溶液充分硫化后再经过真空挥发操作,可使除钼效果进一步提升.由此可见,钼的硫化后液经过真空挥发脱硫,既可以回收过剩的负二价硫,又可以进一步促进硫化反应,为后续钨钼分离创造有利的条件.
| 表 5 静置硫化时间和真空挥发时间对硫挥发率和钼萃取率的影响 Table 5 Effect of static sulfidation time and vacuum volatilization time on sulfur volatilization rate and molybdenum extraction rate |
 |
| 点击放大 |
4 结论
1)铵存在下,采用真空挥发的方式可使溶液中部分游离负二价硫进入气相.铵硫比和挥发温度是影响硫挥发率的重要因素.铵分解产生的氢离子可促进硫化氢的生成.挥发温度高时,氨和硫化氢在溶液中的溶解度降低,使硫挥发速度和程度均得到提升.在真空度-80 kPa、挥发温度60 ℃、铵硫物质的量比大于3,可获得较优的硫挥发效果.
2)真空挥发过程中,铵分解产生的氢离子可促进钼酸根的硫化反应.含钼溶液经静置硫化后,再经过真空挥发操作,在季铵盐萃取的条件下可使钨钼分离效果进一步提升.因此,钼的硫化后液经过真空挥发脱硫,既可以回收过剩的负二价硫,又可以促进钼的硫化反应,为后续钨钼分离创造有利的条件.
3)溶液中铵浓度过高,真空挥发到一定程度会使钨酸根大量转化为仲钨酸根,并使钨结晶析出,破坏了溶液的稳定性.因此,对于含钨较高的溶液,应当控制铵硫比或者真空挥发的程度,降低仲钨酸铵析出的可能性.
| [1] |
赵中伟.
钨冶炼的理论与应用[M]. 北京: 清华大学出版社, 2013: 28-36.
|
| [2] |
LASSNER E, SCHUBERT W.
Tungsten: properties, chemistry, technology of the element, alloys, and chemical compounds[M]. New York: Kluwer Academic/Plenum Publishers, 1999.
|
| [3] |
叶波. 钨钼分离专利技术研究进展[J].
矿产保护与利用, 2016(1): 70–73.
|
| [4] |
LI H G. Production of high purity APT from scheelite and complex tungsten raw material with high Mo content[J].
Transactions of Nonferrous Metals Society of China, 2004, 14(2): 366–369. |
| [5] |
ZHAO Z W, GAO L L, CAO C F, et al. Separation of molybdenum from tung state solution—scavenging thiomolybdate by copper compound[J].
Metallurgical and Materials Transactions B, 2012, 43(6): 1284–1289. DOI: 10.1007/s11663-012-9743-2. |
| [6] |
霍广生, 彭超, 陈星宇, 等. 利用弱碱性阴离子交换树脂从硫化后的钨酸钠溶液中吸附除钼[J].
中国有色金属学报, 2014, 24(6): 1623–1628.
|
| [7] |
ROUT P C, MISHRA G K, PADH B, et al. Solvent extraction separation of molybdenum as thio-molybdate complex from alkaline tungsten leach liquor of spent HDS catalyst -A pilot study[J].
Hydrometallurgy, 2017, 174: 140–146. DOI: 10.1016/j.hydromet.2017.10.002. |
| [8] |
LI Z H, ZHANG G Q, GUAN W J, et al. Separation of tungsten from molybdate using solvent extraction with primary amine N1923[J].
Hydrometallurgy, 2017, 175: 203–207. |
| [9] |
ERICKSON B E, HELZ G R. Molybdenum (Ⅵ) speciation in sulfidic waters: stability and lability of thiomolybdates[J].
Geochimica et Cosmochimica Acta, 2000, 64(7): 1149–1158. DOI: 10.1016/S0016-7037(99)00423-8. |
| [10] |
李洪桂, 羊建高, 李昆, 等.
钨冶金学[M]. 长沙: 中南大学出版社, 2010.
|
| [11] |
赵中伟, 李江涛, 陈星宇, 等. 我国白钨矿钨冶炼技术现状与发展[J].
有色金属科学与工程, 2013, 4(5): 11–14.
|
| [12] |
肖连生. 中国钨提取冶金技术的进步与展望[J].
有色金属科学与工程, 2013, 4(5): 6–10.
|
| [13] |
LI Y L, YANG J H, ZHAO Z W. Recovery of tungsten and molybdenum from low-grade scheelite[J].
JOM, 2017, 69(10): 1958–1962. DOI: 10.1007/s11837-017-2440-5. |
| [14] |
赵中伟, 陈星宇, 刘旭恒, 等. 新形势下钨提取冶金面临的挑战与发展[J].
矿产保护与利用, 2017(1): 98–102.
|
| [15] |
蒋克旭, 邓桂春, 姚林, 等. 硫氰酸盐分光光度法测定钼精矿的含钼量[J].
稀有金属与硬质合金, 2012, 38(4): 52–55.
|
| [16] |
徐丙容. 直接碘量法和高锰酸钾褪色法测定维生素C含量的探究实验[J].
生物学教学, 2017, 42(3): 63–64.
|
| [17] |
张晓凡, 许嘉智, 张文达, 等. 间接碘量法测定稀土硫化物中硫[J].
冶金分析, 2016, 36(2): 61–64.
|
| [18] |
HJ/T 60-2000, 水质硫化物的测定碘量法[S].
|
| [19] |
张小林, 戴兴德. 碘淀粉显色稳定性实验探究[J].
化学教育, 2006, 27(11): 54–54.
DOI: 10.3969/j.issn.1003-3807.2006.11.020.
|
| [20] |
李云泽. 碘量法分析应注意的事项及其在制浆造纸分析中的应用[J].
纸和造纸, 2014, 33(4): 59–60.
|
 2018, Vol. 9
2018, Vol. 9


