| 纳滤膜对稀土离子的动态吸附行为及截留特性 |
离子型稀土矿又称风化壳淋积型稀土矿,于20世纪60年代末期首先在江西省龙南足洞发现,尔后相继在福建、湖南、广东、广西等南岭地区均有发现,但以江西赣州储量最为丰富集中[1-2].离子型稀土富含全球稀缺的中、重稀土元素,而重稀土元素广泛应用在钢铁、玻璃、陶瓷、电子、石油等行业,被称为“工业维生素”,重稀土元素同时也是制造尖端武器必不可少的原料,所以我国储量丰富的离子型稀土矿引起了全世界的广泛关注[3-5].正是因为离子型稀土矿中富含世界其他国家所稀缺的稀土元素,而这些稀土元素又与高精尖产业密切相关[6-7],所以我国对离子型稀土矿的开采极为重视[8].经过我国稀土科学工作者的不懈努力,离子型稀土矿的开采技术取得了长足进步[9].离子型稀土矿的开采方法经历了氯化钠浸出法、硫铵浸出法和原地浸矿法三代工艺,目前基本都是采用原地浸矿法,与前两代开采工艺相比,很大程度上减轻了稀土开采对地表植被的破坏[10].目前从原地浸矿工艺的浸出液中提取稀土的方法主要有沉淀法、沉淀浮选法、溶剂萃取法、离子交换法、液膜分离法等[11].但这些方法都不可避免的存在一些重要缺陷:沉淀法消耗草酸或者碳酸的量过大,导致成本太高[12];沉淀浮选法生产效率低下,生产周期较长,导致成本较高;溶剂萃取法一般萃取设备多、前期投资大、萃取流程复杂;离子交换法由于交换剂用量较大,并且利用率低,选择性较差等缺点使稀土分离效果大打折扣;液膜分离法容易带入杂质,大大降低了提取的稀土纯度[13].
纳滤在矿山领域的研究仍处于初步阶段,国内外研究主要是围绕铜矿、磷酸盐矿、铀矿等选矿废水、尾矿库废水处理方面展开[14-17],进一步利用纳滤膜截留其中有价金属离子、酸根离子等,提高出水水质或达回用标准,同时实现废水中有价离子回收利用、酸碱液的分离回收等.钟常明等[18]研究了DK2540纳滤膜对矿山酸性废水金属离子去除效果,结果显示纳滤对水中金属离子的截留率均可达到95 %以上,从而证实了纳滤在矿山重金属废水处理中的应用可行性.由于纳滤膜表面带有各种荷电基团,荷电基团相互之间通过静电作用产生道南效应,使带不同电性、不同价态的离子透过膜的比例不同[19],所以纳滤膜具有离子选择性.正是纳滤膜所具有的离子选择性,使得对二价或多价离子的去除率较高,而对单价离子(如Na+、K+等)去除率较低[20].而稀土离子多呈正三价及更高价态,这就为纳滤膜浓缩提取浸出液中的稀土离子提供了理论依据.然而有关纳滤膜用于浓缩提取浸出液中稀土离子的研究尚未见报道.由于大部分纳滤膜是带负电荷的,所以在截留金属离子的时候,极易被吸附在膜表面,造成膜污染,使膜通量下降很快,使用寿命大打折扣.因此对传统纳滤膜进行改性是十分有必要的,文中采用碳纳米管醇分散剂来对传统纳滤膜进行亲水化改性.利用改性后的亲水化纳滤膜对稀土离子(以La3+、Nd3+、Pr3+、Ce3+和Y3+为例)进行截留特性以及截留机理的研究,同时探究稀土离子在纳滤膜表面的动态吸附行为.
1 实验 1.1 实验材料磷酸钠(分析纯,广东光华科技股份有限公司);无水哌嗪(PIP,分析纯,上海展云化工有限公司);均苯三甲酰氯(TMC,分析纯,青岛三力本诺化学工业有限公司);碳纳米管醇分散液(CNT,秦皇岛市太极环纳米制品有限公司);正己烷,分析纯,天津市致远化学试剂有限公司);偶氮氯膦(分析纯,华东师范大学化工厂);氧化镧、氧化钕、氧化铈、氧化钇和氧化镨的纯度均大于99.99 %,赣州稀土(龙南)有色金属有限公司.
将纯度大于99.99 %的稀土氧化物溶解在稀硫酸中,使稀土元素由氧化态转化为离子态,再加去离子水配制成一定浓度的溶液用于试验探究.本实验选取具有代表性的镧(La)、钕(Nd)、铈(Ce)、钇(Y)、镨(Pr)5种稀土元素作为研究对象.
1.2 实验仪器及装置分析天平(BT 25S型,北京赛多利斯);天平(BT 210S型,北京赛多利斯);恒温磁力搅拌器(SH23-2型,上海梅颖浦仪器仪表制造有限公司);电热恒温干燥箱(DHG-9247A型,上海精宏实验设备有限公司);真空干燥箱(DZF-6050型,上海新苗医疗器械制造有限公司);紫外分光光度计(756PC型,上海光谱仪器有限公司);Zeta电位仪(90Plus型,美国布鲁克海文仪器公司).
实验装置流程如图 1所示.
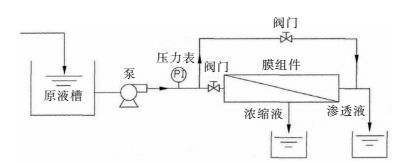 |
| 图 1 实验装置流程 Fig. 1 Flow chart of experimental setup |
1.3 纳滤膜的制备
本实验采用黄万抚等[21]制备的聚砜超滤膜作为纳滤基膜.分别称取质量分数为1.0 % PIP、1.5 % Na3PO4和2 %CNT分散液溶于超纯水中,配成一定量的水相;称取质量分数为0.25 % TMC溶于正己烷中配成一定量的有机相.在常温,湿度适宜的条件下进行界面聚合反应:用耐腐蚀聚氯乙烯框将聚砜基膜固定,做好四角标记后,将水相倒入框中,使聚砜基膜全面浸润,2 min后将水相倒出,晾干后倒入有机相,1 min后将有机相倒出,待晾干后进行第2次水相反应,1 min后倒出,将膜置于70 ℃恒温烘箱中,10 min后取出,浸泡于超纯水中,24 h后即可进行检测和利用.
实验所用自制平板纳滤膜的面积为0.012 69m2.原水、渗透液以及浓缩液中的稀土离子浓度均采用偶氮氯膦—mA分光光度法进行检测分析.
1.4 动态吸附实验新制好的纳滤膜在超纯水中浸泡24 h后,再用超纯水在0.6 MPa压力下预压运行20 min,排空装置中的水后,将配制好的20 L稀土离子溶液以恒定的体积流量(Vf)通过试验装置,进行膜吸附试验,并设置空白实验进行对照,即将稀土离子溶液通过未装膜的装置,试验温度为25 ℃,压力为0.6 MPa.
将配制好的稀土离子溶液通过纳滤膜评价仪时,每隔10 min用吸管取渗透液和浓缩液各2.0 mL,用紫外分光光度计分析渗透液和浓缩液中稀土离子浓度,直至渗透液和浓缩液中稀土离子浓度恒定后停止试验,试验总用时160 min.根据稀土离子的质量守恒关系计算稀土离子在试验装置中的吸附量.
| ${C_{\rm{0}}} \times {V_{\rm{0}}}{\rm{ = }}{W_m}{\rm{ + }}{C_{\rm{1}}}{V_{\rm{1}}}{\rm{ + }}{C_{\rm{2}}} \times {V_{\rm{2}}}$ | (1) |
| ${V_{\rm{0}}}{\rm{ = }}{V_{\rm{1}}}{\rm{ + }}{V_{\rm{2}}}$ | (2) |
式(1)、式(2)中:C0为装置进水中稀土离子的浓度,mg/L;C1、C2分别为运行t时间段内收集的渗透液和浓缩液中稀土离子的浓度,mg/L;C2为运行t时间段内收集的浓缩液中稀土离子的浓度,mg/L;Wm为装有膜的试验装置对稀土离子的吸附量;V0为t时间段内总的进水体积,L;V1为t时间段内收集的渗透液体积,L;V2为t时间段内收集浓缩液的体积,L.
为了准确测定纳滤膜对稀土离子的吸附量,需要进行空白对照实验.通过未装膜的试验装置进行试验时,每隔10 min用吸管取出水2.0 mL,用紫外分光光度计分析出水中稀土离子浓度, 直至出水中稀土离子浓度恒定后停止试验.根据稀土离子的质量守恒关系计算纳滤膜表面对稀土离子的吸附量.
| ${C_{\rm{3}}} \times {{\rm{V}}_{\rm{3}}}{\rm{ = }}{W_n}{\rm{ + }}{C_{\rm{4}}} \times {V_{\rm{3}}}$ | (3) |
式(3)中:C3为进水中稀土离子的浓度,mg/L;C4为是运行t时间段内收集的出水中稀土离子的浓度,mg/L;V3为运行t时间段内总的进水(出水)体积,L;Wn为未装膜的试验装置对稀土离子的吸附量.
在进水的初始浓度及流量相同的情况下,根据稀土离子在装有膜和未装膜的实验装置上的吸附量来计算单位膜面积的吸附量.计算公式如下:
| ${\mathit{\Gamma }_{m,t}} = \left( {\left( {{W_m} - {W_n}} \right)} \right)/{\rm{A}}$ | (4) |
式(4)中:A为纳滤膜有效面积,m2;Γm,t为t时刻在单位膜面积上稀土离子的吸附量,μg/m2.
1.5 截留实验从开始实验到膜表面吸附达到平衡,每隔10 min取一次水样,测定通量和截留率.纳滤膜的通量以及对稀土离子的截留率计算方法如下:
| $J{\rm{ = }}{V_p}{\rm{/}}\left( {A \cdot t} \right)$ | (5) |
| $R = \left( {1 - {\rho _p}/{\rho _f}} \right) \times 100\% $ | (6) |
式(5)、式(6)中:J为通量,L/(h·m2);Vp为渗透液体积,L;A为纳滤膜的有效面积,m2;t为运行时间,h;R为截留率,%;ρf为原水中稀土离子的质量浓度,mg/L;ρp为渗透液中稀土离子的质量浓度,mg/L.
2 结果与讨论 2.1 纳滤膜对稀土离子的吸附行为 2.1.1 吸附动力学对江西某离子型稀土矿山稀土浸出液进行了测定,其稀土离子总含量为2.25×105 μg/L.所以本试验测定了0.6 MPa、25 ℃条件下,初始浓度分别为1×105 μg/L,2×105 μg/L和5×105 μg/L时稀土离子(La、Nd、Pr、Ce和Y)在纳滤膜表面的吸附动力学行为,吸附动力曲线如图 2所示.
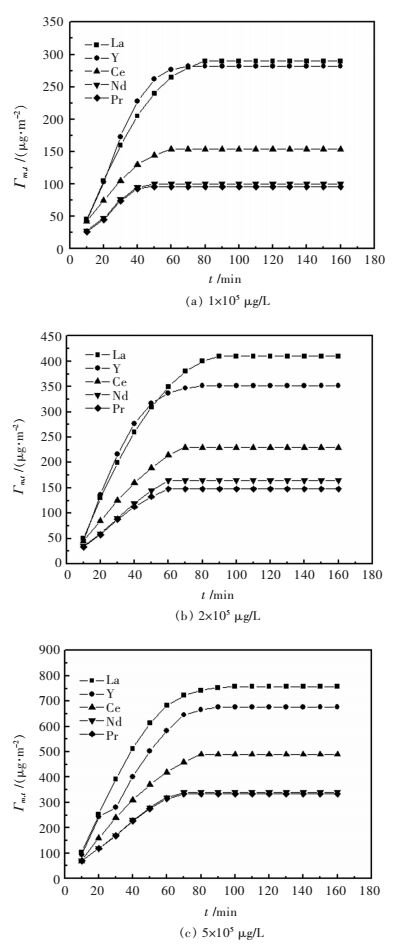 |
| 图 2 稀土离子在不同初始浓度下的纳滤膜表面吸附动力学曲线 Fig. 2 Adsorption kinetics curves of rare earth ions on the surface of nanofiltration membraneat different initial concentrations |
由图 2(a), 图 2(b), 图 2(c)可知,随着稀土离子溶液初始浓度的增加,纳滤膜表面的吸附量也随之增大.在开始阶段,纳滤膜表面对稀土离子的吸附非常迅速,但是随后逐渐减慢,到达某个时间点之后,吸附量达到饱和,基本不再变化.所以,可以将纳滤膜表面对稀土离子的吸附过程分为2个阶段,即快速吸附阶段和缓慢吸附阶段.在吸附前期(0~20 min),纳滤膜表面对稀土离子的吸附速率较快,吸附量与时间近似成线性关系.在前期快速吸附之后,吸附速率减缓,这是由于在前期溶液中稀土离子浓度远高于膜面浓度,稀土离子会迅速向膜面扩散.而随着不断扩散与膜面吸附,溶液中的稀土离子浓度与纳滤膜表面的浓度差值不断减小,进入到第2阶段.随着稀土离子在纳滤膜表面不断累积,到后期吸附在膜表面的稀土离子同时会释放脱落出一部分,随着吸附/释放量比的不断减小,最后接近于1时趋于平衡.
由图 2中还可以看出,稀土离子初始浓度对纳滤膜表面达到吸附平衡的时间有很大影响.由图 2(a)可以看出,当初始浓度较低的时候,吸附达到平衡所需的时间较短.稀土离子很容易被带负电荷的纳滤膜所吸附,浓度较低时,会被吸附在膜表面,甚至进入膜孔;而高浓度时,大量带正电荷的稀土离子在向纳滤膜表面移动时,会出现较强的排斥拥挤现象,所以反而比低浓度时较晚达到吸附平衡.
从图 2又可看出,达到平衡后,相对离子半径较小的Nd3+和Pr3+被吸附的量会比离子半径大的La3+更小,所需时间更长.这是因为离子半径较小的Nd3+和Pr3+更容易通过纳滤膜的孔径,所以被吸附的量会更少、时间更长.
2.1.2 吸附等温线稀土离子的吸附等温线是在一定的温度下,稀土离子与纳滤膜表面达到吸附平衡时,溶液中稀土离子的浓度和纳滤膜所吸附的稀土离子数量之间的关系.在吸附平衡研究中,Langmuir和Freundlich吸附方程是2种常见的吸附等温线表达式. Langmuir方程是基于吸附剂表面是均匀一致的,吸附剂表面能为一个定值,吸附质在吸附剂表面为单分子层吸附,这是基于这些前提条件而导出的吸附方程式. Freundlich吸附方程是基于吸附剂表面是非均一的条件下而提出的经验公式[22].
1)Langmuir吸附方程
| ${\mathit{\Gamma }_{m,{\rm{ }}e}}{\rm{ = }}{Q_{\rm{0}}}b{C_e}{\rm{/}}\left( {{\rm{1 + }}b{C_e}} \right)$ | (7) |
将式(7)两边取倒数,整理得:
| $\mathit{1/}{\mathit{\Gamma }_{m,{\rm{ }}e}} = \left( {{\rm{1 + }}b{C_e}} \right)/{Q_{\rm{0}}}b{C_e}$ | (8) |
式(8)中:Γm, e为平衡吸附量,μg/m2;Ce为平衡浓度,μg/L;Q0为饱和吸附量,μg/m2;b为吸附常数,μg/L.
2)Freundlich吸附方程
| ${\mathit{\Gamma }_{m,{\rm{ }}e}} = K \times C_e^{1/n}$ | (9) |
将式(9)两边取对数,整理得:
| $\ln {\mathit{\Gamma }_{m,{\rm{ }}e}} = \left( {1/n} \right)\ln {C_e} + \ln K$ | (10) |
式(10)中:Γm, e为平衡吸附量,μg/m2;Ce为平衡浓度,μg/L;1/n和K为吸附常数.在纳滤膜表面的吸附等温线中,分别用Langmuir和Freundlich方程拟合稀土离子,拟合的参数如表 1所列,拟合的吸附等温线如图 3所示.
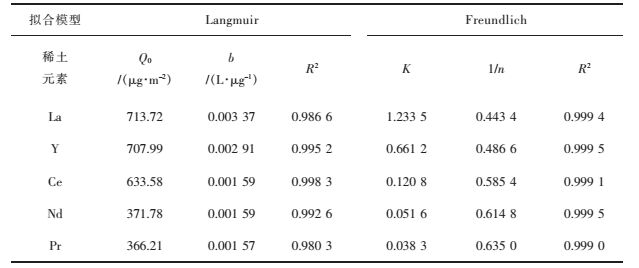
| 表 1 Langmuir和Freundlich吸附方程所对应的拟合参数 Table 1 Langmuir and Freundlich adsorption equation corresponding to the fitting parameters |
 |
| 点击放大 |
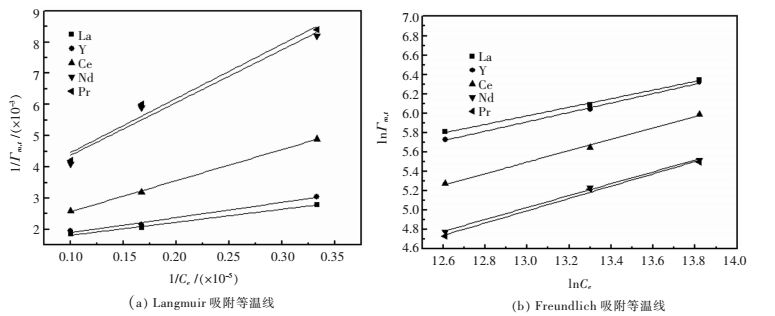 |
| 图 3 纳滤膜对稀土离子的吸附等温线 Fig. 3 Adsorption isotherms of nanofiltration membranes on rare earth ions |
由表 1中2种方程的拟合参数可以看出,都能很好地拟合稀土离子在纳滤膜表面上的吸附行为.但是Freundlich等温线的拟合结果比Langmuir更加稳定可靠,其相关度系数R2均在0.999以上,这是因为纳滤膜表面是非均一的,所以更合适用Freundlich吸附方程来描述稀土离子在纳滤膜表面的吸附行为.在Freundlich吸附等温式中,吸附容量指数1/n是表征膜吸附容量的一个重要参数. 1/n的大小反映了纳滤膜表面吸附量随浓度增加的程度.一般情况下,如果0.1﹤1/n﹤0.5,表明稀土离子容易被纳滤膜所吸附;如果1/n﹥2,则表明稀土离子难以被纳滤膜所吸附.从表 1中可以看出,La、Nd、Pr、Ce和Y的1/n均在0.4~0.7之间,这说明了试验的5种稀土离子容易被纳滤膜所吸附. Freundlich吸附等温式中吸附常数K的大小则表示纳滤膜的吸附容量.由表 1中看出K值依次减小,表明纳滤膜对La、Y、Ce、Nd和Pr的吸附容量依次减小,即La>Y>Ce>Nd>Pr.
2.2 纳滤膜对稀土离子的截留特性在运行压力为0.6 MPa,温度为25 ℃,初始浓度为2×105 μg/L条件下,纳滤膜对稀土离子的截留特性如图 4(a)所示.从图 4中可以看出,纳滤膜对5种稀土离子的截留率和通量都是随着运行时间的延长而逐渐降低,La、Nd、Pr、Ce和Y的截留率分别从初始的99.75 %、91.74 %、93.17 %、96.68 %、90.93 %下降到吸附达到平衡时的94.21 %、81.25 %、85.80 %、89.90 %、81.18 %;通量分别从初始的36.16、41.62、47.37、50.25、50.94下降到吸附达到平衡时的32.40、38.46、42.90、46.04、46.40.这是因为随着运行时间的增加,稀土离子在纳滤膜表面由于吸附而逐渐累积增多,达到吸附平衡后吸附量就保持不变.这就使纳滤膜对5种稀土离子的截留作用分为2个阶段:第1个阶段,即为初始阶段,主要是由于道南效应,纳滤膜对稀土离子的膜表面吸附截留起主要作用;在第2个阶段,达到吸附平衡后,经zeta电位仪测得zeta电位为0.073 mV,表示纳滤膜表面此时接近于电中性,已经达到了吸附平衡,该阶段主要是纳滤膜对稀土离子的膜孔机械筛分起主导作用.这与Yoon J[23]和Kiso Y[24]的研究结果是相一致的,即膜面吸附作用只有过滤初期起主导作用,当膜面吸附达到饱和后,在膜表面富集吸附的稀土离子会有一部分扩散甚至穿透膜,使得纳滤膜的截留效果较初期反而有所下降.
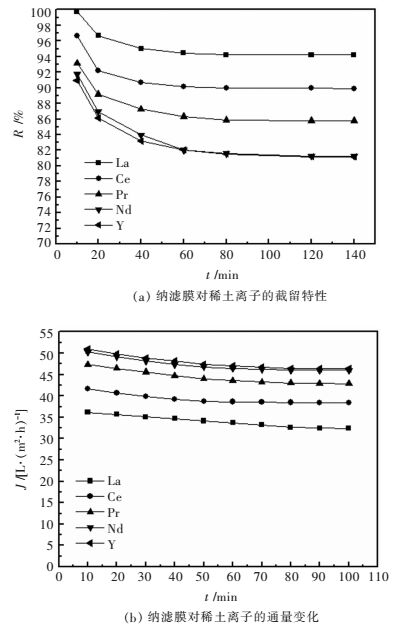 |
| 图 4 纳滤膜对稀土离子的截留率及通量变化 Fig. 4 Interceptionrate and flux change of rare earth ions by nanofiltrationmembrane |
稀土离子半径大小对纳滤膜截留性能的影响如图 5所示.由图 5中可以看出,在吸附达到平衡后,纳滤膜对稀土离子的截留率随离子半径的增大而升高,膜通量是随离子半径的增大而降低.这就充分说明了纳滤膜对稀土离子的截留特性是由离子电荷的道南效应以及膜孔的机械筛分效应共同起作用的.
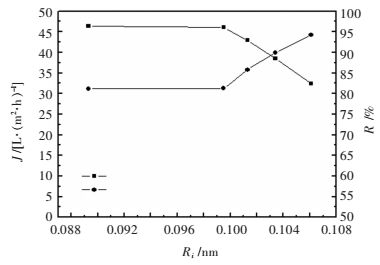 |
| 图 5 稀土离子半径Ri对纳滤膜截留性能的影响 Fig. 5 Effect of rare earth ion radius Ri on retention performance of nanofiltration membrane |
3 结论
1)稀土离子(La3+、Nd3+、Pr3+、Ce3+和Y3+)在自制改性亲水性纳滤膜表面的吸附行为可用Ferundlich吸附动力学模型来较好描述,拟合后的相关系数R2均在0.999以上,吸附容量K分别为1.233 5、0.661 2、0.120 8、0.051 6、0.038 3,吸附容量指数1/n分别为0.443 4、0.486 6、0.585 4、0.614 8、0.635 0.
2)纳滤膜对稀土离子(La3+、Nd3+、Pr3+、Ce3+和Y3+)的截留特性表现主要分为2个阶段,即初始阶段和吸附平衡阶段.在初始阶段,以道南效应造成的纳滤膜的膜面吸附为主;吸附平衡阶段,截留效果主要取决于膜孔的机械筛分作用.对质量浓度为2×105 μg/L的稀土离子(La3+、Nd3+、Pr3+、Ce3+和Y3+),在温度为25 ℃,运行压力为0.6 MPa,纳滤膜表面达到吸附平衡状态下,纳滤膜对稀土离子La3+、Nd3+、Pr3+、Ce3+和Y3+的截留率分别为94.21 %、81.25 %、85.80 %、89.90 %和81.18 %.
| [1] |
饶振华, 冯绍健. 离子型稀土矿发现、命名与提取工艺发明大解密[J].
稀土信息, 2007, 3(8): 28–31.
|
| [2] |
池汝安, 田君.
风化壳淋积型稀土矿化工冶金[M]. 北京: 科学出版社, 2006.
|
| [3] |
徐光宪.
稀土[M]. 北京: 冶金工业出版社, 1995.
|
| [4] |
韩福军, 熊家齐. 中国稀土的国际地位[J].
稀土, 1999, 20(3): 71–75.
|
| [5] |
KANAZAWA Y, KAMITANI M. Rare earth minerals and resources in the world[J].
Journal of Alloys & Compounds, 2006, 412(19): 1339–1343. |
| [6] |
池汝安, 田君. 风化壳淋积型稀土矿评述[J].
中国稀土学报, 2007, 25(6): 641–650.
|
| [7] |
TIAN J. Leaching hydrodynamics of weathered elution-deposited rare earth ore[J].
Chinese Journal of Nonferrous Metals, 2001, 11(3): 434–437. |
| [8] |
赵靖, 汤洵忠, 吴超. 我国离子吸附型稀土矿开采提取技术综述[J].
云南冶金, 2001, 30(1): 11–14.
|
| [9] |
田君, 唐学昆, 尹敬群, 等. 风化壳淋积型稀土矿浸取过程中基础理论研究现状[J].
有色金属科学与工程, 2012, 3(4): 48–52.
|
| [10] |
郑磊. 离子型稀土开采工艺的合理选择[J].
有色金属(矿山部分), 2015, 67(s1): 19–21.
|
| [11] |
李春, 邵亿生. 离子型稀土矿原地浸矿中反吸附问题的探讨[J].
有色金属科学与工程, 2001, 2(4): 5–8.
|
| [12] |
邱廷省, 方夕辉. 磁处理对稀土浸出液稀土沉淀的影响研究[C]//中国稀土资源综合利用研讨会暨第五届中国稀土学会地采选专业委员会第一次学术会议论文集. 深圳: 中国稀土协会, 2009.
|
| [13] |
钱有军. 低浓度稀土溶液碳酸氢铵沉淀及结晶过程研究[D]. 赣州: 江西理工大学, 2013.
|
| [14] |
AlZOUBI H, RIRGER A, STEINBERGER P, et al. Nanofiltration of acid mine drainage[J].
Desalination & Water Treatment, 2010, 21(1): 148–161. |
| [15] |
陈乡, 王海珍, 孙全庆, 等. 用纳滤法去除某铀矿山废水中硫酸根的试验研究[J].
湿法冶金, 2014(1): 64–66.
|
| [16] |
THANU D P R, RAGHAVAN S, KESWANI M. Effect of water addition to choline chloride–urea deep eutectic solvent (DES) on the removal of post-etch residues formed on copper[J].
Semiconductor Manufacturing IEEE Transactions on, 2012, 25(3): 516–522. DOI: 10.1109/TSM.2012.2190998. |
| [17] |
李胤龙, 杨晓松, 刘伟, 等. 纳滤法去除模拟矿山废水中金属离子的研究[J].
北京化工大学学报(自然科学版), 2011(1): 21–25.
|
| [18] |
钟常明, 方夕辉, 许振良. 纳滤膜脱除矿山酸性废水中重金属离子试验研究[J].
环境科学与技术, 2007(7): 10–12.
|
| [19] |
杨庆娟, 魏宏斌, 王志海, 等. 纳滤膜去除饮用水中无机离子的中试研究[J].
中国给水排水, 2009, 25(5): 52–55.
|
| [20] |
王薇, 李国东, 杜启云. 纳滤膜的离子选择性[J].
天津工业大学学报, 2007, 26(4): 5–7.
|
| [21] |
黄万抚, 梁娟, 李新冬. 铸膜液成分对聚砜超滤膜的影响[J].
化工新型材料, 2016, 44(7): 108–114.
|
| [22] |
近藤精一, 石川达雄, 安部郁夫.
吸附科学[M]. 北京: 化学工业出版社, 2006.
|
| [23] |
YOON J, SNYDER S A, WESTERHOFF P, et al. Removal of 17β estradiol and fluoranthene by nanofiltration and ultrafiltration[J].
Journal of Environmental Engineering, 2004, 130(12): 1460–1467. DOI: 10.1061/(ASCE)0733-9372(2004)130:12(1460). |
| [24] |
KISO Y, SUGIURA Y, KITAO T, et al. Effects of hydrophobicity and molecular size on rejection of aromatic pesticides with nanofiltration membranes[J].
Journal of Membrane Science, 2001, 192(1): 1–10. |
 2017, Vol. 8
2017, Vol. 8


