| NiO催化臭氧氧化降解水中双酚A的研究 |
环境中内分泌干扰物(EDCs)通过各种途径进入人体,已严重危害到人体健康而备受人们关注[1].双酚A(BPA)是一种最典型的EDCs,其主要用于合成聚碳酸酯(PC)和环氧树脂等材料,据国内外关于双酚A的研究结果表明,双酚A具有一定的胚胎毒性和致畸性,会导致人体内分泌失调,威胁胎儿和儿童的健康[2-4].常见的双酚A处理方法主要包括生物法[5]、Fenton氧化法[6]、催化湿式氧化法[7]、催化臭氧氧化法[8]等.
催化臭氧氧化技术因能产生大量强氧化性自由基氧化污染物而广泛用于有机废水处理,主要分为利用金属离子催化的均相催化臭氧氧化和利用金属氧化物或氢氧化物催化的多相催化臭氧氧化[9-10].多相催化臭氧氧化技术处理水中双酚A具有处理效率高、能耗低、操作简单、氧化能力强、催化剂便于回收等优点[11-12].文章采用均匀沉淀法制备金属氧化物催化剂NiO催化臭氧氧化降解水中双酚A,并利用XRD、SEM、BET及孔径分析等表征手段对催化剂结构和性质进行表征.研究不同pH、臭氧流量、催化剂投加量、反应时间等因素对双酚A降解效果的影响,并对催化机理进行简单分析.
1 材料与方法 1.1 实验材料双酚A(国药集团化学试剂有限公司),氯化镍(国药集团化学试剂有限公司),25 %氨水(广东光华科技股份有限公司),氢氧化钠(西陇化工股份有限公司),盐酸(江西洪都生物化学有限公司),所有实验试剂均为分析纯,实验用水为去离子水.
1.2 实验方法 1.2.1 催化剂制备采用化学均匀沉淀法在搅拌状态下,往配制的100 mL 1 mol/L的NiCl2溶液中逐滴加入2.5 %的NH3·H2O溶液,调节溶液pH为9,继续搅拌1 h,然后放入恒温活化箱活化一段时间,再抽滤,所得沉淀物用去离子水和乙醇洗涤,洗涤后的沉淀物于90 ℃的恒温干燥24 h,研磨干燥后的沉淀物至无明显颗粒感,将研磨后的粉末用马弗炉在500 ℃条件下焙烧2 h,焙烧后的催化剂即为镍氧化物催化剂.
1.2.2 催化臭氧氧化实验配制100 mg/L的双酚A作为反应溶液,加入适量的催化剂,连接好反应装置(如图 1所示),打开臭氧消毒机,调节臭氧流量,开始曝气,反应到实验所需时间后取样测定双酚A浓度并计算其降解率.
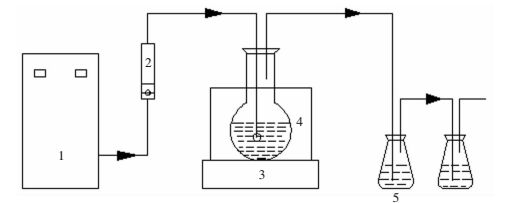 |
| 1.臭氧发生器;2.气体流量计;3.磁力搅拌器;4.恒温水浴装置;5.KI尾气吸收液. 图 1 实验装置示意 Fig. 1 Experimental apparatus chart |
1.2.3 分析方法
实验溶液中双酚A的测定方法采用紫外分光光度法进行测定,双酚A降解率(η)的计算公式如下:
| $\eta {\rm{ = }}\frac{{{C_0} - {C_{\rm{e}}}}}{{{C_0}}} \times 100{\rm{\% }}$ | (1) |
式(1)中:C0为双酚A初始浓度,mg/L;Ce为反应后双酚A剩余浓度,mg/L.
2 结果与讨论 2.1 催化剂的表征 2.1.1 XRD分析该实验制备的镍氧化物XRD图谱如图 2所示.从图 2可以看出,镍氧化物在2θ角为37.46°、43.28°、62.92°、75.44°、79.50°处出现的衍射峰分别对应(111)、(200)、(220)、(311)、(222)晶面,通过与NiO标准图谱(JCPDS NO.71-1179)对比,发现所制备的催化剂与NiO具有相似的衍射峰,说明催化剂为NiO,属立方型晶形结构.
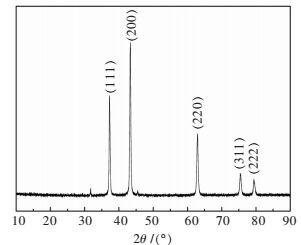 |
| 图 2 催化剂XRD分析结果 Fig. 2 XRD analysis of catalyst |
2.1.2 SEM分析
如图 3为制备的NiO催化剂SEM图,由图 3可知,催化剂成絮状结构,催化剂表面蓬松且粗糙,颗粒大小均匀且较小,在催化氧化当中可提供较多的反应活性位点,这正体现了该催化剂在催化臭氧氧化降解水中双酚A时表现出较强的活性.
 |
| 图 3 NiO扫描电镜像(×20 000) Fig. 3 SEM image of NiO (×20 000) |
2.1.3 BET及孔径分析
经测定得制备的NiO催化剂比表面积为16.862 5 m2/g,催化剂具有较大的比表面积.如图 4为NiO催化剂N2吸脱附曲线.由图 4可知,NiO催化剂吸脱附曲线为第4类型吸脱附曲线,曲线具有明显的滞后环,说明制备的NiO催化剂具有介孔结构[13],而介孔材料不但孔径介于微孔与大孔之间,而且是一种具有巨大比表面积和三维孔道结构的新型材料,介孔结构能够优化催化剂表面的活性位点,从而具有优良的催化性能[14].如图 5为NiO催化剂孔径分布曲线图.由图 5可知,NiO催化剂孔径分布为单峰,孔径分布范围为2~50 nm介孔,平均孔径为4.10 nm,催化剂这种孔径结构将更有利于与水中双酚A的接触,将更有利于催化反应的进行.
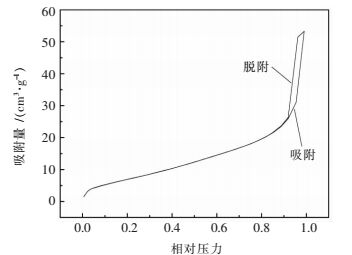 |
| 图 4 NiO催化剂N2吸脱附曲线 Fig. 4 N2 adsorption-desorption isotherms of NiO |
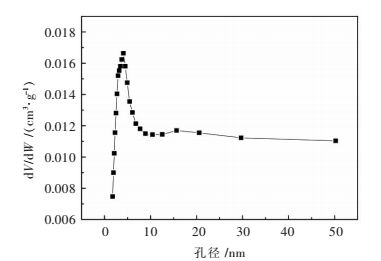 |
| 图 5 BJH孔径分布曲线 Fig. 5 BJH pore size distribution |
2.2 初始pH对降解效果影响
双酚A初始浓度为100 mg/L,催化剂投加量为1.0 g/L,臭氧流量为10 mg/min,反应时间为60 min,分别调节溶液pH值为2、4、6、8、10、12,考察溶液pH对催化臭氧氧化降解双酚A的影响,结果如图 6所示.由图 6可知,NiO催化剂的加入使双酚A的降解率明显提高,且随着pH的升高,双酚A的降解率也随之升高,当pH升高至8时,此时双酚A的降解率最大,为92.1 %,但当pH继续升高时,双酚A的降解率反而下降.这主要是由于在酸性条件下,O3与双酚A的反应以直接反应为主,双酚A降解效率较低,当pH大于8时,溶液中的臭氧、羟基自由基等发生链式反应,导致臭氧利用率降低,从而导致双酚A的降解率下降[15].故实验中取溶液初始pH为8.
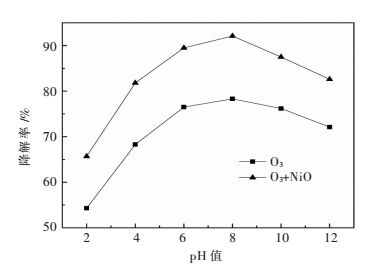 |
| 图 6 初始pH对双酚A降解效果影响 Fig. 6 Effect of initial pH on degradation of bisphenol A |
2.3 反应时间对降解效果影响
双酚A初始浓度为100 mg/L,催化剂投加量为1.0 g/L,臭氧流量为10 mg/min,溶液初始pH为8条件下分别反应15 min、30 min、45 min、60 min、75 min、90 min、120 min,考察反应时间对催化臭氧氧化降解双酚A的影响,结果如图 7所示.由图 7可知,随着反应时间的延长,溶液中双酚A的降解率逐渐升高,当反应时间达到75 min时,双酚A的降解率趋于稳定,反应达到平衡,此时双酚A的降解率达到95.3 %.故实验中反应时间取75 min.
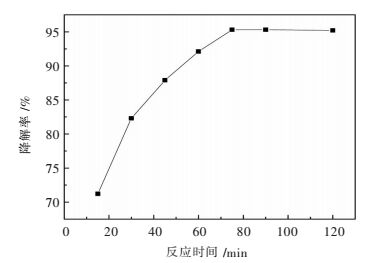 |
| 图 7 反应时间对双酚A降解效果影响 Fig. 7 Effect of reaction time on degradation of bisphenol A |
2.4 臭氧流量对降解效果影响
实验中,双酚A初始浓度为100 mg/L,催化剂投加量为1.0 g/L,反应时间为75 min,溶液初始pH为8条件下分别调节臭氧流量为4 mg/min、6 mg/min、8 mg/min、10 mg/min、12 mg/min、15 mg/min,考察臭氧流量对催化臭氧氧化降解双酚A的影响,结果如图 8所示.由图 8可知,溶液中双酚A的降解率随着臭氧流量的增加而逐渐升高,当臭氧流量达到10 mg/min而继续增加臭氧流量时,双酚A的降解率变化不大.这主要是由于臭氧流量的增加可以提高臭氧与溶液中双酚A的反应几率,从而提高双酚A的降解率,但当臭氧流量一直增加时,由于催化剂催化能力等原因的限制,双酚A的降解率不再升高,而是保持平衡.综合考虑臭氧利用率和双酚A降解率,在接下来的实验中臭氧流量选择10 mg/min.
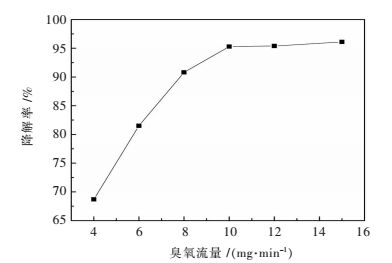 |
| 图 8 臭氧流量对双酚A降解效果影响 Fig. 8 Effect of ozone flux on degradation of bisphenol A |
2.5 催化剂投加量对降解效果影响
在非均相催化臭氧氧化的过程中,催化剂可以促进臭氧的分解,产生氧化性更强的·OH自由基等,以降解溶液当中的双酚A.在该实验中,双酚A初始浓度为100 mg/L,臭氧流量为10 mg/min,反应时间为75 min,溶液初始pH为8条件下催化剂投加量分别为0.2 g/L、0.4 g/L、0.6 g/L、0.8 g/L、1.0 g/L、1.2 g/L,考察催化剂投加量对催化臭氧氧化降解双酚A的影响,结果如图 9所示.由图 9可知,双酚A的降解率随着催化剂投加量的增加而逐渐升高,这主要是由于随着催化剂投加量的不断增加,能够为催化反应提供的活性位点也越来越多,促进了臭氧的分解,从而提高了双酚A的降解率.当催化剂投加量为1.0 g/L时,双酚A降解率基本保持平衡,降解率为95.3 %.故实验中催化剂的投加量选择1.0 g/L.
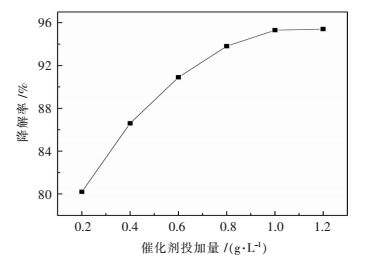 |
| 图 9 催化剂投加量对双酚A降解效果影响 Fig. 9 Effect of catalyst dosage on degradation of bisphenol A |
2.6 催化机理探讨
臭氧与溶液中双酚A的反应途径可能有2种,一是O3直接氧化双酚A,二是由O3被催化分解产生的·OH间接氧化水中双酚A[16].为验证反应途径,选用·OH抑制剂进行探究.叔丁醇是一种应用广泛的·OH抑制剂[17],其结构非常稳定,很难与O3直接发生反应,但它与·OH的反应却很迅速.如果反应是由·OH间接氧化,那么叔丁醇的加入,可以抑制反应的进行,叔丁醇浓度对双酚A降解效果影响见图 10.
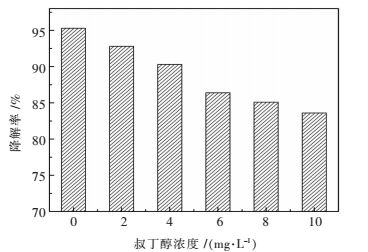 |
| 图 10 叔丁醇浓度对双酚A降解效果影响 Fig. 10 Effect of TBA concentration on degradation of bisphenol A |
从图 10可以看出,加入叔丁醇的浓度越高,双酚A的降解率越低.说明叔丁醇的加入抑制了双酚A的降解,说明NiO催化臭氧氧化降解水中双酚A主要为催化剂催化O3分解产生·OH间接氧化水中的双酚A.
3 结论1)表征结果显示,制备的NiO催化剂成絮状结构,催化剂表面蓬松且粗糙,催化剂比表面积较大,且成介孔结构,平均孔径为4.10 nm,在催化反应中可提供较多的反应活性位点.
2)NiO催化剂催化臭氧氧化浓度为100 mg/L的双酚A较为适宜的反应条件为:溶液pH为8、臭氧流量为10 mg/min、催化剂投加量为1.0 g/L、反应时间为75 min,此时双酚A的降解率为95.3 %.
3)叔丁醇抑制实验表明,NiO催化臭氧氧化降解水中双酚A主要为催化剂催化O3分解产生·OH间接氧化.
| [1] |
MAGDA C, BOSTJAN E, PETAR D, et al. Catalyst support materials for prominent mineralization of bisphenol A in catalytic ozonation process[J].
Environmental Science and Pollution Research, 2016, 23(10): 10223–10233. DOI: 10.1007/s11356-016-6251-y. |
| [2] |
YANG Y, GUO H G, ZHANG Y L, et al. Degradation of bisphenol A using ozone/persulfate process: kinetics and mechanism[J].
Water, Air, & Soil Pollution, 2016, 227(2): 1–12. |
| [3] | 叶林静, 关卫省, 李宇亮. 高级氧化技术降解双酚A的研究进展[J]. 化工进展, 2013, 32(4): 909–918. |
| [4] |
RUTA I G, JUOZAS K, IRINA B, et al. Laccase-catalyzed bisphenol A oxidation in the presence of 10-propyl sulfonic acid phenoxazine[J].
Journal of Environmental Sciences, 2015(30): 135–139. |
| [5] | 王紫嫣, 王荣昌, 袁红丹. 硝化-膜生物反应器去除双酚A的机理分析[J]. 中国给水排水, 2014, 30(1): 1–5. |
| [6] | 胡玲, 高乃云. Fenton试剂降解内分泌干扰物双酚A的研究[J]. 中国给水排水, 2011, 27(7): 80–83. |
| [7] | 彭艳蓉, 王久玲, 王鹏, 等. 催化湿式共氧化降解内分泌干扰物双酚A的研究[J]. 中国环境科学, 2015, 35(8): 2417–2425. |
| [8] | 刘昕, 罗婷玉, 姚坚, 等. 纳米态β-MnO2催化臭氧降解BPA的研究[J]. 化学研究与应用, 2016, 28(9): 1120–1124. |
| [9] | 花朵, 施春红, 袁蓉芳, 等. Fe3+掺杂纳米管TiO2光催化臭氧化去除水中腐植酸[J]. 环境科学研究, 2014, 27(12): 1505–1512. |
| [10] |
KHAN M H, JUNG J Y. Ozonation catalyzed by homogeneous and heterogeneous catalysts for degradation of DEHP in aqueous phase[J].
Chemosphere, 2008, 72: 690–696. DOI: 10.1016/j.chemosphere.2008.02.037. |
| [11] | 耿媛媛, 侯永江, 杜金梅, 等. 多相催化臭氧化技术中催化剂的研究进展[J]. 工业水处理, 2011, 31(2): 8–11. DOI: 10.11894/1005-829x.2011.31(2).8. |
| [12] | 马宁, 刘操, 黄涛, 等. 多相催化臭氧氧化-纳滤工艺污水深度净化研究[J]. 环境科学与技术, 2014, 37(12): 182–186. |
| [13] |
KRUK M, JARONIEC M. Gas adsorption characterization of ordered organic-inorganic nanocomposite materials[J].
Chemical Materials, 2001, 13(10): 3169–3183. DOI: 10.1021/cm0101069. |
| [14] |
MOHAMED M M, BAYOUMY A, KHAIRY M. Structural features and photocatalytic behavior of titania and titania supported vanadia synthesized by polyol functionalized materials[J].
Microporous and Mesoporous Materials, 2008, 109: 445–457. DOI: 10.1016/j.micromeso.2007.05.055. |
| [15] | 侯甲才. 臭氧化降解水中双酚A的效能及动力学[D]. 济南: 山东农业大学, 2014. |
| [16] | 李欣欣. A12O3负载金属氧化物催化臭氧化水中苯酚[D]. 大连: 大连理工大学, 2014. |
| [17] | 韩帮军. 臭氧催化氧化除污染特性及其生产应用研究[D]. 哈尔滨: 哈尔滨工业大学, 2007. |
 2017, Vol. 8
2017, Vol. 8


