| 钠源对正极材料Na3V2(PO4)3性能的影响 |
在当今能源储备技术中,锂离子电池充当着重要角色[1-3],如:电脑,手机,电动汽车等.自然界的锂以化合态的形式存在,含量只有0.006 5 %,由于锂资源的需求量大幅度增加[4],价格也大幅度上升,开发低成本、长寿命、高安全性的新型储能器件迫在眉睫.钠的储量丰富,且分布广泛、提炼简单,并且钠与锂具有相似的电化学性质.钠离子电池的工作原理与锂离子电池类似,因此,发展针对于大规模储能应用的钠离子电池技术具有重要的战略意义[5-7]. NASICON(钠超离子导体)结构材料具有三维开放离子输运通道[8-11], 是一类快离子导体材料,高离子迁移速度、高放电比容量,是钠离子电池的热门正极材料. Uebon等[12]以Na3PO4制备出NASICON斜方六面体结构的Na3V2(PO4)3,负极用金属钠,测得2个电压平台在1.6 V和3.4 V. Jian等[11]以NaH2PO4为钠源用一步高温固相法合成了Na3V2(PO4)3,在2.7~3.8 V内充放电比容量分别达到98.6 mAh/g和93 mAh/g. Soo Yeon Lim等[13]用溶胶凝胶法以NaOH为钠源合成Na3V2(PO4)3,在1 C倍率下充放电50次容量保持在66.5 mAh/g,50次之后,容量损失率只有2.7 %. Song等[14]以Na2CO3为钠源加入乙炔黑为碳包覆材料合成Na3V2(PO4)3放电比容量达到114 mAh/g. Saravanan等[15]以CH3COONa为钠源制得具有碳包覆多孔结构的Na3V2(PO4)3纳米材料,比容量达到了理论容量的98.6 %,在高倍率充放电测试条件下都有高的容量保持率.据不同钠源合成Na3V2(PO4)3材料性能差异较大,采用溶胶凝胶法合成前驱体,预烧350 ℃,高温烧结得到Na3V2(PO4)3,对比以NaOH和Na2CO3为钠源,研究材料形貌,结构以及循环稳定性等电化学性能的影响.
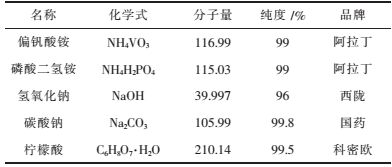
1 实验 1.1 Na3V2(PO4)3的合成表 1所列为实验所用的原料.首先将NaOH、NH4VO3、NH4H2PO4按化学计量比为3.15:2:3,Na2CO3,NH4VO3,NH4H2PO4为3.15:4:6称取一定量的材料,搅拌配成混合溶液;以NH4VO3:C6H8O7·H2O=1:1称取柠檬酸配成酸溶液,通过恒流蠕动泵将酸溶液加入混合溶液中,在室温条件下搅拌12 h,放入水浴锅中加热到80 ℃搅拌蒸干,然后放入鼓风干燥箱中干燥24 h,研磨得到前驱体,放于马弗炉中对材料进行预烧,除去材料中含有的NH4,H2O,CO2,温度为350 ℃;研磨后将材料置于小方舟中,在管式炉中,通入氩气,温度为800 ℃进行焙烧,制得正极材料Na3V2(PO4)3.
| 表1 实验原料一览 Table 1 Experimental raw materials |
 |
| 点击放大 |
1.2 Na3V2(PO4)3材料形貌与结构表征
实验采用荷兰PANalytical X’Pert PRO型转靶X射线衍射仪(Cu-Kα射线,λ=0.150 6 nm,扫描速度8 °/min,扫描范围为10 °~80 °,步长为0.02 °)测试样品的晶体结构,采用荷兰飞利浦XL30W/TMP型扫描电镜测试样品的表面形貌进行分析.
1.3 材料Na3V2(PO4)3的电化学测试依据质量比8:1:1分别称取活性物质Na3V2(PO4)3,乙炔黑和黏结剂聚偏氟乙烯(PVDF), 加入N-甲基吡咯烷酮(NMP)混合均匀制成适宜的浆料,用自动涂膜机将制备的浆料涂覆在铝箔集流体上,放置于120 ℃的鼓风干燥机中烘干,对辊后通过手动冲片机制成正极片,在充满氩气的手套箱中制成CR2032型纽扣电池,采用自制得的钠片为负极,隔膜使用的是Whatman GF/D,电解液是NaClO4/EC:DMC=1:1和5 %FEC.
采用NEW ARE BTS 5 V 30 mA型电池测试系统对电池的电性能进行测试,充放电在2.5~4.0 V,测试条件为25 ℃.
2 结果与讨论 2.1 Na3V2(PO4)3的晶体结构图 1所示为用不同钠源合成Na3V2(PO4)3的XRD谱.由图 1可以看出,用不同钠源即NaOH(样品1),Na2CO3(样品2)合成试样主要衍射峰为Na3V2(PO4)3的特征峰,该材料属于三方晶系,空间点群为R-3c,各衍射峰强度高而且尖锐,样品1在23 °和33 °左右有微小的杂峰,而且样品2衍射峰强度也比样品1的衍射峰强度高,所以以Na2CO3为钠源合成的材料即样品2纯度比样品1的高,结晶度比样品1更好. 表 2所列为Na3V2(PO4)3的晶胞参数和粒径.
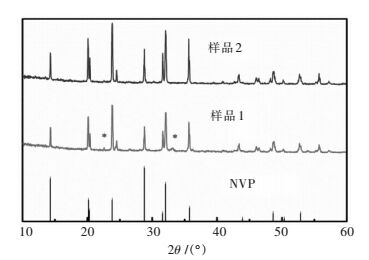 |
| 图 1 Na3V2(PO4)3的XRD结果 Fig. 1 XRD patterns of Na3V2(PO4)3 |
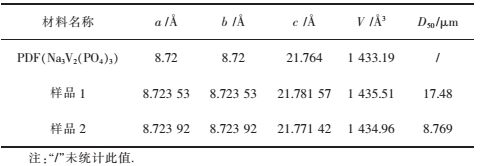
| 表2 Na3V2(PO4)3的晶胞参数 Table 2 Lattice parameters and particle size of Na3V2(PO4)3 |
 |
| 点击放大 |
2.2 Na3V2(PO4)3的表面形貌
表 2所列为中位径D50和图 2所示为SEM图像,合成材料颗粒表面形貌清晰规则,样品2(以Na2CO3为钠源)合成的Na3V2(PO4)3颗粒比样品1(以NaOH为钠源)颗粒平均粒径更小,更符合当今材料纳米化发展方向[16].颗粒粒径越小,提供的比表面积越大,使颗粒与电解液充分接触,有利于电荷在相界面之间的转移. NaOH为晶状颗粒,结晶度大且颗粒较粗,影响配料的均匀性;Na2CO3熔点高,但其稳定性比较好,不含结晶水,易控制原料配比而得到晶形比较完整、结晶度较好的正极材料. Na2CO3作为钠源,用高温固相法合成,会产生少量气体,CO2气体溢出,材料中生成气孔,增加了材料的比表面积.比表面积大,离子具有较短的分散路径,具有更快的动力学[17].
 |
| 图 2 Na3V2(PO4)3的SEM像 Fig. 2 SEM images of Na3V2(PO4)3 |
2.3 Na3V2(PO4)3的电化学性能表征
用不同钠源材料合成的Na3V2(PO4)3制成正极片,作成CR2032纽扣电池,在25 ℃温度条件下,恒流充电一步完成,用0.05 mA电流直接充电到4 V,再以0.025 mA电流恒压充电,静置1 min后以0.05 mA电流放电到2.5 V结束,首次充放电曲线如图 3所示,2种材料的充放电电压平台都在3.4 V附近,过渡金属氧化还原电对V4+/V3+在3.4 V附近[18],且电压平台较为稳定. Na3V2(PO4)3的理论比容量为117.6 mAh/g,样品1(NaOH)的首次放电比容量为79.6 mAh/g,库仑效率为69.7 %,样品2(Na2CO3)的首次充放电比容量为110.8 mAh/g,库仑效率为93.8 %,以Na2CO3为钠源合成的Na3V2(PO4)3有较高的放电比容量和库仑效率.
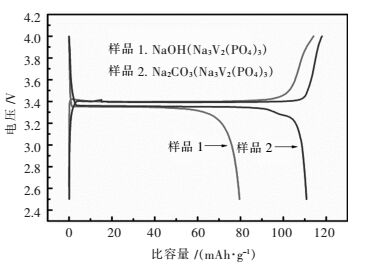 |
| 图 3 不同钠源合成Na3V2(PO4)3首次充放电曲线 Fig. 3 First charge/discharge curves of Na3V2(PO4)3 at different Sodium source |
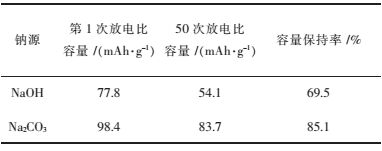
据图 4与表 3所示,以Na2CO3为钠源合成的Na3V2(PO4)3材料有较高的放电比容量,较好的循环性能,经过50次循环后,放电比容量为83.7 mAh/g,容量保持率为85.1 %. Na2CO3作为钠源,用高温固相法合成,会产生少量气体,CO2气体溢出,材料中生成气孔,增加了材料的比表面积,有利于钠离子的脱嵌,从而使其有高的比容量和良好的循环性能.
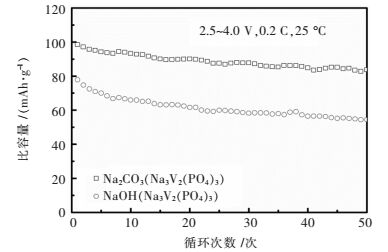 |
| 图 4 不同钠源合成的Na3V2(PO4)3比容量衰减曲线 Fig. 4 Cycle performance of Na3V2(PO4)3 synthesized at different sodium source |
| 表3 不同钠源合成的Na3V2(PO4)3的电化学性能 Table 3 Electrochemical performance of Na3V(PO4)3 synthesized at different sodium source |
 |
| 点击放大 |
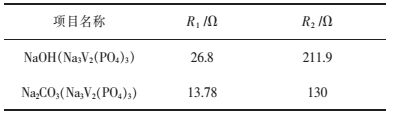
图 5所示为不同钠源合成的Na3V2(PO4)3的交流阻抗谱(EIS),以0.2 C电流循环3次并充电至3.7 V.阻抗曲线是由高频区的半圆和低频区的直线构成,高频区半圆源于电荷转移阻抗,低频区的直线源于钠离子在点击材料体相中的扩散阻抗. R1为电池的欧姆电阻,R2为材料的电荷转移电阻,表 4所示EIS图谱拟合数据表明,以Na2CO3为钠源合成的Na3V2(PO4)3材料有较小的电荷转移阻抗,材料表面由于CO2溢出,产生气孔,有利于钠离子脱嵌.
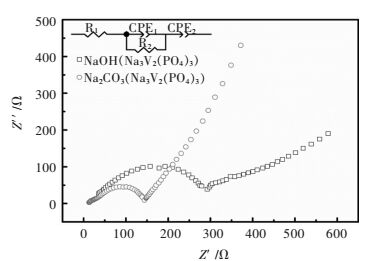 |
| 图 5 不同钠源合成的Na3V2(PO4)3的交流阻抗谱(EIS) Fig. 5 EIS spectra of Na3V2(PO4)3 synthesized at different sodium source |
| 表4 EIS图谱拟合数据 Table 4 Fitting data of EIS patterns |
 |
| 点击放大 |
3 结论
采用溶胶凝胶法和高温固相法烧结合成正极材料Na3V2(PO4)3.结果表明,钠源对正极材料Na3V2(PO4)3性能的影响较大,以Na2CO3为原料合成的材料具有较小的颗粒尺寸,CO2逸出产生气孔,表面积增大,减小钠离子的分散途径,所得材料在25 ℃,2.5~4 V,0.2 C倍率下首次充放电比容量为110.8 mAh/g,50次循环后容量保持达到85.1 %.
| [1] |
LI L J, LI X H, WANG Z X, et al. A simple and effective method to synthesize layered LiNi0.8Co0.1Mn0.1O2 cathode materials for lithium ion battery[J].
Power Technology, 2011, 206(3): 353–357. DOI: 10.1016/j.powtec.2010.09.010. |
| [2] | 钟盛文, 钟凤娣, 张骞. 锂离子电池正极材料LiNi0.5Mn0.3Co0.2O2的合成与掺杂Al的性能研究[J]. 有色金属科学与工程, 2013, 4(4): 11–16. |
| [3] | 马全新, 孟军霞, 杨磊, 等. 锂离子电池正极材料LiNi0.5Co0.2Mn0.3O2的制备及电化学性能[J]. 中国有色金属学报, 2013(2): 456–462. |
| [4] |
YABUUCHI N, KUBOTA K, DAHBI M, et al. Research development on sodium-ion batteries[J].
Chemical Reviews, 2014, 114(23): 11636–11682. DOI: 10.1021/cr500192f. |
| [5] |
CAO Y, Xiao L, SUSHKO M L, et al. Sodium ion insertion in hollow carbon nanowires for battery applications[J].
Nano Letters, 2012, 12(7): 3783–3787. DOI: 10.1021/nl3016957. |
| [6] | 李慧, 吴川, 吴锋, 等. 钠离子电池:储能电池的一种新选择[J]. 化学学报, 2014, 72(1): 21–29. |
| [7] | 王秋月. 正极材料Na3V2(PO4)3的研究[D]. 哈尔滨: 哈尔滨师范大学, 2016. |
| [8] |
GOPALAKRISHNAN J, RANGAN K K. A novel NASICON-type vanadium phosphate synthesized by oxidative deintercalation of sodium from sodium vanadium phosphate (Na3V2(PO4)3)[J].
Chemistry of Materials, 1992, 4(4): 745–747. DOI: 10.1021/cm00022a001. |
| [9] |
ZATOVSKY I V. NASICON-type Na3V2(PO4)3[J].
Acta Crystallographica, 2001, 66(2): 12. |
| [10] |
REN W, ZHENG Z, XU C, et al. Self-sacrificed synthesis of three-dimensional Na3V2(PO4) 3, nanofiber network for high-rate sodium-ion full batteries[J].
Nano Energy, 2016, 25: 145–153. DOI: 10.1016/j.nanoen.2016.03.018. |
| [11] |
JIAN Z, YUAN C, HAN W, et al. Atomic structure and kinetics of NASICON NaxV 2(PO4) 3, cathode for sodium-Ion batteries[J].
Advanced Functional Materials, 2014, 24(27): 4265–4272. DOI: 10.1002/adfm.v24.27. |
| [12] | UEBON Y, KIYBU T, OKADA S, et al. The reports of institute of advanced material study[R]. Kyushu University, 2002, 16:1-5. |
| [13] |
LIM S Y, KIM H, SHAKOOR R A, et al. Electrochemical and thermal properties of NASICON structured Na3V2(PO4)3 as a sodium rechargeable battery cathode: A combined experimental and theoretical study[J].
Journal of the Electrochemical Society, 2012, 159(9): A1393–A1397. DOI: 10.1149/2.015209jes. |
| [14] |
SONG W, JI X, PAN C, et al. A Na3V2(PO4)3 cathode material for use in hybrid lithium ion batteries[J].
Physical Chemistry Chemical Physics Pccp, 2013, 15(34): 14357–14363. DOI: 10.1039/c3cp52308j. |
| [15] |
SARAVANAN K, MASON C W, RUDOLA A, et al. The first report on excellent cycling stability and superior rate capability of Na3V2(PO4)3, for sodium ion batteries[J].
Advanced Energy Materials, 2013, 3(4): 444–450. DOI: 10.1002/aenm.v3.4. |
| [16] |
HU Y, ZHOU Y, WANG J, et al. Preparation and characterization of macroporous LiNi1/3Co1/3Mn1/3O2, using carbon sphere as template[J].
Materials Chemistry & Physics, 2011, 129(1/2): 296–300. |
| [17] |
LI J, DANIEL C, WOOD D. Materials processing for lithium-ion batteries[J].
Journal of Power Sources, 2011, 196(5): 2452–2460. DOI: 10.1016/j.jpowsour.2010.11.001. |
| [18] |
LEE K T, RAMESH T N, NAN F, et al. Topochemical synthesis of sodium metal phosphate olivines for sodium-ion batteries[J].
ChemInform, 2011, 42(44): 3593–3600. |
 2017, Vol. 8
2017, Vol. 8


