| 硼和稀土对铝阴极板耐腐蚀性能的影响 |
传统的湿法炼锌过程是以酸性硫酸锌溶液作为电解液,纯铝板作为阴极板的电解过程[1-2],在湿法炼锌过程中,铝阴极板长时间浸泡在含少量F-( < 50 mg/L)和Cl-( < 200 mg/L)的有较强酸性的硫酸锌溶液中.阴极板的耐腐蚀性能显著影响其使用寿命,同时铝阴极板表面腐蚀程度对剥离得到的电解锌质量也有较大影响[3].
铝及铝合金中的化学成分,尤其是Fe和Si的含量会显著影响其力学性能和耐腐蚀性能. Fe在铝基体中的溶解度极低,室温下只有0.05 %,不溶于α-Al的Fe容易偏聚在铝基体的晶界处并易与合金中的其它元素形成各种复杂的中间相[4-5],主要有FeAl3相、Al8Fe2Si相(α-Fe)和Al5FeSi相(β-Fe).对含FeAl3相金属块的腐蚀研究发现[6-8],铝合金被溶液腐蚀脱落而使得金属块表面形成富铁层,呈现多孔状,将会增大铝合金腐蚀表面积,还可能促进氧化还原反应的进行.富Fe相主要集中于晶界处,使得铝合金基体相对其呈现阳极电位而容易出现点腐蚀并易沿晶界发展,表面晶粒的晶界容易被腐蚀而脱落,腐蚀形式将会由点腐蚀转变成剥落腐蚀.合金中Fe含量越高,相同条件下的腐蚀程度越严重.
在合金化法除Fe领域,张磊[9]、王耀武[10]和Timelli等[11]在添加Mn和Cr元素方向上已经取得一定的成果.近年来,高建卫等[12]发现通过硼砂与熔体中的Fe反应来生成Fe2B沉降至熔体底部,可以达到除Fe的目的.另外,有很多报道指出,稀土元素对于铝合金有着良好的变质作用[13-15].杨怀德[16]通过S和稀土Ce的复合添加,可以将粗大的α-Fe相细化,同时进一步净化熔体.
基于上述分析,拟通过在铝熔体中加入适量的B和稀土元素对杂质Fe相进行变质处理,以提升铝阴极板耐腐蚀性能.
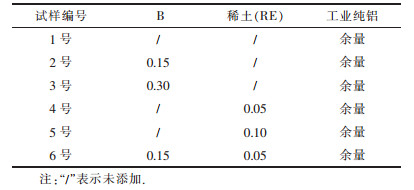
1 实验 1.1 试样材料实验合金成分设计如表 1所列.其中基体金属为工业纯铝(铝质量分数WAl≥99.7 %),B元素以Al-2.5B中间合金形式加入;稀土以Al-10RE中间合金形式加入,中间合金中稀土组分为Ce和La,含量(质量分数)分别为6.5 %和3.5 %.熔炼时,由于中间合金的应用,各元素烧损率大大减少,故本实验中各组分的含量均用名义成分表示.
| 表1 实验合金的设计成分/(质量分数,%) Table 1 Designed component of experimental alloy/(mass fraction, %) |
 |
| 点击放大 |
采用电阻炉进行熔炼实验.将铝锭加热至740 ℃完全熔化后,用铝箔包裹B和稀土中间合金压入熔体中,充分搅拌,待熔体温度回升至740 ℃时,采用NaCl+KCl+C2Cl6进行除气除渣,静置15 min后,浇注在铁模中凝固.铸坯经铣面后进行热轧和冷轧,铝板终轧厚度约为2 mm,剪切成30 mm×30 mm大小的试样用于腐蚀实验.
1.2 腐蚀性能测试湿法炼锌实际工业生产环境中,铝阴极板处在含Zn2+以及多种微量有价金属离子的酸性环境中,溶液pH值为1左右.为了排除电解反应时有价金属离子沉积造成的复杂影响,实验采用含F-(50 mg/L)和Cl-(50 mg/L)的10 %的硫酸溶液近似地模拟工业环境中铝阴极板的工作条件.将试样放在装有腐蚀溶液的烧杯中,并置于35 ℃的恒温水浴加热箱中保温.通过称量试样随着放置时间增长的减重变化确定试样的腐蚀情况.
极化曲线和阻抗谱的测定采用三电极测试体系进行,选用模拟工业正常环境下的溶液作为电解质,以抛光面作为工作电极,Pt环为辅助电极,饱和甘汞电极(SCE)为参比电极.采用德国ZAGNER公司研发的IM6e型电化学工作站.动电位极化曲线的扫描电位范围为-800~500 mV,扫描速率为20 mV/s.电化学阻抗谱在开路电位下测定,频率范围是10 mHz~100 kHz.实验结束后通过Origin软件对阻抗谱数据进行分析,通过作图法求得阻抗弧的大小,以此来表征试样耐腐蚀性能的优劣.
1.3 检测分析采用ICP-OES方法检测各试样的化学成分.采用FEI-Quanta-200型环境扫描电镜以二次电子或者背散射电子观察合金中含铁第二相的形貌与分布以及腐蚀后试样的腐蚀形貌.
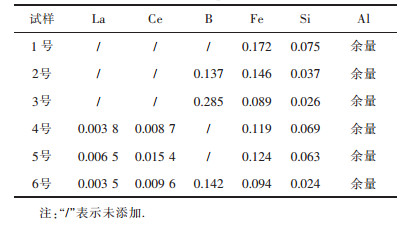
2 结果及分析 2.1 铸态成分及组织分析采用ICP-OES法测定6个试样的化学成分,结果如表 2所列.与1号纯铝试样对比发现,添加B和混合稀土元素后试样中的Fe和Si杂质含量均有一定变化.加入B元素后(2号、3号试样),Fe和Si含量均有所降低,而且加入的B元素越多,除杂效果越好.加入稀土元素后(4号、5号试样),Fe和Si含量也均有所降低,但增加稀土元素含量并不会显著提高除杂效果,除Si效果不明显,而且除Fe效率降低.对比B和稀土元素的除杂效果,发现在除铁效果相当的情况下,稀土元素除Si的作用小.同时添加B和稀土元素时(6号),Fe和Si元素含量都大幅下降,除杂效果最好.
| 表2 ICP成分分析结果/(质量分数,%) Table 2 ICP analysis of component /(mass fraction, %) |
 |
| 点击放大 |
图 1所示为利用扫描电镜观察到的各组试样铸态组织.通常,铝基体中的富Fe相能通过其各自的典型形态来加以区别,α-Fe相的典型形貌呈现短棒状(或骨骼状),弥散分布在铝基体中,β-Fe相在三维空间上是片状相,在二维空间上呈现出的形貌是盘状的截面,也就是针片状,一般分布在大角度晶界处.针片状的β-Fe相除了会割裂铝基体,使得铝合金的强度、韧性等力学性能下降以外,还会显著降低材料的耐腐蚀性能.铝合金表面氧化膜的连续性将会因为β-Fe相的存在而遭到破坏,含Fe杂质夹杂在铝合金的表面将会形成小阳极和大阴极,从而加快铝合金的腐蚀速率,使得铝合金的表面质量变差[17-18].
 |
| 图 1 各试样实验合金铸态组织(SEM) Fig. 1 SEM of cast structure for test alloys |
对比图 1中的添加不同元素的铸态组织可以发现,添加B元素后(2号和3号),铝基体中第二相明显减小,未添加B元素时(1号)呈短棒状的第二相基本都呈点状分布,但针状第二相依然弥散分布于基体各处;增加加入的B元素含量后,针状第二相含量减少,点状第二相含量增加,说明B元素的加入不仅可以减少含铁相,还可以改善含铁相的形貌与分布.添加稀土元素(4号和5号),含铁相减少,原本在晶界上连续分布的针状第二相与稀土反应后,变得不再连续,成为细小的点状,分布在铝基体之中;加入稀土含量越高,点状第二相分布越均匀,点状也更加细小. B和稀土混合添加时(6号),针片状第二相基本消失,点状第二相的含量也明显减少,均匀分布在基体中.
比较添加B、稀土元素、(B+稀土元素)的成分分析结果和铸态扫描组织,添加(B+稀土元素)后,试样中的杂质含量少,且含铁第二相分布均匀,形貌对试样腐蚀性能影响最小.
2.2 浸泡实验结果分析大小相同的铝阴极板在模拟工业环境溶液浸泡实验中减重随时间变化的结果如图 2所示.可以看到,由于氧化膜的存在,在最初的24 h内,试样的减重量增加非常缓慢,重量的减少几乎呈现线性规律,随着浸泡时间的增长,腐蚀速度加快.在最初的24 h内,各试样减重基本相同;在同等长时间(>24 h)浸泡下,1号工业纯铝试样减重最多,6号同时添加B和稀土元素的试样减重最少.在模拟工业环境溶液中浸泡时,腐蚀后试样会发生减重,减重越多,腐蚀性能越差,表明其耐腐蚀性能最差的是工业纯铝试样,耐腐蚀性能最好的是硼和稀土混合添加的6号试样,其次则是添加含量较多硼元素的3号和添加少量稀土元素的4号试样.
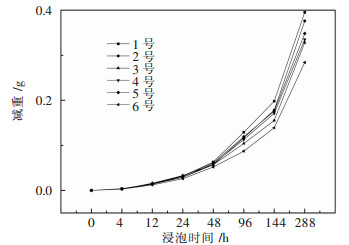 |
| 图 2 模拟工业环境溶液浸泡实验减重变化曲线 Fig. 2 Mass loss of samples after soaking in stimulated industrial solution |
实验样品模拟工业环境中浸泡288 h后腐蚀微观形貌如图 3所示.由图 3可见,试样在酸溶液中浸泡后,腐蚀程度不同,表面会形成大小不同、深浅不一的腐蚀坑. 1号纯铝试样经过腐蚀后表面的腐蚀坑极不均匀,还有一些腐蚀坑连接形成长条状腐蚀条纹;相比之下,添加较多B元素的3号试样、添加少量稀土元素的4号试样腐蚀坑较为细小均匀,同时添加B和稀土元素的6号试样腐蚀坑最少.说明试样在模拟工业环境浸泡288 h后,6号试样的耐腐蚀效果最好,其次是添加过量B元素的3号试样、添加少量稀土元素的4号试样,工业纯铝1号试样最易腐蚀.
 |
| 图 3 各试样浸泡288 h后的腐蚀形貌(SEM) Fig. 3 Surface morphologies of samples after soaking for 288 h (SEM) |
除了从正面观察腐蚀形貌之外,还从试样的横截面观察腐蚀层的侧面形貌和腐蚀深度,模拟工业环境浸泡288 h后试样腐蚀层的截面形貌金相组织如图 4所示.由图 4可知,1号试样的表面出现一层颜色较深的腐蚀层,表面凹凸不平.用腐蚀层的厚度来表征试样的耐腐蚀性能,可以发现,1号试样腐蚀层最厚,腐蚀最深;6号试样的腐蚀层明显变薄,而且表面不连续,只有部分区域出现腐蚀层.
 |
| 图 4 各试样浸泡288 h后的截面形貌图(OM) Fig. 4 Cross section morphologies of samples after soaking for 288 h (OM) |
通过对模拟工业环境浸泡后试样的减重变化和表面腐蚀形貌观察,发现同时添加B和稀土元素的6号试样耐腐蚀性最强,其次是添加较多B元素的3号试样和添加少量稀土元素的4号试样.
2.3 电化学阻抗谱分析电化学阻抗谱技术(EIS)在测试的系统中施加一定的扰动信号(通常为小振幅的正弦激励电压),来测试系统的响应电流,并通过软件数据处理,来分析试样电化学行为.通过分析阻抗弧的大小,可以判断试样耐腐蚀性能的好坏,阻抗弧越大,试样的耐腐蚀性越好. 图 5为各组试样电化学阻抗谱拟合后的图,其中图 5(a)为全图,图 5(b)为图 5(a)局部放大后的数据图.
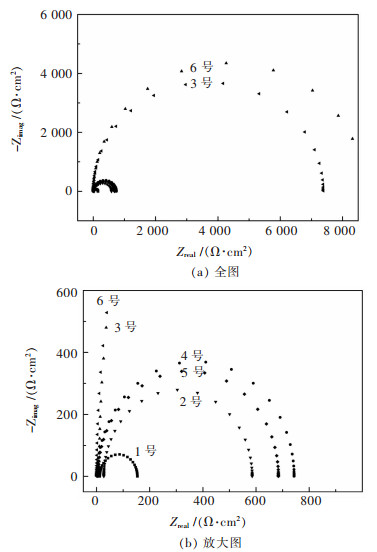 |
| 图 5 试样的电化学阻抗谱的Nyquist谱 Fig. 5 Nyquist figure of EIS result |
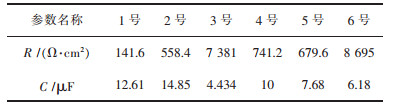
图 5阻抗弧上的每一点到原点的距离代表其阻抗的模值大小,阻抗弧的半径越大,则试样的耐腐蚀性能越好. 表 3所列为各试样交流阻抗的电容和阻抗数据,由此数据可知,阻抗弧半径由大至小的试样依次为6号、3号、4号、5号、2号、1号,其中3号、6号试样的阻抗弧半径大小分别是1号试样的52倍、61倍.综上所述,3号和6号试样的耐腐蚀性能较其他试样更好.
| 表3 各试样交流阻抗数据 Table 3 Impedance data of samples |
 |
| 点击放大 |
3 结论
1)添加适量B元素和稀土元素可有效降低铝合金中铁、硅杂质含量,并改变富铁相形态,使得针片状的β-铁相的形核和长大过程受到阻碍,生成颗粒状或者短棒状铁相.
2)模拟工业环境浸泡实验和电化学阻抗谱的结果表明,添加B元素和稀土元素均能有效改善铝阴极板的耐腐蚀性能,其中混合添加B和稀土元素能显著减少浸泡时的减重,拟合的电化学阻抗谱半径最大,耐腐蚀效果最好.
| [1] | 何正夫, 林波, 王荣莉, 等. 1070铝合金阴极板性能的控制[J]. 有色金属加工, 2010, 39(1): 20–22. |
| [2] | 梅光贵, 王德润, 周敬元. 湿法炼锌学(精)[M]. 长沙: 中南大学出版社, 2004. |
| [3] | 栗韬, 黄惠, 郭忠诚. 超硬铝合金作为阴极在锌电积过程中的电化学行为[J]. 北京科技大学学报, 2016, 38(6): 767–772. |
| [4] |
TAYLOR J A. Iron-Containing intermetallic phases in Al-Si based casting Alloys[J].
Procedia Materials Science, 2012(1): 13–19. |
| [5] |
MBUYA T O, ODERA B O, NG'ANG'A S P. Influence of iron on castability and properties of aluminium silicon alloys: Literature review[J].
International Journal of Cast Metals Research, 2003, 16(5): 451–465. DOI: 10.1080/13640461.2003.11819622. |
| [6] | 彭淳. 铸造铝合金中有害铁相的变质及去除技术研究[D]. 广州: 华南理工大学, 2012. |
| [7] | AMBAT R, DAVENPORT A J, SCAMANS G M, et al. Effect of iron-containing intermetallic particles on the corrosion behaviour of aluminium[M]. Berlin: Springer Berlin Heidelberg, 2010: 409-430. |
| [8] | 李劲风, 郑子樵, 任文达. 第二相在铝合金局部腐蚀中的作用机制[J]. 材料导报, 2005, 19(2): 81–83. |
| [9] | 张磊, 焦万丽, 尉海军, 等. 锰结合预先热处理对铝硅合金中富铁相组织和力学性能的影响[J]. 中国有色金属学报, 2005, 15(3): 368–373. |
| [10] | 王耀武, 冯乃享, 尤晶, 等. 氯化锰去除铝硅合金中铁杂质的研究[J]. 稀有金属与硬质铝合金, 2008(4): 10–13. |
| [11] |
BONOLLO F, TIMELLI G. The influence of Cr content on the microstructure and mechanical properties of AlSiCu3(Fe) die-casting alloys[J].
Materials Science and Engineering A, 2010, 528(1): 273–282. DOI: 10.1016/j.msea.2010.08.079. |
| [12] |
GAO J W, XIE M X. Effects of boron and lanthanum on the impurity iron in aluminum melts[J].
Mineral Processing and Extractive Metallurgy, 2011, 120(3): 172–176. DOI: 10.1179/1743285511Y.0000000019. |
| [13] | 陈永禄, 傅高升, 陈文哲. 微量稀土对Al-1Mn-1Mg合金中杂质相的变质作用探讨[J]. 中国稀土学报, 2005(增刊2): 99–103. |
| [14] | 王孟云. 稀土元素在铝合金中作用的研究[J]. 铸造技术, 2013(3): 290–292. |
| [15] | 杨怀德. S和稀土对再生铝合金富Fe相变质行为的影响[J]. 特种铸造及有色合金, 2009, 33(9): 848–851. |
| [16] | 陈冰泉, 彭军波, 缪鄂. 稀土、镍、锰对铝硅合金熔敷金属中铁相形态的影响[J]. 机械工程材料, 2003, 27(4): 14–17. |
| [17] |
DINNIS C M, TAYLOR J A, Dahle A K. As-cast morphology of iron-intermetallics in Al-Si foundary alloys[J].
Scripta Materialia, 2005, 53(8): 955–958. DOI: 10.1016/j.scriptamat.2005.06.028. |
| [18] |
CAO X, CAMPBELL J. The solidification characteristics of Fe-rich intermetallics in Al-11.5Si-0.4Mg cast alloys[J].
Metallurgical and Materials Transactions A, 2004, 35(5): 1425–1435. DOI: 10.1007/s11661-004-0251-0. |
 2017, Vol. 8
2017, Vol. 8


