| 萃取法提取铬(Ⅲ)分离铁(Ⅱ)的研究 |
电镀污泥含有多种重金属元素,是可再生利用的资源,也属于危险废弃物,如果不加处理排放,将会造成严重的环境污染及资源浪费[1].针对电镀污泥的特点及其危害性,工业上从最初的简单填埋、固化处理到现在系统的回收电镀污泥中的有价金属,使得电镀污泥逐渐得到资源化和无害化利用[2-3].目前,工业上趋向于采用湿法冶金技术来实现电镀污泥中有价金属资源回收.电镀污泥的浸出溶解主要有酸浸和氨浸2种工艺[4].酸浸浸出液中含有Fe、Zn、Ni、Cu、Cr等金属[5-6],Zn、Ni、Cu通常通过化学沉淀法或萃取法进行回收,但溶液中还含有铬、铁等离子.由于铬铁性质相似,工业上常用的除铁法对于铬的损失率较高,易形成铬铁渣,造成二次污染,现阶段对于铬铁分离尚无高效实用的技术[7-8].目前,电镀污泥浸出液中铬铁分离及铬的回收技术主要有化学沉淀法、溶剂萃取法、离子交换法等[9-11].
化学沉淀法作为一种最普遍的金属离子分离方法,操作简单,但具有工艺流程长、沉淀剂和酸碱消耗量大等缺点;离子交换法工艺操作简单,金属离子选择性好,但树脂交换量相对较小,对浸出液体系稳定性要求高,对于高浓度的浸出液应用较少.溶剂萃取法反应速度快、操作连续性强、分离效果好,适用于组分复杂的溶液,所以相较于沉淀法、离子交换法,溶剂萃取法更适合于提取、分离电镀污泥浸出液中的有价金属[12].李雪飞[13]釆用P204-煤油体系进行了萃取铁分离铬的工艺研究,虽然经P204萃取使得铬铁得到分离,但在高效除铁的同时,铬的萃取率也高达25 %,铬损失较大.孙永会[14]等采用5 %P204-95 %煤油体系萃取制革污泥淋滤液中的Cr3+和Fe3+,进过2级萃取,分离系数可以达到2 000以上,实现了铬和铁的深度分离,但铬损失率为7 %,同时萃余液中铬未得到富集.
该研究针对电镀污泥硫酸浸出液展开,目前,工厂通过萃取工艺已实现Zn、Ni、Cu、Co等有价金属回收富集,但萃余液中含有大量Cr(Ⅲ)及少量Fe(Ⅱ).针对这一问题,采用P204-磺化煤油-硫酸萃取体系共萃铬铁,选择性反萃,探索萃取分离回收浸出液中的铬和铁及富集铬的工艺条件.
1 实验 1.1 材料、试剂和仪器材料:实验课题来源于某厂电镀污泥硫酸浸出液,经过溶剂萃取已将浸出液中Zn、Cu、Ni、Co等有价金属回收,余下有价金属主要为铬和铁.溶液中铬和铁含量大约为8 g/L和0.5 g/L左右,铬在浸出液中存在形态为Cr(Ⅲ),铁存在形态为Fe(Ⅱ),溶液的pH值在1.5~2.0之间.配制相关的模拟料液进行试验研究,其中铬浓度7.16 g/L,铁浓度0.469 g/L,pH=1.70.
试剂:P204、磺化煤油、NaOH、H2SO4、HCl、H2C2O4、FeSO4·7H2O、Cr2(SO4)3·6H2O、30 %H2O2溶液.
仪器:125 mL梨型分液漏斗,SHZ-82恒温水浴冷冻振荡器(江苏金坛亿通电子有限公司),iCAP 7000型电感耦合等离子发射光谱仪, PHS-3C型pH计(上海精密科学仪器有限公司).
1.2 分析方法水相中金属离子浓度和负载有机相中金属离子浓度经处理后采用电感耦合等离子体发射光谱仪(ICP)测定;采用pH计测定水相pH值.
1.3 实验方法P204是一种酸性磷性萃取剂,在萃取过程中与金属离子发生阳离子交换反应,释放出氢离子,使得溶液中的平衡pH值降低,萃取率也随之降低.因此,萃取剂P204必须先进行皂化[15].本实验采用10 mol/L的NaOH溶液进行皂化,先将萃取剂按比例配好,计算出萃取剂相应的皂化率所需的NaOH量,振荡混合均匀.
按照特定相比(VO/VA)用量筒量取一定体积的有机相及水相,在设置的萃取条件下,将有机相和水相混合于分液漏斗中,置于振荡器上均匀振荡相应的时间,使有机相和水相混合均匀,振荡完后静置分相,记录分相过程中实验现象及分相时间,分析水相及有机相目标元素浓度并计算萃取率、反萃率、分离系数等参数.
1.4 实验原理实验选择的萃取剂P204为常用的酸性磷性萃取剂,该类萃取剂广泛应用于金属阳离子的萃取分离.在硫酸溶液中,铬、铁以阳离子或者水合阳离子形式存在,采用酸性磷性萃取剂,萃取机理为阳离子交换反应[16].
| $ {{\rm{M}}^{n + }} + n{({\rm{HR}})_{2({\rm{O}})}} = {\rm{M}}{({\rm{H}}{{\rm{R}}_2})_{n({\rm{O}})}} + n{{\rm{H}}^ + } $ |
P204在同一pH下优先萃取Fe2+,但对Fe2+,Cr3+金属离子的萃取能力相近,分离系数较低[17],在高平衡pH下容易共萃进入有机相中.反萃时,只要降低水相的pH值,反应逆向进行,Cr3+返回水相,萃取剂恢复酸结构,但萃取进入P204的Fe2+由于与含磷酸类萃取剂能形成配位效应,结合能力强,低浓度的无机酸很难反萃下来[18],从而可以实现铬铁分离.
2 结果与讨论 2.1 萃取结果与讨论 2.1.1 P204的皂化率对萃取富集铬的影响萃取条件:有机相为30 %P204+70 %磺化煤油,水相为实验料液,相比VO/VA=1/1,VO=25 mL,温度为18 ℃,振荡时间10 min.实验结果如图 1所示.
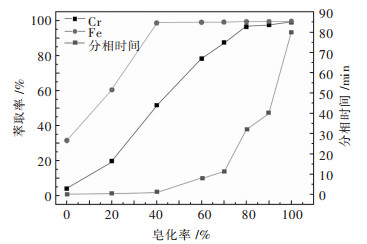 |
| 图 1 P204的皂化率对铬铁萃取率的影响 Fig. 1 Effect of saponification rate of P204 on extraction rate of chromium and iron |
从图 1可以看出,铬的萃取率随着P204的皂化率的增加而迅速提高,同时铁的萃取率也随之增加.皂化率的增加提高了萃取时平衡pH,使得萃取剂P204对铬和铁的萃取率随之增加,为了使铬得到富集,萃取时要保证铬有较高的萃取率.但是过高的皂化率会使平衡pH过高,使得水相中的铬离子发生水解,不利于后续的串级萃取,同时,萃取时分相时间迅速增加,影响生产效率.结合铬的萃取率和分相时间综合考虑,实验选择萃取剂P204的皂化率为70 %.
2.1.2 P204浓度对萃取富集铬的影响萃取条件:有机相为P204+磺化煤油,水相为实验料液,相比VO/VA=1/1,VO=25 mL,温度为21 ℃,振荡时间10 min,萃取剂P204的皂化率为70 %,改变P204浓度.实验结果如图 2所示.
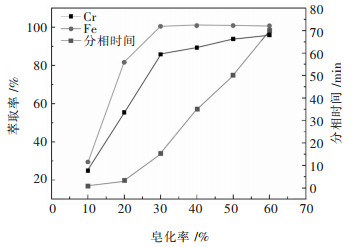 |
| 图 2 P204浓度对铬铁萃取率的影响 Fig. 2 Effect of P204 concentration on extraction rate of chromium and iron |
P204的体积分数的提高增加了有机相中与铬、铁结合的萃取剂分子,同时,也使得水相平衡pH增加,萃取率会随之提高.从图 2可以看出,铬的萃取率随着P204的体积分数的增加而迅速提高,浓度达到30 %时,铬萃取率达到85.7 %,同时铁的萃取率也随之增加.为了使铬得到富集,萃取时要保证铬有较高的萃取率.继续增加P204的体积分数,铬的萃取率增加较小,但萃取时分相时间却大大增加.结合铬的萃取率和分相时间综合考虑,实验选择萃取剂P204的体积分数为30 %.
2.1.3 料液pH对萃取富集铬的影响该部分料液pH通过添加NaOH溶液来调控.萃取条件:有机相为30 %P204+70 %磺化煤油,P204皂化率为70 %,水相为实验料液,使用NaOH溶液调节pH值,相比VO/VA=1/1,VO=25 mL,温度为18 ℃,振荡时间10 min.实验结果如图 3所示.
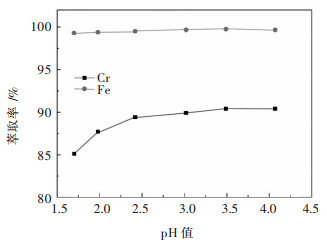 |
| 图 3 料液pH对铬铁萃取率的影响 Fig. 3 Effect of pH on extraction rate of chromium and iron |
由图 3可以看出,随着料液pH的增加,水相平衡pH也随之增加,但是水相平衡pH主要通过皂化率来控制,所以水相平衡pH变化较小,所以铬的萃取率随着料液pH的升高而升高,但铬萃取率仅从85.2 %增加到90.4 %,当pH达到2.42时,铬的萃取率趋于稳定.所以选择料液pH为2.42.
2.1.4 振荡时间对萃取的影响萃取条件:有机相为30 %P204+70 %磺化煤油,皂化率为70 %,水相为实验料液,pH=2.42,相比VO/VA=1/1,VO=25 mL,温度为26 ℃.实验结果如图 4所示.
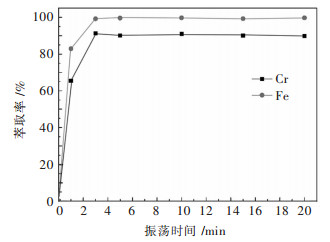 |
| 图 4 振荡时间对铬铁萃取率的影响 Fig. 4 Effect of contact time on extraction rate of chromium and iron |
从图 4可以看出,在3 min后铬的萃取率已经达到了最大值并保持稳定.这表明萃取反应十分迅速,在振荡3 min后反应已经达到了平衡.为了保证在实际操作中稳定效果,实验选择萃取时间为5 min.
2.1.5 温度对萃取的影响实验研究在15 ℃、20 ℃、25 ℃、30 ℃、40 ℃下P204共萃铬铁的影响,萃取条件:有机相为30 %P204+70 %磺化煤油,皂化率为70 %,水相为实验料液,pH=2.42,相比VO/VA=1/1,VO=25 mL,振荡时间为5 min.实验结果如图 5所示.
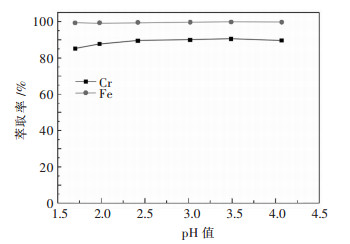 |
| 图 5 温度对铬铁萃取率的影响 Fig. 5 Effect of temperature on extraction rate of chromium and iron |
从图 5可以看出,随着萃取温度从15 ℃增加到40 ℃,有机相对铬的萃取率从88.1 %升高到90.2 %,对铁的萃取率无明显影响.这说明P204萃取铬的萃取反应为吸热反应,但随着温度的增加,萃取率变化较小.提高萃取温度会加大有机相的挥发损失,同时也会增加工业成本,因温度的变化对铬萃取率影响较小,故选择室温下进行萃取操作即可.
2.1.6 相比对萃取的影响萃取条件:有机相为30 %P204+70 %磺化煤油,皂化率为70 %,温度为26 ℃,水相为实验料液,pH=2.42,振荡时间5 min,选择相比VO/VA分别为1/10、1/5、1/2、1/1、2/1、3/1和5/1.实验结果如图 6所示.
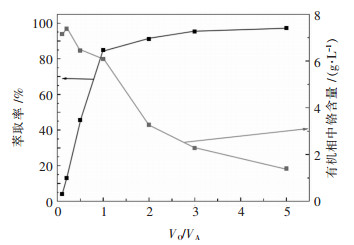 |
| 图 6 相比对铬铁萃取率的影响 Fig. 6 Effect of VO/VA ratio on extraction rate of chromium and iron |
由图 6可以看出,随着相比由1/10增加到5/1,铬萃取率从4.1 %迅速增加到97.2 %,在相比大于1/1后铬的萃取率逐渐趋于稳定,但是有机相铬负载量随着相比的增加急剧减小.在实际生产中,在考虑单级萃取效果的同时,还应该尽可能提高萃取剂的利用率及铬的富集浓度.综合考虑下,选择萃取相比1/1为后期串级实验的操作相比.
2.1.7 萃取等温线与理论萃取级数的确定实验通过连续接触法测定了25 ℃时铬的萃取等温线,如图 7所示.萃取条件:有机相为30 %P204+70 %磺化煤油,皂化率为70 %,水相为实验料液,其中铬浓度7.15 g/L,铁浓度0.465 g/L,pH=2.42,相比VO/VA=1/1,VO=25 mL,温度为25 ℃,振荡时间5 min.从图 7中可以发现有机相负载铬饱和容量为8.4 g/L.同时依照逆流萃取原理,绘制铬萃取的McCabe-Thiele图,按照相比VO/VA=1/1绘制铬的萃取操作曲线.从图 7可以发现,经过5级逆流萃取,理论上水相中铬浓度可以降低至1 mg/L左右.
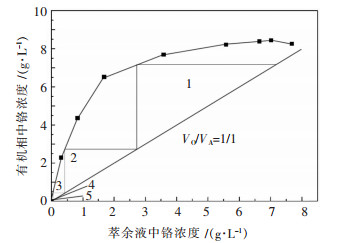 |
| 图 7 P204萃取铬的萃取等温线和操作性 Fig. 7 Chromium extraction distribution isotherm at 25 ℃ and its McCabe–Thiele diagram |
2.1.8 铬铁共萃串级试验
实验选择6级逆流,采用分液漏斗模拟逆流萃取,操作方式采用两头同时出料的“矩阵”式模拟法.萃取条件为有机相为30 %P204+70 %磺化煤油,皂化率为70 %,水相为实验料液,其中铬浓度7.16 g/L,铁浓度0.469 g/L,pH=2.42,相比VO/VA=1/1,VO=20 mL,温度为28 ℃,振荡时间5 min.萃取结果如表 1所示.
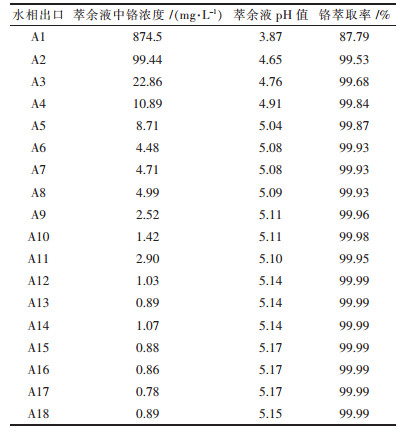
| 表1 6级逆流萃取铬结果 Table 1 Six-stage countercurrent extraction of chromium |
 |
| 点击放大 |
从表 1可以看出,6级逆流萃取达到平衡之后,出口水相铬浓度为0.9 mg/L左右,铬萃取率为99.99 %.萃余液中铁浓度为0.8 mg/L左右,实现了铬铁共萃.根据1998年1月1日实施的中国人民共和国国家标准污水综合排放标准中第1类污染物最高允许排放浓度规定,总铬为1.5 mg/L,Cr(Ⅵ)为0.5 mg/L[19],出口水相Cr(Ⅲ)浓度满足国家污水污染物排放限值对铬的最高允许排放浓度规定.
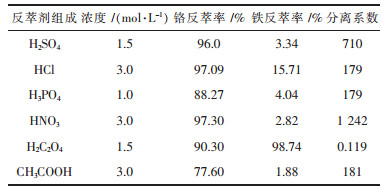
2.2 反萃结果与讨论 2.2.1 选择性反萃铬的研究1)反萃剂的选择.反萃是将负载有机相中的金属离子重新转移到反萃液中的过程,在该过程中可以实现对金属的分离、转型和富集的作用.为了将负载有机相中的铬离子反萃下来,实验研究了硫酸、盐酸、硝酸、磷酸、草酸和醋酸作为反萃剂时对负载有机相P204中金属离子的反萃效果,相比VO/VA=1/1,有机相为所有萃取实验收集汇总的负载有机相,负载有机相组成为30 %P204-70 %磺化煤油,含铬7.309 g/L,含铁438.9 mg/L.反萃结果如表 2所示.
| 表2 不同反萃剂对有机相中金属离子的反萃效果 Table 2 Effect of different stripping agents on stripping of metal ions from organic phase |
 |
| 点击放大 |
从表 2可以看出,硫酸、盐酸、磷酸、硝酸、醋酸优先反萃铬,铁的反萃率很低,这是由于萃取进入P204的Fe2+由于与含磷酸类萃取剂能形成配位效应,结合能力强,低浓度的无机酸很难反萃下来,从而可以实现铬铁分离.其中硫酸、盐酸、硝酸对铬的反萃效果较好,硝酸为反萃剂时,分离系数最大,硫酸次之,盐酸较小.结合铬反萃率、分离系数和经济成本综合考虑,选择硫酸作为反萃剂.
2)反萃剂浓度的影响.实验条件:有机相采用萃取实验收集的有机相;水相:不同浓度的硫酸溶液;反萃条件:相比VO/VA=1/1,温度28 ℃,振荡时间10 min.改变反萃剂硫酸溶液浓度,实验结果如图 8所示.
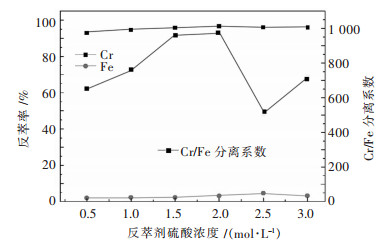 |
| 图 8 反萃剂硫酸浓度对反萃铬铁的影响 Fig. 8 Effect of sulfuric acid concentration on stripping chromium and iron |
从图 8可以看出,在硫酸浓度为0.5 mol/L时,铬的反萃率为92.93 %,随着硫酸浓度增加至2 mol/L,铬的反萃率增加到96.65 %,铁的反萃率为3.09 %分离系数达到最大值.然后继续增加硫酸浓度,铬的反萃率基本不变,铁的反萃率会上升.因此,反萃剂硫酸浓度选择为2 mol/L.
3)振荡时间对反萃的影响.实验条件:有机相采用萃取实验收集的有机相;水相:2 mol/L硫酸溶液;反萃条件:相比VO/VA=1/1,温度为28 ℃.改变振荡时间,实验结果如图 9所示.
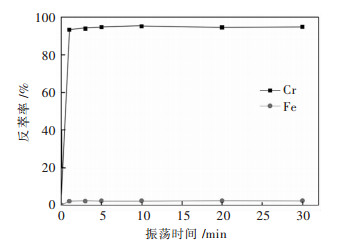 |
| 图 9 振荡时间对反萃铬铁的影响 Fig. 9 Effect of contact time on stripping chromium and iron |
从图 9可以看出,在1 min后铬的反萃率达到了最大并保持稳定.这表明反萃反应十分迅速,在振荡1 min后机达到了平衡.为了保证在实际操作中稳定效果,实验选择反萃振荡时间为5 min.
4)相比对反萃铬的影响.实验条件:有机相采用萃取实验收集的有机相;水相:2 mol/L硫酸溶液;反萃条件:温度32 ℃,振荡时间5 min.改变相比,实验结果如图 10所示.
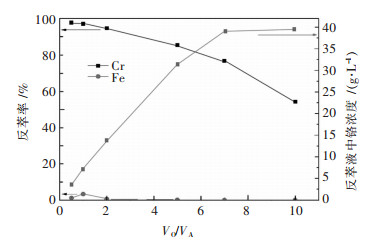 |
| 图 10 相比对反萃铬的影响 Fig. 10 Effect of VO/VA ratio on stripping chromium |
由图 10可以看出,随着相比的增加,反萃液铬浓度提高,铬反萃率下降.在实际生产中,在考虑单级反萃效果的同时,还应该尽可能提高反萃剂的利用率、分离系数及铬的富集浓度.在VO/VA=5/1时,铬反萃率为85.37 %,有着较高的反萃率,铁的反萃率只有0.12 %,同时达到了铬的富集及铬铁的分离的目的.
5)反萃等温线与理论反萃级数的确定.实验通过改变相比法测定了负载铬有机相在32 ℃时铬的反萃等温曲线,如图 11所示.按照相比VO/VA=1/5的操作线绘制了含7.31 g/L铬的反萃McCabe-Thiele图.经过3级逆流反萃,负载有机相中的铬可以降低至0.1 g/L左右,反萃液中的铬含量可达到35 g/L左右.
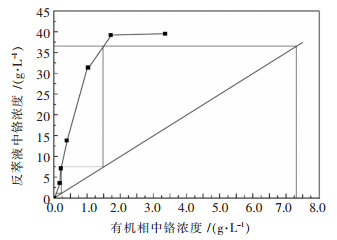 |
| 图 11 32 ℃下铬反萃等温线和操作线 Fig. 11 Chromium stripping distribution isotherm at 32 ℃ and its McCabe-Thiele diagram |
6)模拟逆流反萃实验.反萃级数选择3级逆流反萃,采用分液漏斗模拟逆流反萃.有机相采用萃取实验收集的有机相;水相:2 mol/L硫酸溶液;反萃条件:相比VO/VA=5/1,温度为32 ℃,振荡时间5 min.
在模拟逆流反萃试验中,第1排出口体系分相良好,但第2排、第3排出口体系产生乳化现象,分相缓慢.经分析,此时这两排反萃剂连续接触2次新鲜有机相,反萃液铬浓度过高,产生乳化现象,影响分相.为了解决分相问题,前三排反萃剂硫酸浓度改为3.5 mol/L,到第4排时硫酸浓度改为2 mol/L.最终稳定后,反萃液中铬浓度在29.5 g/L,铁浓度为10 mg/L,有机相铬残留为0.2 g/L,铬反萃率为97.5 %,并且连续操作正常,分相良好,相界面清晰,水相澄清,无结晶析出.
2.2.2 负载有机相中铁的反萃实验条件:有机相为负载有机相经硫酸反萃铬后的有机相,组成为30 %P204+70 %磺化煤油,负载有机相中铬0.2 g/L,含铁544.8 mg/L,温度为34 ℃,振荡时间10 min,相比VO/VA=1/1.
萃取进入P204的Fe2+由于与含磷酸类萃取剂能形成配位效应,结合能力强,低浓度的无机酸很难反萃下来.由表 3可以看出,低浓度的硫酸和盐酸对于负载有机相P204中Fe2+反萃率很低,加入H2O2对铁反萃率的提高不明显.高浓度的盐酸、草酸及氢氧化钠对铁的反萃效果很好.用高浓度的盐酸反萃时,反萃充分振荡时Fe2+易氧化为Fe3+,Fe3+在高浓度盐酸溶液中与Cl-合生成络合阴离子FeCl4-从而被反萃下来,所以相较于其它无机酸,盐酸对于Fe2+反萃效果最好,但是,由于负载有机相P204中含铁544.8 mg/L,浓度较低,高浓度盐酸利用率很低,反萃液中酸浓度很高,草酸价格相对较贵.由图 12可以看出,采用氢氧化钠作为反萃剂时,两相混合振荡完后静置20 min后,有棕色沉淀产生,这是因为反萃振荡时有机相和空气中氧充分接触,Fe(OH)2易氧化为Fe(OH)3沉于水相底部,但分相良好,相界面清晰.铁反萃率达到98.94 %,相较于草酸,氢氧化钠廉价易得,同时达到萃取剂P204皂化的目的,所以采用氢氧化钠作为反萃铁的萃取剂.反萃后,P204皂化率为100 %,由于本实验选取的P204皂化率为70 %,所以采用2 mol/L硫酸溶液进行再生.计算出萃取剂相应的皂化率所需的硫酸用量,使得P204的皂化率为70 %,从而进行循环利用.
 |
| 图 12 氢氧化钠反萃负载有机相中铁静置20 min后分相情况 Fig. 12 Separation phase of iron in organic phase by sodium hydroxide stripping after 20 min |
| 表3 反萃剂对有机相中Fe2+的反萃效果 Table 3 Effect of different stripping agents on stripping of iron from organic phase |
 |
| 点击放大 |
3 结论
1)萃取剂P204经皂化后在低酸度硫酸体系中对Cr(Ⅲ)有很好的萃取性能.
2)在硫酸体系中,水相为实验料液,其中铬浓度7.15 g/L,铁浓度0.465 g/L,pH=2.42,萃取有机相组成为30 %P204+70 %磺化煤油,皂化率为70 %,相比VO/VA=1/1,萃取温度为28 ℃,振荡时间5 min.经6级逆流,出口水相铬浓度为0.9 mg/L左右,铬萃取率为99.99 %.
3)分步选择性进行反萃,采用2 mol/L硫酸优先反萃铬,相比VO/VA=5/1,温度为32 ℃,振荡时间5 min.经过3级逆流反萃,反萃液中铬浓度在29.5 g/L,铁浓度为10 mg/L,达到铬、铁分离,同时反萃液中的铬得到富集.
4)采用氢氧化钠溶液反萃铁,有沉淀生成,分相良好,相界面清晰,反萃率达到98.94 %.
| [1] | 陈可, 石太宏, 王卓超, 等. 电镀污泥中铬的回收及其资源化研究进展[J]. 电镀与涂饰, 2006, 26(5): 43–46. |
| [2] | 季文佳, 黄启飞, 王琪, 等. 电镀污泥资源化与处置方法的研究[J]. 电镀与环保, 2010(1): 42–45. |
| [3] |
WU H X, LU C, KANG K, et al. Electroplating sludge metal recovery technology resources research[J].
Applied Mechanics and Materials, 2014, 443: 684–688. |
| [4] | 何炎庆, 张广柱. 从电镀污泥中回收有价金属的工艺探究[J]. 再生资源与循环经济, 2010, 3(8): 39–42. |
| [5] | 黄卫东, 张焕然. 电镀污泥资源化利用技术及处置工艺现状[J]. 世界有色金属, 2016(2): 32–36. |
| [6] |
JI W J, HUANG Q F, WANG Q, et al. A study of methods for resourcization and disposal of electroplating sludge[J].
Electroplating & Pollution Control, 2010, 30(1): 42–45. |
| [7] | 郭峰. 混合电镀污泥中铬资源化工艺研究[D]. 赣州: 江西理工大学, 2014. |
| [8] | 邬建辉, 阳伦庄, 湛菁, 等. 铬铁合金中的铬、铁分离研究[J]. 湿法冶金, 2011, 30(1): 51–55. |
| [9] | 袁文辉, 王成彦, 徐志峰, 等. 含铬电镀污泥资源化利用技术研究进展[J]. 湿法冶金, 2013, 32(5): 284–287. |
| [10] |
CHEN L, LIU F Q, LI D B. Ultrasound-assisted cloud point extraction for speciation and indirectspectrophotometric determination of chromium(Ⅲ) and (Ⅵ) in water samples[J].
Spectrochimica Acta Part A, 2012, 92: 189–193. DOI: 10.1016/j.saa.2012.02.073. |
| [11] | 郑顺, 李金辉, 李洋洋, 等. 电镀污泥氯化焙烧—弱酸浸出工艺研究[J]. 矿冶工程, 2014, 34(6): 105–109. |
| [12] | 张焕然, 王俊娥. 电镀污泥资源化利用及处置技术进展[J]. 矿产保护与利用, 2016, 3: 73–78. |
| [13] | 李雪飞. 电镀污泥中铬的分离工艺研究[D]. 武汉: 华中科技大学, 2006. |
| [14] | 孙永会, 马宏瑞, 李冬雪. 制革污泥中铁和铬的连续萃取分离工艺研究[J]. 中国皮革, 2008, 37(7): 50–53. |
| [15] | 杨钟林, 杭科文. P204萃取剂的皂化技术[J]. 上海金属, 1984, 5(1): 9–13. |
| [16] | 张启修, 张贵清, 唐瑞仁, 等. 萃取冶金原理与实践[M]. 长沙: 中南大学出版社, 2014. |
| [17] | 马恩新, 严小敏, 袁承业, 等. 硫酸体系中钒、钛、铬、铁的萃取分离[J]. 稀有金属, 1985(4): 11–14. |
| [18] | 朱屯. 萃取与离子交换[M]. 北京: 冶金工业出版社, 2005. |
| [19] | GB 8978-1996, 中华人民共和国国家标准污水综合排放标准[S]. |
 2017, Vol. 8
2017, Vol. 8


