| 微区电化学扫描技术应用现状 |
随着科学的进步, 电分析化学技术以其较高的灵敏度、优越的选择性、较短的分析时间和简易的操作被认为是现代分析检测的一种重要手段.传统的电化学测试中常常使用恒电位仪测量通过整个电极/电解液界面的平均电流值, 测量过程中很少有样品是完全均质的, 样品通常包含有局部区域的钝化等.在1980-1989年期间Allen Bard教授提出扫描电化学显微镜(Scanning Electrochemistry Microscope,SECM)的技术观点并将其进行系统深入研究[1-2]后, SECM被广泛应用于电化学的各个领域.SECM技术是一种现场空间高分辨的新的电化学方法.SECM集成了定位系统、双恒电位仪及超微电极探针, 其最大特点是可以在溶液体系中对研究标样进行实时、现场和三维空间观测[3]. 2014年美国普林斯顿公司成功研制上市微区扫描电化学工作站Versascan, 它其中所包含的SECM是一个建立在电化学扫描探针的设计基础上进行的超高测量分辨率及空间分辨率的非接触式微区形貌及电化学微区测试系统;该系统的推广使SECM技术更好地应用于生物传感器、反应动力学、多孔薄膜研究、染料电池催化剂和腐蚀机理的研究中.
1 SECM工作原理SECM工作原理如图 1所示, 工作过程中将探针(目前常用探针尺寸为25 μm或50 μm)、参比电极和对电极放置于类似于铁氰化钾的电解质溶液中, 当给探针施加一定的电压后, 电解液中发生氧化还原反应:
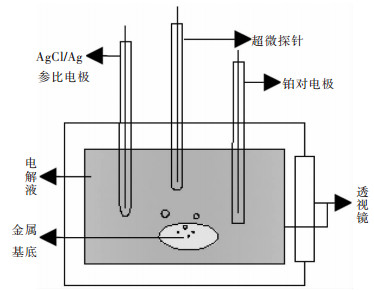 |
| 图 1 SECM电解池 Fig. 1 Electrolytic cell of SECM |
阳极反应:Fe(CN)64--e-→Fe(CN)63-
阴极反应:2H2O→O2+4H++4e-
并产生电流, 且探针电流iT∞=4nFcDa(其中n为转移电子数, F为法拉常数, c为离子浓度,a为探针的直径, D为扩散系数).当探针与基底距离较远时, 探针电流iT=iT∞.而当探针与基底绝缘部分逐渐接近时, 由于氧化性物质在扩散过程中受到阻力, 发生负反馈现象, 此时iT < iT∞.反之, 当探针逼近导体时有部分的还原性物质扩散到基底表面被氧化成氧化性物质, 发生正反馈现象使iT>iT∞.
2 SECM技术应用现状自从Allen Bard教授对SECM技术进行深入的研究后, 几十年的发展使SECM技术的应用渗入到电化学的多个领域. SECM技术较扫描参比电极技术(Scanning Reference Electrode Technique, SRET)等电化学方法具有较高的空间分辨率和多种应用模式[4]被广泛应用.在生物方面SECM技术可用于类似于光合作用过程、酶稳定性和生物大分子的电化学反应特性等复杂生化过程[5-6].同时SECM独特的反馈模式、产生收集模式和氧化还原竞争模式被应用于电源技术领域[7].除此之外在腐蚀领域,SECM能够提供独特的局部区域图像功能.SECM利用探针技术可分辨电极表面微区的电化学不均匀性, 反映导体和绝缘体表面的形貌, 测定溶液中的动力学行为[8-12].
2.1 SECM在生物分析中的应用研究进展生命科学是一项以研究生物体生命规律、发育规律以及和环境之间关系的科学.对生命科学的成功研究可以推动人类生命的发展与进步.因此近年来多种电化学测试手段被用于研究生命体征.而早期发展起来的扫描隧道显微镜技术、原子力显微镜和激光力学显微镜技术等虽分辨率都可达纳米级别, 并且可对生物体进行三维成像, 但是它们均不能提供物质的电化学相关信息.
1991年Bard结合前任已有的技术使用超微电极首次提出SECM技术并将这项技术付诸实践[13].SECM特殊的成像技术以其优越的分辨率在测量过程中可提供关于样品的电化学信息, 但不会污染样品.基于SECM特殊的性能, 从而使SECM的反馈收集模式被广泛应用于代谢产物的活动分析.
SECM最早被应用于植物叶片的形貌分析.LEE等[14]通过SECM技术的反馈模式对光合作用中的叶片进行形貌分析.实验中将叶片浸泡在20 mmol/L K4Fe(CN)6和0.1 mol/L的KCl溶液中, 使用半径为1 μm的铂电极和半径5.5 μm的碳微盘电极.当给探针施加一定电压时, 在探针尖端会发生Fe(CN)64- -e→Fe(CN)63-的反应从而产生电流.测量叶片的不同区域的电流(current)-距离(distance)关系图, 结果不同.当探针靠近某些区域时二者成正比关系, 而靠近某些区域时则成反比关系.研究表明在进行光合作用的叶片上, 每个叶孔附近均有一个自我保护细胞, 对于开放的气孔这些细胞往往比较膨胀, 闭合气孔中这些细胞又往往会下凹.SECM探针对这些细胞形成反馈作用.在靠近膨胀的细胞时探针电流会急剧减小, 反之靠近下凹的细胞时电流又会增加.通过SECM的这种特有的工作模式可以判断植物光合作用时的叶片形貌.
SECM还可用于细胞活动检测与成像.LI等[15]采用SECM技术对培养基中的HeLa细胞活性进行研究.以二茂铁甲醇的氧化和溶解氧还原电流对癌细胞进行成像.由于HeLa细胞对不同离子反馈情况存在差异性, 在反应中二茂甲铁醇离子在探针尖端被氧化时活的HeLa细胞对二茂铁甲铁醇的氧化电流表现出正反馈作用.而暴露在毒性环境下的HeLa细胞对在二茂铁甲铁醇的氧化电流却表现出负反馈作用.作者推断反应过程中细胞参与二茂铁甲醇的氧化还原反应, 从而推进SECM在检测培养基中细胞活性中的作用.MICHELLE MENG-Ni ZHANG[16-18]则使用SECM技术对单个膀胱癌细胞进行分析检测, 癌细胞在生长分解过程中会释放出ROS作为氧化还原媒介, 利用SECM的产生收集模式可以对这种信号进行收集.由此对人体膀胱癌细胞T24在不同时间段的形貌特征、细胞膜的渗透性与抗癌药物之间的演变关系进行检测分析, 从而得到关于细胞的生理和药理信息. LI M等[19-21]也使用SECM技术对T24细胞的形貌特征和渗透性等进行了一系列的研究.而SRIDHAR A[22]、ABE H[23]和UMMADI J G[24]则使用SECM对单体活细胞做类似的研究.
此外SECM广泛应用于分子成像.BARD等[17, 25]在对DNA等大分子成像时使用信号灵敏度小于0.05 pA的SECM/STM组合技术.纳米级探针被置于潮湿的空气中并形成超薄液膜, 形成的液膜进行成像分析得到首例SECM的分子图像.此外BARD[26]小组还使用SECM仪研究不同电子介体在DNA修饰电极上的转移过程, 介体带电类别对DNA分子影响存在差异.实验中将葡萄糖、氧化酶、匙孔血蓝蛋白、DNA和小白鼠单克隆抗原等大分子固定在云母片上, 使用超微探针进行分析检测时荷负电电子介体如Fe(CN)63-、Fe(CN)64-、Fe(EDTA)-等与DNA骨架上的磷酸根相互排斥, 阻碍荷负电电子介体在DNA修饰的金电极上的电子传递, 而带正电的电子及中性电子则不受影响.PALCHETTI等[17]将HS-ODN固定于金基底电极表面, 通过HS-ODN与目标寡核苷酸杂交后, 再与生物素标记的信号探针进行杂交, 并且加入亲和素标记的碱性磷酸酯酶, 反应后期磷酸酯酶催化硝基兰四唑混合物并生成沉积在基底表面上的沉淀物, 使金基底传导性能改变.采用SECM对这种变化目标进行成像检测分析, 测定实际产物, 从而检测到PCR扩增物.
SECM技术虽然已广泛应用于生物科学领域, 但随着生物分子、生物细胞以及基因工程等检测要求的提高, 现有的SECM终将无法满足需求, SECM与生物体的长期接触不免会影响试样的内部结构, Z轴与样品的距离在测量过程中要求严格, 因此SECM必须从提高类似于分辨率等测量手段入手, 改进设备以满足生物检测科学的需求.
2.2 SECM在电源方面的应用随着能源需求的加速增长, 化石燃料日渐枯竭, 面对严重的环境问题以燃料电池、太阳能电池和锂离子电池等为代表的新能源技术被广泛应用.各类电池反应过程中所涉及的电化学过程比较复杂.而SECM特殊的工作模式可对其进行表征.因此SECM被应用于各类电池的界面化学反应研究.
燃料电池是一种将化学能转变为电能的特殊装置.在工作过程中以氧还原(ORR)反应为主, 电池的正极反应直接影响着电池的效应.研究正负极反应可优化电池的性能.SANCHEZ-SNCHEZ等[27]使用SECM中的产生收集模式(TG/TC)对Pt纳米颗粒表面的氧化还原过程进行研究, 采用SECM特殊的成像系统对球形、立方、六角和四面体/八面体形的Pt纳米颗粒的催化活性进行比较.结果表明六角形颗粒在酸性电解质中活性较高, 而立方和四面体/八面体颗粒的活性却随溶液中阴离子的吸附程度的差异发生变化.通过计算ORR过程中的转移电子数可以来研究产生收集模式的机制[27].作者还采用这种方法来计算在ORR过程中过氧化氢酸性溶液中Hg在电极上的量, 推测电极反应.SDNCHEZ-SANCHEZ和Bardtn[28-29]还采用SECM的TG/TC模式研究在使用不同金属和双金属作为催化剂时H2O2的产生量.而在样品上施加不同电压时, 可以计算出每产生一个氧分子所需转移的电子数.SECM技术中的离子跃迁模式则被用于研究不同基底的电催化过程.
太阳能电池作为一种光电转换装置, 在光化学反应过程中光催化剂的活性也可通过SECM进行区分.LEE等[30-31]应用SECM技术迅速筛选光催化剂.实验过程中将一个400 μm的光纤连接一个150 W氙灯后与SECM相连, 将纤维通过一个9 091五轴纤维模型耦合到Xe灯, 以1 mol/L KOH或0.1 mol/L的Na2SO4的溶液作电解质.实验进行中光纤被z轴定位于垂直于工作电极表面, 采用500 μm/s或300 μm/s的扫描速度快速扫描xe灯照射下光催化剂阵上的光点.结果显示:光催化剂点使用的是不同组分但尺寸大小相近的阵列, 其结果可以在掺氟的氧化锡(Fro)基底上沉积获得, 以此来评估各个点的光催化性能.通过比较发现使用的Fe-Eu、Fe-Rb和Fe-Pd等氧化物与纯α氧化铁相比, 它们的光催化活性更具有优势.类似于BiVO3的更强的光电流会在三元氧化物中产生, 并在光纤周围则会形成一个收集电化学产物的光环.LIU和BARD[23]用这种方法研究沉积在FTO上的CulnSe2和CulnMSe2(M为Ga、Zn和Cd)点阵列, 结果显示产生最高催化活性的组分取决于退火温度.
锂离子电池是一种二次电池(充电电池), 是现代高性能电池的代表.它在充电过程中, 从LiMCO2(M=Co, Mn, Ni)中电离出Li+, 电池质量的性能直接由分布在电极表面的固态电解质决定, 而SECM可帮助分析界面的电化学反应.F XU等[32]采用SECM的产生收集模式研究LiCOO2电极充电过程中在界面上的Li+的析出过程.在实验过程中他们使用Li作为参比电极, 铂丝作为对电极, 半径3.22 mm LiCoO2电极作为工作电极, 实验结果表明在接近基底处, 超分子Li+(EC)m浓度增加的原因是因为电解液内部的非均匀分布, 这导致电流在不同电压下峰值不同, 而且通过SECM特殊的成像系统可以反映出这种电解液的不均匀特性.
虽然SECM已被成功应用于各类电池的界面化学反应研究, 但在使用过程中关于探针到基底距离的测定技术目前还不够成熟.精确的距离控制可以较好地反映各类电化学信息, 这将是今后发展的一个重要方向.除此之外, 如果SECM可以和其他技术结合可以进行更广范围的测试, 如通过SECM表征流体强度的变化来测试锂离子电池石墨阳极的膨胀行为等.
2.3 SECM在研究腐蚀机理中的应用腐蚀是金属材料失效的重要原因之一, 但由于金属材料总是在一定的介质中使用且金属腐蚀在热力学上又是一种自发过程[33], 因此金属腐蚀的研究对于腐蚀科学尤为重要.常见的腐蚀分为全面腐蚀和局部腐蚀, 局部腐蚀中较为常见是点蚀的发生.点蚀过程中往往伴随着一系列电化学行为, SECM独特的成像功能可以对点蚀过程的电荷转移和局部图像进行清晰表述, 为进一步分析点蚀发生条件、影响因素及转变过程提供依据.因此常被用于不锈钢腐蚀研究、Mg-Al合金界面腐蚀形貌分析和涂层失效鉴定等方面.
RNODE S.等[34]采用SECM研究不锈钢腐蚀过程中的影响因素.通过改变实验条件如调整探针扫描速率、Cl-的溶解速率和参比电极的电位(将参比电极电位控制在10 mV、0 mV、300 mV、360 mV)进行对比实验, 反应过程中由于Fe2+发生氧化反应导致溶液中的电流增大, 这种微电流被探针反映出来.而从SECM的图像显示器中可观测到溶液中离子越集中, 基质溶解越快, 电流变化曲线越明显, 从而判断不锈钢表面发生点蚀.
NIU等[35]模拟海洋气氛使用SECM研究304型不锈钢的微区腐蚀行为.采用感光耦合原件(chare-coupled device CCD)确定探针与基底的距离, 通过测定循环伏安曲线得到氧化峰电位.实验结果表明点蚀受浸泡时间、极化电流和电位的影响.在使用SECM技术的产生收集模式时也成功验证点蚀发生的位置、形成的轮廓以及不同时间段的点蚀的图像变化. IZQUIERDO J[36]使用SECM研究304钢在阳极极化下的腐蚀行为. MARTINS C M B[37]则使用SECM研究304自来水管的腐蚀行为.
ZHU和WILLIAMS[38]还使用SECM观测不锈钢中电极被高压极化时硫化物中点蚀坑的演变, 结果表明电化学活动在含有夹杂物的区域是频繁发生的.CASILLAS等[39-41]使用SECM检测钛的腐蚀, SIMOES等[42]使用SECM在镁电偶中电气连接或分离过程中观察外露金属表面状况.
DONG[43]利用SECM成像技术分析不锈钢合金AISI2205在0.1 mol/L NaCl溶液下的腐蚀电位.将基底电流设置为5 pA时, 扫描过程中随着浸泡时间的增加体系电流增大到70 pA, 表明体系发生腐蚀.对应电流下的电位即为金属的腐蚀电位.而GONZALEZS组[44-46]使用SECM研究有机涂层在氯离子存在条件下控制氧含量不同时有机涂层的失效行为, 结果表明较粗糙的样品在含有氯离子的电解质溶液中使用寿命要比正常情况下少1 h, 并推断出离子迁移是在涂层浸出电解质溶液时就开始发生.
ZHOU等[47]应用SECM研究1016铝合金和2A12铝合金在10 mmol/L Na2SO4和5 mmol/L KI溶液中的点蚀行为. 2A12铝合金作为一种硬质铝合金, 延展性较差.实验过程中电位降低, 2种铝合金的腐蚀区域均增大, 且2A12铝合金的腐蚀电位比1016铝合金更低.而引起这种结果的原因是某些金属化合物颗粒中的边界区域优先溶解, 金属不同溶解能力也不同. 2A12铝合金因为自身性质,溶解电位低于1060铝合金.但在研究过程中作者并没有体现出探针是如何工作的.
Mg是一种活泼金属,在空气中易生成不致密的钝化氧化膜.该合金的腐蚀行为在溶液中容易进行.浙江大学曹发和[48]的课题组应用SECM的产生收集模式和反馈模式对Mg合金的腐蚀行为进行系统研究.他们使用SECM的收集模式研究在NaCl和Na2SO4溶液中Mg合金腐蚀过程中的点线面析氢行为和活化点的转变过程.实验过程中首先在0.1 mol/L NaCl和0.1 mol/L Na2SO4溶液中施加-0.2 V、-0.1 V、0.1 V、0.3 V的极化电位考察合金的析氢行为, 结果表明无论在这两种的任一种溶液中阴极极化和阳极极化均促进析氢行为, 但析氢行为在点线面中均波动不大.析氢行为随着NaCl浓度增大而增加, 随着Na2SO4溶液浓度减小而增大.随后在0.1 mol/L NaCl和0.5 mol/L NaCl溶液中浸泡合金24 h, 观察活性点随时间的变化, 并施加极化电位对其极化, 结果表明阳极极化对活性点的产生有促进作用.除此之外他们还研究了AM60镁合金在1.0 mmol/L FeMeOH+0.1 mol/L NaCl溶液中的SECM成像[4], 实验过程中将浸泡0.5 h和1.5 h的试样进行对比实验, 扫描面积设定200 μm×200 μm, 探针电位为0.5 V.实验结果表明反应初期镁合金表面膜破裂, 随着反应时间的增加生成的腐蚀产物对镁合金的保护增强, 抑制了合金的进一步腐蚀, 且Cl-的浓度会影响合金表面的腐蚀产物. JAMALI S S[49]使用SECM研究缓冲剂中的AZ31镁合金的局部腐蚀行为,实验中配置由NaCl和Na2CO3组成的缓冲液,并准备NaOH作为pH调节剂,设定扫描面积为200 μm×200 μm,进行正负反馈扫描、面扫和pH-E图,在扫描过程中可观察到产生H2的区域大多为绝缘区域或pH较高的溶液,以此来研究镁合金的活化与钝化行为.
除了在金属腐蚀方面的应用, SECM在涂层失效方面也有一定的应用. GONZALEZ-GARCIA[50-52]应用SECM成像技术研究关于有机涂层的界面电化学行为, 以溶解氧气作为还原性物质, 使用SECM的反馈模式研究不同离子的表面腐蚀形貌特征.结果表明Cl-会引起涂层的早期失效, 探针到基底的距离也会影响反应的进行.DOBRZENIECKA A等[53-55]则使用SECM技术对多壁碳纳米管和纳米管/COP在电解质溶液中的氧化还原动力学行为进行表征.
腐蚀科学作为一门应用科学, 交叉于多个领域, 且随着科技的进步, 对测量手段的要求极为严格.SECM虽已广泛应用于腐蚀研究, 但还需与其他技术结合, 从而以满足对金属表面处理与防腐蚀性能的研究需要.
3 SECM技术的前景展望SECM作为一种新的电化学技术, 可用于测量微区成像和动力学研究.与传统的电化学相比, SECM无论是从分辨率还是测量精度都更胜一筹, 特别是在金属腐蚀应用方面.但尚有一些技术有待加强:
1)在SECM的使用过程中, 探针的尺寸会影响到测量效果, 而目前使用的SECM设备中探针直径主要有10 μm、25 μm和50 μm 3个级别, 直径太大无法满足实验要求, 但如果尺寸过小探针又容易损坏, 对此SECM还需进行一些成像度的改进.
2)SECM的使用中较常用的是反馈模式和产生收集模式, 这两种模式均需要在反应溶液中添加氧化还原物质后, 将探针精确定位后才可测量.且探针在定位过程中精确定位很难实现.
3)在电化学过程中, 多数情况下会要求使用多种仪器进行测量, 例如在腐蚀动力学测量中已有的将SECM与电化学石英微晶天平相结合的技术, SECM和电导显微镜(SICM)的混合使用[56], 在未来的研究中这种结合将会更加多样化, 且被广泛应用于高性能化学电源材料、新型光电催化材料和纳米薄膜等功能材料的研究.
| [1] |
BARD A, FA NF, PIERCE D T, et al. Chemical imaging of surfaces with the scanning electrochemical microscope[J].
Science, 1991, 254(5028): 68–74. DOI: 10.1126/science.254.5028.68. |
| [2] |
BARD A J, FAN F R F, KWAK J, et al. Scanning electrochemical microscopy. Introduction and principles[J].
Analytical Chemistry, 1989, 61(2): 132–138. DOI: 10.1021/ac00177a011. |
| [3] | 王贵会. 喷射成形7055铝合金应力腐蚀与电化学腐蚀性能研究[D]. 镇江: 江苏科技大学, 2012. |
| [4] | 曹发和, 夏妍, 刘文娟, 等. SECM基本原理及其在金属腐蚀中的应用[D]. 杭州: 浙江大学, 2013. |
| [5] | 乔志刚. 扫描电化学显微镜技术理论及应用研究[D]. 兰州: 西北师范大学, 2011. |
| [6] | BARD A J, FAULKNER L R, LEDDY J, et al. Electrochemical methods: fundamentals and applications[M]. New York: Wiley, 1980. |
| [7] | 张赟, 吴晓梅, 曾小勤, 等. 扫描电化学显微镜在电源技术领域的应用[J]. 电源技术, 2015, 39(5): 1129–1131. |
| [8] |
LUO H, WEI D, DONG C, et al. Development of electrochemical studies in microzone of metallic corrosion (1) scanning electrochemical microscopy[J].
Corrosion & Protection, 2009(7): 27–32. |
| [9] |
WANG LW, LI X G, DU C W, et al. Recent advances in local electrochemical measurement techniques and application in corrosion research[J].
Journal of Chinese Society for Corrosion and protection, 2010, 30(6): 498–503. |
| [10] |
WITTSTOCK G, BURCHARD M, PUST S E, et al. Scanning electrochemical microscopy for direct imaging of reaction rates[J].
Angewandte Chemie International Edition, 2007, 46(10): 1584–1617. DOI: 10.1002/(ISSN)1521-3773. |
| [11] |
SUN P, LAFORGE F O, MIRKIN M V. Scanning electrochemical microscopy in the 21st century[J].
Physical Chemistry Chemical Physics, 2007, 9(7): 802–823. DOI: 10.1039/B612259K. |
| [12] | 马芬. 扫描电化学显微镜研究适体与凝血酶的相互作用[D]. 西安: 陕西师范大学, 2008. |
| [13] |
LIU H Y, FAN F R F, LIN C W, et al. Scanning electrochemical and tunneling ultramicroelectrode microscope for high-resolution examination of electrode surfaces in solution[J].
Journal of the American Chemical Society, 2002, 108(13): 3838–3839. |
| [14] |
LEE C, KWAK J, BARD A J. Application of scanning electrochemical microscopy to biological samples[J].
Proceedings of the National Academy of Sciences, 1990, 87(5): 1740–1743. DOI: 10.1073/pnas.87.5.1740. |
| [15] |
LI X, BARD A J. Scanning electrochemical microscopy of HeLa cells–Effects of ferrocene methanol and silver ion[J].
Journal of Electroanalytical Chemistry, 2009, 628(1): 35–42. |
| [16] | 张梦霓. 扫描电化学显微镜对人膀胱癌的单细胞分析[D]. 上海: 华东理工大学, 2012. |
| [17] | 李保华, 马燕, 黄蕾. 扫描电化学显微镜及其在生物分析中的应用研究进展[J]. 化学通报, 2013, 76(2): 124–131. |
| [18] |
ZHANG M N, LONG Y T, DING Z. Filming a live cell by scanning electrochemical microscopy: label-free imaging of the dynamic morphology in real time[J].
Chemistry Central Journal, 2012, 6(1): 1–6. |
| [19] |
HENDERSON J D, FILICE F P, LI M S, et al. Tracking live cell response to cadmium (Ⅱ) concentrations by scanning electrochemical microscopy[J].
Journal of Inorganic Biochemistry, 2015, 158: 92–98. |
| [20] |
LI M S M, FILICE F P, DING Z. Determining live cell topography by scanning electrochemical microscopy[J].
Journal of Electroanalytical Chemistry, 2016, 779: 176–186. DOI: 10.1016/j.jelechem.2016.02.042. |
| [21] |
FILICE F P, Li M S, HENDERSON J D, et al. Mapping Cd2+ -induced membrane permeability changes of single live cells by means of scanning electrochemical microscopy[J].
Analytica Chimica Acta, 2016, 908: 85–94. DOI: 10.1016/j.aca.2015.12.027. |
| [22] |
SRIDHAR A, DE BOER H L, VAN D B A, et al. Microstamped Petri dishes for scanning electrochemical microscopy analysis of arrays of microtissues[J].
Plos One, 2014, 9(4): 936–954. |
| [23] |
ABE H. A Non-invasive and sensitive method for measuring cellular respiration with a scanning electrochemical microscopy to evaluate embryo quality[J].
Journal of Mammalian Ova Research, 2016, 24: 70–78. |
| [24] |
UMMADI J G, JOSHI V S, GUPTA P R, et al. Single-cell migration as studied by scanning electrochemical microscopy[J].
Analytical Methods, 2015, 7(20): 8826–8831. DOI: 10.1039/C5AY01944C. |
| [25] |
FAN F R F, BARD A J. Imaging of biological macromolecules on mica in humid air by scanning electrochemical microscopy[J].
Proceedings of the National Academy of Sciences, 1999, 96(25): 14222–14227. DOI: 10.1073/pnas.96.25.14222. |
| [26] |
LIU B, BARD A J, LI C Z, et al. Scanning electrochemical microscopy. 51. Studies of self-assembled monolayers of DNA in the absence and presence of metal ions[J].
The Journal of Physical Chemistry B, 2005, 109(11): 5193–5198. DOI: 10.1021/jp045050v. |
| [27] |
SANCHEZ-SANCHEZ C M, SOLLA-GULLON J, VIDAL-IGLESIAS F J, et al. Imaging structure sensitive catalysis on different shape-controlled platinum nanoparticles[J].
Journal of the American Chemical Society, 2010, 132(16): 5622–5624. DOI: 10.1021/ja100922h. |
| [28] |
SDNCHEZSANCHEZ C M, JOAQUIN RODRIGUEZLOPEZ A, BARD A J. Scanning electrochemical microscopy. 60. Quantitative calibration of the SECM substrate generation/tip collection mode and its use for the study of the oxygen reduction mechanism[J].
Analytical Chemistry, 2008, 80(9): 3254–60. DOI: 10.1021/ac702453n. |
| [29] | 张赟. 镁空气电池电极材料及电解液的优化[D]. 上海: 上海交通大学, 2015. |
| [30] |
LEE J, YE H, PAN S, et al. Screening of photocatalysts by scanning electrochemical microscopy[J].
Analytical Chemistry, 2008, 80(19): 7445–7450. DOI: 10.1021/ac801142g. |
| [31] |
YE H, LEE J, JANG J S, et al. Rapid screening of BiVO4-based photocatalysts by scanning electrochemical microscopy (SECM) and studies of their photoelectrochemical properties[J].
The Journal of Physical Chemistry C, 2010, 114(31): 13322–13328. DOI: 10.1021/jp104343b. |
| [32] |
XU F, BEAK B, JUNG C. In situ electrochemical studies for Li+ ions dissociation from the LiCoO2 electrode by the substrate-generation/tip-collection mode in SECM[J].
Journal of Solid State Electrochemistry, 2012, 16(1): 305–311. DOI: 10.1007/s10008-011-1325-8. |
| [33] | 曹楚南. 金属腐蚀与防护机理的研究[J]. 中国科学基金, 1990(4): 216–219. |
| [34] |
RHODE S, KAIN V, RAJA V S, et al. Factors affecting corrosion behavior of inclusion containing stainless steels: A scanning electrochemical microscopic study[J].
Materials Characterization, 2013, 77: 109–115. DOI: 10.1016/j.matchar.2013.01.006. |
| [35] |
YIN Y, NIU L, LU M, et al. In situ characterization of localized corrosion of stainless steel by scanning electrochemical microscope[J].
Applied Surface Science, 2009, 255(22): 9193–9199. DOI: 10.1016/j.apsusc.2009.07.003. |
| [36] |
IZQUIERDO J, RODRIGUEZ-RAPOSO R, SANTANA J J, et al. Scanning microelectrochemical characterization of the effect of polarization on the localized corrosion of 304 stainless steel in chloride solution[J].
Journal of Electroanalytical Chemistry, 2014, 728(25): 148–157. |
| [37] |
MARTINS C M B, MOREIRA J L, MARTINS J I. Corrosion in water supply pipe stainless steel 304 and a supply line of helium in stainless steel 316[J].
Engineering Failure Analysis, 2014, 39(4): 65–71. |
| [38] |
ZHU Y, WILLIAMS D E. Scanning electrochemical microscopic observation of a precursor state to pitting corrosion of stainless steel[J].
Journal of the Electrochemical Society, 1997, 144(3): 43–45. DOI: 10.1149/1.1837487. |
| [39] |
CASILLAS N, CHARLEBOIS S J, SMYRL W H, et al. Scanning electrochemical microscopy of precursor sites for pitting corrosion on titanium[J].
Journal of the Electrochemical Society, 1993, 140(9): 142–145. DOI: 10.1149/1.2220897. |
| [40] |
CASILLAS N, CHARLEBOIS S J, SMYRL W H, et al. Pitting corrosion of titanium[J].
Journal of The Electrochemical Society, 1994, 141(3): 636–642. DOI: 10.1149/1.2054783. |
| [41] |
JAMES P, CASILLAS N, SMYRL W H. Simultaneous scanning electrochemical and photoelectrochemical microscopy by use of a metallized optical fiber[J].
Journal of the Electrochemical Society, 1996, 143(12): 3853–3865. DOI: 10.1149/1.1837308. |
| [42] |
SIMOES A M, BATTOCCHI D, TALLMAN D E, et al. SVET and SECM imaging of cathodic protection of aluminium by a Mg-rich coating[J].
Corrosion Science, 2007, 49(10): 3838–3849. DOI: 10.1016/j.corsci.2007.03.045. |
| [43] |
DONG C F, LUO H, XIAO K, et al. In situ characterization of pitting corrosion of stainless steel by a scanning electrochemical microscopy[J].
Journal of materials engineering and performance, 2012, 21(3): 406–410. DOI: 10.1007/s11665-011-9899-y. |
| [44] |
SOUTO R M, GONZALEZ-GARCIA Y, IZQUIERDO J, et al. Examination of organic coatings on metallic substrates by scanning electrochemical microscopy in feedback mode: revealing the early stages of coating breakdown in corrosive environments[J].
Corrosion Science, 2010, 52(3): 748–753. DOI: 10.1016/j.corsci.2009.10.035. |
| [45] |
GONZALEZ S, SANTANA J J, GONZALEZ-GARCIA Y, et al. Scanning electrochemical microscopy for the investigation of localized degradation processes in coated metals: Effect of oxygen[J].
Corrosion Science, 2011, 53(5): 1910–1915. DOI: 10.1016/j.corsci.2011.02.008. |
| [46] |
CARBONELL D J, GARCIA-CASAS A, IZQUIERDO J, et al. Scanning electrochemical microscopy characterization of sol-gel coatings applied on AA2024-T3 substrate for corrosion protection[J].
Corrosion Science, 2016(6). |
| [47] |
ZHOU H R, LI X G, DONG C F, et al. Corrosion behavior of aluminum alloys in Na2SO4 solution using the scanning electrochemical microscopy technique[J].
Journal of Mineral Metallurgy and materials, 2009, 16(1): 84–88. DOI: 10.1016/S1674-4799(09)60014-5. |
| [48] | 王新印, 夏妍, 周亚茹, 等. 基于扫描电化学显微镜产生/收集和反馈模式研究纯Mg腐蚀行为[J]. 金属学报, 2015, 51(5): 631–640. DOI: 10.11900/0412.1961.2014.00602. |
| [49] |
JAMALI S S, MOULTON S E, TALLMAN D E, et al. Applications of scanning electrochemical microscopy (SECM) for local characterization of AZ31 surface during corrosion in a buffered media[J].
Corrosion Science, 2014, 86(3): 93–100. |
| [50] |
GONZALEZ-GARCIA Y, SANTANA J J, GONZALEZ-GUZMAN J, et al. Scanning electrochemical microscopy for the investigation of localized degradation processes in coated metals[J].
Progress in Organic Coatings, 2010, 69(2): 110–117. DOI: 10.1016/j.porgcoat.2010.04.006. |
| [51] |
SOUTO R M, GONZALEZ-GARCIA Y, IZQUIERDO J, et al. Examination of organic coatings on metallic substrates by scanning electrochemical microscopy in feedback mode: revealing the early stages of coating breakdown in corrosive environments[J].
Corrosion Science, 2010, 52(3): 748–753. DOI: 10.1016/j.corsci.2009.10.035. |
| [52] |
SANTANA J J, GONZALEZ-GUZMAN J, IZQUIERDO J, et al. Sensing electrochemical activity in polymer-coated metals during the early stages of coating degradation by means of the scanning vibrating electrode technique[J].
Corrosion Science, 2010, 52(12): 3924–3931. DOI: 10.1016/j.corsci.2010.08.010. |
| [53] |
DOBRZENIECKA A, ZERADJANIN A R, MASA J, et al. Evaluation of kinetic constants on porous, non-noble catalyst layers for oxygen reduction—a comparative study between SECM and hydrodynamic methods[J].
Catalysis Today, 2016, 262: 74–81. DOI: 10.1016/j.cattod.2015.07.043. |
| [54] |
WEI C, BARD A J, MIRKIN M V. Scanning electrochemical microscopy. 31. application of SECM to the study of charge transfer processes at the liquid/liquid interface[J].
The Journal of Physical Chemistry, 1995, 99(43): 16033–16042. DOI: 10.1021/j100043a050. |
| [55] |
JAMALI S S, MOULTON S E, TALLMAN D E, et al. Evaluating the corrosion behaviour of magnesium alloy in simulated biological fluid by using SECM to detect hydrogen evolution[J].
Electrochimica Acta, 2015, 152: 294–301. DOI: 10.1016/j.electacta.2014.11.012. |
| [56] |
TAKAHASHI Y, SHEVCHUK A I, NOVAK P, et al. Simultaneous noncontact topography and electrochemical imaging by SECM/SICM featuring ion current feedback regulation[J].
Journal of the American Chemical Society, 2010, 132(29): 10118–10126. DOI: 10.1021/ja1029478. |
 2017, Vol. 8
2017, Vol. 8


