随着造船技术的发展, 对我国的船舶行业提出了更高的要求[1-2]. DH36船板钢是我国目前使用较为广泛的造船用钢, 在实际工业生产中常常采取控轧控冷、热处理等工艺来起到细化奥氏体晶粒, 控制夹杂物及纳米析出物的生成、大小和分布, 以提高钢材的机械性能.其中加入的微合金元素Nb、Ti为强碳氮化物形成元素, 会以碳化物、氮化物的形式析出, 起到钉扎晶界、细化晶粒的作用[3-6].其中合金元素M (M=Nb、Ti) 与间隙原子X (X=C、N) 结合形成MX, 大部分为NaCl型的面心立方结构, 晶格常数相近可以互溶为多元合金碳氮化物.近些年来为研究碳氮化物的生成规律应用了一系列模型, 理想溶液近似是最简单的用于分析碳氮化物生成的热力学模型, 对微合金钢中碳氮化物析出规律及影响条件进行分析[7-11].然而理想溶液近似对组元的宏观热效应及微观结构等有严格要求, 实际材料中满足条件的体系很少, 相继发展了正规溶液、亚正规溶液、Bragg-Williams近似及双亚点阵模型等, 而以双亚点阵模型对碳氮化物研究中应用最为广泛.
利用双亚点阵模型, 前人对微合金钢中纳米碳氮化物在奥氏体中的平衡热力学分析做了大量工作.Zou等[12]将双亚点阵模型与动力学模型相结合, 分析微合金钢(Tix, Nb1-x)(Cy, N1-y) 在奥氏体中的形成过程和尺寸分布, 发现随粒子的长大内外层Ti/Nb逐渐降低. Inoue等[13]根据晶格常数对组元间的相互作用参数进行研究, 将其应用于双亚点阵模型分析钢中(Nb, V, Ti)(C, N) 与基体平衡关系.陈泓业等[14-15]通过双亚点阵模型分析含Ti、Nb、V、Mo低合金钢中碳氮化物析出规律, 指出由高温到低温分别生成TiN、(Nbx, Ti1-x)(Cy, N1-y) 及富V复合碳化物、
通过采用双亚点阵模型, 对DH36钢中碳氮析出物的析出热力学进行分析, 求出C、N、Nb、Ti在任意温度下的奥氏体中的质量百分数, 分析高温区、低温区(Nb, Ti)(C, N) 的析出规律, 为碳氮纳米析出物的研究提供相关数据以及对工业实际生产的控轧控冷制度提供依据.
1 实验
实验钢材DH36取自河北某钢厂, 工艺流程为: KR铁水预处理→120 t BOF转炉冶炼→120 t LF精炼→1号连铸机→中厚板轧机.
具体实验步骤如下:
1) 试样准备:取实验用的10 mm×10 mm×20 mm试样2个, 将这些试样用砂纸抛光到6.5 μm;
2) 机械抛光;
3) 用浓度为4 %的硝酸酒精溶液侵蚀抛光表面;
4) 在试样的抛光表面蒸镀30 nm厚的碳膜;
5) 在浓度为8 %的硝酸酒精溶液中萃取, 并用铜网捞取脱落的碳膜, 经酒精、去离子水清洗, 干燥保存.
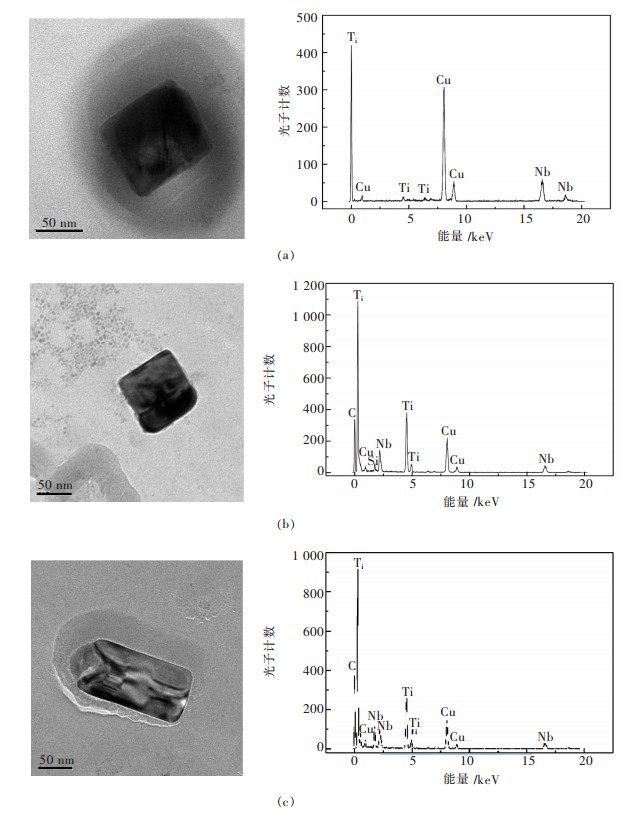
图 1所示为在透射电镜下观察到的纳米级(Nb, Ti) (C, N) 析出物的TEM像, 图 1(a)、图 1(b)、图 1(c)为析出物的不同形貌.其中在EDS谱中, 出现Cu的波峰是因为铜网的原因, 又因为轻质C、N元素的特征X射线能量低, 在样品基体内容易被吸收, 所以C、N的波峰不容易被观察到, EDS能谱中观察到C的波峰为碳膜中C的波峰.
2 热力学模型描述
Nb, Ti合金元素与C、N形成复合碳氮化物(Nbx, Ti1-x)(Cy, N1-y), 双亚点阵模型假设合金元素M和非金属元素X分别进入一种点阵, 每一组元只能进入一种亚点阵而不能进入另一种亚点阵, 在每一点阵内组元之间近似符合正规溶液.忽略空位影响, 四元碳氮化物满足理想化学配比. DH36船板钢碳氮化物表达式为(Nbx, Ti1-x)(Cy, N1-y), 1 mol该物质看做是xy mol NbC、x(1-y) mol NbN、(1-x)y mol TiC、(1-x)(1-y) mol TiN混合而成.
|
$
\begin{array}{l}
{G_{\rm{m}}} = {G_{{\rm{N}}{{\rm{b}}_x}{\rm{T}}{{\rm{i}}_{1-x}}{{\rm{C}}_y}{{\rm{N}}_{1-y}}}} = xyG_{{\rm{NbC}}}^0 + x\left( {1-y} \right)G_{{\rm{NbC}}}^0 + \\
\left( {1 - x} \right)G_{{\rm{TiC}}}^0 + \left( {1 - x} \right)\left( {1 - y} \right)G_{{\rm{TiC}}}^0 - TS_{\rm{m}}^1 + G_{\rm{m}}^{\rm{E}}
\end{array}
$
|
(1) |
式(1) 中:GNbC0为在某一温度下NbC的摩尔自由能, GNbN0、GTiC0、GTiN0代表的意义与之类似, T为热力学温度, SmI为理想摩尔混合熵, GmE为反应的过剩自由能.
|
$
-\frac{{S_{\rm{m}}^{\rm{I}}}}{R} = x\ln x + \left( {1-x} \right)\ln \left( {1-x} \right) + y\ln y + \left( {1 - y} \right)\ln \left( {1 - y} \right)
$
|
(2) |
式(2) 中: R是气体常数.
|
$
y\left( {1-y} \right)\left( {1-y} \right)L_{{\rm{CN}}}^{{\rm{Ti}}}
$
|
(3) |
式(3) 中: LM1M2M3表示M1、M2原子之间的相互作用能, 其中M1、M2处于同一亚点阵中而M3完全占据另一亚点阵.当两相中溶质的偏摩尔吉布斯自由能相等时碳氮化物从奥氏体中不再析出, 即:
|
$
\Delta {G_{{\rm{NbC}}}} = {{\bar G}_{{\rm{NbC}}}}-\bar G_{{\rm{Nb}}}^{\rm{r}}-\bar G_{\rm{C}}^{\rm{r}} = 0
$
|
(4) |
|
$
\Delta {G_{{\rm{NbN}}}} = {{\bar G}_{{\rm{NbN}}}}-\bar G_{{\rm{Nb}}}^{\rm{r}}-\bar G_{\rm{N}}^{\rm{r}} = 0
$
|
(5) |
|
$
\Delta {G_{{\rm{TiC}}}} = {{\bar G}_{{\rm{TiC}}}}-\bar G_{{\rm{Ti}}}^{\rm{r}}-\bar G_{\rm{C}}^{\rm{r}} = 0
$
|
(6) |
|
$
\Delta {G_{{\rm{TiN}}}} = {{\bar G}_{{\rm{TiN}}}}-\bar G_{{\rm{Ti}}}^{\rm{r}}-\bar G_{\rm{N}}^{\rm{r}} = 0
$
|
(7) |
式(4)~式(7) 中: GNbC、GNbr、GCr分别表示NbC、Nb、C在奥氏体中的偏摩尔吉布斯自由能, 其余与之类似.其中奥氏体中的溶质元素M的偏摩尔吉布斯自由能可用式(8) 求解:
|
$
{{\bar G}_{\rm{m}}} = RT\ln {a_{\rm{m}}}
$
|
(8) |
互易相的化学势与摩尔吉布斯自由能的关系见式(9)~式(12).在各亚点阵中应用正规溶液模型.因为正规溶液模型考虑了过剩混合热, 比较接近实际溶液.在求解摩尔吉布斯自由能对Xi的偏微分时对Xi认为其与其它成分变量无关.再通过式(13)~式(21) 求出互易相中化合物组元的化学势.
|
$
\begin{array}{l}
{{\bar G}_{{\rm{NbC}}}} = {G_{\rm{M}}} + \frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{{\rm{Nb}}}}}} + \frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{\rm{C}}}}}-\\
\left( {{X_{{\rm{Nb}}}}\frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{{\rm{Nb}}}}}} + {X_{{\rm{Ti}}}}\frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{{\rm{Ti}}}}}} + {X_{\rm{C}}}\frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{\rm{C}}}}} + {X_{\rm{N}}}\frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{\rm{N}}}}}} \right)
\end{array}
$
|
(9) |
|
$
\begin{array}{l}
{{\bar G}_{{\rm{NbN}}}} = {G_{\rm{M}}} + \frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{{\rm{Nb}}}}}} + \frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{\rm{N}}}}}-\\
\left( {{X_{{\rm{Nb}}}}\frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{{\rm{Nb}}}}}} + {X_{{\rm{Ti}}}}\frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{{\rm{Ti}}}}}} + {X_{\rm{C}}}\frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{\rm{C}}}}} + {X_{\rm{N}}}\frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{\rm{N}}}}}} \right)
\end{array}
$
|
(10) |
|
$
\begin{array}{l}
{{\bar G}_{{\rm{TiC}}}} = {G_{\rm{M}}} + \frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{{\rm{Ti}}}}}} + \frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{\rm{C}}}}}-\\
\left( {{X_{{\rm{Nb}}}}\frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{{\rm{Nb}}}}}} + {X_{{\rm{Ti}}}}\frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{{\rm{Ti}}}}}} + {X_{\rm{C}}}\frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{\rm{C}}}}} + {X_{\rm{N}}}\frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{\rm{N}}}}}} \right)
\end{array}
$
|
(11) |
|
$
\begin{array}{l}
{{\bar G}_{{\rm{TiN}}}} = {G_{\rm{M}}} + \frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{{\rm{Ti}}}}}} + \frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{\rm{N}}}}}-\\
\left( {{X_{{\rm{Nb}}}}\frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{{\rm{Nb}}}}}} + {X_{{\rm{Ti}}}}\frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{{\rm{Ti}}}}}} + {X_{\rm{C}}}\frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{\rm{C}}}}} + {X_{\rm{N}}}\frac{{\partial {G_{\rm{M}}}}}{{\partial {X_{\rm{N}}}}}} \right)
\end{array}
$
|
(12) |
|
$
\left. {{{\bar G}_{{\rm{NbC}}}} = G_{{\rm{NbC}}}^0 + \left( {1-x} \right)\left( {1-y} \right)\Delta G-RT\ln xy + \bar G_{{\rm{NbC}}}^{\rm{E}}} \right)
$
|
(13) |
|
$
\begin{array}{l}
\bar G_{{\rm{NbC}}}^{\rm{E}} = \left( {1-x} \right)\left( {x + y-2xy} \right)L_{{\rm{NbTi}}}^{\rm{C}} + \left( {1-x} \right)\left( {1 - y} \right)\left( {1 - 2x} \right)L_{{\rm{NbTi}}}^{{\rm{NC}}} + \\
\left( {1 - y} \right)\left( {x + y - 2xy} \right)L_{{\rm{CN}}}^{{\rm{Nb}}} + \left( {1 - x} \right)\left( {1 - y} \right)\left( {1 - 2x} \right)L_{{\rm{CN}}}^{{\rm{Ti}}}
\end{array}
$
|
(14) |
|
$
{{\bar G}_{{\rm{NbN}}}} = G_{{\rm{NbN}}}^0-y\left( {1-x} \right)\Delta G-RT\ln x\left( {1 - y} \right) + \bar G_{{\rm{NbN}}}^{\rm{E}}
$
|
(15) |
|
$
\begin{array}{l}
\bar G_{{\rm{NbC}}}^{\rm{E}} = \left( {1-x} \right)y\left( {1-2x} \right)L_{{\rm{NbTi}}}^{\rm{C}} + \left( {1-x} \right)\left( {1 - x - y + 2xy} \right)L_{{\rm{NbTi}}}^{\rm{N}} + \\
y\left( {1 - x - y + 2xy} \right)L_{{\rm{CN}}}^{{\rm{Nb}}} + y\left( {1 - x} \right)\left( {2y - 1} \right)L_{{\rm{CN}}}^{{\rm{Ti}}}
\end{array}
$
|
(16) |
|
$
{{\bar G}_{{\rm{TiC}}}} = G_{{\rm{TiC}}}^0-x\left( {1-y} \right)\Delta G + RT\ln \left( {1-x} \right)y + \bar G_{{\rm{TiC}}}^{\rm{E}}
$
|
(17) |
|
$
\begin{array}{l}
\bar G_{{\rm{TiC}}}^{\rm{E}} = x\left( {1-x-y + 2xy} \right)L_{{\rm{NbTi}}}^{\rm{C}} + x\left( {1-y} \right)\left( {2x - 1} \right)L_{{\rm{NbTi}}}^{\rm{N}} + \\
x\left( {1 - y} \right)\left( {1 - 2y} \right)L_{{\rm{CN}}}^{{\rm{Nb}}} + \left( {1 - y} \right)\left( {1 - x - y + 2xy} \right)L_{{\rm{CN}}}^{{\rm{Ti}}}
\end{array}
$
|
(18) |
|
$
{{\bar G}_{{\rm{TiN}}}} = G_{{\rm{TiN}}}^0 + xy\Delta G + RT\ln \left( {1-x} \right)\left( {1-y} \right) + \bar G_{{\rm{TiN}}}^{\rm{E}}
$
|
(19) |
|
$
\begin{array}{l}
\bar G_{{\rm{TiN}}}^{\rm{E}} = xy\left( {2x-1} \right)L_{{\rm{NbTi}}}^{\rm{N}} + x\left( {x + y-2xy} \right)L_{{\rm{NbTi}}}^{\rm{N}} + \\
xy\left( {2y-1} \right)L_{{\rm{CN}}}^{{\rm{Nb}}} + y\left( {x + y - 2xy} \right)L_{{\rm{CN}}}^{{\rm{Ti}}}
\end{array}
$
|
(20) |
|
$
\Delta G = G_{{\rm{NiN}}}^0 + G_{{\rm{TiC}}}^0 + G_{{\rm{NiC}}}^0 + G_{{\rm{TiN}}}^0
$
|
(21) |
碳氮化物形成元素的正规溶液模型参数热力学数据不足, 只能对偏摩尔吉布斯自由能计算做简化处理.目前仅已知
LCNTi=-4 260 J/mol, 假设LCNNb=LCNTi, LNbTiC=0, LNbTiN=0经推导得:
|
$
\bar G_{{\rm{MC}}}^{\rm{E}} = {\left( {1-y} \right)^2}L_{{\rm{CN}}}^{\rm{M}}
$
|
(22) |
|
$
\bar G_{{\rm{MN}}}^{\rm{E}} = {y^2}L_{{\rm{CN}}}^{\rm{M}}
$
|
(23) |
式(4)~式(7) 只有3个相互独立的平衡方程, 即平衡方程组由这3个相互独立的方程来线性组合, 因此:
|
$
y\Delta {G_{{\rm{NbC}}}} + \left( {1-y} \right)\Delta {G_{{\rm{NbN}}}} = 0
$
|
(24) |
|
$
x\Delta {G_{{\rm{NbC}}}} + \left( {1-x} \right)\Delta {G_{{\rm{TiC}}}} = 0
$
|
(25) |
|
$
x\Delta {G_{{\rm{NbN}}}} + \left( {1-x} \right)\Delta {G_{{\rm{TiN}}}} = 0
$
|
(26) |
将变量代入式(24)~式(26) 简化得:
|
$
y\ln \frac{{xy{K_{{\rm{NbC}}}}}}{{\left[{{\rm{N}}{{\rm{b}}_{\rm{s}}}} \right]\left[{{{\rm{C}}_{\rm{s}}}} \right]}} + \left( {1 - y} \right)\ln \frac{{x\left( {1 - y} \right){K_{{\rm{NbN}}}}}}{{\left[{{\rm{N}}{{\rm{b}}_{\rm{s}}}} \right]\left[{{{\rm{N}}_{\rm{s}}}} \right]}} + y\left( {1 -y} \right)\frac{{{L_{{\rm{CN}}}}}}{{RT}} = 0
$
|
(27) |
|
$
x\ln \frac{{xy{K_{{\rm{NbC}}}}}}{{\left[{{\rm{N}}{{\rm{b}}_{\rm{s}}}} \right]\left[{{{\rm{C}}_{\rm{s}}}} \right]}} + \left( {1 - x} \right)\ln \frac{{y\left( {1 - x} \right){K_{{\rm{TiC}}}}}}{{\left[{{\rm{T}}{{\rm{i}}_{\rm{s}}}} \right]\left[{{{\rm{C}}_{\rm{s}}}} \right]}} + \left( {1 -y} \right)\frac{{{L_{{\rm{CN}}}}}}{{RT}} = 0
$
|
(28) |
|
$
x\ln \frac{{x\left( {1- y} \right){K_{{\rm{NbC}}}}}}{{\left[{{\rm{N}}{{\rm{b}}_{\rm{s}}}} \right]\left[{{{\rm{N}}_{\rm{s}}}} \right]}} + \left( {1 - x} \right)\ln \frac{{\left( {1 - x} \right)\left( {1 - y} \right){K_{{\rm{TiN}}}}}}{{\left[{{\rm{T}}{{\rm{i}}_{\rm{s}}}} \right]\left[{{{\rm{N}}_{\rm{s}}}} \right]}} + {y^2}\frac{{{L_{{\rm{CN}}}}}}{{RT}} = 0
$
|
(29) |
式(27)~式(29) 中: KNbC、KNbN、KTiC、KTiN分别为NbC、NbN、TiC、TiN的平衡溶度积. [Ms]为平衡态下奥氏体中溶质元素(Nb、Ti、C、N) 的摩尔分数.式(27)~式(29) 中含有6个未知数3个方程, 还需根据质量守恒原理构建方程, 可得:
|
$
\left[{{\rm{N}}{{\rm{b}}_0}} \right] = \left( {\frac{x}{2}} \right)f + \left( {1 - f} \right)\left[{{\rm{N}}{{\rm{b}}_{\rm{s}}}} \right]
$
|
(30) |
|
$
\left[{{\rm{T}}{{\rm{i}}_0}} \right] = \left( {\frac{{1 - x}}{2}} \right)f + \left( {1 - f} \right)\left[{{\rm{T}}{{\rm{i}}_{\rm{s}}}} \right]
$
|
(31) |
|
$
\left[{{{\rm{C}}_0}} \right] = \left( {\frac{y}{2}} \right)f + \left( {1 - f} \right)\left[{{{\rm{C}}_{\rm{s}}}} \right]
$
|
(32) |
|
$
\left[{{{\rm{N}}_0}} \right] = \left( {\frac{{1 - y}}{2}} \right)f + \left( {1 - f} \right)\left[{{{\rm{N}}_{\rm{s}}}} \right]
$
|
(33) |
式(30)~式(33) 中: f表示析出物的摩尔分数. [M0]代表钢中溶质元素(C、N、V、Ti) 的初始摩尔分数.式(27)~式(33) 为含有7个未知数7个方程的方程组.
由该方程组可以求解出在任意温度下DH36钢中平衡基体的成分、析出物的成分以及析出物的摩尔分数.在求解过程中还需要知道碳化物、氮化物在奥氏体中的平衡溶度积, 其中平衡溶度积求解公式为, log K[M][X]=B-A/T, A, B为常数, [M]、[X]分别代表金属原子与间隙原子的质量分数.在方程组中都用摩尔分数来表示浓度和溶度积, 二者之间转换关系如式(34):
|
$
{K_{\left[{\rm{M}} \right]\left[{\rm{X}} \right]}} = \frac{{{{\left[{{\rm{Fe}}} \right]}^2}}}{{{{10}^4}\left[{\rm{M}} \right]\left[{\rm{X}} \right]}} \times {10^{B -A/{\rm{T}}}}
$
|
(34) |
计算过程所采用的热力学数据[16], 如表 1所列.
表1(Table 1)
|
表1 奥氏体中碳化物、氮化物的平衡溶度积
Table 1 Solubility product of carbides and nitrides in austenite
|
表1 奥氏体中碳化物、氮化物的平衡溶度积
Table 1 Solubility product of carbides and nitrides in austenite
| 化合物 |
A值 |
B值 |
| NbC |
9 393 |
45988 |
| NbN |
1 101 |
5.376 |
| TiC |
10 745 |
55330 |
| TiN |
8 000 |
0.322 |
|
 |
| 点击放大 |
3 计算结果与分析
实验用钢成分如表 2所列.
表2(Table 2)
|
表2 研究所用的DH36船板钢的化学成分
Table 2 Composition of pipeline steel
|
表2 研究所用的DH36船板钢的化学成分
Table 2 Composition of pipeline steel
| 元素 |
C |
S |
0 |
N |
Si |
Mn |
P |
Ni |
Al |
Cu |
Ti |
Nb |
| 含量/1 |
0.110 |
0.007 |
0.002 |
0.004 |
0.640 |
1.420 |
0.020 |
0.020 |
0.070 |
0.013 |
0.011 |
0.019 |
|
 |
| 点击放大 |
使用双亚点阵模型进行DH36钢中碳氮化物计算时, 首先用1st0pt软件, 采用模拟退火和遗传算法进行初步计算, 再将上述数值解作为Matlab中牛顿-拉普生算法的初值进行运算.
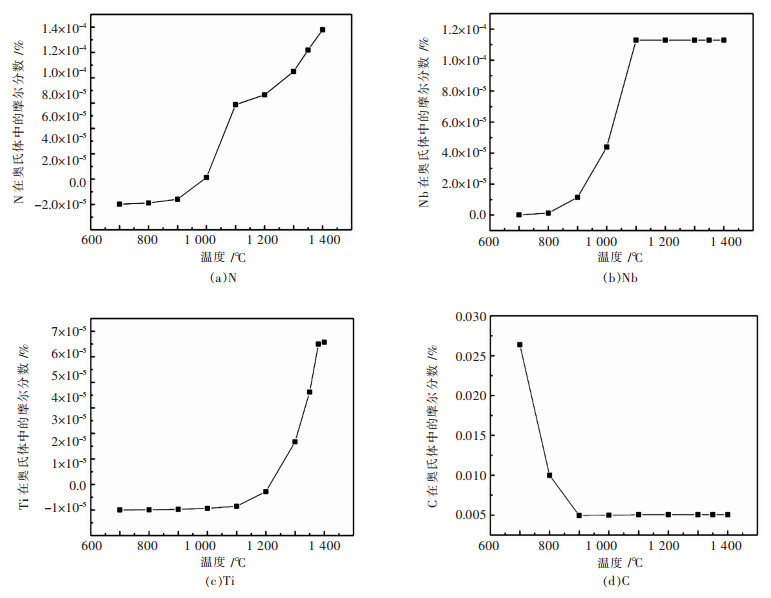
计算结果表明Nb和Ti的碳氮化物析出温度分别为1 100 ℃和1 380 ℃(如图 2(b)、图 2(c)所示).在1 100~1 400 ℃高温区C在奥氏体中的含量变化不显著, Ti、N的含量显著降低, 析出物为Ti (C、N), 尤其是TiN所占比例很大; 在900~1 100 ℃, Nb的碳氮化物开始大量析出, 在此温度区间Ti与C的结合能力大于Ti与N的结合能力, TiC大量析出, 由图 2(d)和图 2(a)可以看出, C的变化量比N大得多(N的摩尔分数远远小于C的摩尔分数); 在700~900 ℃低温区, N在奥氏体中的含量基本不变, 即在低温区碳氮析出物的主要成分为(Nb, Ti) C.其中图 2(d)中C的摩尔百分数在900~1 400 ℃区间上有一个下降趋势, 是因为在这个温度区间有C从奥氏体中析出与Nb、Ti结合生成NbC、TiC.在900 ℃, C有一个激增的趋势, 是因为随着温度的降低到900 ℃开始进入奥氏体和铁素体的两相区, 奥氏体中的Fe大量进入铁素体中, 导致奥氏体中的C的摩尔分数激增.
碳氮化物的组成很大程度上取决于奥氏体的温度, 在1 100~1 400 ℃的温度区间, TiN是最主要的析出相, 起到钉扎晶界影响奥氏体晶粒生长的重要作用[17].在低温阶段, 随着温度的逐渐降低, 碳化物(Nb, Ti) C所占的比例开始增加.因此细小的NbC和TiC在抑制奥氏体再结晶及再结晶后的奥氏体晶粒长大方面起重要作用.此外在900 ℃以下, 氮含量变化趋于平稳, 这是由于高温阶段N大量析出所引起的低温阶段基体贫氮所致.
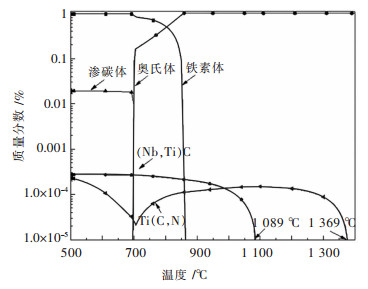
为了验证双亚点阵模型在DH36钢中碳氮析出物的热力学计算的适用性, 利用Thermo-Calc软件进行了热力学相图计算, 得到了温度对奥氏体中所有相影响的性质图, 如图 3所示.
在图 3中700~1 400 ℃为奥氏体区, 700~850 ℃为奥氏体和铁素体的两相区, 700 ℃以下为铁素体区.其中Ti (C, N) 的析出温度为1 369 ℃, (Nb, Ti) C的析出温度为1 089 ℃, 在高温区(1 100~1 400 ℃) 以Ti (C, N) 析出为主, 在700~1 100 ℃区间(Nb, Ti) C比Ti (C, N) 的析出物摩尔分数高出一个数量级, 析出相以(Nb, Ti) C主.从1 100 ℃开始, Ti (C、N) 的质量百分数开始下降, (Nb、Ti) C的质量百分数开始增加, 到700 ℃左右Ti (C、N) 的质量百分数达到最低, 是因为从1 100 ℃开始, Ti主要与C结合, 进入(Nb、Ti) C相, 700 ℃左右(Nb、Ti) C相质量百分数达到最大. 700 ℃以下Ti (C、N) 无法突破能垒转化成(Nb、Ti) C, 所以在铁素体中以Ti (C、N) 相析出. Thermo-Calc中各析出相摩尔分数相图均与双亚点阵模型做到了很好的佐证, 证明双亚点阵模型在DH36钢中求解碳氮析出物的热力学条件实用、可靠.
4 结论
通过应用双亚点阵模型对Fe-Nb-Ti-C-N系统进行热力学分析, 并得到以下结论:
1) Ti (C, N) 的析出温度为1 380 ℃, 在1 100~1 400 ℃的高温区, 主要析出物为TiN, 并且TiN为影响DH36钢奥氏体均热阶段晶粒长大的主要因素.
2) (Nb, Ti) C的析出温度为1 100 ℃, 在1 100 ℃以下的低温区析出相主要以碳化物为主, NbC、TiC是抑制DH36钢奥氏体再结晶及再结晶后奥氏体长大的重要因素.


 2017, Vol. 8
2017, Vol. 8


