| N263从钼酸钠溶液中萃取分离钼钒 |
钼是一种重要的稀有金属, 被广泛应用于钢铁工业、电子工业、机械制造、石油化工、生物医药、国防军事等领域, 是不可或缺的重要资源.我国钼资源丰富, 已探明的钼金属储量840万t, 居世界第2位, 钼产品产量居世界第3位, 占世界钼总产量的24 %~25 %[1].
随着科学技术的发展, 钼及其化合物的应用范围也在不断扩大, 加强二次资源的回收利用显得尤为重要.石油炼制和化学工业中广泛采用的加氢脱硫催化剂HDS, 在使用的过程中, 由于原料中钒、镍、硫的沉积而逐渐失去活性, 因此每年都有大量的废催化剂必须处理, 淘汰下来的废催化剂含Mo 3 %~12 %、V 0.5 %~12 %、Co 0 %~3 %、As 0 %~0.3 %、SiO2 0.5 %~15 %、P 0 %~5 %和一定量的S和C[2], 处理此类固体废弃物既能解决环境污染的问题, 又可以回收有价金属.
目前, 国内回收此类废催化剂的方法主要有酸浸法[3-4]、碱浸法[5]、盐焙烧浸出法[6]等.上述处理HDS废催化剂, 并生产合格的钒产品和钼产品的工艺, 均需要进行钼钒分离[7-8].钼钒分离通常采用铵盐沉钒法、离子交换法、溶剂萃取法.张报清等[9]采用化学沉淀法从钼酸铵溶液中分离除钒, 控制实验条件, 可得纯度在98.5 %以上的偏钒酸铵沉淀.此类方法具有沉钒效率高, 工艺简单等优点, 但是无法实现钼钒的深度分离.肖超等[10]采用特种阴离子交换树脂从钼酸铵溶液中分离钒, 在料液pH=8.01, 接触时间60 min, 处理料液为67倍树脂体积时, 除钒率达到99.83 %.离子交换法除钒效果好, 但是普遍存在交换容量低、废水排量大等缺点.溶剂萃取法作为钼钒深度分离的常用方法, 具有回收率高、工序少、设备简单等优点, 越来越受到国内外学者的重视.但是从高浓度钼酸钠溶液中分离钒的研究还未见报道.文中采用季铵盐萃取剂N263从高浓度的钼酸钠料液中选择性萃取钒[11].此法可为钠盐体系下, 钼钒的分离研究提供借鉴.
1 实验 1.1 实验原理实验采用的萃取剂为常见的季铵盐萃取剂N263, 该萃取剂被广泛应用于钒的选择性萃取[12-15].当溶液pH值在7~9时, 钒主要是以偏钒酸根离子(V3O93-和VO3-) 的形式存在, 而钼则以钼酸根离子(MoO42-) 的形态存在[16].由于V3O93-所带的电荷比MoO42-所带的电荷多, N263选择吸附钒(对V3O93-亲和力大) 而基本不吸附钼(对MoO42-亲和力小), 从而选择性地将钒从钼酸钠溶液中分离开来[9].以氯型季铵盐为例, 萃取过程反应原理如下:
| $ \begin{array}{l} {{\rm{V}}_{\rm{3}}}{\rm{O}}_{\rm{9}}^{{\rm{3-}}}{\rm{ + 3}}\overline {{{\rm{R}}_{\rm{4}}}{\rm{NCl}}} {\rm{ = }}\overline {{{\left( {{{\rm{R}}_{\rm{4}}}{\rm{N}}} \right)}_{\rm{3}}}{{\rm{V}}_{\rm{3}}}{{\rm{O}}_{\rm{9}}}} {\rm{ + 3C}}{{\rm{l}}^{\rm{-}}}\\ {\rm{VO}}_{\rm{3}}^{\rm{-}}{\rm{ + }}\overline {{{\rm{R}}_{\rm{4}}}{\rm{NCl}}} = \overline {{{\rm{R}}_{\rm{4}}}{\rm{NV}}{{\rm{O}}_{\rm{3}}}} {\rm{ + C}}{{\rm{l}}^{\rm{ - }}}\\ {\rm{MoO}}_{\rm{4}}^{{\rm{2 - }}} + 2\overline {{{\rm{R}}_{\rm{4}}}{\rm{NCl}}} = \overline {{{\left( {{{\rm{R}}_{\rm{4}}}{\rm{N}}} \right)}_{\rm{2}}}{\rm{Mo}}{{\rm{O}}_4}} {\rm{ + 2C}}{{\rm{l}}^{\rm{ - }}} \end{array} $ |
萃取实验所用料液为配制模拟料液.配制的钼酸钠溶液含Mo 100 g/L、V 10 g/L (钒含量以V2O5计), 原料液pH值为8~9.
萃取剂为三辛基甲基氯化铵(N263, 纯度99 %); 稀释剂为磺化煤油; 相调节剂为分析纯仲辛醇.萃取前, 有机相用1.5 mol/L HCl处理两次, 然后用2 mol/L NaCl洗5次, 确保N263为氯型.
1.3 实验方法萃取实验之前, 先用NaOH或H2SO4将料液pH调至预定值, 静置一天使料液pH稳定.萃取和反萃实验均是将有机相和水相按一定相比(VO/VA) 混合于梨型分液漏斗中, 并且置于水浴恒温振荡器上充分摇匀.振荡完毕后, 取出静置分相, 分析水相中Mo、V的浓度.
萃取实验和洗涤实验水相中钒的分析均采用硫酸亚铁铵还原滴定法, 钼的分析采用硫氰酸铵吸光光度法.反萃实验水相中钒的分析采用磷钨钒酸吸光光度法, 钼的浓度采用IRIS Inerpid II XPS电感耦合等离子发射光谱仪进行分析.
1.4 数据分析与处理实验过程中, Mo、V的萃取率(EMe)、分配比(DMe)、及V与Mo的分离系数(βV/Mo) 的计算方法如式(1)、(2)、(3) 所示:
| $ {E_{Me}} = \left( {1- \frac{{{{\left[{Me} \right]}_a} \times {V_a}}}{{{{\left[{Me} \right]}_F} \times {V_F}}}} \right) \times 100\% $ | (1) |
| $ {D_{Me}} = \frac{{{{\left[{Me} \right]}_O}}}{{{{\left[{Me} \right]}_s}}} $ | (2) |
| $ {\beta _{{\rm{V/Mo}}}} = \frac{{{D_{\rm{V}}}}}{{{D_{{\rm{Mo}}}}}} $ | (3) |
式中Me表示Mo、V, [Me]a表示萃余液中Me的浓度, g/L; [Me]F表示原料液中Me的浓度, g/L; [Me]0和[Me]s分别表示有机相中Me的浓度和水相中Me的浓度, g/L; Va为萃余液的体积, mL; VF为原料液的体积, mL.
2 结果与讨论 2.1 钒的萃取 2.1.1 萃取剂浓度对钼钒萃取的影响保持有机相中仲辛醇的浓度12 %不变, 改变萃取剂浓度.在料液pH=8.99, 相比VO/VA=1: 2, 混合时间10 min, 温度25 ℃的条件下进行实验, 结果如图 1所示.从图 1可以看出, 随着萃取剂浓度的增加, 钒的萃取率不断升高, 而钼的萃取率基本不变; 钒钼的分离系数先升高后降低, 在萃取剂浓度为15 %时最高, 达到779.74.当萃取剂浓度大于20 %时, 萃取分相时间变长, 且水相和有机相混浊, 这是因为萃取剂浓度升高时, 有机相中萃取的钼钒浓度升高, 钼钒的萃合物质量较大, 使得有机相和水相间密度差减小, 导致分相困难.故选取萃取剂浓度为15 %.
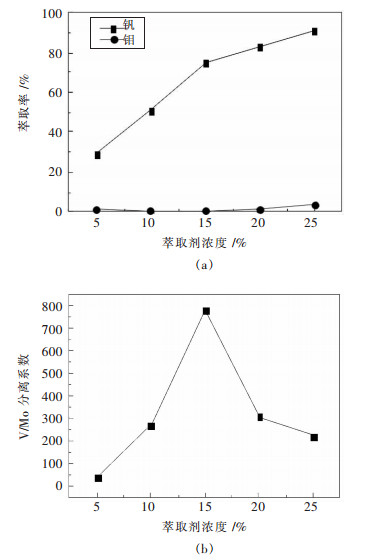 |
| 图 1 萃取剂浓度对钼钒萃取率及萃取分离系数βV/Mo的影响 Fig. 1 Effects of extraction agent concentration on molybdenum, vanadium extraction and βV/Mo |
2.1.2 相调节剂浓度对钼钒萃取的影响
相调节剂(仲辛醇) 可以提高萃取剂在有机相中的溶解性能, 并且有助于改善分相性能.萃取剂浓度15 %, 改变仲辛醇浓度.在料液pH=8.98, 相比VO/VA=1: 2, 混合时间10 min, 温度25 ℃的条件下进行实验, 结果如图 2所示.从图 2可知, 在4 %~12 %的仲辛醇浓度下, 钒的萃取率均高于80 %.随着仲辛醇浓度的升高, 钒的萃取率缓慢降低.这是因为仲辛醇与N263有较强的相互作用, 降低了N263的萃取能力.由于N263对钒的结合能力较钼强, 萃取的钼会被钒取代, 所以萃取剂对钼的萃取处于一个较低的水平, 钼的萃取率基本不变.但仲辛醇浓度低于8 %时体系分相效果变差, 水相和油相不清亮, 因此选择仲辛醇浓度为12 %.
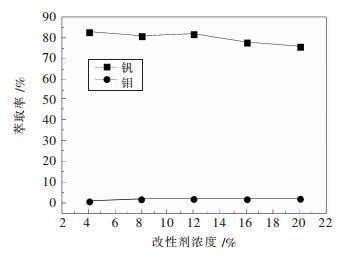 |
| 图 2 改性剂浓度对钼钒萃取率的影响 Fig. 2 Effects of modifier concentration on molybdenum and vanadium extraction |
2.1.3 平衡pH对钼钒萃取的影响
预先用NaOH和H2SO4调节pH值, 通过改变料液pH值来考察不同平衡pH值对萃取的影响.实验中有机相组成为15 %N263、12 %仲辛醇, 相比VO/VA=1: 2, 混合时间10 min, 温度为25 ℃, 结果如图 3所示.由图 3可知, 平衡pH值为8~9时, 萃取剂对钒有较好的萃取效果, 并且基本不萃钼.随着平衡pH的升高, 钒的萃取率降低, 当平衡pH值大于9时, 钒萃取率快速降低.这是由于pH值在8~9时, 钒主要是以偏钒酸根(VO3-) 的形式存在, 随着pH的升高, 特别是高碱度时, 钒主要以VO4-单阴离子形态存在, 使得萃取率降低.因此, 分离钼钒的pH范围可选择8~9之间.
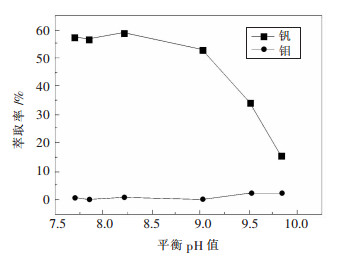 |
| 图 3 平衡pH对钼钒萃取率的影响 Fig. 3 Effects of equilibrium pH value on molybdenum and vanadium extraction |
2.1.4 温度对钼钒萃取的影响
有机相组成为15 %N263、12 %仲辛醇, 在料液pH=8.95, 相比VO/VA=1: 2, 混合时间10 min的条件下进行实验, 考察不同温度对钼钒萃取的影响, 实验结果如图 4所示.从图 4中可以看出, 随着温度的升高, 钒的萃取率稍有下降, 而钼的萃取率基本保持不变, 这说明萃取钒过程伴随轻微放热.由于温度对钼和钒萃取率的影响较小, 为方便实验条件的控制可选择在室温25~30 ℃的条件下进行实验.
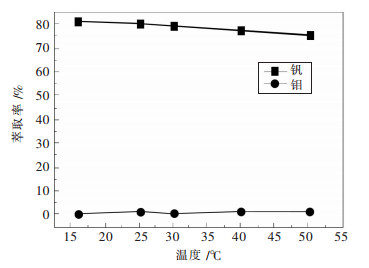 |
| 图 4 反应温度对钼钒萃取率的影响 Fig. 4 Effects of reaction temperature on molybdenum and vanadium extraction |
2.1.5 相比对钼钒萃取的影响
有机相组成为15 %N263、12 %仲辛醇, 在料液pH=9.01, 混合时间10 min, 温度25 ℃的条件下进行实验, 考察萃取相比对钼钒萃取的影响, 结果见图 5(a).由图 5(a)可知, 钼钒的萃取率均随着相比的减小而逐渐降低, 在相比VO/VA为2/1~1/1的范围内, 钒萃取率均在95 %以上, 此时钼的萃取率也较高.为了进一步提高钒的萃取率, 并且降低钼的萃取, 实验中常采用多级逆流萃取的方式来优化萃取效果.为此, 通过改变相比法, 绘制钒萃取等温曲线, 并且根据逆流萃取的原理绘制马克-齐利图.按照相比VO/VA=1/2绘制操作曲线, 由图 5(b)可知, 经过3级逆流萃取, 可以将萃取液中钒的浓度降低至0.10 g/L以下, 考虑萃取过程中的级效应, 实际操作时选取5级逆流萃取.
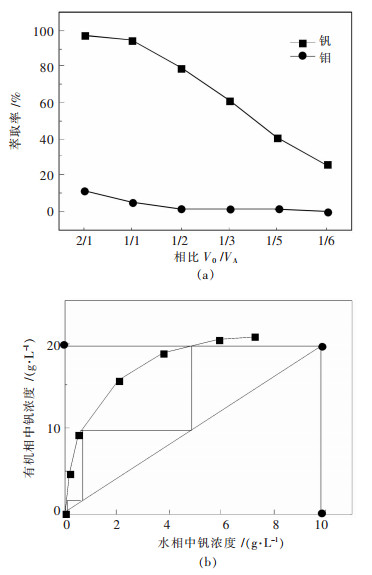 |
| 图 5 VO/VA对钼钒萃取率的影响及钒逆流萃取的McCabe-Thiele曲线 Fig. 5 Effects of VO/VA on Mo and V extraction rate and McCabe-Thiele diagram for V countercurrent extraction |
2.1.6 逆流串级萃取试验
有机相组成为15 %N263、12%仲辛醇, 在料液pH=8.50, 相比VO/VA=1: 2, 混合时间5 min的条件下, 采用矩阵式摇瓶模拟5级逆流萃取实验, 14~17排出口水相中, 钒的萃取率分别为99.84 %、99.68 %、99.68 %、99.72 %, 而钼的萃取率均在0.5 %以下, 萃余液含Mo 96.89 g/L, V 0.027 g/L.经五级逆流萃取可以将99.6 %以上的钒萃到有机相中, 而钼基本不萃, 钒钼的分离系数βV/Mo超过63 000, 已经达到选择性萃钒的目的.在此条件下测得负载有机相含钒20.42 g/L.
2.2 洗涤除钼在完成逆流萃取后, 测得负载有机相中含钒20.42 g/L, 钼1.14 g/L, 如果直接进行反萃, 有机相中的钼会进入反萃液, 使得反萃液中钼的含量升高, 从而影响钒的产品纯度.所以, 在反萃前要先对有机相进行洗涤, 除去其中的钼.
由于所选用的萃取剂为氯型N263, 因此洗涤剂选用NaCl溶液.这是根据季铵盐阳离子对偏钒酸根离子的结合能力比钼酸根强, 所以可选择低浓度的NaCl溶液洗去负载有机相上的钼.有文献指出[17], 在平衡pH=8.5左右, N263对钼的萃取能力较差, 所以本研究通过在NaCl溶液中加入NaHCO3作为pH缓冲剂使洗水pH值维持在8~8.5来增加钼的洗脱率.
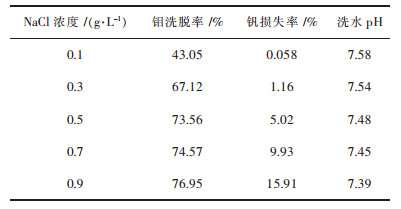
2.2.1 NaCl浓度对洗涤的影响以NaCl溶液为洗涤剂, 在相比VO/VA=5: 1, 混合时间10 min, 温度25 ℃的条件下进行洗涤实验, 考察NaCl浓度对洗涤的影响, 实验结果如表 1所列.从表 1中可以看出, 随着NaCl浓度的升高, 钼的洗脱率升高, 而钒的损失率也快速升高, 当洗水中NaCl浓度大于0.3 mol/L后, 钼的洗脱率增加缓慢.为了防止过多的钒被洗水带走, 选择0.1 mol/L NaCl作为洗涤剂.
| 表1 NaCl浓度对洗涤的影响 Table 1 Effects of NaCl concentration on washing |
 |
| 点击放大 |
2.2.2 NaHCO3浓度对洗涤的影响
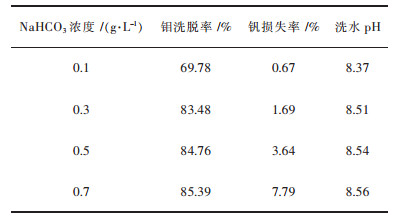
洗涤剂为NaCl+NaHCO3混合体系, 其中NaCl浓度为0.1 mol/L, 改变NaHCO3浓度, 在相比VO/VA=5: 1, 混合时间10 min, 温度25 ℃的条件下进行实验, 考察NaHCO3浓度对洗涤的影响, 结果见表 2.由表 2可知, 随着洗涤剂中NaHCO3浓度的升高, 钼的洗脱率升高, 而钒的损失率也升高, 当浓度大于0.3 mol/L后, 钼的洗脱率提高较少, 而钒的损失率增长较快.考虑到在提高钼洗脱率的同时降低钒的损失率, 洗涤剂中NaHCO3浓度选择0.3 mol/L.此时, 洗水pH值为8.51, 这与逆流萃取所用料液pH值一致, 可以考虑将洗水返回到逆流萃取段的料液中.
| 表2 NaHCO3浓度对洗涤的影响 Table 2 Effects of NaHCO3 concentration on washing |
 |
| 点击放大 |
2.2.3 相比对洗涤的影响
采用0.1 mol/L NaCl+0.3 mol/L NaHCO3为洗涤剂, 混合时间10 min, 温度25 ℃的条件下进行实验, 考察相比对洗涤的影响, 实验结果见图 6.从图 6中可以看出, 钼的洗脱率和钒的损失率均随着相比的增大而减小.考虑到洗涤过程中对于出水量的控制, 应尽量选取高相比进行实验, 但过高的相比会使钼的洗脱效果变差, 且分相时间过长.在相比VO/VA=5: 1的条件下, 钼的洗脱率仍能达到70 %以上, 且洗涤过程中, 钒基本不损失, 故选择相比为5: 1.
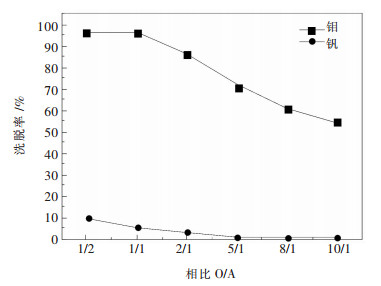 |
| 图 6 相比对洗涤的影响 Fig. 6 Effects of VO/VA ratio on washing |
2.2.4 5级逆流洗涤实验
为了进一步提高钼的洗脱率, 采用逆流串级洗涤的方式处理负载有机相.经过预实验探索, 确定逆流洗涤的级数为5级.采用0.1 mol/L NaCl+0.3 mol/L NaHCO3为洗涤剂, 负载有机相含钼2.66 g/L, 钒21.78 g/L, 在相比VO/VA=5: 1, 混合时间5 min, 温度25 ℃的条件下, 采用宝塔式摇瓶模拟5级逆流洗涤实验, 取10~12级出口水相, 测得其中钼的含量分别为: 14.70、14.70、14.54 g/L, 钒的浓度分别为: 0.43、0.43、0.44 g/L.洗涤后负载有机相中钼的浓度低于0.03 g/L, 钼的洗脱率达到98.87 %.由此可见, 经过5级逆流洗涤, 负载有机相中钼的洗脱效果很好, 且钒的损失率低, 可以实现负载有机相中钼的选择性洗涤.
2.3 反萃洗涤后的负载有机相采用2 mol/L NaCl+0.7 mol/L NaOH的溶液反萃, 有机相含钒25.73 g/L, 在相比VO/VA=2: 1, 混合时间10 min, 反应温度25 ℃的条件下进行实验.钒的单级反萃率可达99.76 %, 反萃液中含钒51.33 g/L, 钼0.06 g/L[18].
3 结论1) 季铵盐萃取剂N263在弱碱性条件下对钒的选择性很好, 以其为萃取剂时, 钼钒的分离系数很大.在料液pH=8.50、有机相组成为15 %N263+12 %仲辛醇、相比VO/VA=1: 2、振荡时间5 min、温度25 ℃的条件下, 进行5级逆流萃取, 萃余液中钒浓度降到0.03 g/L以下, 钒萃取率达到99.60 %以上, 而钼的萃取率仅在0.5 %以下.
2) 负载有机相采用0.1 mol/L NaCl+0.3 mol/L NaHCO3为洗涤剂, 在相比VO/VA=5: 1、混合时间5 min、温度25 ℃的条件下进行5级逆流洗涤, 洗涤后负载有机相中钼的浓度低于0.03 g/L, 钼的洗脱率达到98.87 %, 且钒的损失率在0.4 %以下.
3) 负载有机相经洗涤除钼之后, 用2 mol/L NaCl+0.7 mol/L NaOH的溶液反萃, 在最佳条件下, 钒的单级反萃率可达99.76 %, 实现钼钒的分离.
| [1] | 马宝平. 中国钼工业发展报告[J]. 中国钼业, 2004(2): 3–6. |
| [2] | 施友富, 王海北. 废催化剂中钼和钒的分离[J]. 中国钼业, 2004(2): 39–41. |
| [3] |
BISWAS R K, WAKIHARA M, TANIGUCHI M. Characterisation and leaching of the heavy oil desulphurization catalyst[J].
Powder Metallurgy, 1997, 40(4): 228–237. |
| [4] | 吴国元, 戴永年. 失效贵金属催化剂中贵金属的富集[J]. 稀有金属, 2002(3): 231–234. |
| [5] |
ZENG L, CHENG C Y. A literature review of the recovery of molybdenum and vanadium from spent hydrodesulphurisation catalysts : Part I: Metallurgical processes[J].
Hydrometallurgy, 2009, 98(1/2): 1–9. |
| [6] | 李培佑, 张能成, 林喜斌. 从废催化剂中回收钼的工艺流程研究[J]. 中国钼业, 1999(1): 14–19. |
| [7] |
El-NADI Y A, AWWAD N S, NAYL A A. A comparative study of vanadium extraction by Aliquat-336 from acidic and alkaline media with application to spent catalyst[J].
International Journal of Mineral Processing, 2009, 92(3/4): 115–120. |
| [8] | 宋夏月. 除掉高浓度钼酸铵溶液中钒的研究[J]. 大众科技, 2012(1): 58–59. |
| [9] | 张报清, 雷霆, 方树铭, 等. 钼酸铵溶液化学沉淀法和离子交换法除钒研究[J]. 稀有金属, 2012(3): 466–471. |
| [10] | 肖超, 肖连生, 曹佐英. 特种离子交换树脂从钼酸铵溶液中深度分离钒[J]. 有色金属(冶炼部分), 2010(6): 41–44. |
| [11] | 李尚勇, 谢刚, 俞小花. 从含钒浸出液中萃取钒的研究现状[J]. 有色金属, 2011(1): 100–104. |
| [12] | 姚建培, 袁文光, 孟凡中. 季胺盐萃取剂N263从高碱高硅含钒溶液中提取高纯V2O5[J]. 钢铁钒钛, 1982(3): 11–21. |
| [13] | 周小舟, 曹佐英, 肖连生, 等. 硫酸型季铵盐从石煤苏打浸出液中萃取钒的研究[J]. 矿冶工程, 2015(1): 68–71. |
| [14] | 齐兆树, 李青刚. 从碱性含钒溶液中萃取钒的研究[J]. 有色金属(冶炼部分), 2014(10): 43–48. |
| [15] | 刘波, 冯光熙, 黄祥玉, 等. 用N-263从钒溶液中回收钒[J]. 化学研究与应用, 2003, 15(1): 54–57. |
| [16] | 曾理, 肖连生, 李青刚, 等. 离子交换法从钼酸铵溶液中分离钼钒的研究[J]. 稀有金属与硬质合金, 2006(2): 1–4. |
| [17] | 周新花, 郑洁修, 马玉龙. 溶剂萃取法从含钒水浸溶液中分离钒和钼[J]. 武汉大学学报, 1991(4): 83–88. |
| [18] |
BAL Y, BAL K E, COTE G. Kinetics of the alkaline stripping of vanadium (V) previously extracted by Aliquat336[J].
Minerals Engineering, 2002(15): 377–379. |
 2017, Vol. 8
2017, Vol. 8


