| 氯化挥发的应用与研究进展 |
氯化冶金是一种通过金属氯化物进行冶金的方法,主要利用金属氯化物普遍具有熔点沸点较低、挥发性高、易溶于水等特点[1]。工业生产中常用的氯化冶金方法有:氯化焙烧、氯化焙烧-浸出、氯化浸出、氯化离析、氯化熔炼和氯化精炼[2-7]。通过氯化焙烧和氯化精炼手段,使金属以氯化物形式挥发出来的方法称为氯化挥发,通常用于提高金属矿的品位、回收金属废料、粗金属精炼等方面[8-10]。氯化挥发常用的氯化剂有Cl2、HCl和CaCl2、NaCl和FeCl3等氯化物,一般都具有较强的化学活性,容易与金属及其硫化物、氧化物等反应,生成沸点较低的金属氯化物。根据金属氯化物生成的难易不同和性质差异,通过控制反应温度和产物的蒸汽压等条件,实现金属的选择性氯化挥发。
1 金属矿的处理在金属矿的开采和选矿过程中,低品位的伴生矿和尾矿经常弃置不用,会造成金属资源浪费和环境污染[11]。提高矿石品位不仅可以提高矿石利用率,还能提高冶炼效率和产品质量,对冶炼效果具有十分积极的意义。对金属矿进行氯化焙烧时,矿石中的金属转化为低沸点氯化物从体系中挥发出来,根据氯化物的物理、化学性质差异进行收集,实现有价金属的富集或杂质金属的去除,达到提高金属矿品位的目的。有学者对金属矿的氯化焙烧处理进行研究,并取得良好的冶金效果。
赵刚[12]向难选锡中矿加入焦炭、氯化钙等进行氯化焙烧,锡、铅、砷等挥发率均在90%以上。李金辉[13]通过氯化焙烧方式选择性提取红土矿中的镍、钴,实现有价金属与杂质金属的分离;程瑞学[14]对锡中矿氯化焙烧过程中的微观机理进行研究,认为高温氯化挥发法处理氧化锡中矿要在弱还原气氛中进行。西门子法生产多晶硅过程中[15],入HCl对硅原料进行焙烧处理,生成低沸点的中间产物SiHCl3从体系中挥发,再进行冶炼得到纯净的多晶硅。
1.1 硫化矿工业上常用到的金属硫化矿有黄铜矿和与黄铁矿等,主要用于炼铜、炼铁或者制硫酸[16],硫化矿中铅、锌等杂质金属含量一般较高[17],影响矿的质量。目前多金属硫化矿常用处理方法是氧化焙烧、湿法溶出或浮选[18-20],但是许多工艺比较复杂而且回收有价金属的针对性不强,因此有学者考虑采用氯化挥发处理硫化矿以提高品位。
根据氯化冶金理论可知[1],在Cl2气氛中焙烧复杂硫化矿,铜、锌等金属全部反应生成CuCl、ZnCl2等低沸点氯化物;黄铜矿氯化焙烧过程中会产生CuCl2、CuCl以及络合物Cu3Cl3等,络合反应降低产物的分压,有利于铜的氯化反应进行。BAYER G等[21]使用NaCl在有O2条件下焙烧黄铜矿,发现体系有增重现象,认为体系内部同时进行硫的氧化反应和硫酸化反应。郭持皓等[22]选择CaCl2作氯化剂对含金高砷高硫精矿氯化焙烧,试验表明仅需要添加5%的CaCl2便可以对矿中的金、银、铅等金属进行有效回收,且焙烧后的球团铁可以作为炼铁原料。常耀超等[23]对硫铁矿烧渣进行氯化焙烧,将其中的有色金属挥发收集,并得到高品质的炼铁球团矿,可直接用于炼铁生产。
1.2 钛铁矿沸腾氯化法生产金属钛的工艺十分成熟[24, 25],其原理是以TiO2为原料加入碳和Cl2进行反应,使钛以TiCl4的形式挥发并富集,经过进一步冶炼得到高纯钛。若钛矿中含有杂质金属,势必造成产物TiCl4污染,并降低Cl2的利用率,因此提高钛铁矿的品位对生产有非常重大的意义。KANG J等[26-28]分别使用HCl、CaCl2和MgCl2作氯化剂对钛铁矿进行处理,结果表明钛铁矿中的铁会以FeCl2的形式被完全挥发除去,处理后的钛矿中TiO2含量占90%以上,极大地提高了钛铁矿的品位。
氯化挥发工艺能有效地提高金属矿品位,并实现氯化产物的分级收集,实现低品位金属矿或共生矿的综合利用,是一种有效的金属矿处理方法。固体氯化剂焙烧金属矿还表现出较强的选择性:处理硫化矿时能够实现对锌、铅等金属氯化而不与铁反应;处理钛铁矿时优先将铁氯化挥发而保留矿中的钛。另外研究还发现,高温有利于氯化挥发反应的进行,但同时也会减弱氯化的选择性,因此控制合适的焙烧温度尤为重要。
2 冶金废料的回收冶金过程会产生大量的冶金渣、粉尘等废料,有价金属含量丰富可进行回收利用。常见的湿法处理工艺需要大量的酸、碱,甚至会造成二次污染,因此有学者对冶金废料进行氯化挥发处理研究。陈勇[29]、常耀超等[30]分别对焙烧氰化尾渣、高砷硫酸烧渣等冶金渣进行氯化焙烧处理,有效地挥发和收集其中的金、银等有价金属。丁剑[31]使用氯化挥发法综合处理含金高铁硫酸烧渣,实现铁金分离和炼铁杂质金属的脱除,达到废渣综合利用的目的。近年来氯化挥发工艺处理冶金废料的研究大量涌现,尤其在处理含锌废料及含铜废料方面,有了较好的冶金成果。
2.1 含锌废料水冶锌生产和钢铁冶炼过程中都会产生大量的含锌废料,其中铁的含量已达到炼铁原料的要求,若能回收利用将缓解铁矿石不足的压力[32]。废料中锌含量较多,大都以ZnO、ZnS和ZnFe2O4形式存在,有学者通过氯化挥发方式进行锌的贫化,并取得良好的冶金效果[33-34]。
MATSUURA H等[35]在Cl2-O2混合气体中研究某含锌废料中锌的氯化挥发行为,实验证明ZnO容易被氯化成ZnCl2,增大Cl2分压对氯化反应有利,但同时Fe2O3也会被氯化挥发。DE M G等[36]研究Cl2与ZnO的反应机理,认为反应的限制性环节是孔隙扩散和化学反应混合控速。WANG L等[37]使用HCl气体处理含锌电炉粉尘,在HCl浓度不高的情况下,ZnO相对稳定,即便提高HCl分压也仅有少量的ZnCl2生成。JAAFAR I[38]使用NH4Cl处理含Zn转炉渣,750℃温度下氯化焙烧135 min,能回收97%的锌和30%的铁。
金属氧化物与1mol Cl2反应生成金属氯化物的标准生成吉布斯自由能曲线见图 1,从图中可知,在一段温度范围内,CaCl2和NaCl的吉布斯生成自由能都小于ZnCl2、FeCl2、FeCl3、PbCl2的吉布斯生成自由能[39]。郭婷[40]计算得到ZnCl2、CaCl2、NaCl等金属氯化物在400~2400K 的蒸气压,认为采用CaCl2和NaCl等进行锌的氯化性理论上是可行的,并通过实验实现锌的氯化挥发,达到锌、铁分离的目的。
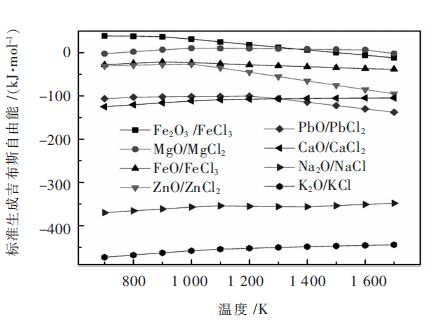 |
| 图 1 金属氯化物的标准生成吉布斯自由能曲线[39] Fig. 1 Standard gibbs free energy of metal chlorides |
胡晓军等[41-43]研究含锌废料氯化焙烧过程中锌的氯化挥发机理,实验表明体系中的ZnO与CaCl2反应并以ZnCl2的形式挥发,体系符合未反应核模型,化学反应是控速环节。实验发现在973K~1073K温度区间内ZnCl2挥发量远大于PbCl2,提高氧分压有利于加速ZnCl2的挥发,且对PbCl2的挥发影响又小,这表明可以对锌、铅等进行选择性氯化。王楠等[44-45]使用固体氯化剂焙烧处理含锌废料发现:在焙烧过程中SiO2、CaO和Fe3O4能促进ZnO、ZnS的氯化挥发,而SiO2、CaO、Al2O3和MgO不利于ZnFe2O4发生氯化反应。
氯化焙烧法处理含锌废料的机理研究较为深入,加入固体氯化剂能很好的对锌、铅等金属进行氯化挥发,比气态氯化剂更能实现金属的选择性氯化和分离。另外,铁以氧化物或钙、铁复合氧化物的形式稳定地保留在残余试样中,处理后的废料成分能达到炼铁原料的要求。
2.2 含铜渣火法炼铜已经积累大量的铜渣,由于渣中的有价金属含量较高,可以考虑进行回收[46-47]。文献表明铜渣中铁含量最高,主要以Fe2SiO4和Fe3O4形式存在,还有少量的Cu2S和Cu2O等含铜物相[48]。以炼铁原料的方式回收铜渣则必须对铜进行贫化,很多学者对铜渣的氯化处理做了大量研究[49-51]。
BRANISLAV R.等[52]研究O2气氛下用CaCl2氯化Cu2S的反应机理,通过热力学分析和实验结果表明,提高温度可以有效地提高Cu2S的氯化挥发率,又进一步计算得出反应活化能,认为铜氯化物的扩散是限制性环节。张仁杰[53]使用CaCl2对铜渣进行氯化焙烧实验,并添加FeSO4促进CaCl2离解产生氯化性气体。试验表明FeSO4会在高温下分解成Fe2O3、SO2和O2,SO2结合离解产物CaO,同时O2提高体系氧分压,共同促进CaCl2离解反应正向进行。
金属氧化物发生氯化反应的难易度不同[54],研究发现CuO、Cu2S和FeO容易被氯化,Fe2O3、Fe3O4和Fe2SiO4较难发生氯化反应,SiO2、CaO和Al2O3则几乎不发生氯化反应。因此,对回收铁的冶金渣进行氯化处理时,必须保证体系中有一定的氧势,尽量使铁以高价态氧化物存在,避免或减少含铁物相发生氯化反应。在O2气氛下对含铜渣进行氯化焙烧,通过控制焙烧温、氧分压和CaCl2添加量等,将含铜物相氯化挥发出来,有效地分离和回收铁和铜。
3 粗金属的精炼通过金属废料或多金属矿冶炼得到的粗金属中杂质金属含量较多,普通的精炼工艺很难进行处理,有学者对粗金属的氯化精炼进行研究,并取得很好的精炼效果。氯化精炼工艺一般用于金属熔体中的有害杂质金属的去除,首先对粗金属中杂质金属进行氯化,再控制条件使杂质金属的氯化物挥发出来。
3.1 粗铜的精炼铜冶炼原料加入的废铜比例逐年上升,导致粗铜中的杂质金属含量偏多,电解精炼后仍有较多含量的锑,严重影响铜的导电性和其他性能[55]。根据前人大量的研究报道可知,杂质金属一般均匀分散在铜液中,因此氯化精炼所加入的氯化剂需要进入粗铜内部发生反应;或者在铜液表面进行反应,使杂质金属氯化并扩散到渣中再挥发去除。
CUI Y等人[56]研究使用CuCl去除粗铜中的金属锑,在1423K温度下进行两组试验,第一组向铜液中加入CuCl-CaO复合溶剂,第二组在Ar气中使用CuCl-Na2CO3复合溶剂处理。实验进行十五分钟后,铜液中锑的去除率均在99%以上,达到粗铜精炼的目的。根据两种不同的复合溶剂的实验结果可见:Na2CO3的分解需要吸收大量的热,对锑的氯化速率较慢,对坩埚的腐蚀性较大,并且释放出大量的烟气,因此使用CuCl-CaO复合溶剂对锑的氯化效果更好。
3.2 粗钢的精炼炼铁原料和废钢带入的杂质金属对钢铁冶金不利,例如碱金属易在高炉中结瘤,铜会导致钢材的热脆。钢铁冶炼中除铜工艺还没有完善,工业中也没有量化应用[10],许多学者对粗钢的氯化精炼进行了大量的研究。
茅洪祥等[57]对固-气反应脱铜进行热力学分析,然后使用89%空气-11%HCl混合气体处理废钢,脱铜率达到74%,而铁损仅为1.8%,并且可以从产物CuCl2中回收95%的铜。松丸幸司等人[58]在高温下进行O2-Cl2混合气体对废钢脱铜的实验,通过热力学分析和实验检测,发现Cl2与废钢中的铜发生反应生成CuCl,认为铜的氯化物向边界层的扩散是控速环节。由上述废钢的氯化焙烧脱铜研究可知,通过控制实验温度和体系气氛使铜氯化物挥发,而铁并没有很大损失,故采用氯化精炼脱除钢液中铜理论上也是可行的。
胡晓军等[59-60]对铁、铜的选择性氯化反应的热力学进行分析,使用FeO-SiO2-CaCl2渣系对钢液中的铜进行选择性氯化挥发。实验表明:酸性氧化物SiO2能显著提高铜的挥发去除率,并且有效抑制铁的损失;渣的氧化性是CaCl2发生氯化反应的重要条件,高氧化性的渣系对铜的选择性氯化效果更好。
SASABE M等[61]使用FeCl2处理碳饱和铁水,旨在将铁水中的铜氯化挥发除去,实验计算铁水中铜与FeCl2压力(1 atm)的平衡时CuCl的分压,并使用小型设备进行试验。实验表明,利用氮气做载气将FeCl2粉末喷吹到碳饱和铁水中,能有效地对铜进行氯化挥发,将铜含量从0.7%降低到0.1%,达到铁水精炼的目的。该实验还研究温度、FeCl2量对反应速度的影响,考察氯化剂的利用率,分析反应的控制环节,并确定反应机理,认为反应的限制性环节极有可能是铁水中铜的扩散过程。
综上可知,氯化精炼处理废钢和铁水均能取得很好的效果,不同的氯化剂冶金效果各有优劣。使用气体氯化剂HCl和Cl2进行氯化精炼,反应机理较为清晰,但是还限于实验阶段,进行工业化生产需要考虑设备寿命和人员安全等因素。固体氯化剂CaCl2、FeCl2对铜有很强的选择性,且相比于气体氯化剂腐蚀性更小,因此固体氯化剂是粗钢精炼的选择之一。
4 氯化挥发机理研究进展综合大量的氯化挥发研究可知,使用的氯化剂有气体和固体两种,应该根据处理对象的特点选择合适的氯化剂。氯化挥发的体系可以分为三种:固-气、固-固和固-液,各体系的氯化挥发机理如下:
4.1 固-气体系氯化挥发气体氯化剂直接参与氯化反应,有利于氯化挥发机理的研究。Cl2的氧化性极强,与金属Me及其化合物一般会直接发生反应:
| $\begin{matrix} Me+C{{l}_{2}}=MeC{{l}_{2}} \\ MeS+C{{l}_{2}}=MeC{{l}_{2}}+S \\ MeO+C{{l}_{2}}=MeC{{l}_{2}}+1/2\text{ }{{O}_{2}} \\ \end{matrix}$ |
De Micco G等[62]建立气—固反应模型,在Ar-Cl2气氛进行纯铜的Cl2氯化实验,通过对反应后的铜氯化物凝聚相进行SEM-EDS分析,推算出铜的氯化反应机理:反应初期,铜的氯化物主要为CuCl2及少量CuCl;随着反应温度升高,CuCl2分解产生CuCl;温度继续升高,产物中主要是CuCl;但是铜的直接氯化是主要原因。
张光德等[63-64]使用O2-Cl2对纯铜进行氯化焙烧处理,该研究确定铜的氯化反应限制性环节是由气体扩散传质和界面化学反应联合控制。实验表明铜的氯化是一个以O2为催化剂的反应过程,即铜先与O2反应生成CuO,再与Cl2反应生成CuCl(l),最后聚合成Cu3Cl3(g)。聚合物的蒸汽压较高,有利于铜的氯化挥发。
由上述研究可见,使用Cl2对含铜物相的氯化焙烧过程中,反应起始温度一般较低,但反应机理较为复杂,在不同温度下铜的氯化产物不同,化合价也不确定。已知铜的氯化物有CuCl2、CuCl和Cu3Cl3,但具体以何种形式挥发还没有定论,有待进一步研究。
高温且有水蒸气存在的情况下,氯化剂常以HCl方式参与反应[65],但HCl氯化能力会随着温度的升高而减弱,如FeO、NiO等只能在较低温度下才能被HCl氯化,因此氯化焙烧过程中要避免生成的金属氯化物发生水解反应,体系中要保持一个较高的HCl/H2O值。
| $\begin{matrix} Me+2\text{ }HCl=MeC{{l}_{2}}+{{H}_{2}} \\ MeS+2\text{ }HCl=MeC{{l}_{2}}+{{H}_{2}}S \\ MeO+2\text{ }HCl=MeC{{l}_{2}}+{{H}_{2}}O \\ \end{matrix}$ |
气体氯化剂的化学活性较强,反应动力学条件较好,反应机理较为清楚,对金属的氯化挥发效果显著。上述研究中但是选择行性氯化反应受氧势影响,需要根据所氯化金属的特性来控制氧势。只是工业生产中需要考虑其强腐蚀性和毒性,对操作人员和生产设备都有较高的要求。
4.2 固-固体系氯化挥发固体氯化剂的来源广、腐蚀小,且具有很好的选择性氯化效果,是工业上常用的氯化剂。固体氯化剂RCl2一般用于氧化物MeO的焙烧处理,反应总方程式一般可以写成:
| $MeO+RC{{l}_{2}}=MeC{{l}_{2}}+RO$ |
固体氯化剂与金属矿的反应机理较为复杂,通常需要氧化气氛和高温等条件,并借助自身分解出的Cl2或HCl参与氯化反应。例如使用CaCl2焙烧Cu2S需要SO2、SiO2等结合产物CaO生成更稳定的盐类,促进其分解产生Cl2再与含铜物相发生反应[52, 66]。
| $\begin{matrix} CaC{{l}_{2}}+{{O}_{2}}+S{{O}_{2}}=CaS{{O}_{4}}+C{{l}_{2}} \\ CaC{{l}_{2}}+1/2\text{ }{{O}_{2}}+Si{{O}_{2}}=CaSi{{O}_{3}}+C{{l}_{2}} \\ C{{u}_{2}}S+1.5\text{ }C{{l}_{2}}+{{O}_{2}}=CuCl+CuC{{l}_{2}}+S{{O}_{2}} \\ \end{matrix}$ |
另外有研究表明在较低的温度下SO2与Na2O等分解产物的结合力更强[67],因为气态的SO2的反应动力学条件良好,二者反应更容易生成为热力学上更稳定的硫酸盐,从而促进固体氯化剂分解产生氯气。由于固态氯化剂CaCl2等来源较广泛,焙烧处理中具有能耗少、污染小等优点,是工业生产应用工艺重点考虑的冶金方法。
4.3 固-液体系氯化挥发CUI Y等[56]研究并讨论铜液中锑的氯化反应机理,认为CuCl-CaO复合溶剂加入后,在渣中反应生成Cu2O,增加了铜液中的氧含量;铜液中的锑被氧化成Sb2O3进入渣中,与CuCl反应生成SbCl3挥发。
| $\begin{matrix} 2\left( CuCl \right)+\left( CaO \right)=\left( C{{u}_{2}}O \right)+\left( CaC{{l}_{2}} \right) \\ \left( C{{u}_{2}}O \right)=2\left[ Cu \right]+\left[ O \right] \\ 2\left[ Sb \right]+3\left[ O \right]=\left( S{{b}_{2}}{{O}_{3}} \right) \\ \left( S{{b}_{2}}{{O}_{3}} \right)+6\left( CuCl \right)=2SbC{{l}_{3}}\left( g \right)+3\left( C{{u}_{2}}O \right) \\ \end{matrix}$ |
胡晓军等[60]使用FeO-SiO2-CaCl2混合渣处理钢水,认为氧化性渣能将钢水中的铜氧化进入到熔渣,再和熔渣中的CaCl2进行反应生成CuCl挥发。氯化挥发机理如下:
| $\begin{matrix} \left( FeO \right)=\left[ Fe \right]+\left[ O \right] \\ 2\left[ Cu \right]+\left[ O \right]=\left( C{{u}_{2}}O \right) \\ \left( C{{u}_{2}}O \right)+\left( CaC{{l}_{2}} \right)=CuCl\left( g \right)+\left( CaO \right) \\ \end{matrix}$ |
SASABE M等[61]通入FeCl2处理铁水,认为FeCl2首先在铁水中气化,然后与铁水中的铜接触发生反应,将铜转变成低沸点的铜盐CuCl、CuCl2或Cu3Cl3。铜的氯化物的蒸气压比FeCl2高,更容易从钢水中挥发。使用FeCl2不会给铁液带入二次夹杂,未反应的FeCl2可经分离后循环利用,生成CuCl(g)则可以回收铜,是一种值得考虑的钢液脱铜方案。
| $2\left[ Cu \right]+FeC{{l}_{2}}\left( g \right)=\left[ Fe \right]+2CuCl\left( g \right)$ |
本文从金属矿处理、金属废料回收和粗金属精炼三个方面介绍氯化挥发的应用及研究进展,通过大量的实验研究及工业生产应用可知,氯化挥发工艺对原料适应性强。对比和分析不同种类氯化剂各的优点,气体氯化剂Cl2、HCl能直接参与氯化反应,有利于氯化挥发机理的研究;固体氯化剂能实现金属的选择性氯化,在氯化焙烧或氯化精炼方面收效明显。总结冶金学者对氯化挥发机理的研究,并归纳在“固-气”、“固-固”和“固-液”三种体系,为氯化挥发体系和氯化剂的选择提供参考。
氯化挥发机理研究非常成熟,在工业生产中也取得了良好的冶金效果,是一种值得重视的冶金手段,可用于选择性去除杂质金属、富集有价金属等方面。随着化工中耐蚀设备的迅速发展,使得氯化挥发十分具有工业化的前景。目前氯化挥发仍存在不足,为进一步完善氯化挥发工艺,仍需要在以下方面进行改进:第一,对未有定论的反应机理进一步探索,完善氯化挥发理论。第二,寻找成本低、来源广的氯化剂,并提高氯化剂利用率。第三,完善氯化挥发工艺,如发展耐蚀设备和氯化产物的回收处理等。
| [1] | 中南矿冶学院冶金研究室. 氯化冶金[M]. 北京: 冶金工业出版社 , 1978: 93. |
| [2] |
CHEN D, ZHU D.Q, CHEN Y. Preparation of prereduced pellets by pyrite cinder containing nonferrous metals with high temperature chloridizing-reduction roasting technology[J].
ISIJ International, 2014, 54(10): 2162–2168. DOI: 10.2355/isijinternational.54.2162. |
| [3] |
CHU G, ZHAO S J, YANG T Z. Extraction of nickel from molybdenum leaching residue of metalliferous black shale by segregation roasting and acid leaching[J].
Journal of Central South University, 2012, 19(19): 340–346. |
| [4] |
LIU W R, LI X H, HU Q Y, et al. Pretreatment study on chloridizing segregation and magnetic separation of low-grade nickel laterites[J].
Transactions of Nonferrous Metals Society of China, 2010, 20(1): 82–86. DOI: 10.1016/S1003-6326(09)60101-1. |
| [5] | 李淑梅, 张福生, 丛自范, 等. 固体氯化铅直接低温熔炼生产粗铅的研究[J]. 有色矿冶, 2011, 27(2): 28–30. |
| [6] |
TANINOUCHI Y, HAMANAKA Y, OKABE T H. Reaction-mediator-based chlorination for the recycling of titanium metal scrap utilizing chloride waste[J].
Materials Transactions, 2015, 56(1): 1–9. DOI: 10.2320/matertrans.M-M2014838. |
| [7] |
HE Y C, XU Z M. Recycling gold and copper from waste printed circuit boards using chlorination process[J].
RSC Advances, 2015, 5(12): 8957–8964. DOI: 10.1039/C4RA16231E. |
| [8] | 李学鹏, 尹久发. 氯化挥发回收含锡尾矿中的有价金属[J]. 有色金属(冶炼部分), 2012(9): 11–14. |
| [9] | 陈正奎. 氯化法在冶金分离富集工艺中的应用进展及展望[J]. 湖南有色金属, 2014(6): 29–33. |
| [10] | 朱立全, 胡晓军, 姜平国, 等. 钢铁冶金过程脱铜方法研究的发展和现状[J]. 钢铁研究学报, 2014, 26(8): 1–7. |
| [11] | 罗骏, 李光辉, 饶明军, 等. 煤系硫铁矿浮选尾矿热化学活化脱硅制备铝精矿[J]. 中国有色金属学报, 2013, 23(12): 3470–3477. |
| [12] | 赵刚.难选锡中矿氯化挥发及氧化固结的应用研究[D].中南工业大学,2000. http://d.wanfangdata.com.cn/Thesis_Y358002.aspx |
| [13] | 李金辉, 李洋洋, 郑顺, 等. 红土镍矿冶金综述[J]. 有色金属科学与工程, 2015, 6(1): 35–40. |
| [14] | 程瑞学. 锡中矿氯化冶金的微观机理[J]. 有色金属:冶炼部分, 1984(1). |
| [15] | 徐远志. 改良西门子法制备工艺及其生产技术现状[J]. 云南冶金, 2011, 40(1): 52–55. |
| [16] | 解志锋, 艾光华, 严华山, 等. 某高铁铜硫矿石的选矿试验工艺研究[J]. 有色金属科学与工程, 2014, 5(5): 135–140. |
| [17] | 叶雪均, 刘子帅, 胡城, 等. 铜锌硫化矿分离技术研究及进展[J]. 有色金属科学与工程, 2013, 3(6): 44–50. |
| [18] | 赵留成, 孙春宝, 张舒婷, 等. 主要载金硫化物黄铁矿的热分解动力学特性[J]. 中国有色金属学报, 2015, 25(8): 2212–2217. |
| [19] | 黄万抚, 袁亚君. 印尼进口某难选铁铜硫多金属矿综合回收研究[J]. 有色金属科学与工程, 2014, 5(5): 111–116. |
| [20] | 李小斌, 李重洋, 齐天贵, 等. 拜耳法高温溶出条件下黄铁矿的反应行为[J]. 中国有色金属学报, 2013(3): 829–835. |
| [21] |
BAYER G, WIEDEMANN H G. Thermal analysis of chalcopyrite roasting reactions[J].
Thermochimica acta, 1992, 198(2): 303–312. DOI: 10.1016/0040-6031(92)85087-C. |
| [22] | 郭持皓, 徐晓辉, 常耀超, 等. 含金高砷高硫精矿综合回收有价金属[J]. 有色金属 (冶炼部分), 2015(8): 46–49. |
| [23] | 常耀超, 徐晓辉, 王云. 硫铁矿烧渣氯化焙烧扩大试验[J]. 有色金属 (冶炼部分), 2013(10): 1–3. |
| [24] |
YUAN Z F, ZHU Y Q, XI L, et al. Preparation of TiCl4 with multistage series combined fluidized bed[J].
Transactions of Nonferrous Metals Society of China, 2013, 23(1): 283–288. DOI: 10.1016/S1003-6326(13)62458-9. |
| [25] | 魏佩杰, 杨正蕾. 简议氯化法生产粗四氯化钛[J]. 有色金属设计, 2014, 41(1): 45–48. |
| [26] |
KANG J, OKABE T H. Thermodynamic consideration of the removal of iron from titanium ore by selective chlorination[J].
Metallurgical and Materials Transactions B, 2014, 45(4): 1260–1271. DOI: 10.1007/s11663-014-0061-8. |
| [27] |
KANG J, OKABE T H. Upgrading titanium ore through selective chlorination using calcium chloride[J].
Metallurgical and Materials Transactions B, 2013, 44(3): 516–527. DOI: 10.1007/s11663-013-9818-8. |
| [28] |
KANG J, OKABE T H. Removal of iron from titanium ore through selective chlorination using magnesium chloride[J].
Materials Transactions, 2013, 54(8): 1444–1453. DOI: 10.2320/matertrans.M-M2013810. |
| [29] | 陈勇. 焙烧氰化尾渣高温氯化提金研究[J]. 中国资源综合利用, 2015, 33(10): 22–25. |
| [30] | 常耀超, 徐晓辉, 王云. 高砷硫酸烧渣脱砷及高温氯化回收金银[J]. 有色金属: 冶炼部分, 2015(6): 46–49. |
| [31] | 丁剑. 氯化挥发综合处理含金高铁硫酸烧渣的研究[D]. 北京: 中国科学院研究生院, 2012. |
| [32] | 黄万抚, 王金敏, 文金磊, 等. 快速浮选提高锌渣中银回收率的试验研究[J]. 有色金属科学与工程, 2015, 6(5): 85–90. |
| [33] |
MATSUURA H, HAMANO T, TSUKIHASHI F. Removal of Zn and Pb from Fe2O3-ZnFe2O4-ZnO-PbO mixture by selective chlorination and evaporation reactions[J].
ISIJ International, 2006, 46(8): 1113–1119. DOI: 10.2355/isijinternational.46.1113. |
| [34] |
SANTOS F, BROCCHI E, ARAúJO V, et al. Behavior of Zn and Fe content in electric arc furnace dust as submitted to chlorination methods[J].
Metallurgical and Materials Transactions B, 2015, 46(4): 1729–1741. DOI: 10.1007/s11663-015-0347-5. |
| [35] |
MATSUURA H, YAJIMA K, TSUKIHASHI F. Chlorination and evaporation behaviours of zinc and lead at chlorinating and oxidising atmosphere[J].
Mineral Processing and Extractive Metallurgy, 2011, 120(4): 235–239. DOI: 10.1179/1743285511Y.0000000005. |
| [36] |
DE M G, FOUGA G G, BOHé A E. Chlorination of zinc oxide between 723 and 973 K[J].
Metallurgical and Materials Transactions B, 2007, 38(6): 853–862. DOI: 10.1007/s11663-007-9089-3. |
| [37] | WANG L, JIN Y Y, LI R D. Modeling of Zn migration during the Co-processing of MSWI fly ash with cement kiln[C]. //The Fifth International Conference on Waste Management and Technology. 2010: 559-564. |
| [38] | JAAFAR I. Chlorination for the removal of zinc from Basic Oxygen Steelmaking (BOS) by-product[D]. Wales: Institute of Sustainability and Environment, School of Engineering, Cardiff University, 2014. |
| [39] | (土耳其)伊赫桑?巴伦主编. 纯物质热化学数据手册[M]. 北京: 科学出版社 , 2003. |
| [40] | 郭婷. ZnO-Fe2O3体系选择性氯化分离行为的研究[D]. 北京: 北京科技大学, 2010. http://cpfd.cnki.com.cn/Article/CPFDTOTAL-ZGYY201004001084.htm |
| [41] |
WANG C G, HU X J, MATSUURA H, et al. Evaporation kinetics of the molten PbCl2-ZnCl2 system from 973 to 1073 K[J].
ISIJ international, 2007, 47(3): 370–376. DOI: 10.2355/isijinternational.47.370. |
| [42] |
GUO T, HU X J, MATSUURA H, et al. Kinetics of Zn removal from ZnO-Fe2O3-CaCl2 system[J].
ISIJ international, 2010, 50(8): 1084–1088. DOI: 10.2355/isijinternational.50.1084. |
| [43] | 郭婷, 胡晓军, 侯新梅, 等. ZnFe2O4与CaCl2氯化反应机理[J]. 北京科技大学学报, 2011, 33(4): 474–478. |
| [44] | 王楠, 邹宗树, 山口周. 垃圾焚烧灰渣熔融处理重金属氯化-挥发反应分[J]. 东北大学学报(自然科学版), 2005, 26(9): 874–877. |
| [45] |
ZHU D Q, CHEN D, PAN J, et al. Chlorination behaviors of zinc phases by calcium chloride in high temperature oxidizing-chloridizing roasting[J].
ISIJ international, 2011, 51(11): 1773–1777. DOI: 10.2355/isijinternational.51.1773. |
| [46] | 刘瑜, 吴彩斌, 雷存友, 等. 从冶炼渣选铜尾矿中综合回收铁新工艺研究[J]. 有色金属科学与工程, 2014, 5(5): 141–144. |
| [47] | 王云, 朱荣, 郭亚光, 等. 铜渣还原磁选工艺实验研究[J]. 有色金属科学与工程, 2014, 5(5): 61–67. |
| [48] | 李磊, 王华, 胡建杭. 铜渣熔融还原过程中硫的行为特征[J]. 有色金属科学与工程, 2014, 5(5): 18–22. |
| [49] | 李磊, 胡建杭, 魏永刚, 等. 铜渣中铜的回收工艺及新技术[J]. 材料导报A: 综述篇, 2013, 27(6): 21–26. |
| [50] | 赵洁婷, 李伯超. 氯化焙烧法分离铜渣中铁铜的可行性分析[J]. 山西冶金, 2014, 37(5): 8–10. |
| [51] | 赵洁婷. CuS 氯化焙烧行为初探[J]. 黑龙江冶金, 2014, 34(4): 24–25. |
| [52] |
MARKOVIC B R, SOKIC M D, MATKOVIC V L, et al. Kinetics of the chlorination of copper(I) sulphide by calcium chloride in the presence of oxygen[J].
Journal of Chemistry and Chemical Engineering, 2011, 5(3): 264–268. |
| [53] | 张仁杰, 李磊, 韩文朝. 氯化焙烧法回收铜渣中铜的热力学研究[J]. 工业加热, 2014, 43(1): 4–9. |
| [54] | 朱立全. Fe、Cu氧化物体系的选择性氯化分离[D]. 北京: 北京科技大学冶金与生态工程学院, 2013. |
| [55] |
CUI Y, MATSUURA H, HAMANO T, et al. Removal of antimony from liquid copper by using CuCl-Na2CO3 fluxes at 1423 K[J].
ISIJ international, 2008, 48(1): 23–27. DOI: 10.2355/isijinternational.48.23. |
| [56] |
CUI Y, MATSUURA H, HAMANO T, et al. Removal and recycling of antimony from liquid copper by using CuCl-CaO fluxes at 1423 K[J].
Metallurgical and Materials Transactions B, 2007, 38(3): 485–489. DOI: 10.1007/s11663-007-9045-2. |
| [57] | 茅洪祥, 朱宏利. 固体废钢脱铜新装置[J]. 湖南冶金, 2001(4): 39–41. |
| [58] | 松丸幸司, 須佐匡裕, 永田和宏. 塩素-酸素混合ガスよるによる鉄スタうヅプからの銅の選択除去[J]. 鐵と鋼: 日本鐡鋼協會々誌, 1996, 82(10): 799–804. |
| [59] |
HU X J, JIANG P G, YAN Z, et al. Selective chlorination reaction of Cu2O and FeO mixture by CaCl2[J].
ISIJ International, 2013, 53(3): 541–543. DOI: 10.2355/isijinternational.53.541. |
| [60] |
HU X J, YAN Z, JIANG P G, et al. Removal of copper from molten steel using FeO-SiO2-CaCl2 flux[J].
ISIJ International, 2013, 53(5): 920–922. DOI: 10.2355/isijinternational.53.920. |
| [61] |
SASABE M, HARADA E, YAMASHITA S. Removal of copper from carbon saturated molten iron by using FeCl2[J].
Journal of the Iron and Steel Institute of Japan-Tetsu to Hagane, 1996, 82(2): 129–134. |
| [62] |
DE M G, BOHé A E, PASQUEVICH D M. A thermogravimetric study of copper chlorination[J].
Journal of alloys and compounds, 2007, 437(1): 351–359. |
| [63] | 张光德, 阎立懿, 解希元, 等. 氧化气氛下铜的氯化机理研究[J]. 钢铁研究, 2000(2): 25–27. |
| [64] | 张光德, 阎立懿, 解希元, 等. 氧化气氛下铜的氯化过程动力学分析[J]. 化工冶金, 2000, 21(3): 288–293. |
| [65] |
TANG J H, CHEN X, FEI Z Y, et al. HCl oxidation to recycle Cl2 over a Cu/Ce composite oxide catalyst. Part 1. Intrinsic Kinetic Study[J].
Industrial & Engineering Chemistry Research, 2013, 52(34): 11897–11903. |
| [66] |
LI L, WANG H, HU J H. Smelting chlorination method applied to removal of copper from copper slags[J].
Journal of Central South University, 2015, 22(1): 59–65. DOI: 10.1007/s11771-015-2494-x. |
| [67] | 孙进, 李清海, 李国岫, 等. 城市生活垃圾焚烧中NaCl迁移转化的实验和热力学平衡分析[J]. 中国电机工程学报, 2014, 34(2): 272–278. |
 2016, Vol. 7
2016, Vol. 7

