| 石油醚-甲醇提取茶油和茶皂素工艺研究 |
油茶籽枯饼是油茶籽压榨后的副产物,目前我国年产量约60余万t[1],油茶籽枯饼中含有5 %~8 %的残油,10 %~15 %的茶皂素[2],还含有多糖,蛋白,单宁,咖啡因等多种活性物质,具有经济价值[3-5]。然而,目前我国对油茶籽枯饼的利用并不充分,部分出口到东南亚国家,大部分作为燃料烧弃,浪费资源、污染环境。
油茶籽枯饼传统的利用方法[6-8]是用非极性溶剂提取油脂,再用热水或含水醇提取茶皂素。此法分两步提取,工艺复杂,生产周期长,能耗较高。这也是油茶籽枯饼在我国得不到充分利用的原因之一。为此,必须要寻找流程短、操作简单、能耗低的方法提取其中的茶油、茶皂素等有价物质[9-14],以改变我国油茶籽枯饼的利用现状。
混合溶剂法是采用非极性与极性溶剂联合使用提取油脂的一种方法,在工业中应用广泛,尤其采用烃-醇-水混合溶剂在提取植物油、棉酚、茶皂素方面效果较好。由于烷烃对植物油脂溶解力好,而短链醇类物质极性相对较大,含水醇溶液对棉酚、茶皂素、抗氧化性物质等水溶性物质有较好的溶解力,因此混合溶剂体系一步就能提取得到多种产品,缩短工艺流程,减少了烷烃的使用量,改善了传统提取工艺,使油茶籽枯饼得到充分开发与利用。
以油茶籽枯饼为原料,研究石油醚-甲醇提取茶油籽枯饼中的茶油和茶皂素的工艺,分析甲醇浓度、混合溶剂用量,烃醇质量比,萃取温度及萃取时间等因素对萃取效果的影响,确定最佳工艺参数,并通过检测手段分析粗茶油的性质,最后研究混合溶剂萃取茶油的机理。
1 实验 1.1 试剂与仪器油茶籽枯饼(江西省某榨油厂)。茶油(市售一级茶油),茶皂素,石油醚,甲醇,正己烷,无水碳酸钠,硫酸钠,浓硫酸,香草醛,冰乙酸,氢氧化钾,乙醚,无水乙醇,邻苯二甲酸氢钾,碘,碘化钾,硫代硫酸钠,淀粉,试剂均为AR。美国Agligent 6890 B型气相色谱仪,FID检测器,尤尼克(上海)UV/VIS 2802PCS紫外可见光分光光度计。
1.2 实验方法 1.2.1 茶皂素含量测定茶皂素标准曲线建立:采用浓硫酸-香草醛显色法测定茶皂素含量[15]。茶皂素与香草醛在564 nm波长处有特征吸收峰,测定该处不同浓度茶皂素溶液的吸光度,作标准曲线,见图 1。
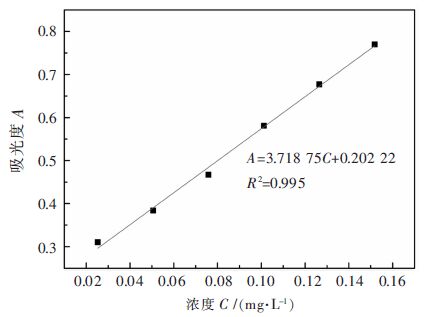 |
| 图 1 茶皂素标准曲线 Fig. 1 Standard curve of tea saponin |
茶皂素含量测定:实验提取粗茶皂素m (g),取其中m1 (g)粗茶皂素溶于80 %甲醇溶液定容到50 mL,取0.5 mL按上述方法测定其含量。则茶皂素得率计算公式如下:
| ${\text{茶皂素得率}}/\% = \frac{{\frac{m}{{{m_1}}} \times (100{\text{A - }}2{\text{0}}{\text{.2}})}}{{{\text{原料茶籽油枯饼质量}}}} \times 100{\text{ }}\% {\text{ }}$ |
油茶籽枯饼中粗茶油含量测定参见GB/T14488.1—2008;茶皂素含量测定采用70%甲醇提取,提取步骤参见GB/T14488.1—2008,提取后萃取液烘干得粗茶皂素,采用上述浓硫酸-香草醛法检测粗茶皂素含量。水分含量测定参见GB/T14489.1—2008。原料中粗茶油和茶皂素含量见表 1。
| 表1 油茶籽枯饼中粗茶油和茶皂素含量/(质量分数,%) Table 1 Content of crude camellia oil and tea saponin in camellia seed cake/(mass fraction,%) |
 |
| 点击放大 |
1.2.3 混合溶剂提取茶油和茶皂素工艺
将油茶籽枯饼粉碎,取粒径为0.25 mm颗粒100 g于三口烧瓶中,加入石油醚100 g、甲醇100 g和适量的水,调整搅拌速率50 r/min,50 ℃水浴加热萃取油茶籽枯饼中的茶油和茶皂素。90 min后趁热过滤,分离油茶籽饼渣和萃取液。油茶籽枯饼渣经2次萃取后,蒸馏脱溶得茶油籽枯饼渣,合并2次萃取液,移入分液漏斗冷却、静置分层,分液,下层为茶皂素浓缩液,干燥后得粗茶皂素,上层为混合油,水洗、蒸馏后得粗茶油。实验工艺流程见图 2。粗茶油得率、残油率计算公式如下:
| $\eqalign{ & 粗茶油得率/\% = \frac{{{\text{提取所得茶质量}}}}{{{\text{原料茶油籽枯饼质量}}}} \times 100{\text{ }}\% {\text{ }} \cr & 残油率/\% = \frac{{{\text{残余的油量}}}}{{{\text{茶油籽枯饼渣质量}}}} \times 100{\text{ }}\% {\text{ }} \cr} $ |
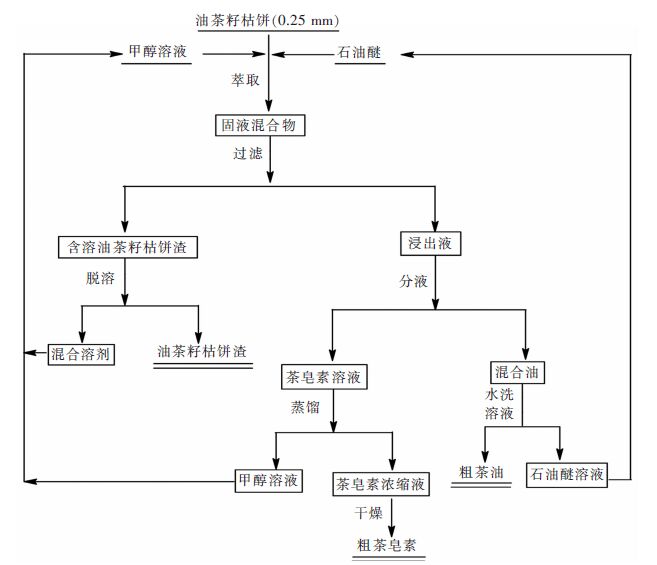 |
| 图 2 混合溶剂提取茶油和茶皂素工艺流程 Fig. 2 Process of mixed solvent extraction of camellia oil and tea saponin |
1.2.4 茶油检测
茶油酸值测定参见国家标准GB/T5530-2005。茶油皂化值测定参见国家标准GB/T5534-2008。茶油中碘值测定采用碘-乙醇溶液加成法测定[16-17]。茶油脂肪酸甲酯化参见国家标准GB/T17376-2008。
采用气相色谱仪检测茶油脂肪酸甲酯成分含量[18],气相色谱条件为:HP-5高效毛细管柱(30 m×0.32 mm×0.25 mm);色谱柱内载气流量1 mL/min;分流比50:1;进样量1 μL;汽化室温度280 ℃;FID检测器温度300 ℃;起始柱温45 ℃,保持1 min,以10 ℃/min升温速率升至175 ℃,保持2 min;以2 ℃/min速率升至210 ℃,保持5 min;以8 ℃/min速率升至280 ℃,保留5 min。
2 结果与讨论 2.1 石油醚-甲醇提取工艺研究 2.1.1 甲醇溶液浓度对提取效果的影响考察甲醇含水量对提取茶油和茶皂素效果的影响。实验甲醇浓度分别为100 %、95 %、90 %、85 %和80 %。从图 3中得出,随着甲醇浓度的升高,残油率降低,,而茶皂素得率也呈下降趋势。这是由于甲醇相中含水量增加,对茶皂素溶解力增加,茶皂素得率上升。当甲醇溶液浓度为80 %以下时,油茶籽枯饼颗粒吸水溶胀而变得胶黏,极易沉积在甲醇溶液中和瓶壁上,即使在搅拌下,石油醚与固体物接触效果也受到影响,减压抽滤困难。综合考虑,确定最佳甲醇溶液浓度为90 %。
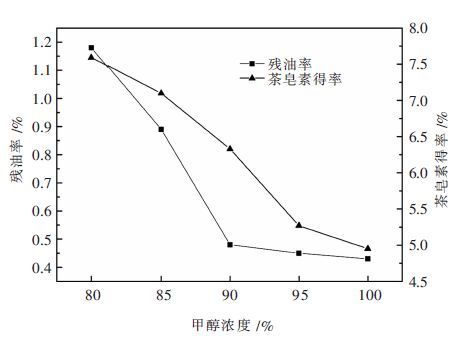 |
| 图 3 甲醇浓度对萃取效果的影响 Fig. 3 Effect of methanol concentration on extraction |
2.1.2 固液比对提取效果的影响
考察固液比对茶油和茶皂素提取效果的影响。固液比即是油茶籽枯饼与萃取溶剂之间的质量比,反映了提取溶剂用量对萃取效果的影响。实验固液比分别为1:1、1:1.5、1:2、1:2.5和1:3。从图 4得出,随着溶剂投入量的增加,粗茶油得率和茶皂素得率均呈上升趋势。这是由于溶剂量增加,溶剂对茶油和茶皂素溶解量增加,且茶油和茶皂素在两相中扩散速率加快,提取效果好。当固液比为1:1时,溶剂刚刚浸没固体颗粒,搅拌困难,浸出传质困难,提取效果差。当在1:1.5时,茶油得率显著上升,继续增加提取剂用量,茶油上升速率逐渐缓慢,这是由于石油醚相本身对茶油溶解能力很强,和茶油互溶,提取茶油效果好。95 %甲醇溶液对茶皂素溶解能力有限,因此溶剂量增加到1:2.5后其得率才逐渐趋于稳定。综合考虑最佳固液比为1:2.5。
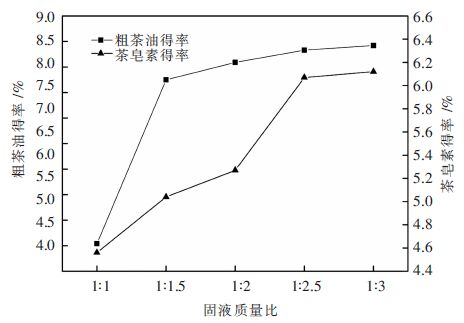 |
| 图 4 固液比对提取效果的影响 Fig. 4 Effect of solid liquid ratio on extraction efficiency |
2.1.3 萃取溶剂中烃醇配比对提取效果的影响
考察烃醇配比即溶剂中石油醚与甲醇溶液之间的质量比对茶油和茶皂素提取效果的影响。实验烃醇质量配比分别为1:3、1:2、1:1、2:1和3:1。从图 5得出,随着石油醚投入比例增加,粗茶油得率呈上升趋势、茶皂素得率呈下降趋势。这是由于甲醇溶液使用量减少,茶皂素在甲醇溶液中的饱和溶解量降低,且甲醇溶液与固体颗粒之间接触不充分,而不利于茶皂素的提取,尤其是烃醇配比在2:1以后茶皂素得率降低得更为明显。相反,石油醚比例增加,石油醚与油茶籽枯饼颗粒接触越充分,粗茶油得率呈上升趋势,但是到了1:1后,茶油得率增长速率变得缓慢,这可能是由于此时石油醚投入量已经较多,对茶油提取效果较好。综合考虑,确定提取溶剂最佳配比为1:1。
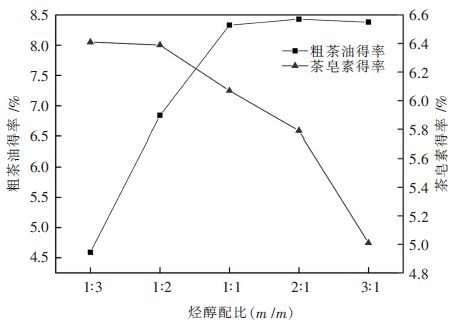 |
| 图 5 烃醇配比对提取效果的影响 Fig. 5 Effect of ratio between solvent on extraction efficiency |
2.1.4 萃取温度对提取效果的影响
考察温度对提取效果的影响。实验温度分别为20 ℃、30 ℃、40 ℃、50 ℃和60 ℃。从图 6得出,随着温度的升高,粗茶油得率和茶皂素得率总体上呈上升趋势。这是由于温度升高,溶剂对茶油和茶皂素的饱和度增加、萃取传质速率加快。当温度在60 ℃时,粗茶油得率下降而茶皂素得率略有所上升,这是由于此时石油醚部分气化沸腾,60 ℃石油醚产生微量气泡,在搅拌和茶皂素作用下气泡量增加,由于气泡的产生,影响了烷烃、甲醇与固体颗粒之间的接触,而不利于提取。综合考虑,确定最佳提取温度为50 ℃。
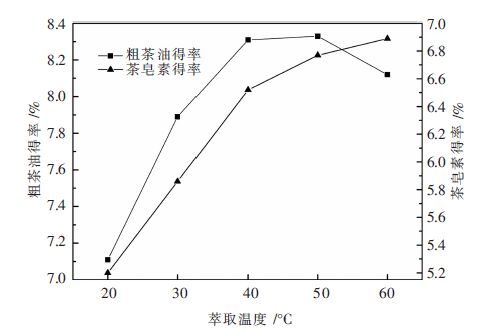 |
| 图 6 萃取温度对萃取效果的影响 Fig. 6 Effect of extraction temperature on extraction efficiency |
2.1.5 时间对提取效果的影响
考察时间对提取效果的影响。实验时间分别为30 min、60 min、90 min、120 min和150 min。从图 7得出,延长提取时间,粗茶油和茶皂素得率均上升。在60 min时,粗茶油得率已基本稳定,说明茶油在此时已达到平衡,而茶皂素得率虽未达到平衡,但是上升空间也已经较小。综合考虑,确定最佳萃取时间为90 min。
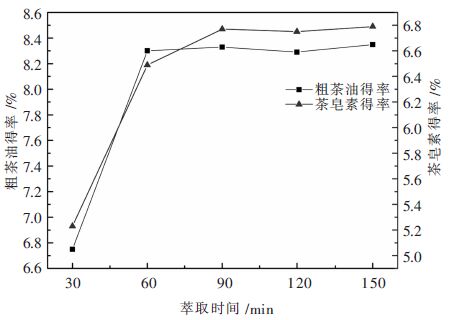 |
| 图 7 萃取时间对萃取效果的影响 Fig. 7 Effect of extraction time on extraction efficiency |
2.1.6 正交实验
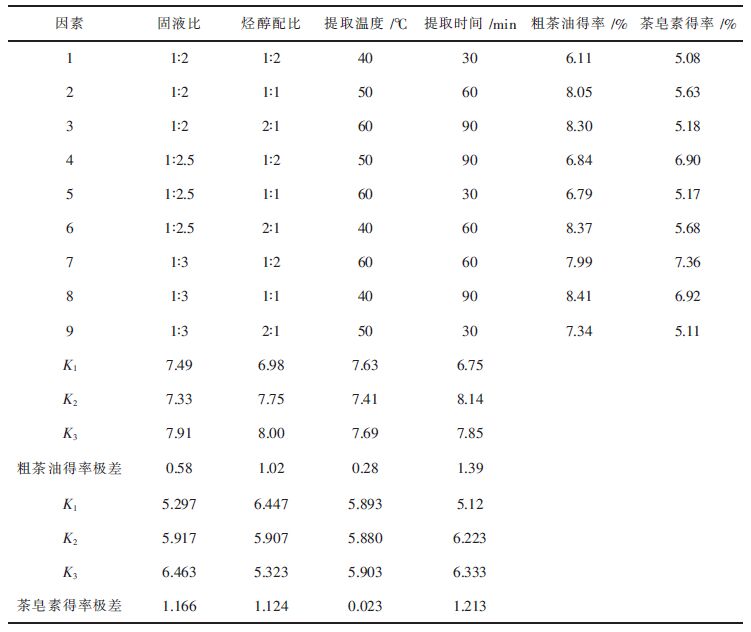
选取固液比(1:2、1:2.5、1:3)、烃醇配比(1:2、1:1、2:1)、提取温度(40 ℃、50 ℃、60 ℃)、提取时间(30 min、60 min、90 min)四因素进行正交实验,考察石油醚-甲醇萃取茶油和茶皂素最佳工艺。结果见表 2。
| 表2 正交实验结果和分析 Table 2 Results and analysis of orthogonal experiment |
 |
| 点击放大 |
从表 2得出,影响因素中对粗茶油得率影响大小顺序为:萃取时间>烃醇配比>固液比>萃取温度,正交实验表明粗茶油最大得率工艺参数为:固液比1:3,烃醇配比1:1,萃取温度40 ℃,萃取时间90 min,粗茶油最大得率为8.41 %。对茶皂素得率影响大小为:萃取时间>烃醇配比>固液比>萃取温度,茶皂素最大得率工艺参数为:固液比1:3,烃醇配比1:2,萃取温度60 ℃,萃取时间60 min,茶皂素最大得率为7.36 %。
比较上述工艺参数得出,粗茶油和茶皂素最大得率时的工艺参数并不一致,主要是溶剂配比造成的,石油醚用量大有利于茶油的提取,而不利于茶皂素的提取,相反则有利于茶皂素的提取。萃取温度对萃取效果影响较小,考虑到60 ℃时石油醚易沸腾,选取最佳温度为50 ℃。延长萃取时间有利于萃取效果,故选取最佳时间为90 min。因此,综合考虑本实验最佳工艺参数为:固液比1:3,烃醇配比1:1,萃取温度50 ℃,萃取时间90 min。在此条件下茶油和茶皂素得率实验结果见表 3。
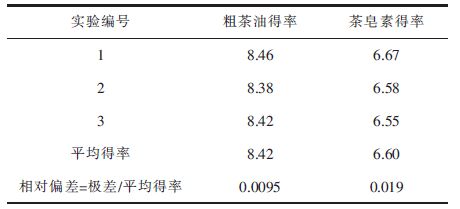
| 表3 最佳工艺条件下实验结果 Table 3 Experimental results under optimal process conditions |
 |
| 点击放大 |
从表 3得出,在此条件下实验重现性好。最佳工艺条件下粗茶油得率为8.42 %,和正交试验粗茶油最大得率相当,茶皂素得率为6.76 %,是正交试验茶皂素最大得率的89.67 %。因此,最佳工艺能较好的兼顾粗茶油最大得率工艺和茶皂素最大得率工艺。
2.2 粗茶油物理性质粗茶油颜色呈黄色,略带褐色,其物理性质见表 4。提取得到的粗茶油酸值较低,国家四级茶油要求酸值小于3 mg(KOH)/g,因此在后续精制工艺中采用萃取脱酸、物理脱酸等方法即可达到降低酸值的目的。
| 表4 粗茶油物理性质 Table 4 Physical properties of crude oil |
 |
| 点击放大 |
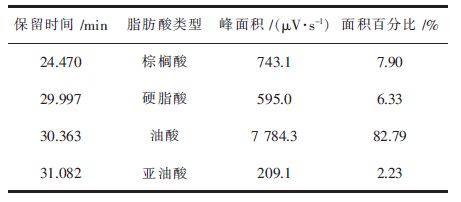
采用气相色谱仪检测粗茶油脂肪酸成分并用面积归一法计算各组分含量。粗茶油中含油酸82.79 %,不饱和脂肪酸85.02 %,具体结果如图 8和表 5所示。
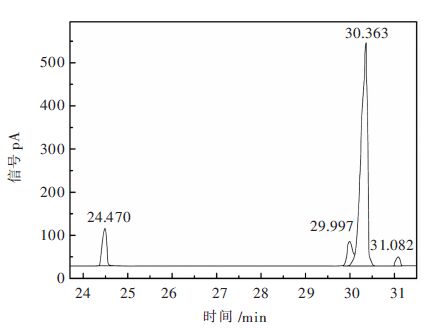 |
| 图 8 脂肪酸甲酯气相检测谱 Fig. 8 Gas chromatogram of fatty acid methyl ester |
| 表5 粗茶油脂肪酸含量 Table 5 Crude oil fatty acid content |
 |
| 点击放大 |
3 石油醚-甲醇溶液提取茶油和茶皂素理论基础
采用混合溶剂体系提取茶油目的是让茶油溶解在石油醚相中而不溶解在甲醇相中。因此混合体系必须保证三个条件,一是,温度在室温时石油醚-甲醇体系容易分层,否则茶油和茶皂素难以分离;二是,石油醚相体积大能与油料作物颗粒充分接触且对茶油溶解力强,否则油茶籽枯饼中油脂难以彻底提取出来;三是,甲醇相溶解茶油量要小,否则影响石油醚相中茶油的得率。
3.1 石油醚和甲醇之间的作用石油醚属于非极性溶剂,短链醇如甲醇、乙醇、异丙醇等偶极矩较大,属极性溶剂[19]。但是由于醇分子之间氢键的作用,醇分子聚合,羟基朝内聚合、疏水基团朝外排列,羟基极性受到一定程度掩蔽而表现出一定非极性。图 9为甲醇能形成的几种聚合体。
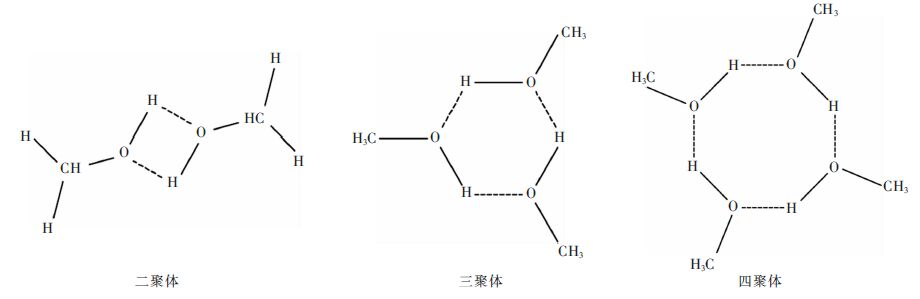 |
| 图 9 甲醇分子形成的聚合体 Fig. 9 Methanol molecule polymer |
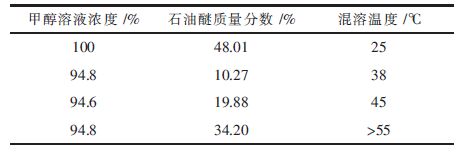
疏水烷烃碳链越长,碳链将羟基包裹在内部越充分,表现出的极性越弱,因此丙醇、乙醇等都能与石油醚混溶。甲醇由于碳链短,空间作用较弱,因而甲醇与石油醚只能部分混溶。从图 10得出,甲醇-石油醚二相区范围小。在石油醚质量分数为0.4时,体系温度降低到20 ℃~25 ℃时,甲醇-石油醚二元物还处于混溶状态,并未分层。研究表明增加水量可促进体系分层。从表 6看出,94.8 %甲醇与石油醚溶解性差,在常温下易分层。
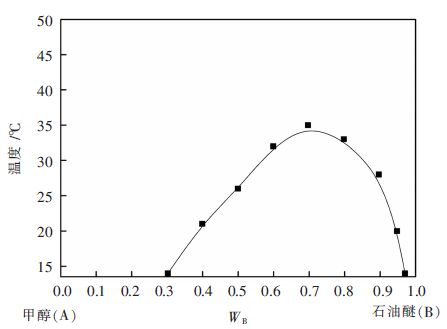 |
| 图 10 甲醇-石油醚温度随组分变化曲线 Fig. 10 Variation of temperature of methanol and petroleum ether with composition |
| 表6 含水甲醇与石油醚溶解情况 Table 6 Dissolution of aqueous methanol and petroleum ether |
 |
| 点击放大 |
3.2 石油醚相溶解茶油能力
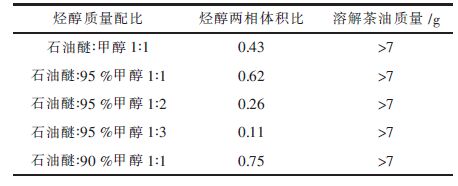
研究石油醚甲醇溶液对茶油溶解力,确保体系能够将油茶籽枯饼的茶油萃取彻底。实验测定石油醚-甲醇体系石油醚相对茶油的溶解力:混合适量甲醇溶液和石油醚,摇晃、微热、冷却静置。移取上层石油醚层4 g,逐步向甲醇相中滴加茶油,摇晃、记录茶油是否溶解。从表 7得出,石油醚相对茶油溶解力强,与茶油有混溶的趋势。石油醚与甲醇1:1混合时石油醚相体积量较大,理论上能够与颗粒充分接触。
| 表7 石油醚相溶解茶油量 Table 7 Amount of dissolved petroleum ether oil |
 |
| 点击放大 |
3.3 甲醇相溶解茶油能力
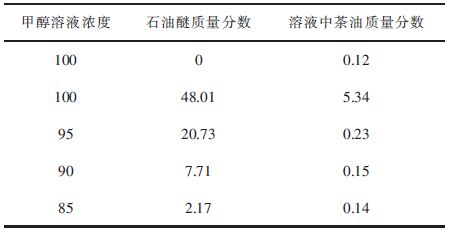
实验测定茶油在石油醚-甲醇溶液中的溶解量:取约20 g甲醇溶液,逐步向甲醇中滴加石油醚,摇晃、微热、冷却静置,直到刚好分层记录石油醚用量。移去上层石油醚层,逐步向下层甲醇相中滴加茶油,摇晃、微热、冷却静置,直到体系分层时记录茶油质量。表 8表明,25 ℃时甲醇能溶解约一倍量的石油醚,此时甲醇溶液中饱和茶油质量分数为5.34 %,不利于茶油的提取和分离。而当甲醇溶液为95 %时,茶油溶解量大大降低。含水量越多,甲醇溶解石油醚量越少,体系分层越容易,甲醇溶液中茶油溶解量也越少。这与水分子氢键作用参与甲醇分子形成聚合体而使甲醇分子极性增加有关。
| 表8 石油醚、茶油在甲醇溶液中的溶解量(25 ℃) Table 8 Dissolved quantity of petroleum ether,oil in methanol solution (25 ℃) |
 |
| 点击放大 |
石油醚甲醇溶液对茶油有一定溶解,甲醇溶液中石油醚含量越高茶油溶解量也越高,因此需要测定茶油在两相中的分配关系:分别取石油醚、甲醇溶液各20 g,再加约5 g茶油,混合均匀,静置、分液,分别蒸馏两相溶液得到溶解在其中的茶油。
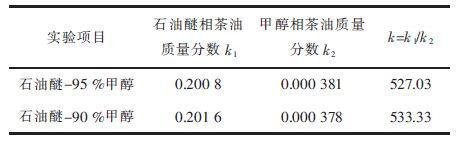
| 表9 茶油在石油醚-甲醇混合溶剂中的分配(25 ℃) Table 9 Oil distribution in mixed solvent of petroleum ether and methanol(25 ℃) |
 |
| 点击放大 |
从表 9得出,尽管石油醚甲醇溶液对茶油有一定溶解力,但是茶油在石油醚和甲醇两相中的分配系数大,茶油基本全部溶解在石油醚相中,甲醇相残留量很少但不影响茶油的得率。
综上所述,含水甲醇与石油醚易分层,甲醇相含油量少,石油醚相对茶油溶解力大,因此石油醚-甲醇溶液作为混合体系理论上是可以用来提取油茶籽枯饼中的茶油。
4 结论采用石油醚-甲醇溶液一步法同时提取油茶籽枯饼中茶油和茶皂素。原料油茶籽枯饼中含残油8.48 %、茶皂素13.21 %。研究考察甲醇浓度、混合溶剂用量,萃取溶剂之间配比,萃取温度、萃取时间对萃取效果的影响,正交实验确定最佳工艺条件:甲醇浓度90 %,固液比1:3,烃醇配比1:1,萃取温度50 ℃,萃取时间90 min,萃取两次,粗茶油得率为8.42 %,茶皂素得率为6.76 %。
提取所得产品粗茶油颜色呈黄色略带褐色,凝固点-2 ℃,酸值6.489 mg(KOH)/g,皂化值199.821 mg(KOH)/g,碘值78.616 g/(100g),气相色谱检测粗茶油中脂肪酸主要成分含量是油酸82.792 %,棕榈酸7.903 %,十八酸6.328 %,亚油酸2.224 %,其中不饱和脂肪酸占85.016 %。采用混合溶剂法提取粗茶油质量较好,有利于后续茶油精制工艺。
通过石油醚-甲醇溶液萃取的过程及机理分析可知,由于醇分子氢键的作用,甲醇溶液和石油醚是部分混溶,含水量越少、温度越高混溶程度越高,溶解茶油能力越强,有利于从油茶籽枯饼中溶解出茶油。但是茶油在石油醚相和甲醇相中分配系数大,25 ℃下茶油在石油醚-95 %甲醇分配系数达到527.03,甲醇相中的茶油最终全部转入到石油醚相中,茶油在两相中得到分离,蒸馏石油醚即得粗茶油。
| [1] | 费学谦. 油茶籽油加工业现状、问题及对策分析[J]. 食品工业科技, 2011, 32(10): 449–452. |
| [2] | 李梦丹, 杨伊磊, 陈力力, 等. 油茶籽粕的综合利用[J]. 粮食与油脂, 2016(1): 11–14. |
| [3] | 邓桂兰, 彭超英, 卢峰. 油茶饼粕的综合利用研究[J]. 现代食品科技, 2004, 41(3): 130–132. |
| [4] | 陈德军. 混合溶剂浸取油茶籽及大孔树脂纯化茶皂素的研究[D]. 南京:南京工业大学,2005. http://cdmd.cnki.com.cn/Article/CDMD-10291-2005129308.htm |
| [5] |
WEN T Y, TIAN G Y. Studies on the physicochemical properties, ptructure and antitumor activity of polysaccharide YhPS-1 from the root of cordalis yanhusuo wang[J].
Chinese Journal of Chemistry, 2006, 24(2): 235–239. DOI: 10.1002/(ISSN)1614-7065. |
| [6] | 余华峰. 短碳链醇作油脂浸出溶剂的工艺研究[D]. 武汉:武汉工业学院,2008. http://cdmd.cnki.com.cn/Article/CDMD-10496-2009151087.htm |
| [7] | 刘云. 油茶枯饼的混合溶剂浸提及固态发酵技术的研究[D]. 株洲:中南林学院,2001. http://cdmd.cnki.com.cn/Article/CDMD-10538-2001002893.htm |
| [8] | 梁华. 菜籽冷榨饼油脂萃取混合溶剂的筛选及制油工艺初探[D]. 武汉:华中农业大学,2008. http://cdmd.cnki.com.cn/Article/CDMD-10504-2010010831.htm |
| [9] | 刘北平, 全昌云, 黄小兵, 等. 响应面法优化醇法提取茶皂素工艺研究[J]. 中国油脂, 2013, 38(6): 84–86. |
| [10] | 李林检, 于伟伟, 刘光斌, 等. 茶皂素的提取及其在洗发香波中的应用[J]. 应用化工, 2016(1): 78–81. |
| [11] | 朱俊朋, 罗凡, 王超, 等. 水提-醇萃法提取油茶饼粕中茶皂素[J]. 食品工业, 2016(1). |
| [12] |
SEIED MAHDI P, S S H. Supercritical fluid extraction in plant essential and volatile oil analysis[J].
Journal of Chromatography A, 2007, 1–2: 2–24. |
| [13] | 曹建琦, 高洪乐, 高浩云. 混合溶剂一步法制备脱酚棉籽蛋白工艺的研究[J]. 粮食与食品工业, 2008, 15(6): 8–11. |
| [14] |
MAHMOOD T, L L D. Pilot-scale two-phase extraction of canola[J].
Journal of the American Oil Chemists Society, 1997, 74(3): 201–206. DOI: 10.1007/s11746-997-0124-y. |
| [15] | 陈莹, 刘松柏, 何良兴, 等. 油茶籽粕和茶皂素中皂苷的定量检测方法研究[J]. 中国粮油学报, 2012, 27(2): 105–111. |
| [16] | 苏有勇, 王华. 生物柴油检测技术[M]. 北京: 冶金工业出版社 , 2011. |
| [17] | 舒庆, 余长林, 熊道陵. 生物柴油科学与技术[M]. 北京: 冶金工业出版社 , 2012. |
| [18] | 李昌模, 王玉倩, 张虹. 食用油中脂肪酸检测方法的比较研究[J]. 粮油食品科技, 2013, 21(4): 74–77. |
| [19] | 曾新安, 杨星. 不同浓度下乙醇-水溶液的缔合状态[J]. 华南理工大学学报(自然科学版), 2010, 38(12): 120–123. |
 2016, Vol. 7
2016, Vol. 7


