| 简便高效的测定熔盐电导率的新方法 |
2. 东北大学 材料与冶金学院,沈阳 110819
2. School of Materials and Metallurgy, Northeastern University, Shenyang 110819, China
在熔盐电解领域,电解质的电导率是非常重要的物理化学性质之一。从理论意义上来讲,通过对熔盐电导率的研究,可以间接了解熔盐的离子结构,更好地认识熔盐中离子的迁移过程,从而得到高温熔盐的导电机理。从实践意义上来讲,研究电解质体系熔盐电导率更为重要,在电解过程中,电解质本身电阻损耗的电量是相当可观的,电解质的电压降占整个电解槽电压降的很大一部分,这将直接影响到电解生产的电能消耗,因此这也是评价电解质物理化学性质的重要参数。若使用电导率大的电解质能减小电阻损耗,也可以提高电流效率、节省电能和降低成本。在工业生产中,因为熔盐具有较高的电导率,可以减少电压降,从而减少能耗和提高电流效率,所以研究熔盐电导率是电解法中非常重要的研究内容之一[1-3]。
对于熔盐电导率的测定,据文献报道有多种方法[4],其中具有代表性的有:连续改变电导池常数(CVCC)法[2-3, 5]、电桥法[6]、四电极法[7],交流阻抗法[8-9]和固定电导池法[10-11]等。由于冰晶石熔盐有极强的腐蚀作用和挥发性,以上测定技术得出的实验数据之间存在1%以内的偏差,而且因测量装置复杂、造价昂贵或测量稳定性差等原因,在应用方面具有一定的局限性[4]。
本文提出了自制的管式电导池法,测定了nNaF·AlF3-Al2O3-CaF2熔盐体系电导率,并与Wang经验公式和Choudhary经验公式[12]计算值进行了比较。本文旨在设计出数据精确度高、结构简单、造价便宜、能扩大应用范围的全新测试高温熔体电导率的方法。
1 实验 1.1 化学试剂及熔体制备氧化锆、氟化钠和氟化铝都是分析纯的化学试剂。所用金属铝为特一级原铝。氧化锆和氟化钠在400 ℃下烘3 h脱去附着水后置于干燥柜中保存备用。采用真空升华法处理三水氟化铝来制备无水氟化铝,并将制得的无水氟化铝密封入干燥柜中备用[13]。实验检测用熔盐电解质的初晶温度值见参考文献[14]。
1.2 测量方法采用自制的管式电导池测定熔盐电导率之前,需先用已知电导率的溶液或熔盐标定电导池常数。然后根据式(1)计算出熔盐的电导率:
| $\sigma =G/R$ | (1) |
冰晶石体系具有很强的腐蚀性,而且熔盐电解的操作温度比较高,因此要求材料在高温下具有稳定的尺寸、高度的耐腐蚀性和良好的绝缘性。
1.3 实验装置测定电导率的设备装置包括高温电炉系统和测量系统。高温电炉系统由高温电炉(0~1200 ℃)和程序控温系统组成。测量系统由Anglent数字万用表和Anglent阻抗仪组成。电导率测定装置如图 1所示。
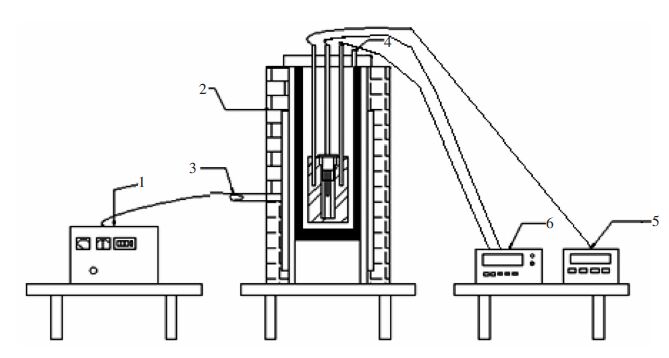 |
| 1-温度控制仪;2-高温炉;3-Pt-Pt10%Rh热电偶;4-氩气入口;5-阻抗仪;6-数字万用表 图 1 电导率测定装置图 Fig. 1 Experimental facilities for conductivity |
电导率的测定在高纯石墨坩埚中进行。将石墨坩埚放在铁坩埚内,采用CKW-3100型控温仪通过Pt-Pt10%Rh热电偶对硅碳棒炉进行控温,硅碳棒炉的恒温带在铁坩埚底以上50 mm。
电导池的设计如图 2所示。电导池以热解氮化硼和热压氮化硼作为主体材料,以1 mm的钨丝作为工作电极。钨丝通过热解氮化硼管进行绝缘,将钨丝连接到高纯石墨制备的石墨盖上,并把石墨盖连接到不锈钢导杆上作为测量阻抗的一端。石墨坩埚与另一根不锈钢导杆连接作为测量阻抗的另一端。在石墨坩埚上端安装一个热压氮化硼圈,以确保绝缘。电导池是由长90 mm,外径9 mm,内径4 mm的热解氮化硼管制作,其理论电导池常数为47.77 cm-1。电导池的设计中需要充分考虑电导池的毛细现象和排气问题,因此在热压氮化硼中间处设计一个直径5 mm的孔,目的是排除测量熔盐过程中产生的气泡,确保实验数据的稳定性和可靠性。在电导池的设计方案中,尽量使电导池常数值大些,以减小测得数据的误差。
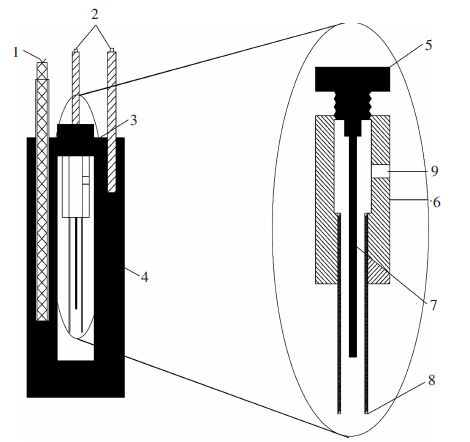 |
| 1-Pt-Pt10%Rh热电偶;2-高温不锈钢管;3-热压NB环;4-石墨坩埚;5-石墨连接附件;6-热压NB连接附件;7-钨丝;8-热解NB管;9-排气口 图 2 电导池示意图 Fig. 2 The sketch of conductivity cell |
电导池中氮化硼在使用前必须经过加热处理,去除其中的水分和粘结剂,否则氮化硼会在加热过程中容易开裂或粉碎。热解氮化硼的预处理方法:将热解氮化硼放置在空气中(或保存在氩气状态中)在700 ℃下加热10 h(升温速率不限),在氩气环境下降温到室温并保存在干燥器内。热压氮化硼的预处理方法:在氩气保护下,以每小时250 ℃的升温速率加热至1000 ℃并保温10 h,在氩气保护下降温至室温并保存在干燥器内[4]。
在实验过程中,不能将氮化硼电导池长时间暴露在潮湿的空气中,并且不能急冷急热。在实验结束后,将氮化硼电导池悬挂在法兰盖上随炉降温至室温后再将其取出,可延长电导池的使用寿命。
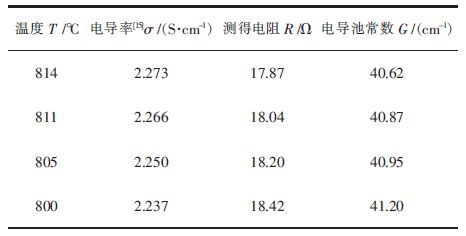
2 结果及讨论 2.1 电导池常数的测定首先将KCl (50 g)放入坩埚中加热至800 ℃,保温半小时,确保KCl完全熔化,将电导池浸入到熔盐中测定KCl的电阻,测完后升高测定温度,分别在805 ℃、810 ℃和815 ℃下以同样的方法测定电阻,将电阻换算成电导率。文献[15]提出KCl在高温下的电导率,利用电导率的计算公式计算出高温下电导池的电导池常数并取平均数,具体实验数据如表 1所示。
| 表1 KCl熔盐电导率测定结果 Table 1 Measurement result of the KCl molten salt |
 |
| 点击放大 |
对各温度下得到的电导池常数取平均值,得到G=40.91cm-1。
2.2 电导率测定方法的可行性分析图 3为采用自制的管式电导池测定nNaF·AlF3(n=2.2~2.6)-3%Al2O3-3%CaF2(均为质量分数)熔盐体系的电导率数据与经验公式求得的冰晶石电导率数据的比较。由图可见,相同条件下电解质电导率值以及随分子比增加电导率的增加速度基本相同。在相同条件下,本实验工作的测定值略小于Wang经验公式和Choudhary[12]经验公式计算值,误差均小于0.5%,说明实验方法可行。
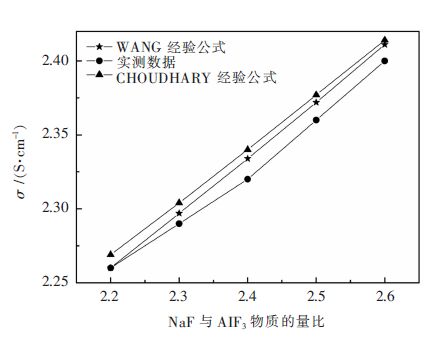 |
| 图 3 实验测得电导率数据和经验公式数据比较 Fig. 3 Density date comparison of our work and empirical formula |
2.3 电导率测定方法的精密度分析
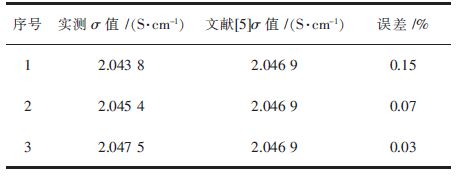
对电导池常数误差进行验证,配制含2.2NaF·AlF3-3%Al2O3-5%CaF2(均为质量分数)的熔盐50 g,升温到959 ℃,测得值与文献值[5]比较见表 2所示。
| 表2 系统误差分析 Table 2 Relative error of system analysis |
 |
| 点击放大 |
由表可见,实验相对误差小于0.2%,说明该法准确可行。
2.4 冰晶石系熔盐电导率的测定图 4为NaF与AlF3摩尔比(n)对nNaF·AlF3(n=2.2~2.6)-3%Al2O3-3%CaF2熔盐体系电导率的影响。由图可见,nNaF·AlF3-3%Al2O3-3%CaF2(均为质量分数)熔盐体系的电导率随着NaF与AlF3摩尔比(n)的升高而逐渐增加。
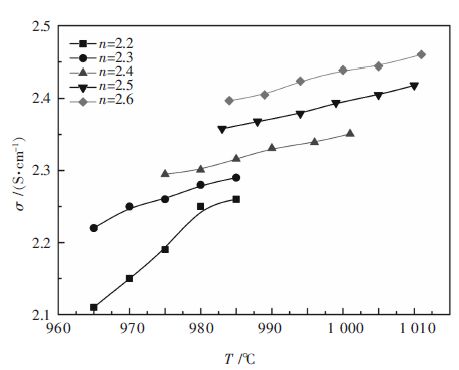 |
| 图 4 NaF与AlF3摩尔比(n)对nNaF·AlF3-3%Al2O3-3%CaF2熔盐电导率的影响 Fig. 4 Effect of molar ratios of NaF/AlF3 on electrical conductivity of nNaF·AlF3-3%Al2O3-3%CaF2 |
这是由于,在冰晶石系熔盐中存在下列反应[16]:
| $\begin{align} & \text{AlF}_{6}^{3\text{-}}\text{=Al}{{\text{F}}_{3}}+\text{ 3}{{\text{F}}^{-}} \\ & \text{AlF}_{5}^{3\text{-}}\text{=Al}{{\text{F}}_{3}}+\text{ 2}{{\text{F}}^{-}} \\ & 3A{{l}_{2}}OF_{8}^{4-}=4AlF_{6}^{3-}+2A{{l}^{3+}}+3{{O}^{2-}} \\ & 3A{{l}_{2}}OF_{8}^{4-}=4AlF_{5}^{2-}+A{{l}_{2}}{{O}_{3}}+4{{F}^{-}} \\ & 3A{{l}_{2}}OF_{6}^{2-}+6{{F}^{-}}=4AlF_{6}^{3-}+A{{l}_{2}}{{O}_{3}} \\ & 3A{{l}_{2}}OF_{6}^{2-}+2{{F}^{-}}=4AlF_{5}^{2-}+A{{l}_{2}}{{O}_{3}} \\ \end{align}$ |
当NaF与AlF3摩尔比(n)增大即AlF3含量减小时,熔液中形成的络合离子也减少,从而使可迁移的自由离子数量增多,这种增多就会使电导率明显增加。另外,体积庞大的络合离子的减少,使离子运动时受到的阻力减小,因此在熔液中定向移动的速度就相对较快,导电率增加。
同时,由图 4可见,当温度升高时体系电导率明显增大。这是因为温度升高,粒子的热运动增强,这种粒子动能的增加使离子与其它离子之间的键能减弱,从而使离子的定向迁移易于进行。此外,高温时,络合离子的解离度增大,体系中的自由离子将增多。这些因素对电导率有较大的贡献。因此高温时,电导率将比低温时有所增大。
图 5为在950 ℃下,NaCl的添加量对2.2NaF·AlF3- 3%Al2O3-3%CaF2(均为质量分数)熔盐体系电导率的影响。由图可见,当2.2NaF·AlF3- 3%Al2O3-3%CaF2(均为质量分数)熔盐中添加NaCl时熔盐的电导率明显增加。这是因为Na+离子半径小,极化作用也小,所以在电解质中受到的阻力小,电场中定向移动速度快,有利于提高熔盐的电导率,因此NaCl的添加量越多熔盐的电导率越高。此结果与文献结果类似[2],说明测试结果准确。
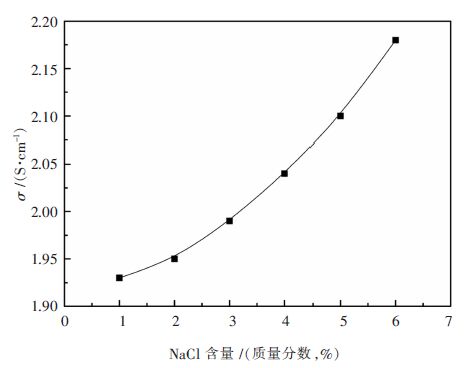 |
| 图 5 NaCl的添加量对2.2NaF·AlF3- 3%Al2O3-3%CaF2熔盐电导率的影响(950 ℃) Fig. 5 Effect of NaCl addition on electrical conductivity of 2.2NaF·AlF3-3%Al2O3-3%CaF2(950 ℃) |
3 结论
采用自制的管式电导池测定的电导率数据与Wang经验公式和Choudhary经验公式计算值相近,误差均小于0.5%,并通过实验证明该方法具有较高的准确性与重现性。管式电导池法是一种准确度高、结构简单、造价便宜、能扩大应用范围测定熔盐电导率的有效测试手段。
| [1] | 胡宪伟, 王兆文, 路贵民, 等. 连续变化电导池常数法测定电导率的等效电路分析及应用[J]. 中国有色金属学报, 2008, 18(3): 551–556. |
| [2] | 阚洪敏.低温铝电解的研究[D].东北大学,2007:60. http://cn.bing.com/academic/profile?id=1532552151&encoded=0&v=paper_preview&mkt=zh-cn |
| [3] | 廖春发, 王坤, 王旭, 等. NaCl-CaCl2-CaWO4熔盐体系电导率的研究[J]. 有色金属科学与工程, 2013, 4(5): 19–22. |
| [4] |
Schiefelbein S L, Sadoway D R. A high-accuracy, calibration-free technique for measuring the electrical conductivity of molten oxides[J].
Metallurgical and Materials Transactions B, 1997, 28B: 1141–1149. |
| [5] | Wang X W, Ray D P, Alton T T. electrical conductivity of cryolitic melts[C]. Light Metals 1992, warrendale: Minerals, Metals&Materials Soc., 1992.5: 481-488. |
| [6] |
Dong Q Y Shen L N, Wang M P, et al. Microstructure and properties of Cu-2.3Fe-0.03P alloy during thermomechanical treatments[J].
Transactions of Nonferrous Metals Society of China, 2015, 25: 1551–1558. DOI: 10.1016/S1003-6326(15)63757-8. |
| [7] | 余翔, 张冰, 林桢, 等. 基于Van Der Pauw原理的溶液电导率计[J]. 浙江大学学报(工学版), 2015, 49(2): 371–375. |
| [8] | 辛秦, 王新东. 温度对氢气还原氧化铁影响及电化学性能研究[J]. 有色金属科学与工程, 2015, 6(1): 41–47. |
| [9] | 章珏, 郑鑫, 梁金, 等. NdF3-LiF-Nd2O3体系熔盐电导率影响因素的研究[J]. 稀有金属与硬质合金, 2014, 42(4): 17–21. |
| [10] |
Korenko M, Vasková Z, Šimko F, et al. Electrical conductivity and viscosity of cryolite electrolytes for solar grade silicon (Si-SoG) electrowinning[J].
Transactions of Nonferrous Metals Society of China, 2014, 24(12): 3944–3948. DOI: 10.1016/S1003-6326(14)63554-8. |
| [11] |
Bao M, Wang Z W, Gao B L, et al. Electrical conductivity of NaF−AlF3−CaF2−Al2 O3−ZrO2 molten salts[J].
Transactions of Nonferrous Metals Society of China, 2013, 23: 3788–3792. DOI: 10.1016/S1003-6326(13)62930-1. |
| [12] | Thonstad J, Qiu Z X, Liu H SH, et al. Aluminium Electrolysis(3rd edition)[M]. Metallurgical Industry Press , 2010. |
| [13] | 包莫日根高娃, 王兆文, 丁晨亮, 等. 铝液还原熔盐中ZrO2制备纯铝锆母合金[J]. 有色金属科学与工程, 2014, 5(4): 13–17. |
| [14] | Bao M, Wang Z W, Gao B L, et al. Effect of the addition of ZrO2 on the liquidus temperature of nNaF•AlF3-Al2O3 Molten Salt System [C]. World Non-Grid-Connected Wind Power and Energy Conference (WNWEC), Nanjing, China; World Wind Energy Institute, 2010:211-213. |
| [15] |
Grjotheim K, Nikolic R, YE H A. Electrical conductivities of binary and ternary melts between MgCl2,CaCl2,NaCl,and KCl[J].
Acta Chemica Scandinavica, 1970, 25: 489–509. |
| [16] |
Kan H M, Wang Z W, Ban Y G, et al. Electrical conductivity of Na3AlF6-AlF3-Al2O3-CaF2-LiF (NaCl) system electrolyte[J].
Transactions of Nonferrous Metals Society of China, 2007, 17(1): 181–186. DOI: 10.1016/S1003-6326(07)60069-7. |
 2016, Vol. 7
2016, Vol. 7

