| 钒在铁液中活度系数的实验研究 |
V是重要的战略资源,广泛应用于钢铁、航空、化工等行业,其中85 %的V用于钢铁行业[1-2]. V在钢铁行业中是一种重要和经济的合金元素之一,可以改善钢的机械性能[3-4]. V在Fe液中的热力学数据涉及含V钢的合金化过程以及含钒氧化物铁矿石的冶炼[5-10].在含V钢合金化过程中,V在Fe液中的活度数据对控制钢水中V含量十分有用.在炼铁过程中,V在Fe液中的活度数据对回收铁矿石中的V进入Fe液也是十分必要的.
科研工作者对V在铁基熔体中的热力学性质进行了相关的研究[11-16].关于V在Fe液中的活度系数,可用的数据十分有限. Dastur和Chipman[17]估算了V在Fe液中的,Fruehan[18]采用电动势法得到V的活度系数与成分的表达式. Dastur和Chipman[17]表明当熔体中V含量小于0.1 %时,与Fe-V-O熔体平衡的氧化物相为FeV2O4,当V含量大于0.3 %时,与Fe-V-O熔体平衡的氧化物相为V2O3. Fruehan[18]为了确保实验中V2O3为稳定氧化物相,控制熔体中V含量大于0.43 %.本研究采用化学平衡法测量V含量小于0.43 %时,Fe液中V的活度系数,并将研究的实验结果与文献[17-18]中的结果进行比较.
1 实验文献[19]中报道了Fe液和Ag液不互溶.利用组元在Fe和Ag之间的分配比,根据组元在Ag液中的活度,便可测定组元在Fe液中的活度.
本研究曾将Ag作为参比金属相来测定V在Fe液中的活度,但由于V在Ag中的溶解度太小,无法精确分析V在Ag中的准确含量.因此,改用Cu替代金属Ag,设计了如下的实验.
每组实验包括2个渣-金平衡体系,在相同实验温度和气氛下完成,一个是Cu液与含V渣平衡体系,另一个是Fe液与含V渣平衡体系,其中渣的成分完全相同.对于这2个平衡体系,其间的渣-金反应均可以用式(1)表达:
| $ \left( {{\rm{V}}{{\rm{O}}_x}} \right) = \left[{\rm{V}} \right] + \frac{x}{2}{{\rm{O}}_2} $ | (1) |
式(1)中,(VOx)表示熔渣中钒氧化物,[V]表示熔体中V.式(1)的平衡常数如式(2)所示,仅是温度的函数,与参比金属相无关.
| $ K = \frac{{{a_{\left[{\rm{V}} \right]}} \cdot P_{{{\rm{O}}_2}}^{x/2}}}{{{a_{\left( {V{o_x}} \right)}}}} $ | (2) |
从式(2)可以看出,当氧分压、温度和钒氧化物的活度相同时,V在Fe液中的活度与Cu液中的活度也相同.因此,可以用式(3)确定V在Fe液中的活度系数.
| $ {{\rm{\gamma }}_{{\rm{V}}\left[{{\rm{Fe}}} \right]}} = \frac{{{{\rm{\gamma }}_{{\rm{V}}\left[{{\rm{Cu}}} \right]}} \cdot {x_{{\rm{V}}\left[{{\rm{Cu}}} \right]}}}}{{{{\rm{\gamma }}_{{\rm{V}}\left[{{\rm{Fe}}} \right]}}}} $ | (3) |
此外,如果Cu-V熔体是稀溶液遵守亨利定律,那么Cu液中V的活度系数可以用亨利常数
| $ {{\rm{\gamma }}_{{\rm{V}}\left[{{\rm{Fe}}} \right]}} = \frac{{{\rm{\gamma }}_{{\rm{v}}\left[{{\rm{Cu}}} \right]}^0 \cdot {x_{{\rm{V}}\left[{{\rm{Cu}}} \right]}}}}{{{x_{{\rm{V}}\left[{{\rm{Fe}}} \right]}}}} $ | (4) |
查阅文献,发现V以固态为标准态,在Cu液中的亨利常数
| $ \ln {\rm{\gamma }}_{{\rm{v}}\left[{{\rm{Cu}}} \right]}^0 = \frac{{14141.21}}{T} -4.72 $ | (5) |
结合式(4)和式(5)可以得到V在Fe液中的活度系数.
图 1所示为实验装置示意图,发热元件是硅钼棒(MoSi2),氧化铝反应管的上方安装一个密闭水冷淬冷室形成一个气密空间,反应管内的温度采用C型热电偶(W-Re5/26)测定,热电偶置于炉内恒温带底部,温度精确控制在±1 K.采用荷兰Bronkhorst气体质量流量计控制CO-CO2混合气(10 mL/min)和Ar气(30 mL/min)的流量比例,其中,CO-CO2混合气比例为99.
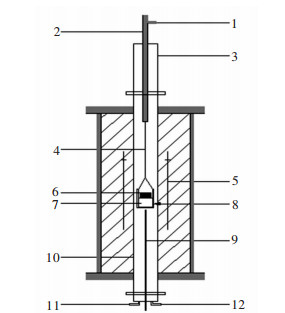 |
| 1.进去口;2.提升杆;3.淬冷腔;4.钼丝;5.硅钼棒;6.渣;7.金属;8氧化铝坩埚;9.钨铼热电偶;10.刚玉管;11.真空泵抽气口;12.进气口. 图 1 实验装置示意图 Fig. 1 Schematic diagram of experimental apparatus |
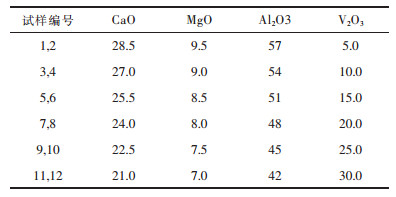
表 1所示为渣的初始成分,其中渣样1#,3#,5#,7#,9#,11#与Cu液进行平衡,渣样2#,4#,6#,8#,10#,12#与Fe液进行平衡.实验采用8 g渣和5 g金属置于氧化铝坩埚保温20 h,当渣-金反应达到平衡后,快速将样品从恒温区提升至淬冷室.将金属和渣分离后,采用ICP-AES分析Fe和Cu中V含量,采用湿化学法分析渣中成分.
| 表1 实验所配渣样的初始成分/(质量分数, %) Table 1 Charge compositions for slag samples /(mass fraction %) |
 |
| 点击放大 |
2 结果与讨论
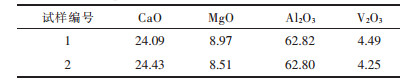
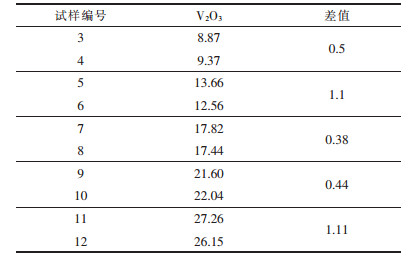
表 2显示平衡后1#渣样和2#渣样的成分几乎相同,对于其余渣样,只分析渣中V的含量,并将分析值转化为V2O3含量,结果如表 3所示. 表 2和表 3的结果表明:认为与Cu液和Fe液平衡的渣成分相同是合理的.
| 表2 实验平衡后渣的成分组成/(质量分数, %) Table 2 Composition of quenched slags after equilibrium/(mass fraction %) |
 |
| 点击放大 |
| 表3 平衡后渣中V2O3的含量/(质量分数, %) Table 3 Contents of V2O3in quenched slag samples after equilibrium /(mass fraction %) |
 |
| 点击放大 |
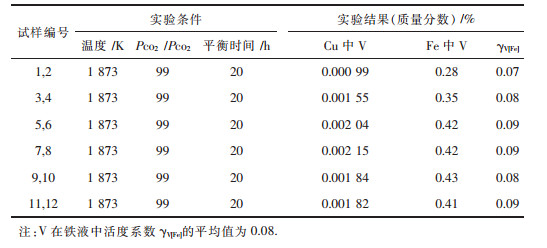
表 4列出了实验的具体条件以及检测得到的Cu液和Fe液中V的含量.再根据式(4)和式(5)计算得到以纯固态V为标准态时Fe液中V的活度系数,结果列入表 4.当Fe液中V含量分别为0.28 %,0.35 %和0.43 %时,计算得到1 873 K条件下V在Fe液中的活度系数分别为0.07,0.08和0.09. V在Fe液中的活度系数平均值为0.08,与Dastur和Chipman[17]得到的活度系数值0.12,以及与Fruehan[18]得到的活度系数值0.1很接近.从表 4的结果可以看出:V在Cu液中含量和V在Fe液中含量的变化趋势相同,随渣中V2O3含量的增加,V在Cu液和Fe液中的含量都是先增加后保持不变.熔体中V含量随渣中V2O3含量的增加保持不变时,说明与熔体平衡的渣相是一种饱和的含钒化合物.
| 表4 实验条件与实验结果 Table 4 Experimental conditions and results |
 |
| 点击放大 |
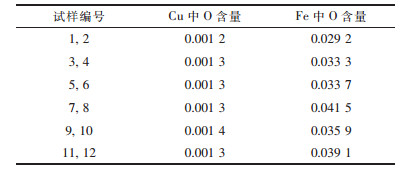
实验另外需要考虑氧是否对Cu-V熔体和Fe-V熔体有影响,从而造成实验误差.因此,对实验样品Cu和Fe中O含量进行检测,结果列于表 5.
| 表5 Cu和Fe液中O含量/(质量分数, %) Table 5 The contents of oxygen in liquid iron and copper/(mass fraction %) |
 |
| 点击放大 |
根据瓦格纳方程,V在Fe液中的活度系数如式(6)所示:
| $ \ln {\rm{\gamma }} = \ln {{\rm{\gamma }}^0} + {\rm{\varepsilon }}_{\rm{v}}^{\rm{v}}{x_{\rm{v}}} + {\rm{\varepsilon }}_{\rm{v}}^{\rm{0}}{x_{\rm{0}}} $ | (6) |
查阅文献[21]得到1 873 K下Fe液中,O对V的活度相互作用系数以及V对V的自身相互作用系数分别为:
| $ {\rm{\varepsilon }}_{\rm{v}}^{\rm{0}} = 63.03, {\rm{\varepsilon }}_{\rm{v}}^{\rm{v}} = 3.23 $ | (7) |
以Fe液中O含量最高的样品进行分析计算,其中O含量为0.041 5 %,V含量为0.42 %,V在Fe中活度系数值为0.09,计算得到:
| $ \ln{\rm{\gamma }} =-2.41, {\rm{\varepsilon }}_{\rm{v}}^{\rm{v}} \cdot {x_{\rm{v}}} = 0.015, {\rm{\varepsilon }}_{\rm{v}}^{\rm{0}} \cdot {x_{\rm{0}}} = 0.092 $ | (8) |
可以看出,
通过表 4和表 5可以看出,O在Cu液中的最高含量为0.001 4 %,V在Cu液中最高含量也仅为0.002 15 %,这2种元素在Cu液中的含量均微乎其微,所以也不必考虑Cu液中O和V之间的相互作用.
3 结论本研究最终得到1 873 K条件下V在Fe液中的活度系数的平均值为0.08,这个值与Dastur和Chipman得到的值0.12,以及与Fruehan采用电动势法得到的值0.1很接近,也说明本研究采用的化学平衡法的可靠性.
| [1] | 王明玉, 王学文.石煤提钒浸出过程研究现状与展望[J]. 稀有金属,2010,1 (34):90–97. |
| [2] | 李兰杰, 张力, 郑诗礼, 等.钒钛磁铁矿钙化焙烧及其酸浸提钒[J]. 过程工程学报,2011,11 (4):573–578. |
| [3] | 董鹏莉.炼钢过程中铬、钒及其氧化物的热力学行为[J]. 中国稀土学报,2012,30 :49–54. |
| [4] |
LANNEBORG R, SIWECKI T, ZAJAC S, et al. The role of vanadium in microalloyed steels[J].
Scandinavian Journal of Metallurgy, 1999,28 (5):186–241. |
| [5] | 陶然, 王益新, 闫柏军.钒在铜液中活度系数的实验研究[J]. 有色金属科学与工程,2015,6 (2):27–31. |
| [6] |
SHIN D Y, WEE C H, KIM M S, et al. Distribution behavior of vanadium and phosphorus between slag and molten steel[J].
Metals and Materials International, 2007,13 (2):171–176. DOI: 10.1007/BF03027569. |
| [7] |
KANG Y B. Critical evaluation and thermodynamic optimization of the VO-VO2.5 system[J].
Journal of the European Ceramic Society, 2012,32 (12):3187–3198. DOI: 10.1016/j.jeurceramsoc.2012.04.045. |
| [8] |
VERMAAK M K G, PISTORIUS P C. Equilibrium slag losses in ferrovanadium production[J].
Metallurgical and Materials Transactions B, 2000,31 (5):1091–1097. DOI: 10.1007/s11663-000-0084-1. |
| [9] | 周勇, 李正邦, 郭培民.钒氧化物矿直接合金化冶炼含钒合金钢工艺的研究[J]. 钢铁研究,2006,34 (3):54–57. |
| [10] | 周勇, 李正邦.V2O5直接合金化的热力学分析[J]. 钢铁钒钛,2006,27 (4):38–42. |
| [11] | 涂世光, 王大光.液态铁中的钒氧平衡[J]. 稀有金属,1986 (1):244–253. |
| [12] | 车萌昌, 冀春霖, 齐国均.Fe-C-V三元熔体中碳与钒的活度相互作用系数[J]. 钢铁研究总院学报,1988,8 (3):7–15. |
| [13] |
LEE B J, LEE D N. A thermodynamic study on the Fe-V-C system[J].
Calphad, 1991,15 (3):293–306. DOI: 10.1016/0364-5916(91)90007-7. |
| [14] | 杨敏, 陈二保.Fe-C-V、Fe-C-B熔体热力学性质[J]. 安徽工业大学学报,2006,23 (2):123–126. |
| [15] |
HUANG W. Thermodynamic properties of the Fe-Mn-V-C system[J].
Metallurgical and Materials Transactions A, 1991,22 (9):1911–1920. DOI: 10.1007/BF02669859. |
| [16] |
JUN P, WANG S, DONG Y. Model of calculating activity of nitrogen and vanadium in Fe-C-V-N moten metal[J].
Journal of Iron and Steel research. International, 2008,15 (5):19–23. DOI: 10.1016/S1006-706X(08)60242-3. |
| [17] |
DASTUR M, Chipman J. Vanadium-oxygen equilibrium in liquid iron[J].
Transaction of American Institute of Mining, Metallurgical, and Petroleum Engineers, 1951,191 (2):111–115. |
| [18] |
FRUEHAN R J. Activities in liquid Fe-V-O and Fe-B-O alloys[J].
Metallurgical and Materials Transactions B, 1970,1 (8):2083–2088. DOI: 10.1007/BF02643418. |
| [19] |
CHIPMAN J, FLORIDIS T P. Activity of aluminum in liquid Ag Al, Fe Al, Fe Al C, and Fe Al C Si alloys[J].
Acta Metallurgica, 1955,3 (5):456–549. DOI: 10.1016/0001-6160(55)90135-8. |
| [20] |
SIGWORTH G K, ELLOTT J F. The thermodynamics of dilute liquid copper alloys[J].
Canadian Metallurgical Quarterly, 1974,13 (3):455–461. DOI: 10.1179/cmq.1974.13.3.455. |
| [21] |
SIGWORTH G K, ELLOTT J F. The thermodynamics of liquid dilute iron alloys[J].
Metal Science, 1974,8 (1):298–310. DOI: 10.1179/msc.1974.8.1.298. |
 2016, Vol. 7
2016, Vol. 7


