| 石墨烯负载铂催化剂的制备及稳定性 |
b. 北京科技大学,高效钢铁冶金国家重点实验室,北京100083
b. State Key Laboratory of Advanced Metallurgy, University of Science and Technology Beijing, Beijing 100083, China
直接甲醇燃料电池(DMFC)是以甲醇为燃料,将甲醇氧化反应的化学能转变为电能的一种燃料电池.由于其结构简单、能量密度高、环境污染少、价格便宜等优点,使其在新能源应用领域具有良好的前景.阻碍DMFC大规模商业应用的主要问题是其放电性能低、运行稳定性差等,因此如何能使DMFC长时间稳定运行是其实现商业化应用所必须解决的问题[1-5].其中选择合适的高性能和高稳定性的催化剂具有重要的意义.目前,常用的催化剂多为Pt基催化剂,其中DMFC催化剂面临的问题主要有以下几个方面:Pt颗粒由于Ostwald熟化过程造成的颗粒粒径增加[6];Pt容易受甲醇氧化反应中间产物CO毒化而失活;碳载体腐蚀造成Pt颗粒掉落;Pt颗粒的团聚[7];成本问题等.人们通过研究发现采用纳米负载型的催化剂,将活性组分分散成纳米颗粒,这不仅增加了活性材料的表面积,也降低了贵金属用量,加入催化剂的载体,催化剂的活性和稳定性都有了不同程度的提高[8-11].人们对载体材料的性质对催化剂的影响进行了大量研究,发现催化剂载体应该具有良好的导电性、较高的比表面积、合适的孔隙率、较强的耐腐蚀性以及良好的催化活性组分与载体相互作用.石墨烯由于其独特的结构,具有更大的理论比表面积和更好的电子传输能力[12-14],对于提高催化剂的稳定性方面具有良好的应用前景[15-16].
由于石墨烯的这些特性,人们对于石墨烯与金属纳米颗粒的混合进行了大量的研究.Brian Seger[17]以硼氢化钠作为还原剂,同时将GO与H2PtCl6还原得到石墨烯负载的Pt,并测试了其对氢氧燃料电池的性能,催化剂显示出良好的性能.何卫等[18]通过PDDA对石墨烯进行表面功能化,合成了负载有Pt的功能化催化剂,显示出了对氧还原反应的良好性能.Li等[19]通过硼氢化钠还原分别得到石墨烯和XC-72碳黑负载的铂催化剂,石墨烯负载的催化剂显示出更好的甲醇氧化性能.Zhou[20]将石墨烯附着在SiO2基体上,以石墨烯作为模板合成了Ag/GR化合物.Zhang[21]通过微波水热法合成了功能化高载量的石墨烯负载铂催化剂,显示出了良好的甲醇氧化性能.
本文采用浸渍还原法,制备出了石墨烯及石墨烯复合的铂催化剂,并通过X射线衍射(XRD)、扫描电子显微镜(SEM)及拉曼光谱仪(Raman)对其物质组成及形貌特征进行了表征分析.此外,利用电化学工作站(VMP2)对所制备的样品进行了电化学测试.
1 实验 1.1 样品制备氧化石墨烯制备:氧化石墨是由通过改进的Hummers法合成的.将2 g石墨粉和1 g NaNO3加入到干燥的烧杯中,向烧杯中缓慢加入46 mL的浓硫酸,将烧杯置于0 ℃冰浴中,缓慢加入6 g KMnO4,在冰浴中搅拌2 h.随后将烧杯移至35 ℃恒温水浴搅拌1 h.最后向烧杯中加入50 mL二次水加热到95 ℃反应30 min,随后用二次水进行稀释,加入适量5 % H2O2并继续搅拌30 min.完成后用5 % HCl和二次水充分离心洗涤后至滤液pH值为7,将沉淀在60 ℃下真空干燥24 h后得到氧化石墨固体,研磨后密封保存.
催化剂的制备:将氧化石墨粉末加入到乙二醇中,超声2 h使氧化石墨分散,形成1 mg/mL溶液.将前躯体溶液H2PtCl6·6H2O加入后超声30 min,随后将烧杯在120 ℃恒温水浴下持续搅拌6 h.反应完成后用二次水充分离心洗涤后,60 ℃下真空干燥24 h得到Pt/GR催化剂.
1.2 性能测试电极制备:将2 mg催化剂加入到1 mL的溶液中,溶液组成为体积比7:2:1的二次水、异丙醇、Nafion.将溶液超声2 h形成均匀的浆料,用微量移液器移取20 μL的浆料滴加到石墨电极的表面,干燥后待用.
电化学测试:采用三电极体系,在VMP2电化学工作站上进行测试.其中将附有催化剂的石墨电极作为工作电极,铂片电极作为对电极,参比电极为Hg/Hg2SO4/K2SO4(饱和).其中甲醇氧化测试电解液为0.5 mol/L的H2SO4+1 mol/L的CH3OH溶液,电化学活性面积测试电解液为0.5 mol/L的H2SO4,扫描速度均为50 mV/s.
样品表征:用MXP21 VAHF X射线衍射仪分析材料成分,扫速5(°)/min,步长0.02°,管流30 mA,管压40 kV,CuKα,λ=0.154 06 nm;用Labrom HR-Evolution高分辨拉曼光谱仪对材料的分子结构进行分析;用SuprATM55热场发射扫描电子显微镜(FESEM)观察材料的形貌.
2 结果与讨论 2.1 形貌与结构图 1是GR和Pt/GR的XRD结果.由图 1(a)可知,GR在26.1°和43.2°处具有明显的特征峰,说明所制备的GR得到了很好的还原,通过Bragg定律进行计算可知层间距为0.345 nm,与理论值0.335 nm接近;由图 1(b)可以看出,Pt在39.7°、46.2°、67.4°和81.4°具有明显的特征峰,这几个特征峰分别代表了面心立方结构的Pt的(111)、(200)、(220)和(311)晶面.而26°左右也具有GR的特征峰,可以表明成功合成了Pt/GR催化剂.
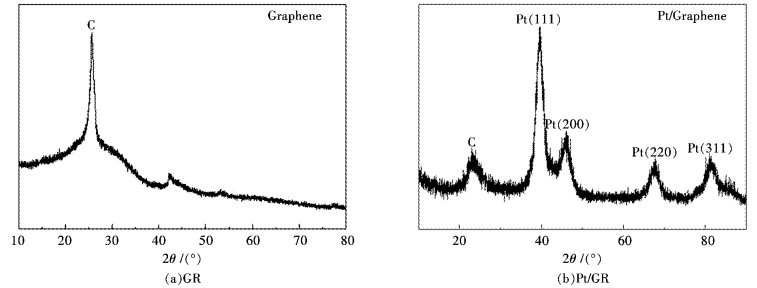 |
| 图 1 GR和Pt/Graphene的XRD结果 Fig. 1 XRD patterns of GR and Pt/Graphene |
图 2是GR和Pt/GR复合材料的SEM像.从图 2(a)可知,GR呈现出褶皱状的片层结构;从图 2(b)可以看出,在石墨烯的片层结构上均匀分布着Pt颗粒,这是由于乙二醇不仅起着还原剂的作用,同时乙二醇作为溶剂可以有效地防止Pt颗粒的团聚,而且Pt颗粒和GR的复合同时防止石墨烯片层的堆垛.
 |
| 图 2 GR和Pt/Graphene的SEM像 Fig. 2 SEM image of GR and Pt/Graphene |
图 3是Pt/GR的Raman光谱.从图 3可以看出,在1 300 cm-1和1 580 cm-1附近的D峰和G峰均为C原子晶体的Raman特征峰.其中D峰代表的是C原子的晶格缺陷,G峰代表的是C原子sp2杂化的面内伸缩振动.Pt/GR的D峰强度比G峰强度大,说明石墨烯的缺陷较多,这是由于在乙二醇的作用下Pt的前驱体和GO共同还原,使Pt颗粒附着在GR表面造成的.
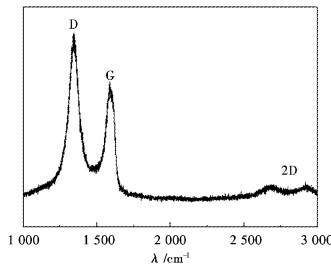 |
| 图 3 Pt/Graphene的Raman光谱 Fig. 3 Raman spectroscopy of Pt/Graphene |
2.2 电化学测试
为了测试所制备的催化剂的性能及稳定性,在0.5 mol/L的H2SO4溶液中对Pt/GR和商用Pt黑催化剂进行测试,为了进行对比,所称量的Pt黑催化剂的质量与Pt/GR相同.实验进行了1 000次循环伏安测试,分别考察了2种催化剂的ESCA衰减情况.如图 4所示.
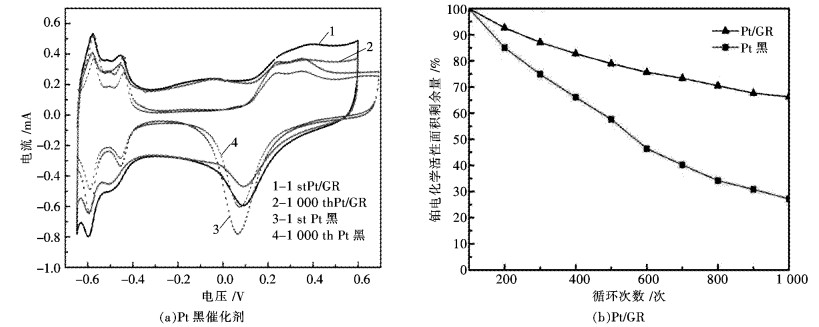 |
| 图 4 Pt黑和Pt/GR的ESCA测试 Fig. 4 ESCA tests of Pt black and Pt/GR |
从图 4(a)可以看出,经过1 000次的循环伏安测试,Pt/GR催化剂和Pt黑催化剂的ESCA均出现不同程度的降低.由图 4(a)的氢吸脱附峰可以通过以下公式得出
| $ ESCA=Q{\rm{/}}\left({m{\rm{ \times }}0.21} \right) $ | (1) |
其中,ESCA为电化学活性面积;Q为积分电荷;m为Pt的质量.
分别计算2种催化剂前后不同的ESCA变化,如图 4(b)所示.经过1 000次的循环伏安测试,Pt/GR催化剂的ESCA与开始相比剩余了66.24 %;而Pt黑催化剂经过1 000次的循环伏安测试后,ESCA与开始相比仅剩余了27.16 %.由此可以看出,相对于Pt黑催化剂,Pt/GR具有更好的稳定性.
为了测试所制备的催化剂对甲醇氧化的性能和稳定性,在0.5 mol/L的H2SO4+1 mol/L的CH3OH溶液中分别对2种催化剂进行了1 000次的循环伏安测试.如图 5所示.
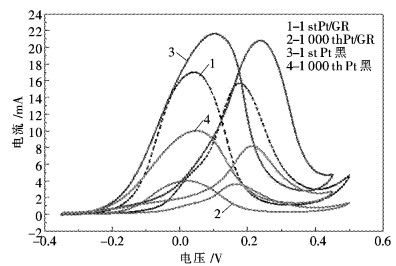 |
| 图 5 Pt黑和Pt/GR的甲醇氧化测试 Fig. 5 Methanol oxidation tests of Pt black and Pt/GR |
从图 5可以看出,相对于Pt黑催化剂,Pt/GR在开始时具有更高的甲醇氧化峰电流密度,这说明Pt/GR对于甲醇氧化反应具有更高的活性.随着反应的进行,在1 000次循环伏安测试后,2种催化剂的活性相对于开始时均出现了不同程度的降低,但是Pt/GR仍具有相对较高的活性.经过计算,Pt黑催化剂相对于开始时,其对甲醇氧化的峰电流密度下降了约81.23 %,而Pt/GR相对于开始时其活性下降了约58.73 %.通过对比可以看出Pt/GR催化剂相对于Pt黑具有更高的活性和稳定性.
为了测试催化剂对甲醇氧化反应的稳定性,还分别对2种催化剂在0.5 mol/L的H2SO4+1 mol/L的CH3OH溶液中进行了计时电流测试,测试选取的电位为甲醇氧化反应的峰电位,如图 6所示.
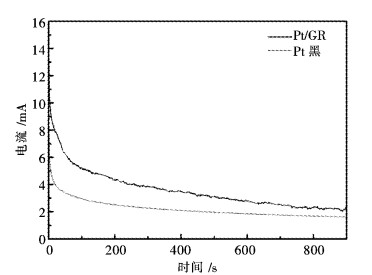 |
| 图 6 Pt黑和Pt/GR计时电流测试 Fig. 6 Chronoamperometry of Pt black and Pt/GR |
从图 6可以看出,随着时间增加,2种催化剂都表现出一定程度的电流衰减,Pt/GR的氧化电流随着时间下降的更加缓慢,而Pt黑催化剂的氧化电流下降较快.这说明Pt黑催化剂受甲醇氧化中间产物毒化更为严重,而Pt/GR催化剂表现出更好的抗CO中毒能力.
3 结论制备出了氧化石墨并通过浸渍还原法合成了Pt和石墨烯的复合催化剂,通过与商用Pt黑催化剂对比进行了电化学的测试.研究表明:Pt/GR催化剂相对于Pt黑催化剂具有更高的电化学活性面积和稳定性;对于甲醇氧化反应Pt/GR也具有更高的活性,而且Pt/GR抗甲醇氧化反应中间产物中毒能力也更好,说明石墨烯负载的铂催化剂具有更好的催化性能.
| [1] |
Dong L F, Raghavendar R S G, Zhou L, et al. Graphene-supported platinum and platinum-ruthenium nanoparticles with high electrocatalytic activity for methanol and ethanol oxidation[J].
Carbon, 2010, 48: 781–787. DOI: 10.1016/j.carbon.2009.10.027. |
| [2] |
Hsin Y L, Hwang K C, Yeh C T. Poly (vinylpyrrolidone)-modified graphite carbon nanofibers as promising supports for PtRu catalysts in direct methanol fuel cells[J].
Journal of the American Chemical Society, 2007, 129(32): 9999–10010. DOI: 10.1021/ja072367a. |
| [3] |
Wang Z B, Li C Z, Gu D M, et al. Carbon riveted PtRu/C catalyst from glucose in-situ carbonization through hydrothermal method for direct methanol fuel cell[J].
Journal of Power Sources, 2013, 238: 283–289. DOI: 10.1016/j.jpowsour.2013.03.082. |
| [4] |
Jehng J M, Liu W J, Pan T C, et al. Preparation of Pt nanoparticles on different carbonaceous structure and their applications to methanol electro-oxidation[J].
Applied Surface Science, 2013, 268: 425–431. DOI: 10.1016/j.apsusc.2012.12.115. |
| [5] |
Xin Y C, Liu J G, Zhou Y, et al. Preparation and characterization of Pt supported on graphene with enhanced electrocatalytic activity in fuel cell[J].
Journal of Power Sources, 2011, 196: 1012–1018. DOI: 10.1016/j.jpowsour.2010.08.051. |
| [6] |
Coloma F, Sepulvedaescribano A, Fierro J L G, et al. Preparation of platinum supported on pregraphitized carbon-blacks[J].
Langmuir, 1994, 10(3): 750–755. DOI: 10.1021/la00015a025. |
| [7] |
Robert M D, Jeremy P M. Kinetic model of platinum dissolution in PEMFCs[J].
Journal of The Electrochemical Society, 2003, 150: 1523–1527. DOI: 10.1149/1.1613669. |
| [8] |
Chang Y Z, Han G Y, Li M Y, et al. Graphene-modified carbon fiber mats used to improve the activity and stability of Pt catalyst for methanol electrochemical oxidation[J].
Carbon, 2011, 49: 5158–5165. DOI: 10.1016/j.carbon.2011.06.099. |
| [9] |
Prabhuram J, Svitlana P, Tim O, et al. Enhanced stability of PtRu supported on N-doped carbon for the anode of a DMFC[J].
Journal of The Electrochemical Society, 2012, 159: 768–778. DOI: 10.1149/2.063211jes. |
| [10] |
Segoo K, Seongyop L, Peck D H, et al. Stability and durability of PtRu catalysts supported on carbon nanofibers for direct methanol fuel cells[J].
International Journal of Hydrogen Energy, 2012, 37: 4685–4693. DOI: 10.1016/j.ijhydene.2011.04.119. |
| [11] |
Liu X W, Duan J L, Chen H L, et al. A carbon riveted Pt/graphene catalyst with high stability for direct methanol fuel cell[J].
Microelectronic Engineering, 2013, 110: 354–357. DOI: 10.1016/j.mee.2013.02.060. |
| [12] |
Kazuma G, Koji K, Eiji F, et al. The use of graphite oxide to produce mesoporous carbon supporting Pt Ru or Pd nanoparticles[J].
Carbon, 2009, 47: 2112–2142. DOI: 10.1016/j.carbon.2009.02.027. |
| [13] |
Li H Y, Zhang X H, Pang H L, et al. PMo12-functionalized graphene nanosheet-supported PtRu nanocatalysts for methanol electro-oxidation[J].
J Solid State Electrochem, 2010, 14: 2267–2274. DOI: 10.1007/s10008-010-1067-z. |
| [14] |
Kou R, Shao Y Y, Wang D H, et al. Enhanced activity and stability of Pt catalysts on functionalized graphene sheets for electrocatalytic oxygen reduction[J].
Electrochemistry Communications, 2009, 11: 954–957. DOI: 10.1016/j.elecom.2009.02.033. |
| [15] |
EunJoo Y, Tatsuhiro O, Tornoki A, et al. Enhanced electrocatalytic activity of Pt subnanoclusters on graphene nanosheet surface[J].
Nano Letters, 2009(9): 2255–2259. |
| [16] |
Byungchul J, Eunjin C, Yuanzhe P. Preparation of well-dispersed Pt nanoparticles on solvotherma graphene and their enhanced electrochemical properties[J].
Materials Research Bulletin, 2013, 48: 834–839. DOI: 10.1016/j.materresbull.2012.11.064. |
| [17] |
Seger B, Kamat P V. Electrocatalytically active graphene-platinum nanocomposites role of 2-D carbon support in PEM fuel cells[J].
The Journal of Physical Chemistry C, 2009, 113: 7990–7995. DOI: 10.1021/jp900360k. |
| [18] | 何卫, 邹亮亮, 周毅, 等. 石墨烯载Pt纳米颗粒的原位还原制备及氧还原电催化性能[J]. 高等学校化学学报, 2012, 33(1): 133–138. |
| [19] |
Li Y M, Tang L H. Preparation and electrochemical performance for methanol oxidation of Pt/graphene nanocomposites[J].
Electrochemistry Communications, 2009, 11: 846–849. DOI: 10.1016/j.elecom.2009.02.009. |
| [20] |
Zhou X Z, Huang X, Qi X Y, et al. In situ synthesis of metal nanoparticles on single-layer graphene oxide and reduced graphene oxide surfaces[J].
The Journal of Physical Chemistry C, 2009, 113: 10842–10846. DOI: 10.1021/jp903821n. |
| [21] |
Zhang M M, Xie J M, Sun Q, et al. Enhanced electrocatalytic activity of high Pt-loadings on surface functionalized graphene nanosheets for methanol oxidation[J].
International Journal of Hydrogen Energy, 2013, 38: 16402–16409. DOI: 10.1016/j.ijhydene.2013.09.108. |
 2015, Vol. 6
2015, Vol. 6


