| 改性萃取剂从高碱度溶液中萃取钒的研究 |
b. 江西理工大学 工程研究院,江西 赣州 341000
b. Institute of Engineering, Jiangxi University of Science and Technology, Ganzhou, 341000, China
钒是一种重要的稀有金属,一般都不会形成单独的矿床,而主要是以伴生矿的形式存在.目前用于提钒的资源主要有石煤、铝土矿、含钒钢渣和废催化剂等[1].氧化焙烧一碱浸—溶剂萃取是目前石煤提取钒的主要发展方向之一,其中钒的碱性浸出液可直接作为萃取的原料液.铝土矿中通常含有约0.1 %的钒,在拜耳法生产氧化铝的碱溶过程中约有30 %~40 %的钒进入碱性铝酸钠溶液,同样可以采用萃取法回收其中碱性溶液中的钒[2].从碱性体系中萃取钒的研究已经引起研究者们的注意.
近年来,科研工作者对从碱性环境中萃取钒的工作进行相关的研究[3-11],取得了阶段性成果.但可以看到,不同的研究者在采用不同的萃取方法时均不是很理想.如采用季铵盐三辛基甲基氯化铵在pH值小于12的溶液中萃取钒效果较佳,萃取率达到90 %以上,但是当溶液中pH值大于12以后,钒的萃取率就急剧下降;以N263为表面活性剂制成的微乳液在pH值为13的铝酸钠溶液中也能达到90 %以上的萃取率,但是微乳液的破乳难度大和对料液碱度的适应性存在问题等,而且这些萃取剂均只能适应碱性较低的体系,而对于高碱度体系萃取效果却很差,如氧化铝生产过程中种分母液就属于强碱性溶液,溶液中含有大量游离的NaOH,其pH值远大于13,用这些传统方法均无法满足高碱度体系中萃取钒的需要.因此,本文在总结前人研究工作的基础上,通过筛选合适的萃取剂,并进行改性后,用于高碱度体系中进行萃取钒研究,取得了较为满意的效果.
1 实验 1.1 试剂及设备 1.1.1 试剂萃取剂:季铵盐三-十八烷基甲基氯化铵、三辛基甲基氯化铵,优级纯,纯度均大于99.5 %;极性改质剂:仲辛醇,分析纯;稀释剂:磺化煤油,市售;料液采用分析纯偏钒酸钠与去离子水配制而成,料液中的碱度采用分析纯氢氧化钠调节,在本实验中提到的碱度均指OH-浓度,单位为mol/L.
1.1.2 实验设备125 mL/250 mL梨型分液漏斗,康氏振荡器,电热套,JJ-1精密增力电动搅拌器,JB-2A型恒温磁力搅拌器,电感耦合等离子体发射光谱仪ICP.
1.2 实验原理萃取:3(R4N)2CO3(O) +2Na3VO4(A)=2(R4N)3VO4 (O)+3Na2CO3(A)
反萃:2(R4N)3VO4(O) +3Na2CO3(A)=3(R4N)2CO3(O)+2Na3VO4(A)
其中:A代表水相,O代表有机相
1.3 实验方法 1.3.1 萃取剂的选择及转型研究近年来,有研究者研究了从高碱性的钨酸钠溶液中直接萃取钨[12-15]的工作,他们采用季铵盐萃取剂甲基三辛基氯化铵组成的萃取体系直接从钨矿苛性钠浸出液和苏打高压浸出液中萃取钨,可达到深度萃取钨的效果,同时解决了萃取体系分相速度慢和反萃液WO3浓度低的问题,为新工艺的产业化排除了障碍.
由于在碱性溶液中钨、钼与钒离子形态存在规律十分相似,因此,本研究拟借鉴从碱性的钨酸钠溶液中直接萃取钨的原理,选择季铵盐三辛基甲基氯化铵和三-十八烷基甲基氯化铵为萃取剂研究从高碱度的含钒料液中直接萃取钒的工作,经过前期探索实验,发现后者的萃取性能要稍优于前者,最终选择三-十八烷基甲基氯化铵为本研究的萃取剂.
实验前需将有机相中的Cl-型季铵盐转型为对钒萃取效果更好的CO32-型季铵盐.将萃取剂三-十八烷基甲基氯化铵、极性改质剂仲辛醇和稀释剂磺化煤油按要求比例混合,搅拌均匀后进行转型处理.转型处理过程中采用ICP分析水相Cl-浓度,当水相Cl-浓度小于0.1 g/L时,即可认为有机相转型完全[16].
1.3.2 萃取实验分别量取一定体积的有机相和水相装入250 mL分液漏斗中,控制好相应的萃取条件,将分液漏斗放在康氏振荡器上进行振荡,振荡结束后,取出分液漏斗,置于萃取架静置分层,取一定量萃余液进行分析.而在考察温度影响因素时,实验中温度控制方法是将有机相与水相混合于烧杯后,置于恒温水浴锅内通过机械搅拌实现的,温度可控制在+0.5 ℃.
水相V2O5浓度采用硫酸亚铁铵容量滴定法测定,有机相V2O5浓度根据萃取前、后的水相的浓度和体积变化按照差减法计算得到.萃取率E计算公式为:
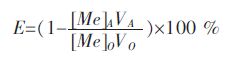
|
其中:[Me]A为萃余液中离子浓度,g/L;[Me]O为料液中离子浓度,g/L;VA为萃余液的体积,L;VO为料液的体积,L.
1.3.3 饱和萃取容量测定有机相的萃钒饱和容量采用饱和浓度法测定,即用一份有机相与数份新鲜料液依次进行萃取,直至萃余液中的V2O5含量不变,则视有机相为饱和,此时有机相中V2O5的含量即为饱和容量.每份萃余水相中和有机相中V2O5浓度,遵照1.3.2方法测定.
2 结果与讨论 2.1 有机相组成对钒萃取率的影响 2.1.1 萃取剂浓度对钒萃取率的影响实验条件为:温度为25 ℃,料液碱度为1.5 mol/L,料液中V2O5浓度为3.57 g/L,固定有机相中仲辛醇的浓度(质量分数,下同)为20 %,相比O/A(有机相体积比水相体积,下同)为2/1,振荡时间为10 min,水相体积为15 mL,实验结果如图 1所示.图 1反映了有机相中萃取剂浓度对钒萃取率和分相时间的影响.
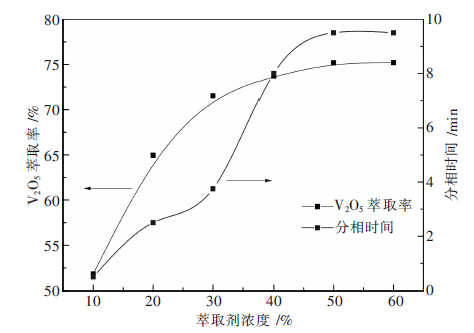 |
| 图 1 萃取剂浓度对钒萃取率及分相时间的影响 |
由图 1可以看出,萃取剂浓度对钒萃取率和分相时间的影响很显著.随着萃取剂浓度的增大,钒萃取率呈上升趋势,但当萃取剂浓度增大到40 %以上时,继续提高有机相中萃取剂浓度,钒萃取率上升的不明显,始终保持在75 %左右.而萃取体系的分相时间随着萃取剂浓度的增大而不断延长,如当萃取剂浓度为10 %时,分相时间仅为30 s,而萃取剂浓度提高到40 %时,分相时间变为8 min左右,之后变化不大,保持在10 min之内.
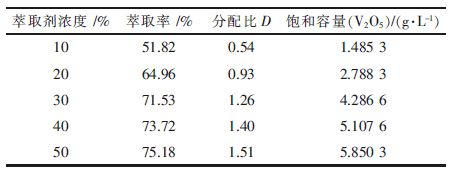
| 表1 不同萃取剂浓度下对萃取的影响 |
 |
| 点击放大 |
表 1反映了与图 1相同条件下不同萃取剂浓度与有机相萃取钒饱和容量的关系.由表 1可以看出,伴随着萃取剂浓度的增大,有机相萃取钒的饱和容量显著增加.有机相中萃取钒饱和容量越大,反萃液中V2O5浓度将越大,这有利于钒的富集与反萃.另外,随着萃取剂浓度的不断增大,有机相黏度也将增大,萃取反应时水相容易出现乳化现象,将都影响萃取体系的分相效果.综合考虑钒的富集与反萃作用和体系的分相性能,选择萃取剂浓度为50 %,此时有机相中萃取钒饱和容量为5.85 g/L V2O5.
2.1.2 仲辛醇浓度对钒萃取率的影响实验条件为:温度为25 ℃,料液碱度为1.5 mol/L,料液中V2O5浓度为3.57 g/L,有机相中萃取剂的浓度为50 %,相比O/A为1/1,振荡时间为10 min,水相体积为25 mL,实验结果如图 2所示.
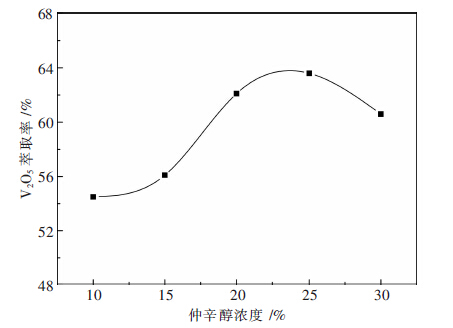 |
| 图 2 仲辛醇浓度对钒萃取率的影响 |
由图 2可看出,随着有机相中仲辛醇浓度的提高,钒萃取率先增大后减小.当仲辛醇浓度为10 %~25 %时,随着仲辛醇浓度的提高,稀释剂的极性越大,季铵盐萃取剂将发生解聚作用,有机相的萃取钒的能力也将增强.当仲辛醇浓度大于25 %时,水相易发生乳化,萃取剂能力也将受到限制,萃取率随之下降.实验中发现,仲辛醇浓度为25 %时,萃取后水相会发生乳化,经长时间静置后水相仍不清亮,综合考虑,选择仲辛醇浓度为20 %时较为合适.
因此,经上述实验及分析可选定从高碱度含钒溶液中萃取钒的合适有机相组成为(质量分数)50 %三—十八烷基甲基氯化铵+20 %仲辛醇+30 %磺化煤油,在后续实验中若无特别说明,均采用该组成的有机相.
2.2 料液碱度对钒萃取率的影响实验条件为:温度为25 ℃,料液中V2O5浓度为3.57 g/L,相比O/A为 2/1,振荡时间为10 min,水相体积为15 mL,改变料液碱度分别为0.5 mol/L、1.0 mol/L、1.5 mol/L、2.0 mol/L,2.5 mol/L、3.0 mol/L,实验结果如图 3所示.
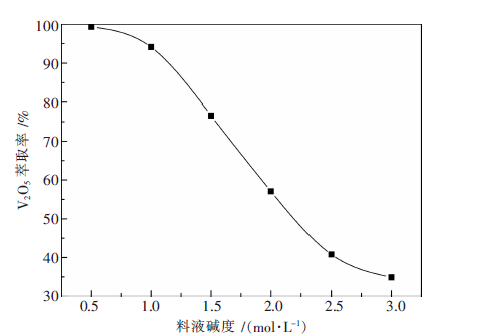 |
| 图 3 料液碱度对钒萃取率的影响 |
由图 3可看出,溶液碱度对钒萃取过程的影响十分显著.随着料液碱度的增加,钒的萃取率呈急剧下降的趋势.当料液碱度为0.5 mol/L时,钒的单级萃取率接近100 %,但当料液碱度大于2.0 mol/L时,钒的单级萃取率不断下降,如当料液碱度为2.5 mol/L时,钒的单级萃取率仅为40.8 %,可见该萃取剂对碱度大于2.5 mol/L的料液萃取钒的能力较弱.从萃取原理上看,料液碱度的增大即OH-的浓度增大,OH-会与VO43-存在竞争萃取的关系,随着料液碱度的增大,有机相中萃入的OH-也越多,这就导致了V2O5的萃取率和萃取钒的饱和容量的下降,此时可以考虑对料液进行预处理,使料液中的钒以有利于萃取的形式存在,从而提高萃取剂对钒的选择性,直接从高碱度料液下萃取钒并达到与杂质离子的分离效果.
2.3 料液初始含钒浓度对钒萃取率的影响由于石煤矿中钒含量和浸出条件的不固定,导致浸出液中钒含量也就不固定.同样,在氧化铝生产体系中不同工序中溶液中钒含量也都不尽相同,为此,可通过本实验考察溶液中初始含钒浓度对钒萃取率的影响.
实验条件为:温度为25 ℃,料液碱度为1.5 mol/L,相比O/A为 2/1,振荡时间为10 min,水相体积为15 mL,改变料液中V2O5浓度分别为1 g/L、2 g/L、4 g/L、6 g/L、8 g/L,实验结果如图 4所示.
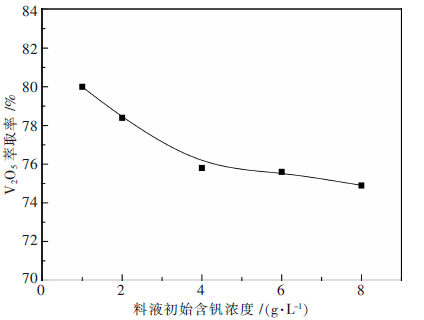 |
| 图 4 料液初始含钒浓度对钒萃取率的影响 |
由图 4看出,料液中初始钒浓度对钒的萃取率有一定的影响.料液初始含钒浓度越低,钒萃取率越高,料液初始含钒浓度越高,钒萃取效果越差,另外,钒的分配比也会随着料液初始钒浓度的增大而减小.当料液初始含钒浓度为8 g/L时,钒的萃取率也达到了75 %.由此可见,该萃取体系可较好地适应不同钒含量的料液.
2.4 相比对钒萃取率的影响实验条件为:温度为25 ℃,料液碱度为1.5 mol/L,料液中V2O5浓度为3.57 g/L,振荡时间为10 min,水相体积均为10 mL,改变相比O/A分别为1/2、1/1、2/1、3/1、4/1,实验结果如图 5所示.
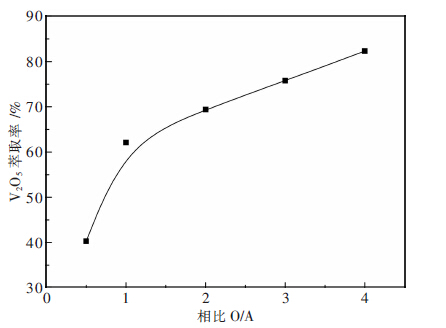 |
| 图 5 相比O/A对钒萃取率的影响 |
由图 5可看出,相比O/A越大,钒萃取率越大.相比O/A较小时,有机相不足,导致无法将水相中的钒完全萃取,表现为低萃取率.当相比O/A大于2/1时,钒萃取率上升速率变缓.实验中还发现,随着相比O/A的增大,萃取体系的分相速度加快、水相由轻微浑浊变至清澈.综合考虑钒萃取率、分相性能和有机相成本等因素,选择相比O/A为2/1为宜.
2.5 振荡时间对钒萃取率的影响实验条件为:温度为25 ℃,料液碱度为1.5 mol/L,料液中V2O5浓度为3.57 g/L,相比O/A为 2/1,水相体积为10 mL,改变振荡时间分别为1 min、3 min、5 min、10 min、15 min,实验结果如表 2所示.
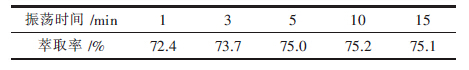
| 表2 振荡时间对钒萃取率的影响 |
 |
| 点击放大 |
由表 2可知,在5 min之内,钒萃取率随着振荡时间的延长而增大,当振荡时间超过5 min后,钒萃取率将保持不变,即萃取体系达到了平衡,为了使萃取反应充分,故选择振荡时间为10 min为宜.
2.6 温度对钒萃取率的影响表 3反映了温度对钒萃取率的影响.实验条件为:料液碱度为1.5 mol/L,料液中V2O5浓度为3.57 g/L,相比O/A为 2/1,振荡时间为10 min,水相体积为10 mL,改变温度为15℃、20 ℃、25 ℃、30 ℃、35 ℃、40 ℃、45 ℃,实验结果如表 3所示.
| 表3 温度对钒萃取率的影响 |
 |
| 点击放大 |
由表 3可看出,随着温度的升高,钒萃取率先升高后下降.当温度较低时,萃取剂活性比较低,导致萃取反应不充分,钒萃取效果不佳;当温度达到30 ℃时,萃取剂效率较高,之后随着温度的升高,钒萃取率反而下降,这是由于温度过高,有机相会因不断挥发而损失,同时温度越高能耗越大,对设备要求也就越高.综合考虑各因素,选择萃取钒的最适宜温度为30 ℃左右.
2.7 饱和萃取容量的测定和萃取等温线的绘制本研究采用饱和浓度法测定了该季铵盐萃取剂的饱和萃取容量,并绘制了钒萃取等温线.有机相组成为50 %三-十八烷基甲基氯化铵+20 %仲辛醇+30 %磺化煤油,料液碱度为1.5 mol/L,料液中V2O5浓度为3.57 g/L,相比O/A为 2/1,温度为25 ℃,振荡时间为10 min,水相体积为10 mL,实验结果如图 6所示.
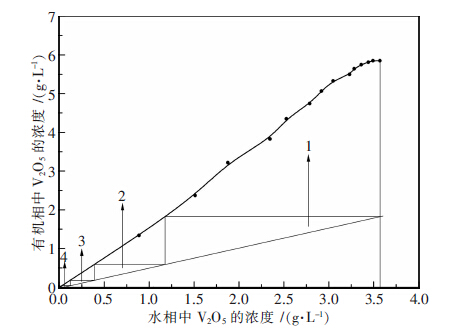 |
| 图 6 钒的萃取等温曲线 |
由图 6可以看出,组成为50 %三-十八烷基甲基氯化铵+20 %仲辛醇+30 %磺化煤油的有机相的饱和萃钒容量(以V2O5计)为5.85 g/L左右,同时该萃取等温线的斜率较大说明了该萃取体系萃取钒的能力较强.按照逆流萃取原理,通过绘制McCabe-Thiele图,可以估算逆流萃取所需级数.假设萃余液中钒浓度为0.05 g/L,按照O/A为2/1,绘制钒的操作曲线,从图 7可以看出,经过4级逆流萃取,水相中钒的浓度可以降低至0.05 g/L以下,考虑到级效应,一般在理论级数加上一级,故该萃取体系需要经过5级逆流萃取萃取钒.
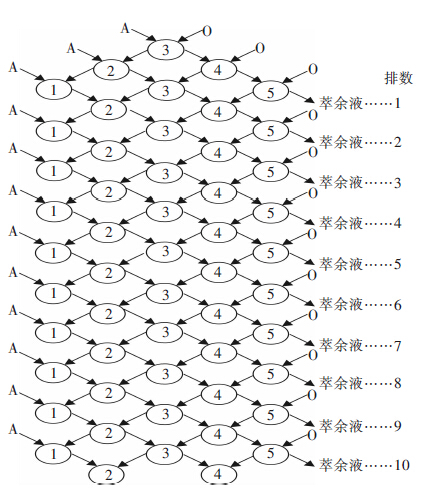 |
| 图 7 模拟五级逆流萃取实验操作流程图 |
本实验中采用5支分液漏斗进行模拟5级逆流萃取实验,实验操作流程图见图 7,图 7中A 代表水相,O代表有机相,圆圈代表分液漏斗,模拟实验排数一般为级数的2倍.实验中发现第6排后萃余液浓度变化不大,说明萃取达到了稳态,取7~10排分析萃余液中钒浓度,其结果见表 4.
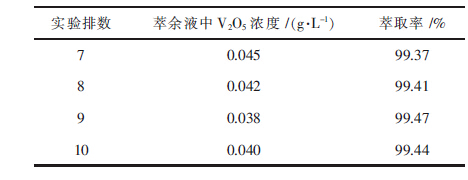
| 表4 模拟五级逆流萃取实验结果 |
 |
| 点击放大 |
由表 4可看出,经过5级逆流萃取后,萃余液中钒的浓度可降为0.05 g/L以下,钒萃取率可达到99.4 %.
3 结论1) 改性季铵盐CO32-型三-十八烷基甲基氯化铵能从高碱度含钒料液中直接萃取钒,随着料液碱度的增大,钒萃取率不断下降.当料液碱度为1.0 mol/L时,钒单级萃取率达到了90 %以上,而当料液碱度提高到3.0mol/L时,钒单级萃取率仅为40 %左右.该萃取剂可适用于萃取一定范围内高碱度的料液中的钒.
2)质量分数组成为50 %三-十八烷基甲基氯化铵 + 20 %仲辛醇 + 30 %磺化煤油的有机相从高碱料液(碱度为1.5 mol/L,V2O5浓度为3.57 g/L)中萃取钒的最佳萃取条件为:温度为30 ℃,相比O/A为2/1,振荡时间为10 min,钒的单级萃取率达到80 %.
3) 通过绘制钒萃取等温曲线可知,钒的饱和容量为5.85 g/L左右,钒的逆流萃取的理论级数为4级.经5级逆流萃取后,水相中钒浓度可降为0.05 g/L以下,钒萃取率可达到99.4 %.
| [1] | 杨守志. 钒冶金[M]. 北京: 冶金工业出版社 , 2010. |
| [2] | 马荣骏. 萃取冶金[M]. 北京: 冶金工业出版社 , 2009: 642. |
| [3] |
Mehra O K, Gupta C K. On the aluminothermic reduction of calcium vanadate[J].
Metallurgical Transactions, 1977, 88: 683–685. |
| [4] |
Pattnaik S P, Mukherjee T K. Ferrovanadium from a secondary soure of vanadium[J].
Metallurgical Transactions, 1983, 14B(133)–136. |
| [5] |
Mukherjee T K, Chakraborty S P, Bidaye A C, et al. Recovery of pure vanadium oxide from bayer sludge[J].
Miner. Eng., 1990, 3(3/4): 345–353. |
| [6] |
Zhao Z, Li X B, Zhao Q J. Recovery of V2O5 from Bayer liquor by ion exchange[J].
RARE METALS, 2010, 29(2): 115–119. DOI: 10.1007/s12598-010-0020-8. |
| [7] |
Zhao Z, Long H M, Li X B, et al. Precipitation of vanadium from Bayer liquor with lime[J].
Hydrometallurgy, 2012, 115(116): 52–56. |
| [8] | 赵卓,周吉奎,曹惠君.一种萃取法提取拜耳法种分母液中五氧化二钒的方法:中国,CN101117238A[P].2008:2-6. |
| [9] | 陈金清, 熊家任. 碱性体系下萃取钒的研究[J]. 有色金属科学与工程, 2014, 5(1): 20–23. |
| [10] | 陈金清, 朱志全, 陈传林. W/O微乳液对强碱体系中钒的萃取[J]. 有色金属(冶炼部分), 2010(4): 29–32. |
| [11] | 陈金清, 陈传林, 朱志全, 等. 强碱性体系提钒微乳液的制备研究[J]. 江西有色金属, 2010, 24(2): 19–22. |
| [12] | 张贵清, 张启修. 一种钨湿法冶金清洁生产工艺[J]. 稀有金属, 2003, 27(2): 254–257. |
| [13] | 张贵清, 关文娟, 张启修. 从钨矿苏打浸出液中直接萃取钨的连续运转试验[J]. 中国钨业, 2009, 24(5): 49–52. |
| [14] | 关文娟, 张贵清. 用季铵盐从模拟钨矿苏打浸出液中直接萃取钨[J]. 中国有色金属学报, 2011, 12(7): 1756–1762. |
| [15] | 柯兆华, 张贵清, 关文娟, 等. 季铵盐从碱性钨酸钠溶液中萃取钨的研究[J]. 稀有金属与硬质合金, 2012, 40(6): 1–5. |
| [16] | 柯兆华.从钨矿苛性钠浸出液中萃取钨制取纯钨酸铵的研究[D].长沙:中南大学,2012:17-18. |
 2015, Vol. 6
2015, Vol. 6

