| 含镉废渣机械力化学稳定研究 |
2. 国家重金属污染防治工程技术研究中心,长沙,410083
2. Chinese National Engineering Research Center for Control and Treatment of Heavy Metal Pollution, Changsha 410083, China
在有色冶炼生产中产生的含镉废渣会对人体健康和环境安全带来极大的危害[1].因此,寻找一种高效、经济、环保的含镉废渣处理技术显得十分迫切.
机械力化学技术在环保领域的应用是近年来的研究热点,特别是在废物处理与功能材料合成领域已开展应用[2-6].该技术是通过高能量机械力的不同作用方式,使受力物体的物理化学性质发生改变,从而提高或抑制其反应活性,并诱发化学反应[7- 8].机械力化学作为一种固体废物处理的新手段具有良好的应用前景,其最直观的效果就是能改变固废颗粒的粒径及表面性质,提高其反应活性.机械力化学在有机固体废物处理方面已有较成熟的应用,但在重金属固体废物处理方面却鲜有相关研究报道[9-11].Li M G等[12]针对市政垃圾焚烧烟灰球磨改性及固铅效果进行了研究,发现重金属铅在飞灰颗粒粒径变小、表面能增大、颗粒团聚过程中被包埋到重新团聚的颗粒中以实现重金属的稳定.Laszlo T [7]和Nomura Y等[10]认为机械力球磨可以促进自蔓延反应的发生.Chai L Y等[13-14]研究锌冶炼中和渣机械硫化时发现在添加单质硫磺情况下机械力球磨过程能将氧化锌硫化生成硫化锌,以达到回收重金属的目的.Montinaro S [15-17]和Palaniandy S等[18]认为机械力化学稳定重金属是由于在机械力诱导作用下,重金属离子进入到晶体网格里,从而形成稳定的化合物.
零价铁粉对重金属的吸附是当前的研究热点之一[19-21].本研究利用机械球磨改性零价铁粉颗粒以达到稳定废渣中镉的目的,并对球磨铁粉稳定镉的机理给出合理的解释.
1 实验材料和方法 1.1 材料含镉废渣样品为湖南某冶炼企业含镉废水经化学沉淀处理后的残渣.将样品在105 ℃下烘干备用.为了检测含镉废渣中重金属含量,将烘干的含镉废渣粉碎,并过150 mm筛,之后用王水进行消解.通过电感耦合等离子体原子发射光谱(ICP,IRIS Intrepid II XSP))检测消解液中各元素浓度.含镉废渣中各元素含量如表 1.
| 表1 含镉废渣元素含量/wt% |
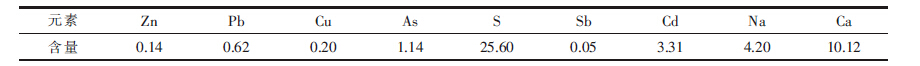 |
| 点击放大 |
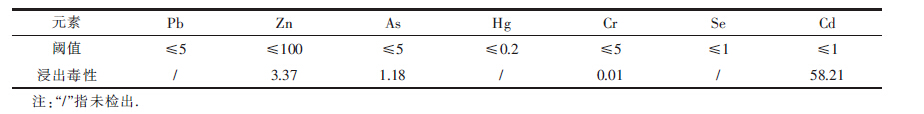
为了检测样品中重金属的浸出毒性,对其进行浸出毒性检测实验,结果如表 2.
| 表2 含镉废渣浸出毒性分析/mg |
 |
| 点击放大 |
实验中采用的球磨机为南京大学仪器厂生产的QM-QX4全方位行星式球磨机,球磨机的相关参数为:单罐容积500 mL,罐体介质为不锈钢,最大装料量为罐体容积3/4,额定转速为公转250 r/min,自转530 r/min.
1.2 实验方法研究主要以浸出毒性为稳定效果的评价指标,重点考察稳定剂种类、球磨介质(刚玉和不锈钢)、稳定剂用量(1%~12%)、球磨时间(0.25~3.5 h)和球料比(B:M =5:1~20:1)等工艺参数对球磨稳定效果的影响.首先将适量含镉废渣和稳定剂的混合物以及400 g小球放入球磨罐,在合适球料比条件下球磨适当时间,等球磨罐冷却至室温后将球磨产物取出,最后将球磨产物进行浸出毒性检测.
1.3 分析方法 1.3.1 浸出毒性浸出毒性按照美国TCLP浸出毒性鉴别方法进行检测[22].
1.3.2 镉的稳定率镉的稳定率是球磨稳定效果的表征指标.c0为球磨前含镉废渣的浸出浓度,cv为球磨后含镉废渣的浸出浓度.
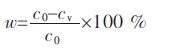
|
1) 酸可提取态:取0.5 g样品于50 mL离心管中,添加浓度为0.11 mol/L的CH3COOH溶液20 mL,室温下振荡16 h后,取上清液离心后过滤,滤液保存于4 ℃环境中.向离心管中加入10 mL去离子水,振荡清洗1 h后离心、洗液舍弃.
2) 可还原态:向上一步清洗后残渣中加入0.1 mol/L盐酸羟胺(pH=2.0)溶液20 ml,振荡16 h,按第1步方法振荡、离心、移液、洗涤.
3)可氧化态:向上一步残渣中加入5 mL H2O2(pH=2.0),盖子松开,于85 ℃恒温水浴中保持1 h,待溶液蒸至近干,冷却后继续添加5 mL H2O2(pH=2.0)重复上述操作.冷却后加入1.0 mol/L醋酸铵(pH=2.0)溶液25 mL,连续振荡16 h后,离心过滤.
4) 残渣态:将第3步残渣用王水消解后测其重金属含量.
2 结果与讨论 2.1 稳定剂种类对含镉废渣稳定效果的影响稳定剂种类是影响机械力球磨稳定效果的决定性因素.有研究表明铁系物质对废水中重金属的去除具有重要作用[24-27].因此,本研究利用零价铁粉、三氧化二铁、硫酸铁等铁类物质作为稳定剂,在不锈钢球磨介质、添加剂用量为4 %、球料比(B/M)为20:1的条件下球磨含镉废渣和稳定剂的混合物1 h.将球磨产物取出并检测其浸出毒性,结果如图 1所示.
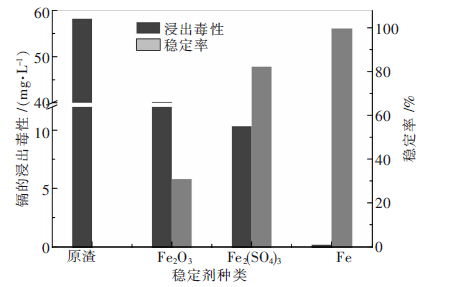 |
| 图 1 不同种类稳定剂对球磨稳定效果的影响 |
由图 1可知,在添加剂为零价铁粉时,镉的浸出毒性为0.159 mg/L、镉的稳定率为99.73 %.当添加剂为硫酸铁时,镉的浸出毒性10.344 mg/L、稳定率为82.23 %.这是因为硫酸铁在溶液中会形成水合氧化物和无定型氧化铁,其对重金属具有吸附作用.但是其吸附能力受体系pH 等影响较大.当稳定剂为氧化铁时镉的浸出毒性为40.192 mg/L,远远超过国家危险废物鉴别浸出毒性鉴别标准的限值.本研究结果说明零价铁粉对镉的稳定效果最显著,是一种良好的重金属球磨稳定剂.
2.2 球磨介质对含镉废渣球磨稳定效果的影响文献[28]报道,不同的球磨介质会影响球磨产物的结构和形貌特征.本研究重点关注了不锈钢球磨介质和刚玉球磨介质对含镉废渣球磨稳定效果的影响.在保持添加剂用量为4 %、球料比为B:M=20:1、球磨转速为500 r/min的条件下,分别用不锈钢介质和刚玉介质球磨含镉废渣和零价铁粉的混合物1 h.将球磨产物取出并检测其浸出毒性,结果如图 2所示.
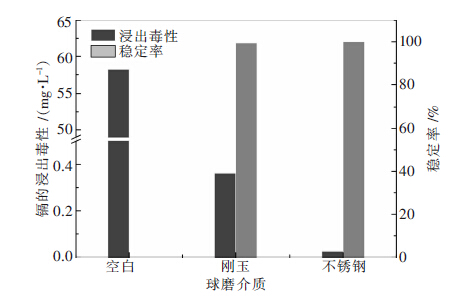 |
| 图 2 球磨介质对球磨稳定效果的影响 |
由图 2可知,利用不锈钢和刚玉介质球磨后的产物镉的浸出毒性分别为0.025 mg/L和0.362 mg/L,稳定率分别为99.96 %和99.38 %.两者在浸出毒性上的微小差别可能是由于不锈钢介质中的铁元素在球磨过程中进入物料,相当于造成了不锈钢介质中稳定剂的添加量大于刚玉介质.因此,本研究认为球磨介质对球磨稳定效果影响非常小.
2.3 稳定剂用量对含镉废渣球磨稳定效果的影响众所周知,反应体系中反应物含量的增加或减少直接影响反应产物的形成.因此,这就意味着只要控制好稳定剂的用量就能直接影响球磨稳定效果.本研究考察了在球磨介质为不锈钢、稳定剂为零价铁粉、球磨时间为1 h、B/M=20:1、球磨转速为500 r/min的条件下,不同稳定剂用量(1%~12%)对球磨稳定效果的影响.结果如图 3所示.
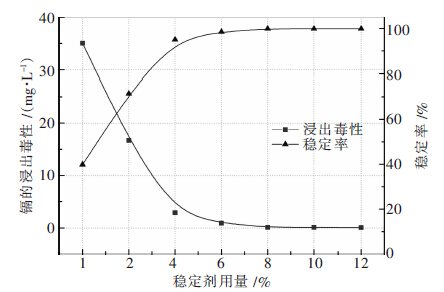 |
| 图 3 稳定剂用量对球磨稳定效果的影响 |
实验结果如图 3,随着稳定剂用量的增加,镉的浸出浓度首先快速降低而后趋于平稳.当稳定剂的用量为6 %时,镉的浸出浓度为0.890 mg/L,镉的稳定率为98.47 %.此时,体系中重金属离子含量已经很低,达到了吸附平衡状态,过多的稳定剂对镉的去除并无显著意义.基于稳定效果及稳定剂用量的考虑,研究认为当添加剂为6 %时,为最佳添加量.
2.4 球料比对含镉废渣稳定效果的影响有研究认为球料比决定了球磨罐中产生的能量密度大小,单位体积球磨罐中球料比越大,产生的能量密度越大,球磨反应越迅速越充分[29].本研究在稳定剂为零价铁粉、稳定剂用量为6 %、球磨介质为不锈钢、球磨时间为1 h、球磨转速为500 r/min的条件下,考察了球料比(B/M=5:1~20:1)对球磨稳定效果的影响.球磨后检测球磨产物的浸出毒性,结果如图 4.
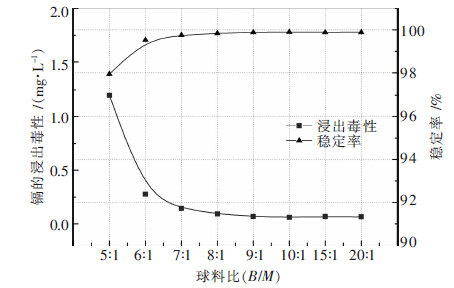 |
| 图 4 不同球料比对球磨稳定效果的影响 |
由图 4可知,随着球料比(B/M)增大,球磨后物料中镉的浸出毒性逐渐降低,最后趋于平稳.当球料比为6:1时,镉的浸出浓度为0.276 mg/L,镉的稳定率为99.53 %.随着球料比增加,单位体积内物料与球碰撞的几率增大,球磨反应效率也会提高,所以镉的浸出毒性会随着球料比增大而下降.基于球磨效率和浸出毒性的考虑,本研究认为当球料比B/M=6:1具有最佳球磨稳定效率.
2.5 球磨时间对含镉冶炼废渣稳定效果的影响球磨时间是球磨反应充分进行的重要保障.因此本研究考察了球磨时间为0.25~3.5 h,不同球磨时间对含镉废渣稳定效果的影响.稳定剂为零价铁粉、球磨介质为不锈钢、球料比B/M=6:1、稳定剂用量为6 %、球磨转速为500 r/min.结果如图 5.
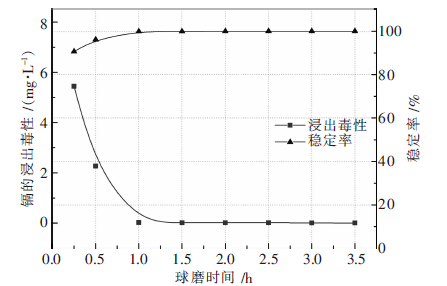 |
| 图 5 球磨时间对球磨稳定效果的影响 |
由图 5可知,废渣中镉的浸出毒性开始随着球磨时间增长而迅速降低,球磨1 h后镉的浸出毒性趋于平稳,球磨1 h后镉的浸出毒性为0.019 mg/L,镉的稳定率为99.97 %.此时球磨颗粒的粒径等已经达到动态平衡的状态,过长的球磨时间并不会对颗粒性质有较大的改变.由此可知,机械球磨反应是一个快速反应过程,过长的球磨时间对实现重金属废渣的稳定并无益处.
2.6 机械力化学稳定机制研究球磨物料在球磨过程中发生的反应十分复杂.为了研究含镉废渣球磨稳定过程中的稳定机制,本研究将零价铁粉和含镉废渣分别单独球磨,然后将原铁粉、球磨铁粉、原渣和球磨渣分别组合进行浸出毒性测试.具体组合方式如下:原渣(S)、原渣和零价铁粉(S+Fe)、球磨废渣和零价铁粉(S(G)+Fe)、原渣和球磨铁粉(S+Fe(G))、球磨废渣和球磨铁粉(S(G)+Fe(G))以及原渣和零价铁粉的混合球磨产物((S+Fe)(G)).不同组合浸出毒性结果如图 6所示.
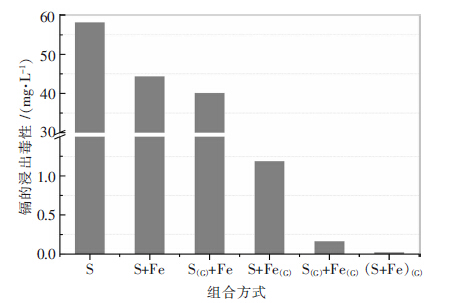 |
| 图 6 不同组合的浸出毒性 |
如图 6所示,从组合(S+Fe)和(S+Fe(G))、(S(G)+Fe)和(S(G)+Fe(G))的比对中可以发现只要体系中存在球磨铁粉,体系浸出毒性就比较小,而当体系中是原铁粉时,浸出毒性都在40 mg/L以上.所以球磨铁粉是实现废渣稳定化的关键,而球磨废渣对稳定化过程的作用有限.此外,从组合(S(G)+Fe(G))和((S+Fe)(G))的对比中可以发现,球磨稳定化过程发生在浸出毒性实验过程中而不是发生在球磨过程中,因为如果稳定过程发生在球磨过程中,那么组合((S+Fe)(G))的浸出毒性将远低于组合(S(G)+Fe(G))的浸出毒性,但实际却是组合(S(G)+Fe(G))和((S+Fe)(G))的浸出毒性差别很小.因此,本研究认为含镉废渣实现稳定化的关键是球磨铁粉,同时稳定过程发生在浸出毒性实验过程中.通过XRD 和 SEM-EDS检测发现:球磨产物中的球磨铁粉在酸性溶液中表面被腐蚀生成一层对镉具有吸附能力的腐蚀层,而这层腐蚀层对镉的吸附正是废渣中镉稳定化的原因.
球磨过程中铁粉物相和形貌的变化特征.球磨过程能极大的改变零价铁粉颗粒的表面性质和颗粒大小.铁粉颗粒粒径越小,其活性越高,在酸性溶液中形成腐蚀层的速度越快、数量越多.因此,将球磨前后零价铁粉颗粒粒径对比发现:球磨后零价铁粉颗粒累积粒径分布从球磨前的105 μm 降低到球磨后的40 μm.结合球磨铁粉SEM图分析可知,球磨过程仅仅改变了零价铁粉颗粒的粒径和表面形貌.球磨前后零价铁粉颗粒累积粒径分布如图 7所示.
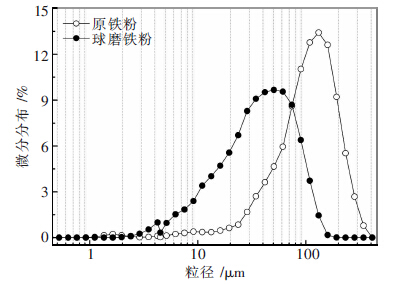 |
| 图 7 球磨前后铁粉颗粒累积粒径分布 |
为了模拟球磨铁粉在酸性环境下物相和形貌的变化,将球磨铁粉浸泡于pH=5.0的醋酸溶液中并翻转振荡18 h.之后将铁粉取出在真空干燥箱中干燥后进行XRD检测.结果如图 8所示.
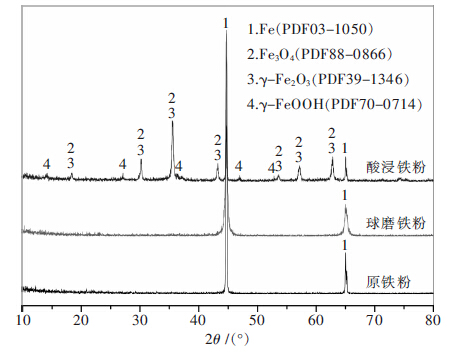 |
| 图 8 不同铁粉的XRD图谱 |
由图 8中原铁粉和球磨铁粉的XRD图谱分析可知,球磨前后两者的特征峰没有明显的变化,球磨铁粉的特征峰比原铁粉的特征峰略宽.但是醋酸浸泡后的球磨铁粉XRD图谱上明显出现了Fe3O4、γ-Fe2O3和γ-FeOOH的特征峰.说明球磨铁粉在醋酸溶液中表面被腐蚀生成了一层铁氧化物和水合氧化铁的腐蚀层.这一层腐蚀层对镉具有较强的吸附作用[30].具体反应方程式如下[21,31-32].
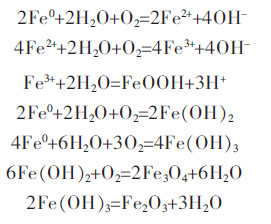
|
为了模拟零价铁粉对镉的吸附过程,本研究将球磨铁粉分别置于pH=5.0的醋酸溶液和浓度为1 000 mg/L,pH=5.0的含镉溶液中翻转振荡18 h.然后过滤收集残渣并用真空干燥箱进行干燥,对干燥后残渣进行SEM-EDS检测.其SEM-EDS结果如图 9所示.
 |
| 图 9 不同铁粉的SEM-EDS图 |
从图 9(a)和图 9(b)可以看出,铁粉颗粒的形状由球磨前的不规则颗粒状变成球磨后的片状.这种纳米级厚度的片状铁粉颗粒对镉的吸附具有重要意义.从图 9(c)中可以看出球磨铁粉在酸性溶液中腐蚀后,其表面会形成一层松散絮状腐蚀层,而图 9(c)-EDS表明此絮状物主要是铁的氧化物.从图 9(d)中可以发现,在含镉溶液中浸泡过的球磨铁粉颗粒表面出现了一层沉积物,而图 9(d)的EDS表明,此表面沉积物中含有大量的镉.其中图 9(d)中沉积物比图 9(c)中絮状物更密实,这是由于絮状腐蚀层吸附了镉,导致松散的腐蚀层变得密实.由此,本研究推断球磨铁粉颗粒在酸性溶液中被腐蚀,其表面产生一层腐蚀层,而这层铁氧化物和水合氧化铁的腐蚀层对镉的吸附是废渣中镉的浸出毒性降低的主要原因.
2.7 球磨后含镉废渣的稳定性评价为评价球磨处理后含镉废渣的环境稳定性以及在不同环境下镉的释放行为,本研究采用Davidson改进的BCR 3步连续浸提法对其进行浸提实验.有研究表明酸可提取态的重金属是对环境造成直接污染的主要原因,而残渣态是表征废渣稳定的主要指标.因此,降低重金属的酸可提取态,提高重金属的残渣态是重金属废渣稳定化研究的目标.由图 10可知,球磨前后废渣中镉的酸可提取态和可还原态的含量都很少,但降低的趋势也十分明显.废渣中镉的主要形态为可氧化态和残渣态.其中可氧化态由球磨前的65.15 %降低到球磨后的53.57 %,残渣态由球磨前的34.71 %增加到球磨后的46.42 %.由此可知球磨过程将活性较高的镉转化为残渣态的镉,整体上对含镉废渣起到了一定的稳定化效果.具体结果如图 10所示.
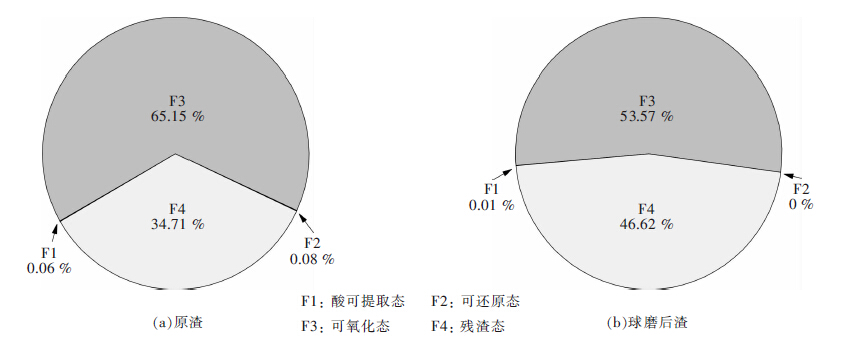 |
| 图 10 球磨前后镉的BCR分析 |
3 结论
在稳定剂为零价铁粉的情况下,用机械力球磨方法能实现含镉废渣的稳定化.基于此研究结果,本研究可以得出以下结论:
1)含镉废渣球磨稳定最佳工艺参数如下:稳定剂为零价铁粉、球磨介质为不锈钢、稳定剂用量为6 %、球料比B/M=6:1、球磨时间为1 h.在最佳工艺条件下镉的浸出浓度由58.212 mg/L 降低至0.019 mg/L,镉的稳定率为99.97 %,球磨后废渣中镉浸出毒性低于国家危险废物鉴别浸出毒性标准.
2) 球磨铁粉在酸性环境下其表面会被腐蚀生成一层铁氧化物和水合氧化铁的腐蚀层,而这层腐蚀层对镉的吸附作用是废渣中镉的浸出毒性降低的主要原因.
3) 机械力球磨能实现含镉废渣的稳定化.球磨后废渣中镉的酸可提取态和可还原态几乎为零,而可氧化态由球磨前的65.15 %降低到球磨后的53.57 %,残渣态由球磨前的34.71 %增加到球磨后的46.42 %.
| [1] | 王积伟, 张培玉, 陈舒, 等. 五种重点关注的重金属废渣的处理方法与利用现状[J]. 环境工程, 2011(增刊1): 212–216. |
| [2] |
Wu S M, Xue Y Z, Zhou L M, et al. Structure and morphology evolution in mechanochemical processed CuInS2 powder[J].
Journal of Alloys and Compounds, 2014, 600(0): 96–100. |
| [3] |
Lu S, Huang J, Peng Z, et al. Ball milling 2,4,6-trichlorophenol with calcium oxide: Dechlorination experiment and mechanism considerations[J].
Chemical Engineering Journal, 2012, 195-196: 62–8. DOI: 10.1016/j.cej.2012.04.042. |
| [4] |
Stellacci P, Liberti L, Notarnicola M, et al. Valorization of coal fly ash by mechano-chemical activation: Part I. Enhancing adsorption capacity[J].
Chemical Engineering Journal, 2009, 149(1/2/3): 11–8. |
| [5] |
Stellacci P, Liberti L, Notarnicola M, et al. Valorization of coal fly ash by mechano-chemical activation: Part II. Enhancing pozzolanic reactivity[J].
Chemical Engineering Journal, 2009, 149(1/2/3): 19–24. |
| [6] |
Setoudeh N, Welham N J. Ball milling induced reduction of SrSO4 by Al[J].
International Journal of Mineral Processing, 2011, 98(3/4): 214–8. |
| [7] |
Takacs L. Self-sustaining reactions induced by ball milling[J].
Progress in Materials Science, 2002, 47(4): 355–414. DOI: 10.1016/S0079-6425(01)00002-0. |
| [8] |
Calos N J, Forrester J S, Schaffer G B. A Crystallographic Contribution to the Mechanism of a Mechanically Induced Solid State Reaction[J].
Journal of Solid State Chemistry, 1996, 122(2): 273–280. DOI: 10.1006/jssc.1996.0113. |
| [9] |
Zhang W, Huang J, Yu G, et al. Mechanochemical destruction of Dechlorane Plus with calcium oxide[J].
Chemosphere, 2010, 81(3): 345–350. DOI: 10.1016/j.chemosphere.2010.07.025. |
| [10] |
Nomura Y, Fujiwara K, Terada A, et al. Mechanochemical degradation of γ-hexachlorocyclohexane by a planetary ball mill in the presence of CaO[J].
Chemosphere, 2012, 86(3): 228–234. DOI: 10.1016/j.chemosphere.2011.09.030. |
| [11] |
Inoue T, Miyazaki M, Kamitani M, et al. Dechlorination of polyvinyl chloride by its grinding with KOH and NaOH[J].
Advanced Powder Technology, 2005, 16(1): 27–34. DOI: 10.1163/1568552053166638. |
| [12] |
Li M G, Sun C J, Gau SH, et al. Effects of wet ball milling on lead stabilization and particle size variation in municipal solid waste incinerator fly ash[J].
Journal of Hazardous Materials, 2010, 174(1/2/3): 586–691. |
| [13] |
Chai L Y, Liang Y J, Ke Y, et al. Mechano-chemical sulfidization of zinc oxide by grinding with sulfur and reductive additives[J].
Transactions of Nonferrous Metals Society of China, 2013, 23(4): 1129–1138. DOI: 10.1016/S1003-6326(13)62575-3. |
| [14] |
Ke Y, Chai L Y, Liang Y J, et al. Sulfidation of heavy-metal-containing metallurgical residue in wet-milling processing[J].
Minerals Engineering, 2013, 53(0): 136–143. |
| [15] |
Montinaro S, Concas A, Pisu M, et al. Remediation of heavy metals contaminated soils by ball milling[J].
Chemosphere, 2007, 67(4): 631–639. DOI: 10.1016/j.chemosphere.2006.11.009. |
| [16] |
Montinaro S, Concas A, Pisu M, et al. Immobilization of heavy metals in contaminated soils through ball milling with and without additives[J].
Chemical Engineering Journal, 2008, 142(3): 271–284. DOI: 10.1016/j.cej.2007.12.003. |
| [17] |
Montinaro S, Concas A, Pisu M, et al. Rationale of lead immobilization by ball milling in synthetic soils and remediation of heavy metals contaminated tailings[J].
Chemical Engineering Journal, 2009, 155(1/2): 123–131. |
| [18] |
Palaniandy S, Azizli K A M, Hussin H, et al. Study on mechanochemical effect of silica for short grinding period[J].
International Journal of Mineral Processing, 2007, 82(4): 195–202. DOI: 10.1016/j.minpro.2006.10.008. |
| [19] |
Kowalski K P, S Gard E G. Implementation of zero-valent iron (ZVI) into drinking water supply – Role of the ZVI and biological processes[J].
Chemosphere, 2014, 117: 108–114. DOI: 10.1016/j.chemosphere.2014.05.088. |
| [20] |
Chang G D, Chen T, Liu H, et al. A new approach to prepare ZVI and its application in removal of Cr(VI) from aqueous solution[J].
Chemical Engineering Journal, 2014, 244: 264–272. DOI: 10.1016/j.cej.2014.01.095. |
| [21] |
Wan J, Pressigout J, Simon S, et al. Distribution of As trapping along a ZVI/sand bed reactor[J].
Chemical Engineering Journal, 2014, 246: 322–327. DOI: 10.1016/j.cej.2014.02.073. |
| [22] |
US A. Environment Protection Agency Office of Solid Waste[J].
Hazardous Waste Characteristics Scoping Study, 1996(3): 1/3. |
| [23] |
Nemati K, Abubakar N K, Sobhanzadeh E, et al. A modification of the BCR sequential extraction procedure to investigate the potential mobility of copper and zinc in shrimp aquaculture sludge[J].
Microchemical Journal, 2009, 92(2): 165–174. DOI: 10.1016/j.microc.2009.03.002. |
| [24] |
Naseri E, Reyhanitabar A, Oustan S, et al. Optimization arsenic immobilization in a sandy loam soil using iron-based amendments by response surface methodology[J].
Geoderma, 2014, 232-234: 547–555. DOI: 10.1016/j.geoderma.2014.06.009. |
| [25] |
Song S, Lopez V A, HERNANDEZ-CAMPOS D J, et al. Arsenic removal from high-arsenic water by enhanced coagulation with ferric ions and coarse calcite[J].
Water Research, 2006, 40(2): 364–372. DOI: 10.1016/j.watres.2005.09.046. |
| [26] |
Liu R P, Sun L H, Qu J H, et al. Arsenic removal through adsorption, sand filtration and ultrafiltration: In situ precipitated ferric and manganese binary oxides as adsorbents[J].
Desalination, 2009, 249(3): 1233–1240. DOI: 10.1016/j.desal.2009.06.032. |
| [27] |
Streat M, Hellgardt K, Newton N L R. Hydrous ferric oxide as an adsorbent in water treatment: Part 3: Batch and mini-column adsorption of arsenic, phosphorus, fluorine and cadmium ions[J].
Process Safety and Environmental Protection, 2008, 86(1): 21–30. DOI: 10.1016/j.psep.2007.10.009. |
| [28] |
Nasiri T B, Honarmandi P, Ebrahimi K R, et al. Synthesis of nanosize single-crystal hydroxyapatite via mechanochemical method[J].
Materials Letters, 2009, 63(5): 543–549. DOI: 10.1016/j.matlet.2008.11.030. |
| [29] |
Kuziora P, Wyszynska M, Polanski M, et al. Why the ball to powder ratio (BPR) is insufficient for describing the mechanical ball milling process[J].
International Journal of Hydrogen Energy, 2014, 39(18): 9883–9890. DOI: 10.1016/j.ijhydene.2014.03.009. |
| [30] |
Sun F, Osseo A K A, Chen Y, et al. Reduction of As(V) to As(III) by commercial ZVI or As(0) with acid-treated ZVI[J].
Journal of Hazardous Materials, 2011, 196(0): 311–318. |
| [31] |
Triszcz J M, Porta A, Einschlag F S G. Effect of operating conditions on iron corrosion rates in zero-valent iron systems for arsenic removal[J].
Chemical Engineering Journal, 2009, 150(2/3): 431–440. |
| [32] |
Ye M, Huang J, Chen R, et al. Removeal of Arsenic (III) from Water by Using a New Class of Zero-Valent Iron Modified Mesoporous Silica Molecular Sieves SBA-15[J].
Advanced Materials Research, 2012, 356: 423–432. |
 2015, Vol. 6
2015, Vol. 6


