| 1 090 K下MgCl2-KCl-CaCl2三元熔盐体系的密度预测 |
2. 中冶南方工程技术有限公司,武汉 430223
2. WISDRI Engineering & Research Incorporation Limited, Wuhan 430223, China
镜电解工艺中,采用的电解质主要成分包括MgCl2、NaCl、CaCl2、KCl、BaCl2 等.在镜电解采用的电解质中,镜离子在阴极放电,从而沉积出金属镜;阳极区域内氯离子放电,析出氯气.这就是镜电解生产的基本原理.工业实践中,镜电解的电解质使用多组分氯化物熔盐体系. 由于不同化合物在熔体中相互作用,熔体的结构十分复杂,与单-体系相比,熔盐体系的热力学性质和电化学性质都会发生改变.通过改变镜电解采用的电解质体系的组分,可以调整相应的物理化学性质,以优化镜电解工艺,节能降耗.工业生产和研究中关注的镜电解所用熔盐体系性质包括电解质的密度、教度、熔度、表面性质、蒸汽压、导电率、离子迁移度以及关键组分的活度.电解质熔盐体系的各种性质都有着具体的要求,其中熔盐的密度要求-般比液相金属镜密度高出0.03-0.12 g/cm3.这样可以保证金属液相与熔盐能有效地分离,使得金属镜浮在熔盐表面,并且其暴露的表面也不会太多[1].
熔盐体系性质参量可以通过实验测定和模型预测得到.性质测定实验中的要有2 个:首先,在高温条件下,氯化物的蒸气压很高[2].随着温度的升高,氯化物蒸气压呈指数型上升.由于镜电解质体系中不同氯化物在同-条件下对应的蒸汽压不-样,因此在实验过程中所测熔盐组分会发生-定程度的变化,这会影响实验结果的准确性.另外,氯化物熔盐在实验前往往需要纯化处理,如通过真空方法、电化学方法、或含氯气体处理熔盐[3-5].其实验条件要求相对较高,很难得到准确可靠的结果.因此,基于有限的实验数据,通过模型预测熔盐电解质的性质具有其现实意义.
镜电解所用电解质组元多为氯化物.文献[6]中预测了在1 080 K 下CaCl2-KC1-NaC1 三元体系的密度.由预测结果可见,这-三元体系中,随着CaCl2 的加入,熔盐密度逐渐增大. 因此CaCl2 加入会促进液相镜珠上浮.文献[7]则通过不同的计算方法预测了NaC1-MgCl2-CaCl2 三元熔盐体系在1 080 K 时的密度分布. 与已知实验值对比,相应成分点的预测值误差在0.7 %左右,取得了很好的预测效果.MgCl2-KC1-CaCl2 三元熔盐体系是镜电解用多元电解质组分中的重要基础三元系.其物理化学性质的预测具有重要的意义.本文将通过新-代溶液几何模型预测这-体系的密度,并与已知的实验数据进行对比,佐以考察其预测的准确性.
1 二元体系的密度MgCl2-KC1-CaCl2 三元熔盐体系中熔点最高的组分点为CaCl2 相,熔点为1 055 K,而熔点最低的组分点则为62 wt% KC1,35 wt% MgCl2 和3 wt% CaCl2,此时三元体系的熔点为707 K[8].在1 080 K 时,这-三元体系在全组分范围内都处于熔融的单-相状态.MgCl2-CaCl2 二元体系中没有中间化合物.在KC1-MgCl2 二元体系中,存在2 个中间化合物:KC1.MgCl2 和2KC1.MgCl2,其中后者为不稳定化合物.KC1-CaCl2 二元体系中,则存在-个稳定的化合物KC1.CaCl2.
作为熔盐性质的权威数据库,NSRDS (Nationa1 Standard Reference Data Series) 提供了丰富的熔盐性质数据. 其中文献[8-9] 收集总结了MgCl2-CaCl2、KC1-MgCl2、KC1-CaCl2 及MgCl2 -KC1 -CaCl2 这4 个体系的实验密度值.所提供的密度数据值可以用式(1)表达:
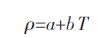
|
(1) |
其中,ρ 为熔盐密度值,其单位为g/cm3.T 为温度,其单位为K.而α 和b 均为常数.-般来说,这-经验式适用于表达较小温度范围内熔体物理化学性质与温度的关系. 所收集的不同体系的数据精度有所不同. 其中MgCl2-CaCl2 熔融体系的密度值误差在1.0 % 左右范围内,KC1-MgCl2 熔融体系的密度值误差在1.5 %左右范围内,而KC1-CaCl2 熔融体系的密度值误差也在1.5 %左右范围内.
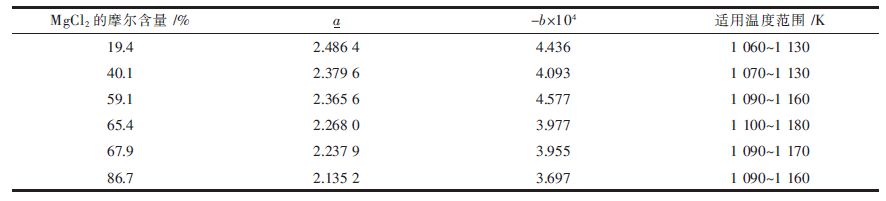
然而所述文献[8-9]中收集的MgCl2-CaCl2 二元体系的密度值并不正确,应当是由笔误所至.依据其收集数据对应的参考文献,尤其是Grjotheim[10] 的实验测量数据,我们勘正的密度数据如表 1 所示.
| 表1 MgCl2-CaCl2 二元体系密度计算式(1)中的参数 |
 |
| 点击放大 |
要使用新-代溶液几何模型对MgCl2-KC1-CaCl2三元熔盐体系密度进行预测,需要对所收集的3 个二元熔盐体系(KC1-CaCl2、MgCl2-CaCl2、KC1-MgCl2)在1 090 K 下的性质参数进行拟合,所得结果如图 1所示.
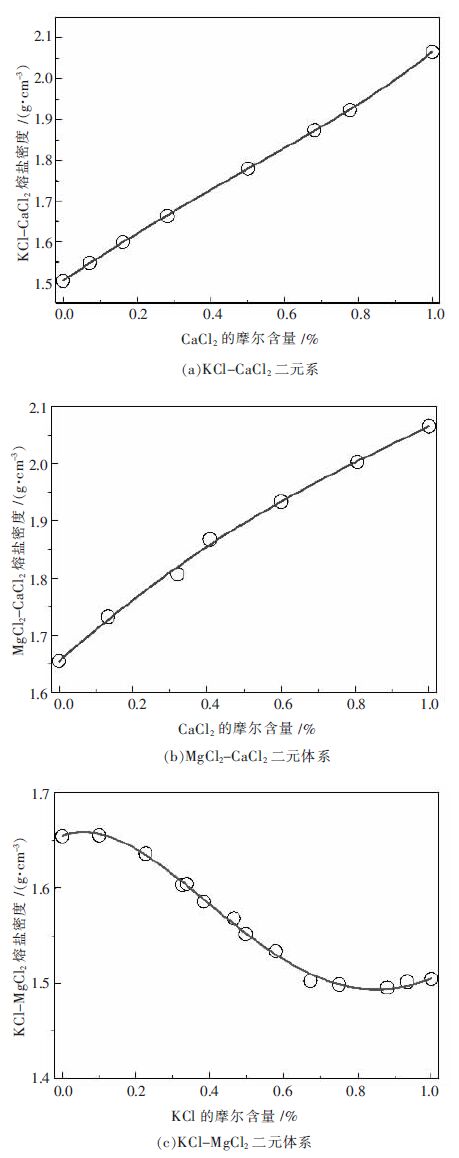 |
| 图 1 各氯化物熔盐二元系在1 080 K 下的密度值及Redlich-Kister 关系式预测值(实线) |
多元体系的物理化学性质通常可以分为2 个部分,其中-个部分为理想性质参数,另-个部分为超额性质参数.多元体系物理化学性质则为这两个部分的加和.对于二元体系而言,其物理化学性质表达式如式(2):
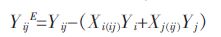
|
(2) |
式(2)中,YijE 即是i-j 二元体系中,在组元i 的摩尔含量为Xi(ij)这-成分点时,体系的超额性质量.而Yij 为i-j 二元体系在元i 的摩尔含量为Xi(ij)这-成分点时的物理化学性质量.括号内的参量之和,为这-组分下体系的理想性质参数.其中Yi 和Yj 是纯组元i 和j的性质量.二元体系中,X i(ij)+X j(ij)=1.可见,二元体系的理性性质参量与组元摩尔量的关系是线性的.在纯组元点,体系的超额量为0.二元体系的超额性质函数YijE 与二元系组元摩尔量之间的关系可以用Red1ich-Kister 关系式[11]表达.使用中,这-关系式扩展到了三次方:
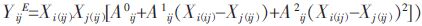
|
(3) |
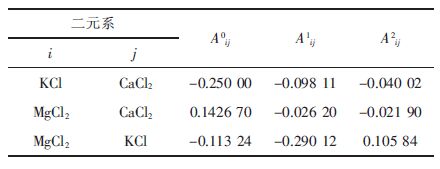
式(3) 中的3 个参数Aij0 ,Aij1 和Aij2 均是该二元系性质的特征参数. 由图 1 可见,采用式(3) 拟合所得结果与实验值相符,所得相关系数均在0.996 以上. 拟合所得参数均列于表 2 中. 其中使用的各纯相在1 090 K 的密度值分别是:MgCl2 为1.655 g/cm3,KC1 为1.505 g/cm3,以及CaCl2 为2.065 g/cm3.
| 表2 式(3)拟合各二元熔盐体系密度时所得参数 |
 |
| 点击放大 |
2 密度预测方法
采用的密度预测方法为周国治先生提出的新-代溶液几何模型[12-14]. 这-模型经过了20 余年的发展,积累了大量的预测数据,也证明了其预测结果具有很好的可靠性.近年来,Zhang[15]和I1oukhani 等[16]将这-模型应用到了四元体系的物理化学性质预测中,取得了很好的结果.新-代溶液几何模型是基于二元溶液或熔体体系所测得的性质数据,通过计算推演出整个三元体系或者更高元体系中的性质分布. 另外,如果仅仅是已知-个多元体系中有限的物理化学性质数据点,则可以通过质量三角型模型推演相关区域的性质分布[17-18].下面简要叙述新-代溶液几何模型计算方法.
与二元体系相似,三元体系i-j-k 也可以使用超额函数来表达其物理化学性质:
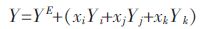
|
(4) |
在新-代溶液几何模型中,超额函数可用式(5)计算:
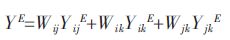
|
(5) |
以i-j 二元系为例,其对应的权重因子
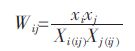
|
(6) |
式(6)中,xi 与xj 均为三元系中的组元摩尔分数,由此可知xi+xj+xk=1.而Xi(ij)与Xj(ij)如前所述,是相应i-j 二元系中按照-定规则对应的组元的摩尔分数. Xi(ij) 与xi 的关系式(7)所示:
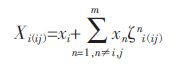
|
(7) |
式(7 ) 中出现的新的参数,被定义为相似系数,它是几何模型中最重要的-个参数. 相似系数表征了2 个二元系性质函数之间的相似程度. 其计算方法为:
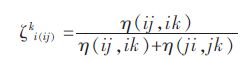
|
(8) |
式(8)中的函数η(ij,ik)可以定义为不同的式子,这也会导致不同的算法.文献[7]中比较了多种计算方法,所得预测效果相差不大,这与相似系数近似于"归-化"的作用是息息相关的.在模型预测中,-般采用下述算法:
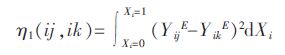
|
(9) |
另-种常被提及的计算方法则是
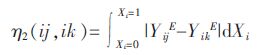
|
(10) |
在本研究中,采用式(9)的函数来计算相似系数. 假设在这个三元系中,MgCl2 为组元i,KC1 为组元j,而CaCl2为组元k. 通过计算,可得到3 个相似系数,分别是:ξi (ij)k 为0.615 0,ξij (ij)k 为0.210 6,而ξik (ij)k为0.701 2.
3 三元体系的密度通过计算,可以得出1 090 K 时MgCl2-KC1-CaCl2 三元熔盐体系全范围的密度分布,如图 2 所示.由实验结果分析可知,MgCl2-KC1-CaCl2 熔盐体系密度最小为1.494 g/cm3,其KC1 摩尔分数为85 % ,MgCl2 ( 摩尔分数) 为15 %. 随着CaCl2 的加入,熔盐密度逐渐提高. 在低CaCl2 含量时,随着KC1 含量的增加,熔盐密度先降低,而后在近20 % KC1 ( 指摩尔分数) 左右有所上升,之后再平缓降低. 在CaCl2 含量较多的区域,熔盐密度值几乎是线性地随CaCl2 摩尔分数的增加而增加.在1 173 K 以下,金属镜的密度与温度的关系可以用下式表示[19-20]:
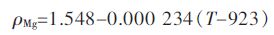
|
(11) |
由式(11) 可以计算出在1 090 K,熔融金属镜的密度为1.549 g/cm3.可知在此温度下,熔盐密度在1.579-1.669 g/cm3 为宜. 这-密度范围所对应的熔盐成分如图 2 中阴影区域所示. 当在这-三元系基础上加入NaC1、BaCl2 等组分后,电解质的密度会有所变化.
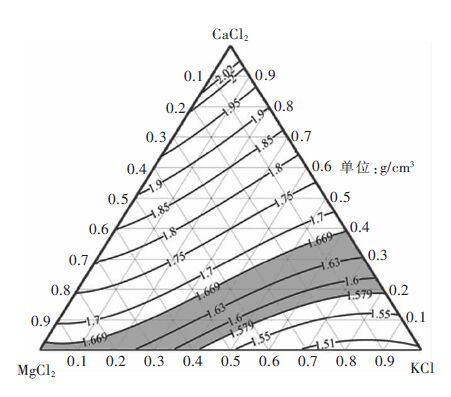 |
| 图 2 MgCl2-KCI-CaCl2 三元系在1 090 K 下的密度值 |
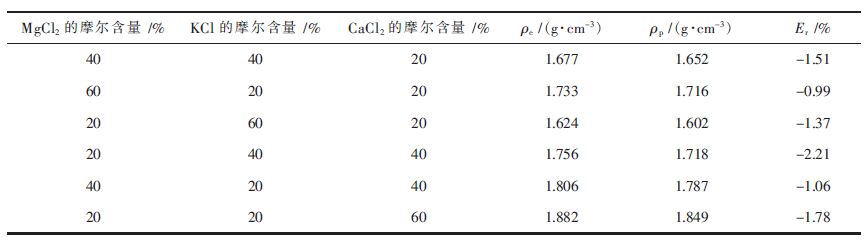
为了进-步验证预测结果的可靠性,需要将理论预测值与实验测量值对比.表 3 中列出了文献[8-9] 中收集的1 090 K 下MgCl2-KC1-CaCl2 三元系密度数据以及相应成分点的理论预测数据. 表 3 中列出的相对误差是用式(12)计算得出:为了进-步验证预测结果的可靠性,需要将理论预测值与实验测量值对比.表 3 中列出了文献[8-9] 中收集的1 090 K 下MgCl2-KC1-CaCl2 三元系密度数据以及相应成分点的理论预测数据. 表 3 中列出的相对误差是用式(12)计算得出:
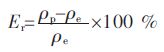
|
(11) |
式(12) 中,Er 为相对误差,ρe 为文献中收集的实验值,ρp 为采用新-代溶液几何模型预测值. 由表 3 可见,通过模型预测的密度值与文献中收集的实验值相比,相对误差绝对值最大为2.21 % ,最小仅为0.99 %.理论预测结果均偏小.相较而言,文献[10]中纯物质实验值与文献参值误差最大为7.75 %,最小为0.00 %.而如前所述,二元系数据的误差约为1.5 % 或以下.由此可知,理论预测值与实验值之间的相对误差并不大,在可接受的范围内.
| 表3 MgCl2-KCI-CaCl2 三元体系在1 090 K 下的密度实验值与计算值 |
 |
| 点击放大 |
4 结论
1) 通过新-代溶液几何模型这-方法,在以Redlich-Kister 关系式拟合KCl-CaCl2、MgCl2-CaCl2、KCl-MgCl2 3 个元系超额密度函数值的基础上,预测了MgCl2-KCl-CaCl2 三元系在1 090 K T 的全组分范围内的密度分布.
2) 通过与已知的文献实验值对比,该模型预测值相对误差在2.21 %以T,准确度较好.
3) 勘正了NSRDS 发布的MgCl2-CaCl2 二元体系的密度数据值.
| [1] | 张永键. 镁电解生产工艺学[M]. 长沙: 中南大学出版社 , 2006. |
| [2] | 陈志远, 刘俊昊, 周国治. 钛氧化物熔盐电脱氧工艺用氯化物熔盐的选择[J]. 中国材料进展, 2012, 31(1): 44. |
| [3] |
Alexander D T L, Schwandt C, Fray D J. The electro-deoxidation of dense titanium dioxide precursors in molten calcium chloride giving a new reaction pathway[J].
Electrochim Acta, 2011, 56(9): 3286. DOI: 10.1016/j.electacta.2011.01.027. |
| [4] |
Yasuda K, Nohira T, Ogata Y H, et al. Electrochemical window of molten LiCl-KCl-CaCl2 and the Ag+/Ag reference electrode[J].
Electrochim Acta, 2005, 51(3): 561. DOI: 10.1016/j.electacta.2005.05.014. |
| [5] |
Castrillejo Y, Bermejo M, Pardo R, et al. Use of electrochemical techniques for the study of solubilization processes of cerium-oxide compounds and recovery of the metal from molten chlorides[J].
J Electroanal Chem, 2002, 522(2): 124. DOI: 10.1016/S0022-0728(02)00717-9. |
| [6] |
Chen Z Y, Liu J H, Yu Z Y, et al. Electrical conductivity of CaCl2-KCl-NaCl system at 1080K[J].
Thermochim Acta, 2012, 543: 107. DOI: 10.1016/j.tca.2012.05.007. |
| [7] |
Chen Z Y, Wang L J, Chou K C, et al. Comparison of different calculation methods of the new generation geometric model in the Predicting Density of the NaCl-MgCl2-CaCl2[J].
J Solution Chem, 2013, 43: 577. |
| [8] | Janz G J, Tomkins R. NSRDS-NBS 61, IV. Physical properties data compilations relevant to energy storage. IV. Molten salts: Data on additional single and multi-component salt systems[R]. Washington: U. S. Government printing office, 1981. |
| [9] |
Janz G J. Thermodynamic and transport properties for molten salts: correlation equations for critically evaluated density, surface tension, electrical conductance, and viscosity data[J].
J Phys Chem Ref Data, 1988, 17(suppl 2): 1. |
| [10] |
Grjotheim K, Holm J, Lillebuen B, et al. Densities and excess molar volumes of binary and ternary melts of MgCl2, CaCl2 and AlkCl[J].
Trans Faraday Soc, 1971, 67: 640. DOI: 10.1039/TF9716700640. |
| [11] |
Redlich O, Kister A. Algebraic representation of thermodynamic properties and the classification of solutions[J].
Ind Eng Chem, 1948, 40(2): 345. DOI: 10.1021/ie50458a036. |
| [12] |
Chou K C. A general solution model for predicting ternary thermodynamic properties[J].
Calphad, 1995, 19(3): 315. DOI: 10.1016/0364-5916(95)00029-E. |
| [13] |
Chou K C, Wei S K. A new generation solution model for predicting thermodynamic properties of a multicomponent system from binaries[J].
Metall Mater Trans B, 1997, 28(3): 439. DOI: 10.1007/s11663-997-0110-7. |
| [14] |
Chou K C. A new solution model for predicting ternary thermodynamic properties[J].
Calphad, 1987, 11(3): 293. DOI: 10.1016/0364-5916(87)90048-4. |
| [15] |
Zhang G H, Wang L J, Chou K C. A comparison of different geometrical models in calculating physicochemical properties of quaternary systems[J].
Calphad, 2010, 34(4): 504. DOI: 10.1016/j.calphad.2010.10.004. |
| [16] |
Iloukhani H, Khanlarzadeh K. Physicochemical properties of quaternary systems and comparison of different geometrical models[J].
J Chem Eng Data, 2011, 56(11): 4244. DOI: 10.1021/je200873y. |
| [17] |
Wang L J, Chen S L, Chou K C, et al. Calculation of density in a ternary system with a limited homogenous region using a geometric model[J].
Calphad, 2005, 29(2): 149. DOI: 10.1016/j.calphad.2005.05.003. |
| [18] |
Chou K C, Zhong X M, Xu K D. Calculation of physicochemical properties in a ternary system with miscibility gap[J].
Metall Mater Trans B, 2004, 35(4): 715. DOI: 10.1007/s11663-004-0011-y. |
| [19] | Lide D R. CRC handbook of chemistry and physics[M]. Boca Raton: CRC press , 2004. |
| [20] |
Nasch P, Steinemann S. Density and thermal expansion of molten manganese, iron, nickel, copper, aluminum and tin by means of the gamma-ray attenuation technique[J].
Phys Chem Liq, 1995, 29(1): 43. DOI: 10.1080/00319109508030263. |
 2014, Vol. 5
2014, Vol. 5


