| 超细氧化钨的制备及其光催化性能研究 |
b. 江西理工大学,钨资源高效开发及应用技术教育部工程研究中心,江西赣州341000
b. Engineering Research Center of High-efficiency Development and Application Technology of Tungsten Resources (Ministry of Education), Jiangxi University of Science and Technology, Ganzhou 341000, China
氧化钨是一种重要的功能材料,具有半导体特性,超细氧化钨因其较高的比表面积而表现出特殊的表面效应[1-2],如催化、隐形等.制备超细氧化钨的方法有液相沉积法、气相沉淀法、热分解法等[3-5].由于超细颗粒具有粒度小,表面积大和表面能高的特点,在气相和液相介质中极易团聚成颗粒较大的二次颗粒,从而导致其性能劣化.所以针对改善颗粒间团聚现象,采取有效的制备途径和方法显得格外重要[6-8].液相法制备钨酸的过程中,钨酸粒子因热力学不稳定性而具有自动聚结的趋势,此外,粒子表面上的自由水分子与自由羟基形成氢键,水分子和相邻颗粒表面上的羟基也容易形成氢键,产生桥连作用并进一步形成硬团聚.钨酸经煅烧后,颗粒度显著增大,影响了其性能发挥.因此,如果能在钨酸形成过程中,提供模板或隔离剂,将钨酸颗粒互相隔离,阻止或抑制水分子与其表面上羟基形成的氢键,以及颗粒间形成的氢键,对改善硬团聚有着重要的意义.
模板法是利用模板为主体去控制和修饰材料的形貌、尺寸,进而改善材料性质的一种制备方法[9-11].利用其空间限域作用和结构导向作用,能够有效防止纳米颗粒二次团聚现象的发生,可对合成颗粒的尺寸、形貌、结构和排列等进行有效的调制.碳纳米管因具有极大的比表面积和化学稳定性[12],以及独特的电子结构、特殊的孔腔空间立体选择性和对反应物种、反应产物的特殊吸附及脱附性能,越来越多地被用作催化剂载体[13-20].
文中将钨酸颗粒直接沉积在碳纳米管管壁上,形成H2WO4-CNTs复合物,经高温煅烧,生成了氧化钨颗粒.由于采用均匀分散的碳纳米管管束作为载体,使钨酸沉淀在整个溶液中由于碳纳米管管束的阻隔,不致于生长过快,从而控制了钨酸颗粒的生长速率,大幅度减少了颗粒间结合力,从而有效地阻止团聚现象的产生.经氧气气氛煅烧后,得到的超细氧化钨粉末颗粒度较小.
1 实验部分 1.1 样品的制备研究所用的碳纳米管(CNTs)为课题组制备碳纳米管薄膜过程中的副产物[21-22].以乙二醇作分散剂,借助超声空化效应作用将CNTs均匀地分散于乙二醇中,并将其剪切成短束状(长度小于5 μm).具体过程为:将10 mg CNTs和100 mL乙二醇加入到密闭试剂瓶中,置于800 W的超声波清洗器中进行超声分散12 h,得到分散均匀的CNTs悬浮液.
分别采用2种方法制备前驱体复合物.具体步骤如下:
一步法:配制100 mL浓度为0.1 mol/L钨酸钠(AR,上海国药集团)水溶液,向其中加入100 mL CNTs乙二醇悬浮液,在80 ℃油浴条件下,边搅拌边滴加4 mL浓度为12 mol/L盐酸,搅拌4 h后,过滤,洗涤,置于干燥箱中,100 ℃真空干燥2 h,得到了前驱体复合物.
二步法:配制100 mL浓度为0.1 mol/L钨酸钠水溶液,在80 ℃油浴条件下,边搅拌边滴加4 mL浓度为12 mol/L盐酸,搅拌2 h,生成了钨酸白色沉淀,再向其中缓慢加入100 mL CNTs乙二醇悬浮液,搅拌2 h,过滤,洗涤,置于干燥箱中,100 ℃真空干燥2 h,得到了前驱体复合物.
将上述制备的前驱体复合物置于管式炉中,在流量为100 mL/min的氧气气氛下,以7 ℃/min的速率升温至600 ℃,煅烧2 h,得到最终样品.
1.2 催化剂的表征采用JEM-2010 F型高分辨率透射电子显微镜(HRTEM)直接观察了复合物前驱体的大小和形貌.采用XL30扫描电子显微镜(荷兰飞利浦)观察了最终样品的形貌.采用UV-2550型(日本岛津)紫外可见分光光度计,测量了所制备催化剂降解亚甲基蓝的紫外可见吸收光谱.采用JW-04型全自动氮吸附比表面仪测定了样品的比表面积.光催化活性测试是在自制的光催化反应器中进行.光反应器中心光源为11 W的日光灯.利用朗伯比尔定律计算亚甲基蓝的降解率.
2 结果分析 2.1 物相分析采用X-射线多晶粉末衍射技术来表征样品的结晶度和晶相.图 1中曲线a,b分别为一步法和二步法制备的前驱体复合物的X射线多晶粉末衍射图(XRD图),曲线c,d分别为一步法和二步法制备的前驱体复合物煅烧后得到的样品的XRD图.
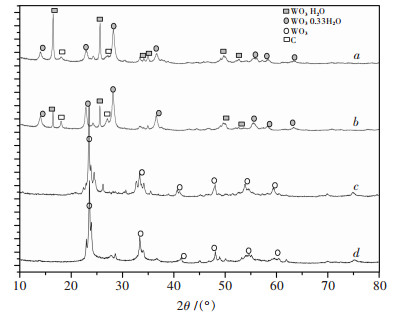 |
| 注:一步法制备的钨酸-CNTs复合物(a)和对应的氧化钨(c);二步法制备的钨酸-CNTs复合物(b)和氧化钨(d) 图 1 不同方法制备的钨酸-CNTs复合物和对应的氧化钨XRD图 |
由图 1中曲线a可知,其中2θ为16.5°、25.6°、34.1°、38.9°、49.6°、52.7°处的衍射峰,分别对应于(020)、(111)、(200)、(022)、(202)、(222)晶面,与PDF卡片84-0886一致,表明产物均为正交晶系结构的H2WO4(H2O).其中2θ为14.1°、23°、28.1°、36.7°、55.9°、58.1°、63.4°处的衍射峰,分别对应于(020)、(002)、(220)、(222)、(262)、(440)、(442)晶面,PDF卡片72-0199一致,表明产物均为正交晶系结构的H2WO4(0.33H2O).此外,2θ为13.6°和27.0°,分别对应于(001)和(002)晶面出现的衍射峰,表明产物中有石墨结构的CNTs.将曲线b与曲线a相比较,衍射峰的位置没有发生变化,说明2种方法制备的复合物的晶型相似,只是由于方法的不同,相应产物的衍射峰强度有所不同.曲线a的衍射峰强度高于曲线b中相应的衍射峰强度,表明一步法制备的样品的结晶度更高.由图 1中曲线c,d可知,均在2θ为23.9°,33.2°,41.4°,49°,54.6°,60.5°,分别对应于(110)、(111)、(201)、(220)、(221)、(311)晶面出现的衍射峰,表明产物均为正交晶系结构的WO3.曲线c的谱图衍射峰有宽化的现象,表明一步法制备的WO3颗粒度更小.
2.2 形貌分析图 2(a)为一步法制备的H2WO4-CNTs复合物的TEM图,样品中含有大量纳米尺度的颗粒,直径在10 nm左右,且制备所得的样品相对比较均匀,形状为类球形.一步法是将均匀分散的短切的CNTs管束加入到Na2WO4溶液中,混合均匀后,向其中滴加盐酸,使H2WO4颗粒直接沉积在CNTs表面.H2WO4在整个溶液中生成时,由于CNTs管束的阻隔,不致于生长过快,从而控制了H2WO4颗粒的生长速率.在此过程中,利用CNTs作为载体,大幅度地减少了颗粒之间的结合力,有效地阻碍了H2WO4颗粒的二次团聚现象的产生,使最终得到的类球状的H2WO4-CNTs复合物的直径达到了纳米级.图 2(b)为二步法制备的H2WO4-CNTs复合物的TEM图,钨酸颗粒的直径大于100 nm.主要是因为首先生成的H2WO4颗粒较大,再将其与CNTs复合,CNTs对H2WO4颗粒团聚的阻碍作用不能得到很好的发挥,所以制备的H2WO4-CNTs复合物颗粒仍然较大.
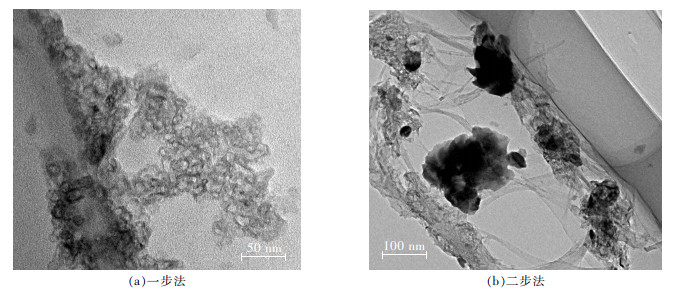 |
| 图 2 不同方法制备的H2WO4-CNTs复合物的TEM像 |
为了观察前驱体煅烧后所制备的WO3的形貌,进行了SEM测试.图 3为不同方法制备的前驱体H2WO4-CNTs经600 ℃煅烧得到的WO3颗粒的形貌图.在氧气气氛下进行煅烧,将前驱体中的CNTs除去,最终得到了WO3,其形状均呈类球形.由一步法制备的WO3颗粒(图 3(a))的形状相对比较均匀,属于纳米级的小颗粒或团簇,直径在250 nm左右.同时,伴随着CNTs的消失,在WO3颗粒之间留下了很多孔隙,说明该样品具有较好的分散性能.由二步法制备的WO3颗粒(图 3(b))的形状也较为均匀,但粒径处于微米级范围,粒径约2 μm,WO3颗粒之间也因为CNTs的消失存在很多孔隙.可见,前驱体颗粒尺寸的大小将对后续的WO3的尺寸有重要的影响,同时说明CNTs载体的加入和去除有效降低了WO3颗粒的尺寸.
 |
| 图 3 不同方法制备的WO3的SEM像 |
2.3 吸附性能分析
氮气吸附测试是在77 K液氮的条件下使被测样品通过物理吸附氦、氮(4:1)混合气体,再升温解吸附,利用纳米材料比表面测试软件,直接得出样品的比表面积.
图 4中曲线a,b分别为一步法和二步法制备的WO3的氮气吸附曲线,经数据整合,比表面积分别为36.53 m2/g和13.99 m2/g.可见,通过氧气气氛焙烧,一步法所制备的WO3的比表面积(36.53 m2/g)明显大于二步法制备的WO3的比表面积(13.99 m2/g).主要是因为,一步法制备的H2WO4/CNTs复合物的平均粒径明显小于二步法制备的复合物的平均粒径(由图 2可知),所以,当高温煅烧除去CNTs后,一步法制备的WO3的平均粒径仍小于二步法制备的WO3的平均粒径(由图 3可知),一步法制备的WO3颗粒间由于CNTs的消失而留下的空隙更多,所以其物理吸附性能更强.
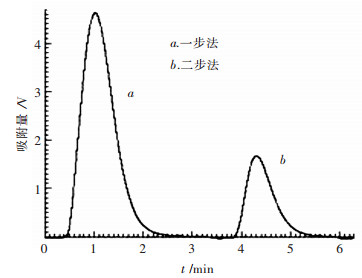 |
| 图 4 不同方法制备的WO3的氮气吸附曲线 |
2.4 紫外可见光谱
将WO3粉末制成薄膜样品,直接在紫外-可见分光光度计上测定其吸收值.
根据半导体的能级结构理论[23],当半导体颗粒尺寸小到纳米级尺寸时,粒子的导带和价带与大粒子相比,导带升高,价带下降,使带隙增宽,在其导带和价带之间有深陷阱和表面态能级.
图 5中,曲线a,b分别为一步法和二步法制备的WO3的紫外可见吸收光谱.2个图谱的形状相似,说明CNTs加入顺序的不同,没有对生成物质造成不同性质的影响.在波长λ=400 nm处附近的可见光区,谱线a的吸收值大于谱线b,说明一步法制备的WO3具有更大的可见光吸收性能.主要是因为一步法制备的WO3颗粒较小,达到了纳米级(250 nm),在可见光区,更容易发生电子由价带向导带的跃迁,所以在300~700 nm范围内的光吸收性质更强,尤其是在可见光区400~500 nm范围内具有更强的光吸收性能,使该样品具有更强的可见光催化性能.
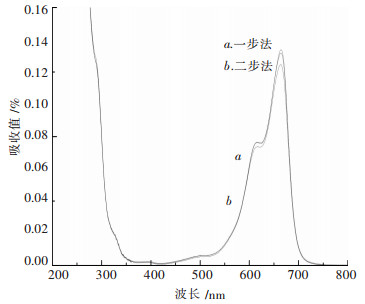 |
| 图 5 不同方法制备的WO3的紫外可见吸收光谱 |
2.5 光催化性能测试
光催化性能测试在自制的环形光催化反应装置中进行,以11 W日光灯为模拟可见光.亚甲基蓝溶液的最大吸收波长为664 nm.
将4mL双氧水(H2O2)加入到60 mL浓度为10 mg/mL亚甲基蓝溶液中,在11 W日光灯照射下,每隔10 min取一次样(3 mL),用高速离心机离心分离,取上层清液,利用紫外可见分光光度计测定其吸光度值.
由图 6可知,向亚甲基蓝溶液中加入H2O2再进行光降解时,只在可见光区664 nm波长处有最大吸收峰,并且随着降解时间的延长,其吸光值变化不大.根据降解率公式,可以计算出吸光值的变化,降解时间为120 min时,亚甲基蓝的脱色率为8.8 %.可见单纯的H2O2无法使亚甲基蓝完全降解.
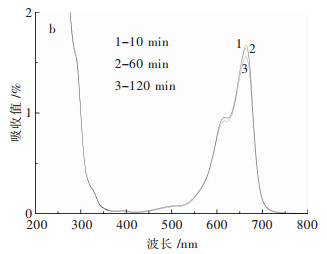 |
| 图 6 亚甲基蓝在双氧水单独作用下的吸光度变化 |
将4 mL H2O2和30 mg WO3同时加入到60 mL浓度为10 mg/mL亚甲基蓝溶液,在光催化反应开始前,避光磁力搅拌30 min,以使亚甲基蓝溶液在催化剂表面达到吸附平衡,每隔10 min取一次样(3 mL),用高速离心机离心分离,取上层清液,利用紫外可见分光光度计测定其吸光度值.加入H2O2的目的是,H2O2在光照作用下能使O-O键断裂生成自由基·OH,但是其反应速率低且产生的自由基·OH有限,而WO3和H2O2两者共存时可产生协同效应[16].
图 7(a),(b)分别为一步法和二步法制备的WO3对亚甲基蓝光催化降解过程中的吸光度变化.当达到暗处吸附平衡时(0 min),图 7(a)中的吸收度值(0.1)明显小于图 7(b)的吸收度值(0.55),可见,一步法制备的WO3吸附了更多的亚甲基蓝,具有更高的物理吸附性能,主要是因为其具有更大的比表面积.
 |
| 图 7 不同方法制备的WO3的光催化降解图谱 |
由图 7(a)可知,随着光照时间的延长,吸光度值迅速减小,当光照时间为30 min时,脱色率达到93.8 %.由图 7(b)可知,随着光照时间的延长,吸光度值在减小,亚甲基蓝溶液的脱色率不断增大,当光照30 min后,溶液脱色率达到79.1 %.可见,一步法制备的WO3具有更好的物理吸附性能和光催化活性.主要原因是,一步法制备的H2WO4-CNTs复合物中,钨酸颗粒的直径大约为10 nm,对应的WO3颗粒粒径为250 nm.而二步法制备的H2WO4-CNTs复合物中,H2WO4颗粒的直径在100 nm左右,对应的WO3颗粒在微米级,直径平均为2 μm.所以,一步法制备的WO3具有更小的颗粒度,更大的比表面积,吸附性能更好,从而具有更优越的光催化活性.
3 结论采用一步法和二步法分别制备了H2WO4-CNTs复合物,在氧气气氛下,600 ℃煅烧2 h,制备了超细WO3.结果表明:
1)一步法制备的H2WO4-CNTs复合物中,H2WO4颗粒的平均粒径为10 nm,煅烧后得到了平均粒径为250 nm的纳米级WO3颗粒,并且结构疏松.而二步法制备的H2WO4-CNTs复合物中,H2WO4颗粒的平均粒径在100 nm左右,焙烧后得到了平均粒径为2 μm的微米级WO3颗粒.
2)由于一步法制备过程中H2WO4直接沉积在CNTs管壁上,复合的效果更好,所以一步法制备的WO3的比表面积(36.53 m2/g)明显大于二步法制备的WO3的比表面积(13.99 m2/g).
3)通过光催化性能测试,在11 W的日光灯照射下,当光照时间为30 min时,一步法和两步法制备的WO3脱色率分别达到93.8 %和79.1 %.一步法制备的WO3显示出更好的吸附性能和光催化活性.
4)通过一步法,采用均匀分散的CNTs管束作为载体,使H2WO4沉淀在整个溶液中,由于CNTs管束的阻隔,不致于生长过快,从而控制了H2WO4颗粒的生长速率,大幅度地减少了颗粒之间的结合力,可以有效地降低颗粒团聚的程度.
| [1] |
Yan A H, Xie C S, Zeng D W, et al. Synthesis, formation mechanism and sensing properties of WO3 hydrate nanowire netted-spheres[J].
Materials Research Bulletin, 2010, 45: 1541–1547. DOI: 10.1016/j.materresbull.2010.05.026. |
| [2] | 宋旭春, 王芸, 林深, 等. 氧化钨纳米颗粒和纳米线的选择合成及光致发光研究[J]. 稀有金属材料与工程, 2007, 36(3): 10–11. |
| [3] |
Bi Y F, Li D D, Nie H. Preparation and catalytic properties of tungsten oxides with different morphologies[J].
Materials Chemistry and Physics, 2010, 123: 225–230. DOI: 10.1016/j.matchemphys.2010.03.086. |
| [4] |
Hidayt D, Purwanto A, Wang W N, et al. Preparation of size-controlled tungsten oxide nanoparticles and evaluation of their adsorption performance[J].
Materials Research Bulletin, 2010, 45: 165–173. DOI: 10.1016/j.materresbull.2009.09.025. |
| [5] | 王醒东, 郑华均, 钟金环, 等. 纳米WO3的结构、制备及应用前景[J]. 化工新型材料, 2009, 37(2): 15–17. |
| [6] |
Yu B, Tang H L, Kong Z P, et al. Preparation and characterization of three-dimensional mesoporous crystals of tungsten oxide[J].
Chemical Physics Letters, 2005, 407: 83–86. DOI: 10.1016/j.cplett.2005.03.066. |
| [7] |
Che G, Lakshmi B B, Martin C R, et al. Chemical vapor deposition based synthesis of carbon nanotubes and nanofibers using a template method[J].
Chem. Mater., 1998, 10: 260–267. DOI: 10.1021/cm970412f. |
| [8] |
Yue Y F, Qiao Z A, Fulvio, et al. Template-free synthesis of hierarchical porous metal-organic frameworks[J].
J Am Chem. Soc., 2013, 135: 9572–9575. DOI: 10.1021/ja402694f. |
| [9] |
Balamurugan J, Pandurangan A, Thangamuthu R, et al. Effective synthesis of well-graphitized carbon nanotubes on bimetallic SBA-15 template for use as counter electrode in dye-sensitized solar cells[J].
Ind. Eng. Chem. Res., 2013, 52: 384–393. DOI: 10.1021/ie3021973. |
| [10] | 李静, 李利军, 高艳芳, 等. 模板法制备纳米材料[J]. 材料导报, 2011, 25: 5–9. |
| [11] |
Ajayan P M, Stephan O, Redlich P H, et al. Carbon nanotubes as removable templates for metal oxide nanocomposites and nanostructures[J].
Nature, 1995, 375: 564–567. DOI: 10.1038/375564a0. |
| [12] |
Lijima S. Helical microtubules of graphitic carbon[J].
Nature, 1991, 354: 56–58. DOI: 10.1038/354056a0. |
| [13] |
Li J, Zhao Q L, Zhang G Y, et al. Synthesis of monoclinic WO3 nanosphere hydrogen gasochromic film via a sol-gel approach using PS-b-PAA diblock copolymer as template[J].
Solid State Sciences, 2010, 12: 1393–1398. DOI: 10.1016/j.solidstatesciences.2010.05.016. |
| [14] |
Li J H, Lee K I, Lu X K, et al. In-situ growth of pine-needle-like tungsten oxide nanowire arrays on carbon nanofibers[J].
Materials Letters, 2013, 99: 131–133. DOI: 10.1016/j.matlet.2013.02.077. |
| [15] | 桂阳海, 崔瑞立, 牛连杰, 等. 碳纳米管掺杂纳米WO3气敏材料的制备及其应用[J]. 化工新型材料, 2011, 9: 62–64. |
| [16] | 尹艳红, 吴子平, 羊建高. 超声场辅助制备碳纳米管/氧化钨纳米棒高效光催化剂的研究[J]. 有色金属科学与工程, 2012, 3(5): 39–44. |
| [17] | 尹艳红, 吴子平, 羊建高, 等.一种以模板法制备超细氧化钨的方法:中国, ZL201110192047.9[P].2013-10-02. |
| [18] |
Tao L, Xue S S, Jinne A, et al. Steering on-surface polymerization with metal-directed template[J].
J Am Chem. Soc, 2013, 135: 3576–3582. DOI: 10.1021/ja311890n. |
| [19] | 宋继梅, 张小霞, 焦剑, 等. 三氧化钨纳米片的制备及其光催化性质研究[J]. 安徽大学学报(自然科学版), 2009, 33(3): 73–77. |
| [20] |
Salmaoui S, Sediri F, Neji G, et al. Hexagonal hydrated tungsten oxide nanomaterials: Hydrothermal synthesis and electrochemical properties[J].
Electrochimica Acta, 2013, 108: 634–643. DOI: 10.1016/j.electacta.2013.07.086. |
| [21] |
Wu Z P, Xia B Y, Wang X X, et al. Preparation of dispersible double-walled carbon nanotubes and application as catalyst support in fuel cells[J].
J Power Sources, 2010, 195: 2143–2148. DOI: 10.1016/j.jpowsour.2009.10.013. |
| [22] |
Wu Z P, Wang J N, Ma J, et al. Methanol-mediated growth of carbon nanotubes[J].
Carbon, 2008, 47(1): 324–327. |
| [23] | 刘守新, 刘鸿. 光催化及光电催化基础与应用[M]. 北京: 化学工业出版社 , 2006: 136-174. |
 2014, Vol. 5
2014, Vol. 5


