| 锌铈液流电池研究进展 |
本世纪人类面临着巨大的能源挑战[1].展望人类未来的能源,除合理的开发和利用煤、石油、天然气,重视水力的开发外,需要进一步开发新能源,主要是核能、太阳能、生物质能、氢能以及各种可再生能源,如地热能、海洋能、风能等,从而构成一个以核能为主角的综合性的世界能源体系.太阳能、风能和海洋能等可再生能源发电具有波动性、随机性的不利特征,会对电网的稳定安全运行造成负面影响.储能技术是保证高效智能电网稳定运行、实现可再生能源大规模应用的关键技术.目前,具有较好应用前景的电力储能技术有抽水电站[2]、压缩空气[3]、飞轮[4]、超导磁[5]、超级电容器[6]和可充电电池[7].
可充电电池在新能源的利用中发挥着重要的作用.铅酸电池[8, 9]是人们最熟悉的一种可充电电池.锂离子电池[10, 11]因有高的储能密度而有望用作动力电源.液流电池最显著的特点是活性物质在电解液中;因而其输出功率和容量相互独立,系统设计灵活.全钒液流电池[13, 14, 15, 16, 17, 18]因使用单一元素钒而避免了电解液交叉污染带来的容量损失问题,不足之处在于单电池电压偏小(大约1.26 V).锌铈液流电池[19]是已知有开发前景的、单电池电压最大的水溶液介质电池,开路电压可达2.5 V以上.本文综述了锌铈液流电池正、负极反应和隔膜的研究概况.
1 电池原理锌铈液流电池是由Clarke[20]在2003年提出来的.他们声称[21-22],该储能系统的容量可达250,000 kWh以上,开路电压为3.33 V.锌铈液流电池以Ce3+/Ce4+为正极活性电对,Zn0/Zn2+为负极活性电对.正、负极电解液分别储存在两个不同的储液罐里(如图 1所示),在输送泵的作用下分别循环流过正、负电极并发生如下的电极反应:
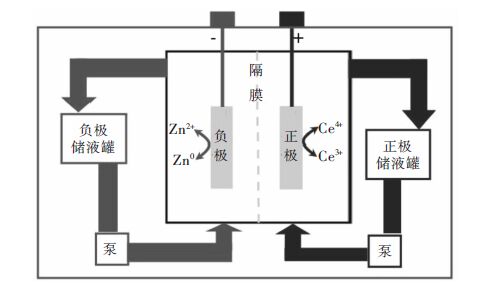 |
| 图 1 锌铈液流电池 |
正极反应
| $2\text{C}{{\text{e}}^{4+}}+2\text{e}\underset{\text{充电}}{\overset{\text{放电}}{\longleftrightarrow}}2\text{C}{{\text{e}}^{3+}},{{E}^{0}}\text{=}1.28\sim 1.72\text{V}\upsilon s.\text{NHE}$ | (1) |
负极反应
| $\text{Zn}\underset{\text{充电}}{\overset{\text{放电}}{\longleftrightarrow}}\text{Z}{{\text{n}}^{2+}}+2\text{e},{{E}^{0}}=-0.762\text{V}\upsilon s.\text{NHE} $ | (2) |
总的电池反应
| $2\text{C}{{\text{e}}^{4+}}+\text{Zn }\underset{\text{充电}}{\overset{\text{放电}}{\longleftrightarrow}}\text{ Z}{{\text{n}}^{2+}}+2\text{C}{{\text{e}}^{3+}}$ | (3) |
与常规化学电源相比,锌铈液流电池系统具有规模大、寿命长、成本低和效率高等特点.锌铈液流电池的功率决定于电极活性表面的大小和电堆的大小,电池的容量取决于储液罐中电解液的多少.通过单电池的串并联可以获得兆瓦级的功率,通过调控电解液的浓度和体积可以获得几十至几百兆瓦时的容量.由于活性物质在电解液中,电极为惰性电极,不参与成流电极反应,因而电池可深度放电,电池的循环寿命可达上万次,使用寿命可达10年以上.经过优化的电池系统充放电能量效率高达80 %以上.目前,锌铈液流电池还处在初期的实验研究阶段,离商业化应用还有一段很远的距离.还需对电解液、电极和隔膜等电池关键材料的设计制备进行系统深入的研究.
2 正极半电池反应的研究锌铈液流电池正极半电池反应的研究内容主要包括Ce3+/Ce4+电极反应动力学及电解液稳定性.影响Ce3+/Ce4+电极反应动力学的因素主要有支持介质、添加剂、电极和温度等.支持介质对Ce3+/Ce4+半电池反应动力学有显著的影响(如表 1所示).在1 mol/L HNO3介质中Ce3+/Ce4+电极反应的标准速率常数为2.0×10-3 cm/s,而在1 mol/L NH2SO3H中变为5.0×10-5 cm/s.Ce3+离子在1 mol/L HNO3介质中的扩散系数为8.8×10-6 cm2/s,而在2 mol/L CH3SO3H中减至5.37×10-6 cm2/s.另外,支持介质的浓度对Ce3+/Ce4+电极反应也有非常显著的影响.在4 mol/L H2SO4介质中[27],Ce3+/Ce4+电极反应峰电位差为400 mV;而在1 mol/L H2SO4介质中峰电位差增加到1200 mV.峰电位差越大表明电极反应动力学越缓慢.
| 表1 支持介质对Ce3+/Ce4+电极反应动力学的影响 |
 |
| 点击放大 |
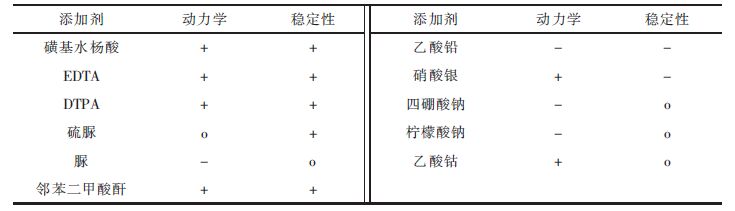
为了改善Ce3+/Ce4+电解液的稳定性和电极反应动力学,一般在电解液制备时加入一定量的添加剂.有些添加剂对电解液的稳定性和电极反应动力学都有积极作用,如表 2所示的磺基水杨酸[28]、DTPA、EDTA、邻苯二甲酸酐这4种添加剂[29]就兼具两方面的改善作用.有些物质只有某一方面的改善作用,比如,硫脲仅能改善铈电解液的稳定性,乙酸钴只能改善Ce3+/Ce4+电极反应的动力学.也有一些物质对某一方面有积极作用而对另一方面有消极作用,比如硝酸银对Ce3+/Ce4+电极反应动力学的改善有积极作用,但对电解液的稳定性有消极作用.这类物质一般不可用.
| 表2 添加剂对Ce3+/Ce4+电极反应动力学和电解液稳定性的影响. |
 |
| 点击放大 |
液流电池的电极为惰性材料,不参与电极反应,只为电极反应提供场所;但电极对活性电对的电极过程动力学有着重要的影响[30].当前针对锌铈液流电池的电极设计制备研究鲜有报道.
温度对Ce3+/Ce4+电极反应动力学有明显影响[23].如表 3所示,25˚C时,6 mol/L HNO3溶液中,Ce3+/Ce4+电极反应的标准速率常数为2.6×10-2 cm/s, 升温到60 ˚C标准速率常数增至4.6×10-2 cm/s.与此同时,Ce3+离子的扩散系数由6.9×10-6 cm2/s增加到1.31×10-5 cm2/s.
| 表3 温度对Ce3+/Ce4+电极反应动力学的影响. |
 |
| 点击放大 |
锌铈液流电池技术发展的瓶颈之一是电池能量密度的提高.可供考虑的做法有:①寻找合适的酸介质.考察Ce3+/Ce4+在不同酸介质中的溶解性,选择Ce3+/Ce4+在其中溶解性大的酸介质可获得高的能量密度;②采用混酸介质[31].Ce3+/Ce4+在混酸中的溶解性比在硫酸中的大.25 ˚C时不含甲基磺酸的0.5 mol/L Ce3+离子溶液中,要使溶液不产生沉淀,SO42-/HSO4-总浓度最大允许值为1.51 mol/L.而在同温度下的含4 mol/L CH3SO3H和0.5 mol/L Ce3+离子的溶液中,SO42-/HSO4-总浓度可达2.88 mol/L;③使用添加剂.添加剂可以改变活性物质的存在形式从而达到总浓度增加的效果;④增加活性电对.比如,在Ce3+/Ce4+电解液中加入亚硝基红盐[32]或铁盐[29],虽不能提高Ce3+/Ce4+的溶解性,但是能显著提高电解液的体积能量密度.采用第4种方法,电池的充放电曲线往往会有多个电压平台.
3 负极半电池反应研究负极半电池反应如式(2)所示,充电时发生锌的沉积反应,放电时发生锌的溶解反应.在电池的充放电反应过程中,除了发生式(2)所示的主反应,同时还存在下列负反应:
| $2{H^ + } + 2e \to {H_2}$ | (4) |
| $C{e^{4 + }} + e \to C{e^{3 + }}$ | (5) |
| $Zn + 2{H^ + } \to Z{n^{2 + }} + {H_2}$ | (6) |
| $Zn + 2C{e^{4 + }} \to Z{n^{2 + }} + 2C{e^{3 + }}$ | (7) |
这4个副反应都会降低电池的能量效率,导致电池性能下降.其中式(4)和式(5)表示的反应属于电化学反应,而式(6)和式(7)表示的反应属于化学反应.H+离子浓度越大式(4)和式(6)所示副反应的影响越严重.隔膜的选择性越差,正、负极电解液交叉混合越严重,式(5)和式(7)所示副反应的影响越大.
氧化铟能抑制析氢反应.在电解液制备时,使用氧化铟做添加剂可以改善电池性能,能量效率可提高11 %[33].在0.01 mol/L Zn(II)的甲基磺酸溶液中锌的沉积为传质控制过程,锌离子的扩散系数为7.5×10-6 cm2/s.增大锌离子浓度,锌的溶解过程减慢,但锌离子的沉积过程加快.随着酸浓度的增加,析氢负反应和锌腐蚀速率加快,库仑效率下降.负极电解液主成分最佳组成为1.5~2 mol/L Ce(CH3SO3)3 + 0.5 mol/L CH3SO3H.
4 隔膜电池隔膜的作用在于提供选择性离子导电通道.针对锌铈液流电池技术开发的隔膜材料研究至今未见详细报道.实验研究中一般使用杜邦公司生产的阳离子交换膜[34].但是,现阶段杜邦公司生产的系列Nafion膜,价格昂贵,不利于锌铈液流电池的推广应用.从理论上分析,适用于锌铈液流电池的隔膜必须能阻止Zn2+、Ce3+和Ce4+离子的透过,而能选择性透过H+离子. 最有可能满足这一要求的隔膜类型包括阳离子交换膜和微孔膜.目前,锌铈液流电池的研究需要首先对国内外这两种类型的、不同厂家生产的商品膜做一全面系统的性能比较;再从中筛选出性价比高的商品膜做进一步的改性研究.同时也要根据锌铈液流电池独特的运行环境来设计专用隔膜.
另外,也有无膜锌铈液流电池的研究报道[35].其优点是可以降低电池成本,不足之处在于电池的能量效率和循环寿命等性能欠佳.单液无膜液流电池面临的最大挑战是如何防止正、负极充电产物之间的直接化学反应;或者说如何使正、负极充电产物之间直接的化学反应速率远远小于正、负极的电化学反应速率.
从当前锌铈液流电池研究报道文献看,正极半电池反应的研究要更充分深入,而负极半电池反应和隔膜的研究相对不足.作为一个整体,锌铈液流电池各部分的研究需要协同推进,才有利于整体性能的提高.
5 展望新能源利用是解决能源问题和环境问题的必然选择.储能技术是新能源利用的瓶颈之一.锌铈液流电池是一种大规模储能技术,有着广阔的应用前景.虽然锌铈液流电池的研究已经取得了一些成绩,但是仍然还处在实验研究阶段,离商业化应用还有一段很远的距离,还有许多问题有待解决:
(1)析氢析氧副反应问题.由于锌铈液流电池单电池电压大,充电时正负极存在析氢析氧副反应.
(2)负极产物锌的防腐蚀和电极反应速率的平衡问题.锌铈液流电池负极电解液含酸介质.充电产物锌会被H+离子腐蚀.一般在电解液中加入防蚀剂来阻止锌的腐蚀.但由此也带来了锌负极放电阻抗的增大.
(3)高化学电化学稳定性、高催化活性和高导电性正极的设计制备问题.锌铈液流电池正极处于强酸性、强氧化性环境中,电极性能的稳定性是锌铈液流电池发展中面临的一个重要的挑战.
(4)电池规模放大的模拟仿真理论及系统集成方法问题.通过模拟仿真和实验验证,认识和理解大规模高效锌铈液流电池的结构与电流密度在电池内不同位置的分布均匀性对电池性能的影响规律,揭示调控机制.
(5)基于锌铈液流电池储能系统应用的发电、储能、电能转换及用电多体系的系统耦合及综合能量管理控制理论问题.
| [1] |
Chu S, Majumdar A. Opportunities and challenges for a sustainable energy future[J].
Nature, 2012, 488(7411): 294–303. DOI: 10.1038/nature11475. |
| [2] |
Caralis G, Papantonis D, Zervos A. The role of pumped storage systems towards the large scale wind integration in the Greek power supply system[J].
Renewable and Sustainable Energy Reviews, 2012, 16(5): 2558–2565. DOI: 10.1016/j.rser.2012.01.068. |
| [3] |
Kim HM, Rutqvist J, Ryu DW, et al. Exploring the concept of compressed air energy storage (CAES) in lined rock caverns at shallow depth: A modeling study of air tightness and energy balance[J].
Applied Energy, 2012, 92: 653–667. |
| [4] |
Nguyen TD, Beng GFH, Tseng KJ, et al. Modeling and position-sensorless control of a dual-airgap axial flux permanent magnet machine for flywheel energy storage systems[J].
Journal of Power Electronics, 2012, 12(5): 758–768. DOI: 10.6113/JPE.2012.12.5.758. |
| [5] |
Bhongade S, Tyagi B. Application of superconducting magnet energy storage to a multi-area automatic generation control scheme suitable in a restructured power system[J].
Journal of Engineering and Technology, 2013, 3(2): 82–89. DOI: 10.4103/0976-8580.113044. |
| [6] |
Jha N, Ramesh P, Bekyarova E, et al. High energy density supercapacitor based on a hybrid carbon nanotube-reduced graphite oxide architecture[J].
Advanced Energy Materials, 2012, 2(4): 438–444. DOI: 10.1002/aenm.v2.4. |
| [7] |
Goodenough JB, Cockrell VH. Evolution of strategies for modern rechargeable batteries[J].
Accounts of Chemical Research, 2013, 46(5): 1053–1061. DOI: 10.1021/ar2002705. |
| [8] |
Osório WR, Freitas ES, Peixoto LC, et al. The effects of tertiary dendrite arm spacing and segregation on the corrosion behavior of a Pb-Sb alloy for lead-acid battery components[J].
Journal of Power Sources, 2012, 207: 183–190. DOI: 10.1016/j.jpowsour.2012.01.060. |
| [9] |
Fan N, Li XH, Li H, et al. The application of spray drying method in valve-regulated lead-acid battery[J].
Journal of Power Sources, 2013, 223: 114–118. DOI: 10.1016/j.jpowsour.2012.09.041. |
| [10] |
Byon HR, Gallant BM, Lee SW, et al. Role of oxygen functional groups in carbon nanotube/graphene freestanding electrodes for high performance lithium batteries[J].
Advanced Functional Materials, 2013, 23(8): 1037–1045. DOI: 10.1002/adfm.v23.8. |
| [11] |
Kumar A, Reddy ALM, Mukherjee A, et al. Direct synthesis of lithium-intercalated graphene for electrochemical energy storage application[J].
ACS Nano, 2011, 5(6): 4345. DOI: 10.1021/nn201527p. |
| [12] |
Wang W, Luo Q T, Wei X L, et al. Recent progress in redox flow battery research and development[J].
Advanced Functional Materials, 2013, 23(8): 970–986. DOI: 10.1002/adfm.v23.8. |
| [13] |
González Z, Sánchez A, Blanco C, et al. Enhanced performance of a Bi-modified graphite felt as the positive electrode of a vanadium redox flow battery[J].
Electrochemistry Communications, 2011, 13(12): 1379–1382. DOI: 10.1016/j.elecom.2011.08.017. |
| [14] |
Li WY, Liu JG, Yan CW. Graphite-graphite oxide composite electrode for vanadium redox flow battery[J].
Electrochimica Acta, 2011, 56(14): 5290–5294. DOI: 10.1016/j.electacta.2011.02.083. |
| [15] |
You DJ, Zhang HM, Chen J. A simple model for the vanadium redox battery[J].
Electrochimica Acta, 2009, 54(27): 6827–6836. DOI: 10.1016/j.electacta.2009.06.086. |
| [16] | 徐波, 齐亮, 姚克俭, 等. 全钒液流电池电解液分布的数值模拟[J]. 化工进展, 2013, 32(2): 313–319. |
| [17] | 汪南方, 刘素琴. 全钒液流电池隔膜的制备与性能[J]. 化学进展, 2013, 25(1): 60–68. |
| [18] | 杜涛, 廖小东, 郝彰翔, 等. 全钒液流电池性能及电极材料研究[J]. 电源技术, 2013, 37(2): 231–233. |
| [19] |
Xie ZP, Liu QC, Chang ZW, et al. The developments and challenges of cerium half-cell in zinc-cerium reodox flow battery for energy storage[J].
Electrochimica Acta, 2013, 90: 695–704. DOI: 10.1016/j.electacta.2012.12.066. |
| [20] | Clarke R, Dougherty B, Harrison S, et al. Lanthanide Batteries. United States, WO 03/017408 A1[P]. 2003-02-27. |
| [21] | Clarke R, Dougherty B, Harrison S, et al. Load leveling battery and methods therefor. United States, US 2004/ 0197649 A1[P], 2004-10-07. |
| [22] | Clarke R, Dougherty B, Harrison S, et al. Mixed electrolyte battery.United States, US 7560189 B2[P], 2009-07-14. |
| [23] |
Wei Y, Fang B, Arai T, et al. Electrolytic oxidation of Ce (III) in nitric acid and sulfuric acid media using a flow type cell[J].
Journal of Applied Electrochemistry, 2005, 35(6): 561–566. DOI: 10.1007/s10800-005-1820-7. |
| [24] |
Liu Y, Xia X, Liu H. Studies on cerium (Ce4+/Ce3+)-vanadium (V2+/V3+) redox flow cell-cyclic voltammogram response of Ce4+/Ce3+ redox couple in H2SO4 solution[J].
Journal of Power Sources, 2004, 130(1/2): 299–305. |
| [25] |
Xie ZP, Zhou DB, Xiong FJ, et al. Cerium-zinc redox flow battery: Positive half-cell electrolyte studies[J].
Journal of Rare Earths, 2011, 29(6): 567–573. DOI: 10.1016/S1002-0721(10)60499-1. |
| [26] |
Xiong FJ, Zhou DB, Xie ZP, et al. A study of the Ce3+/Ce4+ redox couple in sulfamic acid for redox battery application[J].
Applied Energy, 2012, 99: 291–296. DOI: 10.1016/j.apenergy.2012.05.021. |
| [27] |
Paulenova A, Creager SE, Navratil JD, et al. Redox potentials and kinetics of the Ce3+/Ce4+ redox reaction and solubility of cerium sulfates in sulfuric acid solutions[J].
Journal of Power Sources, 2002, 109(2): 431–438. DOI: 10.1016/S0378-7753(02)00109-X. |
| [28] |
Xie ZP, Xiong FJ, Zhou DB. Effect of sulfosalicylic acid on kinetics of Ce3+/Ce4+ electrode reaction[J].
Advanced Materials Research, 2011, 279: 451–455. DOI: 10.4028/www.scientific.net/AMR.279. |
| [29] | 谢志鹏. 锌铈液流电池正极电解液的研究[D]. 长沙:中南大学化学化工学院,2011. |
| [30] |
Leung PK, Ponce-de-Leόn C, Low CTJ, et al. Characterization of a zinc-cerium flow battery[J].
Journal of Power Sources, 2011, 196(11): 5174–5185. DOI: 10.1016/j.jpowsour.2011.01.095. |
| [31] |
Xie ZP, Xiong FJ, Zhou DB. Study of the Ce3+/Ce4+ redox couple in mixed-acid media (CH3SO3H & H2SO4) for redox flow battery application[J].
Energy & Fuels, 2011, 25(5): 2399–2404. |
| [32] |
Xie ZP, Xiong FJ, Zhou DB. Nitroso-R-salt in aqueous solutions for redox flow battery application[J].
Advanced Materials Research, 2011, 239-242: 2813–2816. DOI: 10.4028/www.scientific.net/AMR.239-242. |
| [33] |
Leung PK, Ponce-de-Leόn C, Low CTJ, et al. Zinc deposition and dissolution in methanesulfonic acid onto a carbon composite electrode as the negative electrode reactions in a hybrid redox flow battery[J].
Electrochimica Acta, 2011, 56(18): 6536–6546. DOI: 10.1016/j.electacta.2011.04.111. |
| [34] |
Leung PK, Ponce-de-Leόn C, Low CTJ, et al. Ce (Ⅲ)/Ce (Ⅳ) in methanesulfonic acid as the positive half cell of a redox flow battery[J].
Electrochimica Acta, 2011, 56(5): 2145–2153. DOI: 10.1016/j.electacta.2010.12.038. |
| [35] |
Leung PK, Ponce-de-Leόn C, Walsh FC. An undivided zinc-cerium redox flow battery operating at room temperature (295 K)[J].
Electrochemistry Communications, 2011, 13(8): 770–773. DOI: 10.1016/j.elecom.2011.04.011. |
 2014, Vol. 5
2014, Vol. 5

