| 锂离子正极材料LiNi0.5Mn0.3Co0.2O2的合成与掺杂Al的性能研究 |
锂离子电池在日常生活中随处可见,但其使用过程中出现了较多的问题,比如容量衰减快、稳定性不好、安全性能不佳等.锂离子电池正极材料性能的好坏决定了电池的使用性能,如何改善锂离子正极材料的使用性能一直是广大研究者不懈努力研究的方向.正极材料的合成主要有化学共沉淀法[1]、固相反应法[2]、溶胶-凝胶法[3-4]、喷雾热解法[5]、熔盐法[6]、水热合成法[7]、乳液合成法[8]等方法,这几种方法各有优势,采用不同的合成方法,材料的形貌、电化学性能、热稳定性等也有很大的差异.化学共沉淀法因其操作简单方便,材料混合均匀,合成材料的物理及化学性能较优,在工业生产中使用较多.近年来研究得比较多的是具有高比容量层状结构的LiNixMnyCo1-x-yO2,其有一种协同效应,材料具有较高的放电比容量、成本较低、循环稳定性也不错.而正极材料LiNi1-x-yCoxMnyO2的掺杂改性化合物使其各方面性能一定程度上得到优化,材料稳定性能更好、安全性增高.Liu[9]利用氢氧化物共沉淀法合成正极材料LiNi1/3Co1/3Mn1/3O2,并研究了掺杂Al、Fe 合成LiNi1/3Co1/3-xMxMn1/3O2(M=Fe 和Al),发现少量的Al(x<1/20)掺杂可以提高材料的结构稳定性而改善循环性能,而掺杂Fe 却没有这种作用.Ren等[10]用水热合成法合成了Li[Ni1/3Mn1/3Al1/3-xCox]O2,研究发现当0≤x≤1/6,可以提高材料的常温放电比容量和材料在55 ℃高温的放电比容量,随着x 值的增大,改善效果越显著.张景会[11]采用溶胶-凝胶法合成尖晶石型的LiMN2O4和多元复合掺杂的LiCo0.01Al0.05Mn1.94O0.96F0.05正极材料,研究发现复合掺杂有助于提高材料的常温和高温的放电比容量及循环稳定性.
本文采用共沉淀法合成镍钴锰氢氧化物前躯体,使其和碳酸锂混合均匀后,高温焙烧合成锂离子正极材料LiNi0.5Mn0.3Co0.2O2,并研究了掺杂Al(OH)3对材料综合性能的影响.
1 实验部分 1.1 LiNi0.5Mn0.3Co0.2O2的制备以NiSO4·6H2O、MnCl·4H2O、CoCl2·6H2O 为原料,物质的摩尔量比为5∶3∶2 配制成浓度1.3 mol/L 混合盐溶液,与2.6 mol/L 的NaOH 溶液反应,以NH4OH 为络合剂,在50 ℃恒温,pH=11.0 条件下反应10 h 制得氢氧化物沉淀,陈化12 h 后抽滤洗涤多次,在干燥箱中100 ℃干燥24 h,得到前躯体粉末.
将前躯体与金属离子计量比为1.04 倍的碳酸锂加入适量无水乙醇球磨混合8 h 后取出干燥,将混合粉末装入坩埚压实置于马弗炉中升温至500 ℃,保温2.5 h,然后继续升温至750~900 ℃,焙烧15 h,合成所需要的正极材料.掺杂Al 是在混锂时和碳酸锂一起加入相应摩尔计算量的Al(OH)3混合均匀后再焙烧,烧成制度与未掺杂时性能最优的材料烧成制度一致.
1.2 材料的成分分析与形貌表征使用德国蔡司电镜EVO 10 型电镜对所制备的材料形貌进行检测,加速电压20 kV;用荷兰帕纳科X’Pert Powder 型X 衍射仪分析材料的结构特征,仪器相关参数:管压40 kV,管流40 mA,CuKα靶辐射,λ=0.154 06 nm,扫描步长为0.02° ,扫描角度范围10°~80°.
1.3 电化学性能测试正极材料:导电剂(SP-Li):黏结剂(PVDF)质量比为90∶4∶6 与适量的NMP 混合均匀配成料浆涂到铝箔上制成正极片.负极材料:SP-Li:KS-6:PVDF:草酸为89∶1.5∶1.5∶7∶1 配成浆料涂到铜箔上制成负极片.用美国的Celgard2300 隔膜与正负极片卷绕成14 500 电池,真空干燥后在通有流动干燥空气的干燥房内注入新宙邦生产的LBC322-18 电解液,封装成电池,静置12 h 后用武汉金诺公司的蓝电测试仪进行电性能测试.充放电循环电压为2.75~4.2 V,循环电流为1 C 倍率.
2 结果和讨论 2.1 物相分析在750 ℃、800 ℃、850 ℃、900 ℃ 4 个不同温度下焙烧合成的材料,其中750 ℃的样品为棕黑色,其他样品为黑色.图 1 是不同焙烧温度下所制成样品的XRD 图谱,从图 1 可以看到,不同焙烧温度的材料具有相似的XRD 图谱,各图谱上特征峰峰型尖锐,峰强度大,无杂相峰出现,材料纯度高,晶型形成完整.材料特征峰与PDF 卡片52 -0457 吻合,同时(006,102)和(108,110)峰分裂明显,表明材料具有典型的α-NaFeO2均匀层状结构,属于空间群R-3m[12-14].
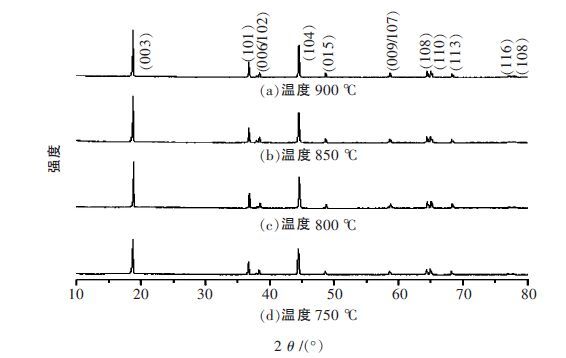 |
| 图 1 不同温度焙烧制得样品的XRD 图谱 |
图 2是掺杂一定量的Al 后在850 ℃下焙烧制得样品的XRD 图谱,从图 2 可以看到,各图谱上特征峰峰型尖锐,峰强度大,无杂相峰出现,表明Al3+成功掺杂进入材料.
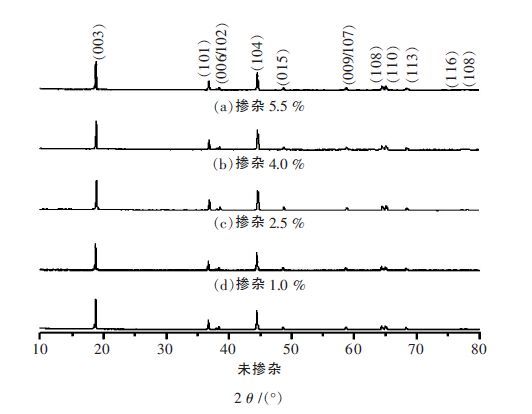 |
| 图 2 掺杂不同摩尔量Al 焙烧制得样品的XRD 图谱 |
2.2 微观形貌分析
图 3 是不同温度焙烧样品的SEM 图.从图 3 可以看出合成温度对样品的形貌和粒径有一定的影响,随着焙烧温度的升高,样品的棱角越分明,表面越光滑,同时粒径有一点点增大,小粒径的材料比例有所下降.通过显微镜观察,与之前合成的前驱体相符合,由此可以看出,合成材料的粒径很大程度上由前躯体的形态决定.
 |
| 图 3 不同温度焙烧制得样品的电镜图 |
图 4 是掺杂不同摩尔量Al 在相同焙烧温度下合成的正极材料,可以看出掺杂Al 对材料的外观形态没有太大的影响,掺杂量的增加一定程度上改善了材料的分散性,材料颗粒组成更均匀.
 |
| 图 4 掺杂不同摩尔量Al 焙烧制得材料的电镜图 |
2.3 电化学性能分析
将在不同温度下焙烧后的正极材料LiNi0.5Mn0.3Co0.2O2做成14 500 电池,用1 C 倍率在2.75~4.2 V 恒温25 ℃环境下进行电化学性能测试.
图 5 是不同焙烧温度制得的材料的首次放电比容量曲线,从图 5 可以看出,不同焙烧温度制得的电池正极材料具有一致的放电平台,放电中压约为3.5 V.
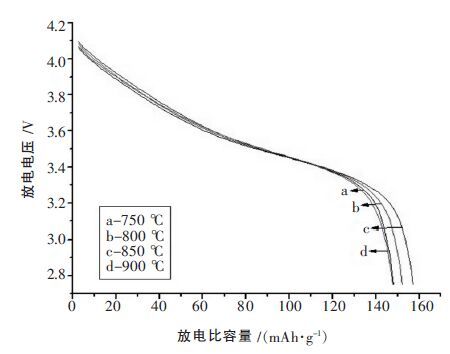 |
| 图 5 不同焙烧温度合成材料的首次放电曲线 |
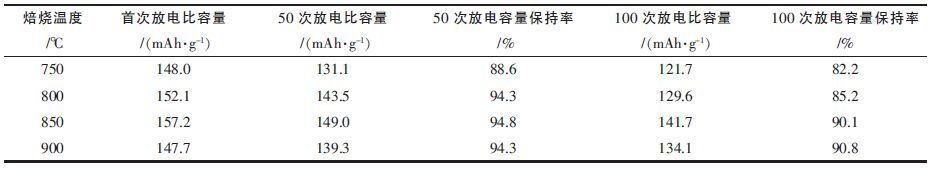
图 6 是不同焙烧温度制得材料的循环性能曲线,结合表 1 可以看到850 ℃温度焙烧出来的材料具有最高的放电比容量,首次放电比容量达到157.2 mAh/g,在循环50 次后放电比容量是149 mAh/g,容量保持率是94.8 %;在循环100 次后放电比容量是141.7 mAh/g容量保持率为90.1 %.750 ℃、800 ℃焙烧合成的材料,因温度低缘故,结晶性不及高温焙烧的材料完整,容量衰减较其他焙烧温度的材料快些,在50 次循环及100 次循环后的容量保持率也较其它的低.900 ℃焙烧的材料有点过烧,比其它温度焙烧的材料硬,材料的振实密度也更大,其放电比容量比850 ℃焙烧的材料低,但是在50 次及100 次循环后材料的放电比容量保持率相差不大,原因可能是材料的结晶性比较完整,所以循环稳定性也较好,但是高温焙烧使得少部分Ni形成没有活性的物质,导致材料的放电比容量有所下降,这与LiNiO2的热稳定性和储存性能差一致.
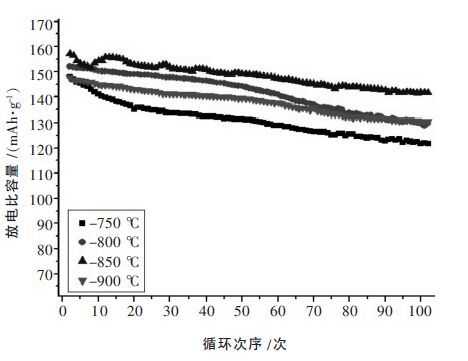 |
| 图 6 不同焙烧温度制得材料的循环曲线 |
| 表1 不同温度焙烧材料首次、50 次、100 次放电比容量及容量保持率 |
 |
| 点击放大 |
将合成的Ni0.5Mn0.3Co0.2 (OH)2前躯体分别与1.0 %、2.5 %、4.0 %、5.5 %摩尔量的Al(OH)3及1.04倍锂配比的碳酸锂混合均匀后,在850 ℃下焙烧制得正极材料LiNi0.5Mn0.3Co0.2AlxO2+σ做成14 500 电池,用1 C 倍率在2.75~4.2 V 恒温25 ℃环境下进行电化学性能测试.
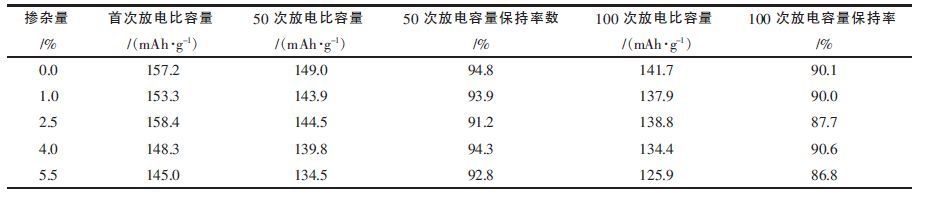
图 7 是掺杂不同摩尔量Al 焙烧制得的材料的首次放电比容量曲线,由图 7 知,掺杂不同摩尔量Al 所得的电池正极材料放电平台比未掺杂的有部分提高,首次放电中压均高于3.5 V.图 8 是掺杂不同摩尔量Al 所得材料的循环性能曲线,据图 8 可知,掺杂Al后材料的放电比容量都有所下降,结合表 2 可知其中掺杂Al 摩尔量为2.5 %在850 ℃温度下,焙烧出来的材料具有最高的放电比容量,首次放电比容量达到158.4 mAh/g,但在循环50 次、100 次后放电比容量保持率有点偏低,整体来看掺杂2.5 %的Al 性能还是较优的.对比可以看到掺杂Al 的材料放电比容量在50 次循环及100 次循环后的容量保持率也并不高,掺杂Al 对正极材料的循环稳定性的改善,在循环100 次前还看不出趋势.
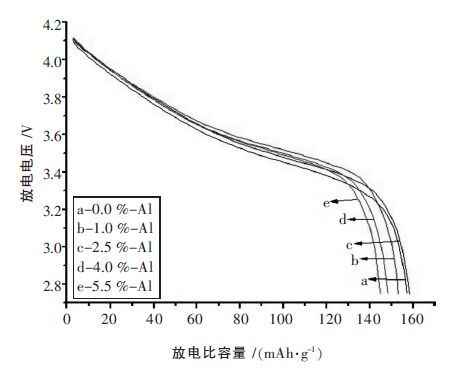 |
| 图 7 掺杂不同摩尔量Al 焙烧制得材料的首次放电曲线 |
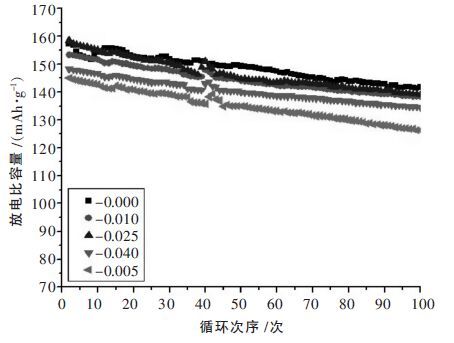 |
| 图 8 掺杂不同摩尔量Al 焙烧制得材料的循环曲线 |
| 表2 掺杂不同摩尔量Al 制得材料首次、50 次、100 次放电比容量及容量保持率 |
 |
| 点击放大 |
3 结论
采用氢氧化物共沉淀法可以制得均匀层状结构的LiNi0.5Mn0.3Co0.2O2锂离子正极材料,其晶型完整,在850 ℃温度下,合成的材料电性能最优,在1 C 倍率下循环,首次放电比容量达到157.2 mAh/g,50 次循环后放电比容量保持率为94.8 %,100 次循环后放电比容量达到90.1 %.掺杂Al 后,材料的放电平台有所提高、比容量有所下降,以100 次循环来看稳定性并没有得到改善.
| [1] |
ZHONG Sheng-kui, LI Wei, LI Yan-hong, et al. Synthesis and electrochemical performances of LiNi0.6Co0.2Mn0.2O2 cathode materials[J].
Trans.Nonferrous Met.Soc.China, 2009(19): 1499–1503. |
| [2] | 张进, 曹高勋, 赵新兵, 等. 固相反应法制备α-LiAIO2包覆 LiNi0.4 Co0.2Mn0.4O2的电化学性能研究[J]. 无机化学学报, 2008, 24(3): 105–110. |
| [3] | 韦旎妮, 赖琼钰, 高媛, 等. 层状LiCo1/3Ni1/3Mn1/3O2正极材料的合成及电化学性能研究[J]. 无机化学学报, 2005, 21(7): 147–154. |
| [4] |
DING Yan-huai, ZHANG Ping, JIANG Yong, et al. Synthesis andelectrochemical properties of LiNi0.375Co0.25Mn0.375-xCrxO2-xFx cathode materials prepared by sol-gel method[J].
Materials Research Bulletin, 2008, 43: 2005–2009. DOI: 10.1016/j.materresbull.2007.10.009. |
| [5] |
SHUI Miao, GAO Shan, SHU Jie, et al. LiNi1/3Co1/3Mn1/3O2 cathode materials for LIB prepared by spray pyrolysis II.Li+ diffusion kinetics[J].
Ionics, 2013, 19: 47–52. DOI: 10.1007/s11581-012-0723-y. |
| [6] |
Helan M, Berchmans John L, Hussain Zahir A, et al. Synthesis of LiMN2O4 by molten salt technique[J].
Ionics, 2010, 16: 227–231. DOI: 10.1007/s11581-009-0379-4. |
| [7] | 欧俊科, 林琳, 郭勇, 等. 水热法合成 LiFePO4及其电化学性能的研究[J]. 化学研究与应用, 2011, 23(12): 66–71. |
| [8] |
TONG Dong-ge, LAI Qiong-yu, JI Xiao-yang, et a1. Synthesis of LiCo1/3Ni1/3Mn1/3O2 as a cathode material for lithium ion battery by water-in-oil emulsion method[J].
Mater Chem Phys, 2005, 94: 423–427. DOI: 10.1016/j.matchemphys.2005.05.025. |
| [9] |
LIU Dao-tan, WANG Zhao-xiang, CHEN Li-quan, et al. Comparison of structure and electrochemistry of Al-and Fe-doped LiNi1/3Co1/3Mn1/3O2[J].
Electrochimica Acta, 2006, 51: 4199–4203. DOI: 10.1016/j.electacta.2005.11.045. |
| [10] |
REN Hai-bo, LI Xiang, PENG Zheng-he, et al. Electrochemical properties of Li[Ni1/3Mn1/3Al1/3-xCox]O2 as a cathode material for lithium ion battery[J].
Electrochimica Acta, 2011, 56: 7088–7091. DOI: 10.1016/j.electacta.2011.05.104. |
| [11] | 张景会, 王俊芳, 张海朗, 等. LiCo0.01Al0.05Mn1.94O0.96F0.05的合成与电化学性能的研究[J]. 电源技术, 2011, 35(9): 123–127. |
| [12] |
Park K S, Cho M H, Jin S J, et al. Structural and electrochemical properties of nanosize layered Li[Li1/5Ni1/10Co1/5Mn1/2]O2[J].
Electrochem Solid State Lett, 2004, 7: A239–A241. DOI: 10.1149/1.1759292. |
| [13] |
Hwang B J, Santhanam R, Chen C H, et al. Effect of synthesis conditions on electrochemical properties of LiNi1-yCoyO2 cathode for lithium rechargeable batteries[J].
Power Sources, 2003, 114: 244–248. DOI: 10.1016/S0378-7753(02)00584-0. |
| [14] |
Kim J M, Chung H T. Role of transition metals in layered Li[Ni,Co,Mn]O2 under electrochemical operation[J].
Electrochim.Acta, 2004, 49: 937–946. DOI: 10.1016/j.electacta.2003.10.005. |
 2013, Vol. 4
2013, Vol. 4

