| 正极材料LiNi1/3Co1/3Mn1/3O2的Mg掺杂及电化学性能 |
锂离子电池因其具有比能量高、电池电压高、工作温度范围宽、存储寿命长等优点得到广泛应用.其正极材料LiNi1/3Co1/3Mn1/3O2综合了LiCoO2良好的电化学性能、LiNiO2的高比容量、LiMn2O4的高安全性及低成本等特点, 因此受到众多研究人员的关注[1-2].然而在动力电池和大规模储能电池等大功率锂离子电池应用过程中, 仍需改善其循环性能.研究表明通过掺杂Mg[3]、Al[4]、Ti[5]等可有效改善正极材料的循环性能.通常采用的方法是将前驱体与掺杂氧化物粉末混合均匀后再进行煅烧[6-7].此外, 溶胶-凝胶法也被运用于正极材料的掺杂研究中[8].本文采用氢氧化物共沉淀法对前驱体进行了Mg掺杂, 合成出掺杂型正极材料Li (Ni1/3Co1/3Mn1/3)1-xMgxO2, 并利用扫描电镜、X-射线衍射、电化学测试等手段, 比较研究了掺杂与未掺杂正极材料的形貌、结构和电化学性能.
1 实验 1.1 正极材料合成(1)对于未掺杂的正极材料, 将NiSO4、CoSO4、MnSO4按产物计量比配成一定浓度的混合溶液.并配制一定浓度的NaOH和氨水的混合溶液.将2种溶液缓慢滴加到温度为40 ℃的一定浓度的氨水溶液中, 搅拌并控制pH值为11[9-10].滴加完成之后继续搅拌陈化12 h.将所得料浆进行过滤、干燥, 得到前驱体粉末.按前驱体与Li2CO3物质的量之比1: 1.05混合并球磨3 h, 之后在空气炉中先在550 ℃预烧6 h, 然后升温至950 ℃煅烧10 h, 冷却至室温, 得到LiNi1/3Co1/3Mn1/3O2未掺杂的正极材料.
(2)对于掺杂的正极材料, 按合成产物计量比, 将NiSO4、CoSO4、MnSO4、MgSO4配制成总离子浓度与(1)相同的混合溶液, 其他条件和步骤与(1)相同, 合成出了Li (Ni1/3Co1/3Mn1/3)1-xMgxO2(x=0.01, 0.02, 0.03, 0.04)掺杂型正极材料.
1.2 正极材料表征采用日本株式会社的SU1510型扫描电子显微镜(SEM)观察正极材料的形貌、粒径.采用欧美克激光粒度测试仪分析正极材料的粒径及粒径分布.采用X-射线衍射仪(CuKα靶)对正极材料进行X-射线衍射物相分析(XRD), 扫描范围10°~80°, 扫描速度8°/min.
1.3 正极材料充放电性能测试按质量比86: 2: 6称取一定量的正极材料、石墨、炭黑置于玛瑙研钵中, 加入质量分数为11 %的聚偏氟乙烯(PVDF), 再用N-甲基吡咯烷酮(NMP)调匀成浆.将料浆均匀涂布在长方形铝箔上然后转移至烘箱中, 在105 ℃干燥12 h.用切片机将铝箔机切成圆形小片并压实得到正极片.将得到的正极片, 与负极的金属锂片, 1 mol/L LiPF6/EC-DMC电解液, Clegard2300隔膜, 在氩气气氛的手套箱中装配成2032扣式电池.在武汉蓝电充放电测试仪上进行电化学性能测试.测试电压为2.7~4.2 V, 测试电流为0.2 C.
2 结果与讨论 2.1 掺镁对正极材料结构的影响图 1为正极材料Li (Ni1/3Co1/3Mn1/3)1-xMgxO2(x=0, 0.01, 0.02, 0.03, 0.04)的XRD谱图, 表 1为其晶胞参数和结构参数.
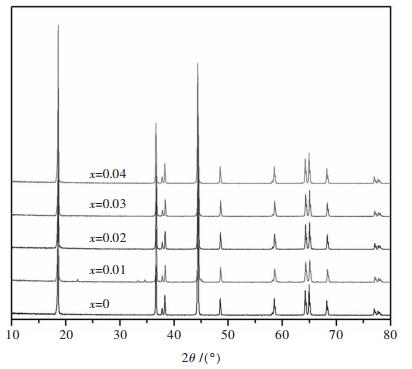 |
| 图 1 Li(Ni1/3Co1/3Mn1/3)1-xMgxO2的XRD谱图 |
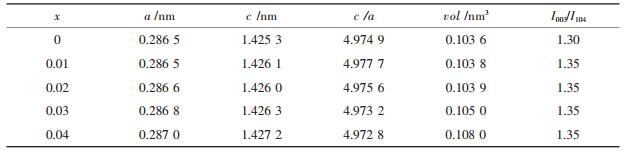
| 表1 LLi(Ni1/3Co1/3Mn1/3)1-xMgxO2的晶胞参数和结构参数 |
 |
| 点击放大 |
由图 1可知, 各峰峰形尖锐且强度较高, (006)峰和(102)峰, (108)峰和(110)峰发生明显的分离, 说明合成的正极材料均属于六方晶系α-NaFeO2层状结构.掺杂型正极材料与未掺杂的正极材料的XRD图类似, 没有出现掺杂元素镁的氧化物的衍射峰, 这可能是Mg进入了LiNi1/3Co1/3Mn1/3O2晶格的缘故.表 1显示, 与未掺杂正极材料相比, Mg掺杂型正极材料的a和c值随着掺杂量的增加而有所增大, 晶胞体积也随之增大, 这有利于Li+在充放电过程中的脱嵌.c/a值是正极材料层状结构的重要标志[11-12], c/a值越大(大于4.96), 表明正极材料层状结构越趋于完整.通常用(003)峰与(104)峰的衍射峰强度之比I003/I104来表示阳离子混排程度, 当I003/I104>1.2时, 表明阳离子混排程度较低.掺杂型正极材料I003/I104值略高于未掺杂的正极材料, 表明Mg的掺入在一定程度上抑制了正极材料的阳离子混排.
2.2 掺镁对正极材料粒径及形貌的影响掺杂与未掺杂正极材料的SEM结果如图 2所示.
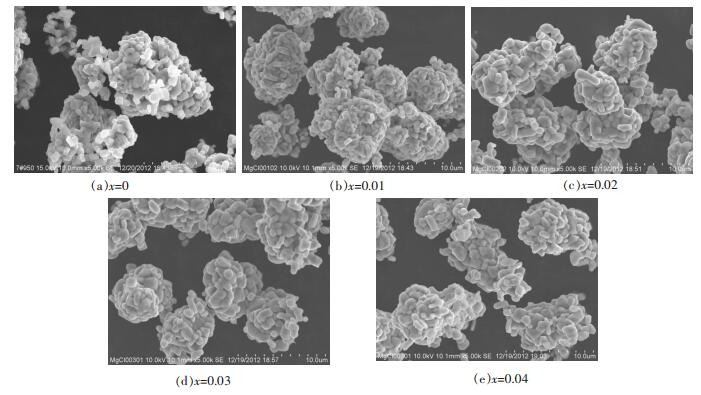 |
| 图 2 Li(Ni1/3Co1/3Mn1/3)1-xMgxO2的SEM照片 |
由图 2可以看出, LiNi1/3Co1/3Mn1/3O2及其掺杂型正极材料均由立方体的一次颗粒聚集形成类球形的大颗粒, 其形貌差别不大, 表明镁的掺入不会改变正极材料的形貌.
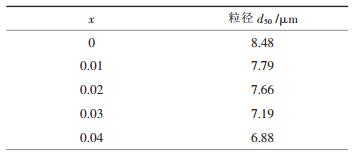
粒度测试结果如表 2所示.由表 2可知, 随着掺镁量的增加, 颗粒粒径有所下降.原因可能是在强碱性溶液中, Mg2+与NH3的配位作用较弱, 在金属离子总浓度不变的情况下, 游离的金属离子浓度增加, 溶液过饱和度升高, 成核速率加快, 生长速率有所降低, 颗粒粒径减小[13].
| 表2 Li(Ni1/3Co1/3Mn1/3)1-xMgxO2的粒径 |
 |
| 点击放大 |
2.3 掺镁对正极材料的电化学性能的影响
图 3、图 4分别为掺杂不同量Mg2+的正极材料的充放电曲线和相应的放电比容量-循环曲线图.由图 3可知, 各正极材料的充放电曲线平滑, 充放电电压平台比较平稳, 均在3.75 V左右.图 4显示, 与未掺杂的LiNi1/3Co1/3Mn1/3O2相比, Mg2+掺杂后正极材料的初始容量有所降低, 这与其中参与电化学反应活性物质减少有关, 因为Mg2+在充放电前后价态不变, 不具有电化学活性.此外, 微量镁可能占据Li+位置, 导致Li+的脱嵌量减少[14].然而掺杂少量的Mg2+之后, 正极材料循环性能有所改善, 这是因为进入锂层的Mg2+能有效地抑制阳离子混排程度, 同时Mg2+半径大于Li+半径, 能起到层间支撑的作用[15].
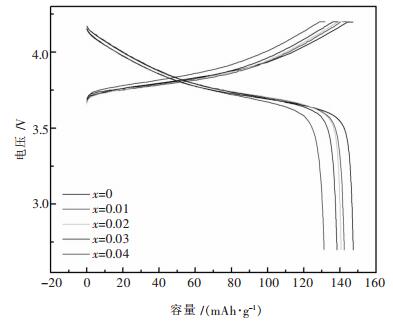 |
| 图 3 Li(Ni1/3Co1/3Mn1/3)1-xMgxO2的充放电曲线 |
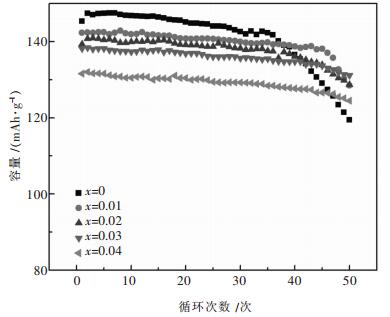 |
| 图 4 Li(Ni1/3Co1/3Mn1/3)1-xMgxO2的放电比容量-循环曲线 |
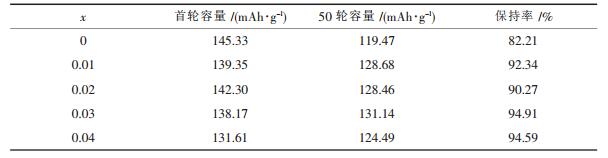
正极材料的放电容量如表 3所示.由表 3可知, 当掺杂量x=0.03时, 循环性能最优, 充放电循环50轮之后正极材料的放电比容量为131.1 mAh/g, 保持率为94.91 %, 高于未掺杂正极材料的119.5 mAh/g和82.21 %.掺杂量进一步增大, 正极材料仍能保持良好的循环性能.
| 表3 Li(Ni1/3Co1/3Mn1/3)1-xMgxO2的放电容量 |
 |
| 点击放大 |
3 结论
(1)采用共沉淀法制备Mg掺杂的前驱体, 并经过混锂、球磨、高温煅烧, 制备出Li (Ni1/3Co1/3Mn1/3)1-xMgxO2正极材料, 掺杂与未掺杂的正极材料都具有单一的α-NaFeO2型层状结构; 无衍射杂峰出现.
(2)掺镁正极材料的首次放电容量均有不同程度的降低, 但具有稳定的充放电平台, 循环性能有明显改善.其中以Mg掺杂量为0.03时, 正极材料Li (Ni1/3Co1/3Mn1/3)1-0.03Mg0.03O2的循环性能最好, 首次放电比容量为138.17 mAh/g, 50次循环后放电比容量为131.14 mAh/g, 容量保持率为94.91 %.
| [1] |
Ohzuku T, Makimura Y. Layered lithium insertion material of LiNi1/3Co1/3Mn1/3O2 for lithium-ion batteries[J].
Chem Lett, 2001(7): 642–643. |
| [2] |
Shaju K M, Subba G V, Chowdari B V. Performance of layered as LiNi1/3Co1/3Mn1/3O2 cathode for Li-ion batteries[J].
Electrochim Acta, 2002, 48: 145–151. DOI: 10.1016/S0013-4686(02)00593-5. |
| [3] |
XIANG Jiang-feng, CHANG Cai-xian, ZHANG Feng, et al. Rheological phase synthesis and electrochemical properties of mg-doped LiNi0.8Co0.2O2 cathode materials for lithium-ion battery[J].
Journal of The Electrochemical Society, 2008, 155(7): 520–525. |
| [4] |
DING Yan-huai, ZHANG Ping, Long Zhi-lin, et al. Morphology and electrochemical properties of Al doped LiNi1/3Co1/3Mn1/3O2 nanofibers prepared by electrospinning[J].
Journal of Alloys and Compounds, 2009, 487(1/2): 507–510. |
| [5] | 肖新颜, 汪冬. Ti掺杂对正极材料LiNi1/3Co1/3Mn1/3O2结构和电化学性能的影响[J]. 华南理工大学学报:自然科学版, 2012, 40(1): 1–7. |
| [6] | 李节宾, 徐友龙, 熊礼龙, 等. 纳米MgO掺杂改善LiNi1/3Co1/3Mn1/3O2正极材料[J]. 物理化学学报, 2011, 27(11): 2593–2599. |
| [7] | 李义兵, 陈白珍, 徐徽, 等. Li (Mn1/3Ni1/3Co1/3)1-yMyO2(M=Al, Mg, Ti)正极材料的制备及性能[J]. 中国有色金属学报, 2006, 16(8): 1474–1479. |
| [8] | 廖力, 王先友, 罗旭芳, 等. Li (Ni1/3Co1/3Mn1/3)1-2xMgxAlxO2的合成与电化学性能[J]. 电源技术, 2007, 31(1): 25–29. |
| [9] |
Deng C, Zhang S, Fu B, et al. Synthetic optimization of nanostructured Li[Ni1/3Mn1/3Co1/3]O2 cathode material prepared by hydroxide coprecipitation at 273 K[J].
Journal of Alloys and Compounds, 2010, 496(1/2): 521–527. |
| [10] |
TANG Ze-xun, GAO De-shu, CHEN Ping, et al. Novel-shaped LiNi1/3Co1/3Mn1/3O2 prepared by a hydroxide coprecipitation method[J].
Pure and Applied Chemistry, 2008, 80(11): 2537–2542. |
| [11] |
Xu K, Ding M S, Zhang S S, et al. An attempt to formulate nonflammable lithiumion electrolytes with alkyl phosphates and phosphazenes[J].
Journal of The Electrochemical Society, 2002, 149(5): 622–626. DOI: 10.1149/1.1467946. |
| [12] |
Watanable M, Tokuda H, Muto S. Anionic effect on ion transport properties in network polyether electrolytes[J].
Electrochimica Acta, 2001, 46(10/11): 1487–1491. |
| [13] | 杨平.基于镍钴锰前驱体的锂离子电池正极材料Li[Ni1/3Mn1/3Co1/3]O2制备与改性研究[D].长沙:中南大学, 2009:79-80. http://cdmd.cnki.com.cn/Article/CDMD-10533-1011180370.htm |
| [14] |
Juliell C, Nazri G A, Rougle A. Electrochemical performances of layered LiM1-yM'yO2(M=Ni, Co;M'=Mg, Al, B) oxides in lithium batteries[J].
Physics and Chemistry of Solids, 2000, 135(1/4): 121–130. |
| [15] | 王希敏, 王先友, 罗旭芳, 等. 锂离子电池正极材料LiCo1/3Ni1/3Mn1/3O2[J]. 化学进展, 2006, 18(12): 1720–1724. |
 2016, Vol. 4
2016, Vol. 4


