1.
江西理工大学冶金与化学工程学院, 江西 赣州 341000;
2.
中国瑞林工程技术有限公司, 南昌 330031
基金项目:国家高技术研究发展计划(863计划)资助项目(2013AA064001);国家自然科学基金资助项目(51164011);福建省区域科技重大合作项目(2011H4025);中国瑞林博士后基金项目(nerin2012冶金(技术开发)第01号)
作者简介: 王瑞祥(1974-), 男, 博士, 副教授, 主要从事湿法冶金与资源综合利用等方面的研究, E-mail:
wrx9022@163.com 收稿日期:2013-03-28
Thermodynamics study of sodium hydroxide roasting in a poly-metallic gold mine
1.
School of Metallurgical and Chemical Engineering, Jiangxi University of Science and Technology, Ganzhou 341000, China;
2.
China Nerin Engineering Co., Ltd., Nanchang 330031, China
近十年来,复杂金矿处理技术[1-6]有了多方向的拓展,并获得长足进步.含硫多金属金矿[7-8]中,金、银多数以微细粒镶嵌在硫化物中,不易直接氰化浸出,常在焙烧预处理后,再氰化浸出金、银.焙烧处理含硫多金属金矿,金矿中各种金属易发生复杂反应,金、银易被包裹,导致其浸出率低下,刘小珍等[9]、陈滨[10]、袁朝新等[11]研究了添加剂焙烧处理技术,抑制了焙烧过程中不利于金、银氰化浸出物质的生成,取得了显著效果.徐盛明等[12]研究了氧化钙焙烧处理银精矿对银物相变化的影响,认为氧化钙可以抑制低熔点硅酸盐的生成,削弱其对金、银的包裹作用.薛光等[13]认为氢氧化钠焙烧银精矿可以减少硅酸银的生成,从而大幅度提高银的浸出率.本文对多金属金矿氢氧化纳焙烧的热力学进行计算、分析,探讨氢氧化纳在焙烧过程中的作用,为焙烧工艺的改良提供理论参考.
1 热力学计算
1.1 反应方向和限度判定
一个反应能否进行以及反应进行的限度是通过计算该反应的吉布斯自由能来判定的.自由能与物质的熵变,焓变的关系可通过热力学第二定律来表示,关系式如下:
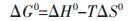
|
(1) |
所有的化学反应都是向着自由能降低的方向进行,当自由能小于零时,反应正向进行,当自由能等于零时,反应达到平衡,当自由能大于零时,反应逆向进行.对于一般化学反应,自由能值越负,反应越容易正向进行,越是能优先进行,且生成物越稳定.
1.2 Gibbs自由能计算公式
多金属复杂金矿焙烧温度一般在298~1 003 K范围内,其中主要的金属硫化物为CuFeS2、Ag2S、ZnS、PbS等,若在此温度范围内有晶型转变,其热力学参数会发生变化,故Gibbs自由能计算公式要采用有相变公式.
根据Gibbs-Helmholtz方程推导可以得到Gibbs自由能ΔGT0的计算公式,其过程如式(2)~式(5)所示:
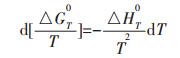
|
(2) |
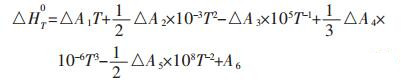
|
(3) |
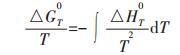
|
(4) |
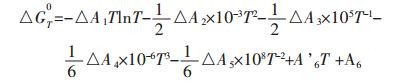
|
(5) |
式(5)中A6和A’6为Gibbs自由能方程的积分常数.A6的计算是通过公式(3)在25 ℃,ΔH2980条件下得到,而A’6是将ΔH2980带入公式(5)中得到.二者的计算公式如式(6)、式(7)所示:
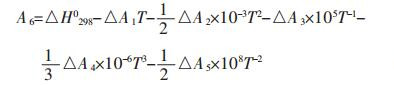
|
(6) |
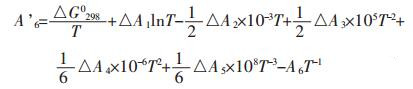
|
(7) |
由于某些反应有晶型或者物态的变化,所以相对ΔHT0采用以下的公式进行计算
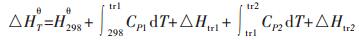
|
(8) |
式(8)中Ttr1,Ttr2为第一次和第二次相变温度,ΔHtr1, ΔHtr2为第一次和第二次相变转变热.
2 热力学分析
2.1 某多金属金矿化学物相分析
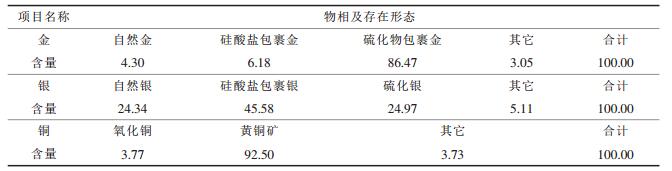
对某黄金冶炼厂提供的多金属金矿中金、银、铜做了化学物相分析,结果如表 1所示.从表 1可知,该多金属金矿中金大部分被硫化物包裹,银主要被硅酸盐包裹,铜大部分以黄铜矿的形式存在.
表1(Table 1)
|
表1 某多金属金矿化学物相分析样/%
|
|
|
 |
| 点击放大 |
2.2 焙烧主要化学反应
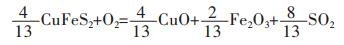
|
(9) |
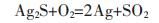
|
(10) |
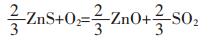
|
(11) |
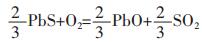
|
(12) |
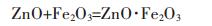
|
(13) |
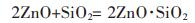
|
(14) |
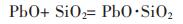
|
(15) |
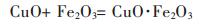
|
(16) |
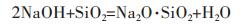
|
(17) |
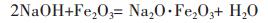
|
(18) |
2.3 ΔGT0-T函数计算
根据以上反应式,查《实用无机物热力学数据手册》得相关热力学计算参数[14],并参照《冶金热力学数据测定与计算方法》[15], 计算反应式(9)~式(18)的ΔGT0-T函数.
以反应方程式(9)为例,在温度为298~830 K时,通过查表计算可得到ΔA1=-1.396, ΔA2=2.999,ΔA3=-4.344, ΔA4=0,ΔA5=0,ΔH2980=-299 033.690 J/mol,ΔS2980=-64.228 J/(K·mol).
又因为
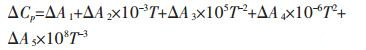
|
(19) |
将计算参数带入公式(19)得:
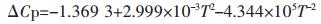
|
(20) |
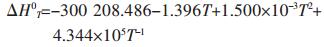
|
(21) |
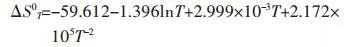
|
(22) |
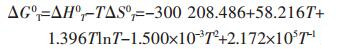
|
(23) |
将T=830 K分别带入式(21)、(22)、(23)得:
ΔH8300=-299 810.967 J/mol,ΔS8300=-66.192 J/(K·mol),ΔG8300=-244 870 J/mol.
在T=830 K时,CuFeS2发生晶型转变,过程为α→β,其熵和焓都会发生改变.
其中ΔHtr,ΔStr为相变热和相变熵.
在830~930 K时,同样通过表 1的计算参数可得
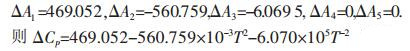
|
(24) |
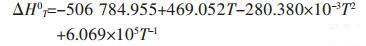
|
(25) |
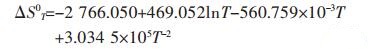
|
(26) |
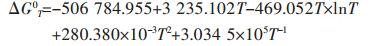
|
(27) |
验证,将T=830 K带入公式(27)得ΔG8300=-244 870.834 J/mol与上文计算结果相符,故该计算是正确的.反应式式(9)~式(18)的吉布斯自由能函数计算方法同理可得,结果列于表 2中.
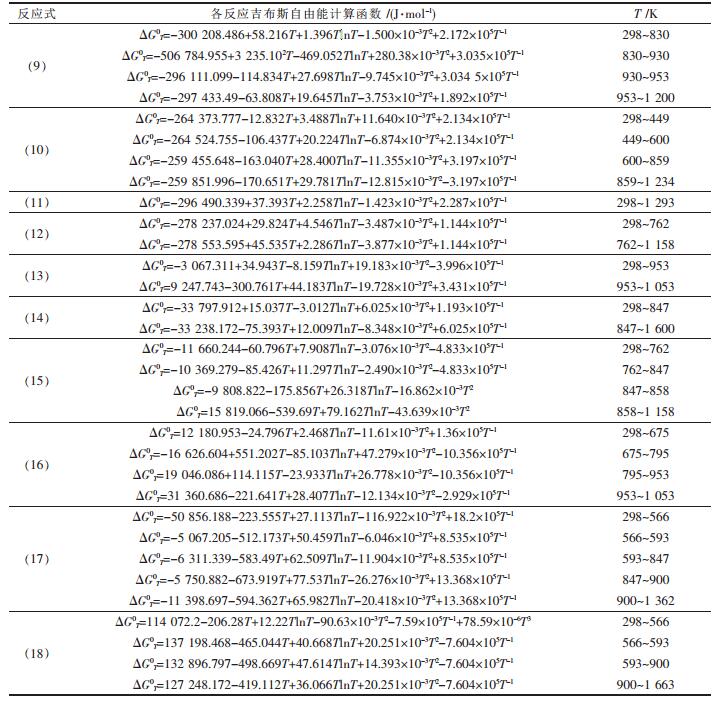
表2(Table 2)
|
表2 各反应的吉布斯自由能计算公式
|
|
|
 |
| 点击放大 |
2.4 ΔGT0-T图绘制和分析
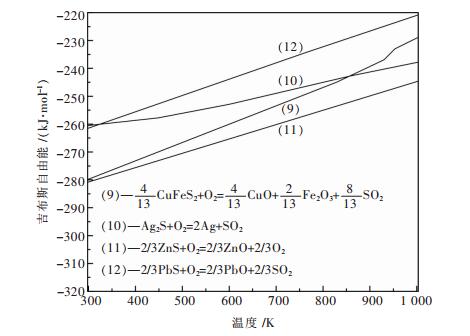
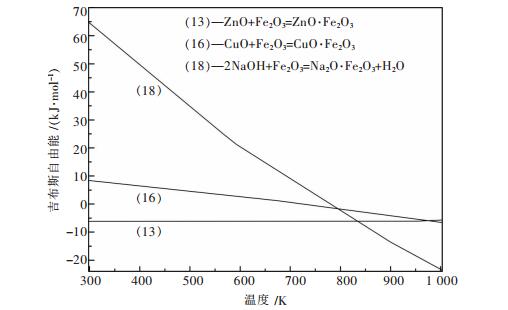
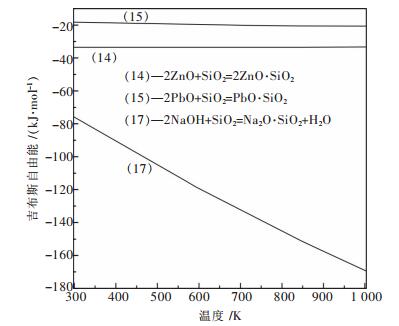
根据表 1中ΔGT0-T函数,绘出反应式(9)~式(18)的ΔGT0与T的关系图,如图 1、图 2、图 3所示.
由图 1知,反应式(9)~式(12)随温度升高,其吉布斯自由能向越正方向靠近,但在298~1 003 K范围均为负,即反应均可正向进行.在T=1 003 K,反应式(9)~式(12)吉布斯自由能分别为-228.851 kJ/mol、-237.799 kJ/mol、-244.537 kJ/mol、-220.823 kJ/mol,即在T=1 003 K氧化分解容易程度由大到小排列为:ZnS>Ag2S>CuFeS2>PbS.
由图 2可知,反应式(16)、式(18)吉布斯自由能均随温度升高,越来越负.反应式(13)的吉布斯自由能随温度升高,向越正的方向缓慢靠近,但其吉布斯自由能在298~1 003 K温度范围内均为负.反应式(18)在T=771.3 K时,ΔGT0=0 kJ/mol.反应式(16)在T=727.2 K, ΔGT0=0 kJ/mol.反应式(18)与反应式(16)的吉布斯能与温度关系曲线在T=783.9 K有交点,该温度下的吉布斯自由能为-1.397 kJ/mol.在771.3 K<T<783.9 K条件下,CuO·Fe2O3的生成几率大于Na2O·Fe2O3的生成几率.在T>783.9 K时,Na2O·Fe2O3的生成几率大于CuO·Fe2O3的生成几率.反应式(18)与反应式(13)的吉布斯自由能与温度关系曲线在T=834.3 K处有交点,该点温度下的吉布斯自由能为-6.829 kJ/mol.在T<834.3 K时,ZnO·Fe2O3的生成几率大于Na2O·Fe2O3的生成几率.T>834.3 K时,Na2O·Fe2O3的生成几率大于ZnO·Fe2O3的生成几率.
由图 3可知,反应式(14)、式(15)、式(17)的吉布斯自由能在298~1 003 K温度范围内均为负,且在相同温度条件下,反应式(17)的吉布斯自由能比反应式(14)、式(15)更负,所以反应式(17)正向反应趋势大于反应式(14)、式(15),即Na2O·SiO2生成几率均大于PbO·SiO2与2ZnO·SiO2生成几率.在T=1 003 K时,反应式(14)、式(15)、式(17)吉布斯自由能分别为-33.415 kJ/mol、-20.681 kJ/mol、-169.399 kJ/mol.
综上可知,多金属金矿NaOH焙烧能降低CuO· Fe2O3、ZnO·Fe2O3、PbO·SiO2、2ZnO·SiO2的生成几率,从而降低了以上物质对Au、Ag的包裹作用.多金属金矿NaOH焙烧的适宜温度为T≥834.3 K.
3 结论
(1)焙烧是一种提高多金属金矿金、银回收率的有效预处理方法,本文通过热力学计算,得到多金属金矿NaOH焙烧主要化学反应ΔGT0-T函数,绘制和分析了ΔGT0-T图,探索NaOH在焙烧过程中的作用,为焙烧工艺的改良提供理论参考.
(2)热力学分析结果表明,多金属金矿NaOH焙烧能降低CuO·Fe2O3、ZnO·Fe2O3、PbO·SiO2、2ZnO· SiO2的生成几率,从而降低了以上物质对Au、Ag的包裹作用.多金属金矿NaOH焙烧的适宜温度为T≥834.3 K.
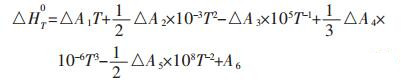
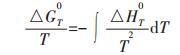
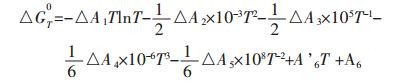
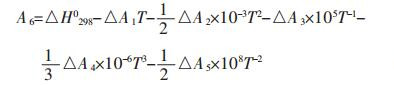
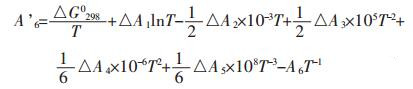
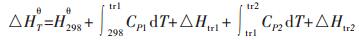

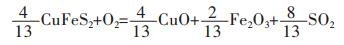
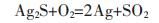
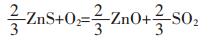
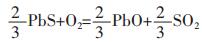
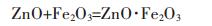
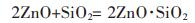
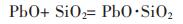
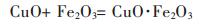
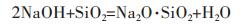
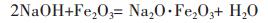
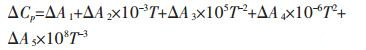
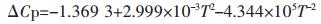
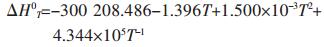
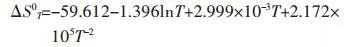
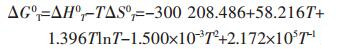
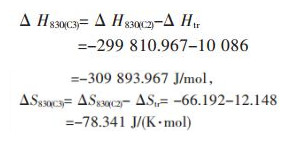
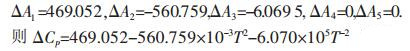
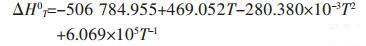
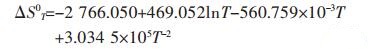
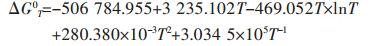

 2016, Vol. 4
2016, Vol. 4 图 1(Fig. 1)
图 1(Fig. 1)


