| 湿法冶金渣中硫的化学回收 |
2. 宝钢湛江钢铁有限公司, 广东 湛江 524000
2. Bao-steel Zhanjiang Iron and Steel Co. Ltd., Zhanjiang 524000, China
很多金属都会和硫伴生成硫化矿,比如:闪锌矿(ZnS)和方铅矿(PbS).在冶金生产过程中,存在火法和湿法两种工艺,但工业上还是以火法处理硫化矿为主.火法处理时产生的SO2国内通常用来制酸,国外通常会用碱液吸收[1],需要大型的喷淋塔[2],这需要高额费用,也有研究用再生装置来强化吸收[3-4],但SO2不会被完全吸收仍有大量的SO2排入大气,污染环境,给人们的生活、健康带来危害[5]并造成资源的浪费.同时在处理低品位、复杂硫化矿时,不能采用火法工艺,应采用湿法工艺来处理.采用湿法冶金工艺处理的硫化矿,硫以元素硫的形式富集到渣中,这样既不会产生SO2污染,也可以综合利用硫资源生产一系列产品.
硫在自然界中广泛分布于煤、石油、天然气还有矿石中[6].我国西南贵定和松藻超高硫煤的原煤中就存在元素硫[7].目前,世界上生产的硫主要来自高硫原油、有色金属硫化物和自然硫矿床等[8].我国是个硫磺用量大国,硫磺资源小国[9],中国硫磺市场供应缺口大,对外依存度超过60 %,加拿大一直是我国进口硫磺的主要来源国,从2005年开始,我国的硫磺进口量大约在800万t左右; 自2012年1月1日起,我国进口硫磺关税由3 %降低至1 %,这使得进口硫磺的成本减少,促进了硫磺进口量增加,预计未来我国进口硫磺资源量将继续增多.硫磺是一种重要的化工产品和基本工业原料,广泛用于化工、冶金、农药、橡胶、燃料、造纸等工业部门,并且现在硫磺的价格正在回升,有很大的经济价值,所以回收湿法冶金渣中的硫是很有必要的.
1 含元素硫物料的来源含元素硫物料主要来源有两个:①氯化浸出硫化矿.三氯化铁或氯化铜浸出黄铜矿[10]; ②氧压酸浸法处理硫化矿.如国外采用此法处理锌精矿生产电锌,浸出后的渣含有元素硫.
这些物料不仅含硫较高,是回收硫很好的原料,其中一些物料还含有一定量的稀有金属和贵金属.回收硫之后,稀有金属和贵金属的品位得到提高,为回收稀贵金属创造良好条件,资源得到充分的利用.
2 化学法回收硫湿法冶金中硫的回收主要有物理法和化学法两类,物理法主要有浮选法、真空蒸馏法、高压倾析法、热过滤法.翟爱峰等[11]曾用丁胺黑药作为浮选捕收剂回收铜浸出渣中的硫,但浮选法回收硫的品位比较低,只能起到富集硫的作用.黄鑫等[12]用真空蒸馏法回收硫化镍电解阳极泥中的硫, 但真空蒸馏法回收硫的成本高,设备要求高,很少使用.加拿大科明科公司和舍利特·高尔登矿业公司曾采用高压倾析法进行了回收氧压酸浸渣中硫的试验,但高压倾析法在回收硫时,金属硫化物也会熔融于其中,得到的硫磺纯度并不高.邓孟俐[13]用热过滤法回收硫化锌浸出渣中的硫,我国金川公司也用此法回收镍高锍电解阳极泥中的硫,但热过滤法适合处理含元素硫量较大的物料,需要设备复杂且要保温过滤,更重要的是硫的回收率并不高.物理法对设备、物料性质要求较高,所以化学法回收硫得到越来越广泛的应用.化学法回收硫主要是基于硫在溶剂中的溶解度,元素硫溶解到溶剂中,再经提取和加工,得到一系列硫磺产品.此类溶剂主要有无机溶剂和有机溶剂两类.化学法回收硫主要有以下几种方法.
2.1 Na2S和SO2脱硫此方法的原理是硫化钠和硫生成多硫化钠,多硫化钠在碱性条件下能稳定存在,pH降低时,多硫化钠分解析出元素硫.化学方程式如式(1)、式(2)所示:
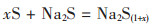
|
(1) |
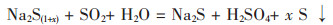
|
(2) |
有研究表明,含元素硫63 %的铜渣氯浸渣,在硫化钠0.5 mol/L、25 ℃,硫化钠与元素硫的摩尔比4:1的条件下,硫的回收率为54.60 %~74.19 %,硫的纯度为99.08 %[14].
此方法在整个过程中SO2全部被消耗,不会对环境造成污染.但Na2S会溶解贵金属,会造成贵金属的损失,所以,在采用此法时要综合考虑硫化钠对硫和贵金属的溶解率,根据不同物料组成找到溶硫较大,而溶贵金属较小时的各参数.
2.2 (NH4)2S法脱硫此方法的原理和硫化钠相似,也是利用硫化铵和硫生成多硫化铵,但不同的是多硫化铵在加热情况下会分解为S和NH3以及H2S,NH3和H2S用水吸收又变成(NH4)2S,重复使用.化学方程式如式(3)、式(4)所示:
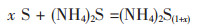
|
(3) |
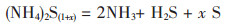
|
(4) |
其脱硫效果取决于物料含硫量及硫化铵的用量.我国金川公司在回收镍电解阳极泥中的硫时,先采用热过滤法回收硫,但得到的热滤渣含S量仍较高,大约为67 %, 然后再采用(NH4)2S法进一步脱硫[15].有研究表明,在(NH4)2S浓度为2.0 mol/L、溶硫温度30 ℃、反应时间60 min、液固比8:1的条件下, 采用(NH4)2S法回收黄铜矿酸浸渣中的硫, 回收率达96 %左右[16].硫化铵法生成的硫化氢和氨气可回收再生成硫化铵,循环使用,且系统简单,易于控制,但硫化铵味臭,见光易分解成有刺激性气味的氨气和有臭鸡蛋气味的硫化氢,操作环境差,最好在密闭环境中操作.而且硫化铵也能溶解贵金属,当物料含有贵金属时,选用硫化铵做溶剂也要综合考虑对硫和贵金属的溶解度,以达到溶硫较多,溶贵金属较少的目的.
2.3 煤油法脱硫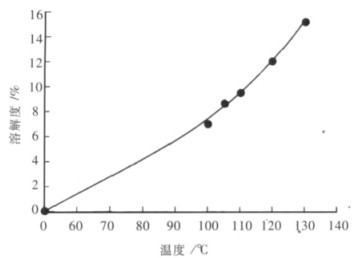 |
| 图 1 煤油溶硫能力与温度的关系 |
根据这种特性,可采用加热溶硫,待固液分离后,再降温,硫析出,煤油可重复使用.金川硫化镍电解阳极泥中的硫就是采用煤油脱除,液固比7.25~8,在120 ℃进行液固分离,两级浸出后,总脱硫率可达97 %,脱硫后贵金属富集了8~9倍.固液分离最好用压滤,可减少煤油的挥发损失.煤油脱硫可基本上除去全部元素硫,且反应快,不会造成贵金属的分散,但煤油易燃、易爆,对设备、操作的要求较高,脱硫渣中残存有煤油,需要燃烧或用其它方法处理[18].
2.4 四氯乙烯法脱硫硫在四氯乙烯中的溶解度也随温度的升高而增大,其二者的关系见表 1[19].
| 表1 不同温度下硫在四氯乙烯中的溶解度 |
 |
| 点击放大 |
其脱硫过程和煤油脱硫过程相似,加热溶硫,固液分离后冷却析硫,四氯乙烯返回使用.四氯乙烯易挥发,脱硫过程应密闭,快速离心过滤.另外,四氯乙烯还会腐蚀橡胶和聚乙烯塑料,脱硫设备要用搪瓷或不锈钢.四氯乙烯与水不互溶,物料不能含水太高,最好在脱硫前先烘干一段时间,以免影响脱硫效果[20].
2.5 二甲苯脱硫二甲苯的溶硫能力也随温度的升高而增大,二甲苯的溶硫能力与温度的关系见表 2[21].
| 表2 元素硫在二甲苯中的溶解度与温度的关系 |
 |
| 点击放大 |
在加热升温的条件下用二甲苯溶解湿法冶金渣中的硫,溶解完后趁热分离,二甲苯中的硫会随着温度的降低而析出,这也是为什么要趁热固液分离的原因.
此方法操作方便,对物料中硫的含量也没有要求,得到的硫磺产品纯度较高.但二甲苯易挥发并具有一定的毒性,所以实验最好在密闭装置中进行.
2.6 Ⅰ*有机溶剂法Ⅰ*有机溶剂是一种特殊的有机溶剂,它是一种饱和链烃,不溶于水,化学性质较稳定.有研究表明,含单质硫54.39 %的硫化锑矿渣,在液固比(指液体体积以毫升计量与固体质量以克计量之比值,下同)10:1,温度150 ℃,加热时间15 min的条件下,脱硫率可达96.6 %[22].
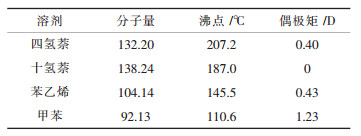
2.7 其它有机溶剂脱硫对于结构类似的溶剂,溶硫能力的大小取决于分子中-Cl取代基的数目以及是否含有C=C键[23].所以,除了上述有机溶剂外,还有一些新的有机溶剂也能溶硫,比如四氢萘、苯乙烯、十氢萘和甲苯,它们的性质见表 3.
| 表3 4种溶剂的性质 |
 |
| 点击放大 |
有研究表明,这4种溶剂的溶硫能力均随温度升高而增大.在同一温度下,四氢萘溶硫能力最好,苯乙烯次之.十氢萘和甲苯对硫磺的溶解度与四氢萘和苯乙烯相比虽然小很多,但是仍可大于文献中选用的很多溶剂[24].
2.8 不溶性硫磺的脱除不溶性硫磺(简称IS)和普通硫磺互为同素异形体,它是一种线型高分子[25],由大量硫原子聚合而成。普通硫磺溶于CS2,IS不溶于CS2,因此CS2是被广泛用作分离高品位不溶性硫磺的萃取剂[26].但CS2沸点低、易挥发,着火点低、易燃,有毒,所以在使用时会带来一系列安全问题.有研究表明,具有环状结构的HAS系列溶剂溶硫能力较大,期望在这些溶剂中找出能替代CS2的萃取剂.也有文献报道, C2Cl4(四氯乙烯)、C7H8(甲苯)、CH2Cl2(二氯甲烷)、C2H3Cl3 (三氯乙烷)、C6H14(正己烷)、CCl4(四氯化碳)、芳香烃、脂肪烃都可作为不溶性硫磺的萃取剂, 采用混合溶剂作为不溶性硫磺的萃取剂的萃取效果有望取代CS2[27-28].
3 硫磺产品我国70 %的硫磺都用于制酸,硫酸产量通常是衡量一个国家工业发展水平的标志[29],它还用于橡胶、医药、食品加工等行业,但硫磺还有一些专门应用,比如Na-S电池[30]、涂硫尿素[31]、硫磺混泥土、荧光级精制硫磺等.
4 结束语物料的性质决定了所选脱硫方法,一般情况下,物料量小时,可选用化学法,若物料中又含有稀贵金属时,可选用化学法中的有机溶剂法,不会造成稀贵金属的损失;物料量较大时,可选用浮选法,设备简单,操作方便,成本较小.根据物料的性质也可采用物理法和化学法联合使用,但不管使用哪种方法,都要注意资源的综合利用.在以后回收硫的研究中可以向寻找新的有效有机溶剂以及将硫转化成一种新的可溶物质方向发展.
| [1] | 姚淑华, 石中亮, 宋守志. 有色金属矿物中硫资源的回收及综合利用[J]. 中国资源综合利用, 2003(8): 14–18. |
| [2] |
Frank R, Rudolf K, Siegfried W. The kinetics of the absorption of sulfur dioxide in calcium hydroxide suspensions[J].
Chem. Eng.Sci, 1991, 46(4): 939–947. DOI: 10.1016/0009-2509(91)85087-E. |
| [3] |
Wang Y G, Li Z H, Zhang W S, et al. Removal of sulfur dioxide from flue gas in rotating packed bed by dual-alkali method[J].
Petro-Chem. Tec, 2009, 38(8): 893–896. |
| [4] |
Akyalaln L, Kaytakoglu S. Flue gas desulfurization by citrate process and optimization of working parameters[J].
Chem. Eng. Process, 2010, 49(2): 199–204. DOI: 10.1016/j.cep.2009.12.008. |
| [5] |
Jiang X P, Liu Y Z, Gu M D. Absorption of sulphur dioxide with sodium citrate buffer solution in a rotating packed bed[J].
Chinese Journal of Chemical Engineering, 2011, 19(4): 687–692. DOI: 10.1016/S1004-9541(11)60042-6. |
| [6] | 王玉芳, 李岚, 王晔. 我国硫磺市场评述[J]. 矿冶, 2005, 14(4): 52–54. |
| [7] | 梁汉东, 张桃英, 冯久舟, 等. 从高硫煤的抽提物和残渣中检测元素硫[J]. 燃料化学学报, 2000, 28(6): 492–495. |
| [8] | 王利, 郭兆熊, 张卫峰, 等. 世界硫资源供需形势分析与中国的应对策略[J]. 化肥工业, 2007, 34(2): 5–9. |
| [9] | 刘向东, 王新. 世界硫资源分布及中国硫磺资源状况[J]. 河北化工, 2009(9): 50–59. |
| [10] | 马荣俊. 湿法炼铜新技术[M]. 长沙: 湖南科学技术出版社 , 1985. |
| [11] | 翟爱峰, 李雷忠, 刘炯天, 等. 从铜浸出渣中浮选回收元素硫的研究[J]. 化工矿物与加工, 2006(9): 1–3. |
| [12] | 黄鑫, 贺子凯. 真空蒸馏硫磺渣提取元素硫[J]. 北京科技大学学报, 2002, 24(4): 410–413. |
| [13] | 邓孟俐. 硫化锌精矿加压浸出元素硫的形成机理及硫回收工艺的研究[J]. 工程设计与研究, 2008, 125(2): 14–18. |
| [14] | 孙培梅, 魏岱金, 李洪桂. 铜渣氯浸渣中有价元素分离富集工艺[J]. 中南大学学报, 2005, 36(1): 38–43. |
| [15] | 周勤俭. 湿法冶金渣中元素硫的回收方法[J]. 湿法冶金, 1997(3): 51–54. |
| [16] | 王宝璐, 李竟菲, 徐敏, 等. 从黄铜矿酸浸渣中回收硫磺的工艺研究[J]. 厦门大学学报, 2008, 47(4): 552–555. |
| [17] | 李竟菲, 王宝路, 徐敏. 含铜金精矿中单质硫的煤油浸取回收工艺[J]. 化学工程, 2011, 37(8): 75–78. |
| [18] | 黎鼎鑫, 王永录. 贵金属提取与精炼[M]. 第2版. 长沙: 中南大学出版社 , 2003. |
| [19] | 李振华, 王吉坤. 闪锌矿氧压酸浸渣中硫的回收研究[J]. 矿业工程, 2011, 6(6): 31–33. |
| [20] | 杨天足. 贵金属冶金及产品深加工[M]. 长沙: 中南大学出版社 , 2005. |
| [21] | 杨天足, 赵天从. 用二甲苯从湿法冶金残渣中提取元素硫[J]. 中南矿冶学报, 1990, 21(2): 171–176. |
| [22] | 宋剑飞, 李立清, 李静, 等. 从硫化锑矿渣中回收硫实验研究[J]. 环境污染治理技术与设备, 2004, 5(8): 47–48. |
| [23] | 欧阳福生, 毕玉晓, 李波. 萃取剂分子结构对不溶性硫磺分离效果的影响[J]. 华东理工大学学报, 2008, 34(4): 482–486. |
| [24] | 张克娟, 夏新兴. 硫磺新溶剂研究[J]. 化学试剂, 2012, 34(1): 55–57. |
| [25] | 张惠民, 汪树军, 刘红研. 熔融法生产聚合硫的研究[J]. 辽宁化工, 2004, 33(1): 23–26. |
| [26] | 李国平, 邵永春, 李娜. 不溶性硫磺的生产[J]. 硫酸工业, 2002(3): 6–11. |
| [27] | Hagemann Jorg, Zurlo Christ oph. Process of or the production of polymeric sulfur: US, 0 050 143 507[P], 2005-06-30. |
| [28] | 邱祖民, 陈玉虎, 张玉英, 等. 不溶性硫磺的提纯及高温稳定性研究[J]. 南昌大学学报:理科版, 2002, 26(2): 103–105. |
| [29] | 汤桂花. 硫酸[M]. 北京: 化学工业出版社 , 1999. |
| [30] | 胡文宾, 高淑美, 郝国阳, 等. 硫磺的几种专门应用[J]. 精细石油化工, 2000(5): 23–24. |
| [31] | 李正西, 秦旭东, 宋洪强, 等. 硫磺新产品的开发与利用[J]. 精细化工原料及中间体, 2008(5): 15–18. |
 2013, Vol. 4
2013, Vol. 4


