| 超声场辅助制备碳纳米管/氧化钨纳米棒高效光催化剂的研究 |
2. 东南大学毫米波国家重点实验室,南京 210096
2. State Key Lab of Millimeter Waves, Southeast University, Nanjing 210096, China
当今世界能源危机和环境污染问题日益加剧,随着人类对绿色氢能源的需求日益增长,用来处理一系列污染源的投资费用将不断增加.半导体氧化物[1-7]作为光催化剂,具有高效节能、清洁无毒、无二次污染和工艺简单等优点,同时具有超强的光催化降解氧化能力,使其在污水处理及生活用水的深度处理等方面有着广阔的应用前景.纳米氧化钨因具有较宽的光吸收带、光稳定性和价格便宜、容易制备等特点,使其具有较强的光催化能力,是一种非常高效的光催化剂[8-19],在信息存储、变色窗、燃料电池、化学传感器等领域有着广泛的应用前景.纳米材料的尺寸和形貌对其应用至关重要[20].碳纳米管由于它本身的管状结构,在纳米材料制备中具有重要的作用,它不仅能够改善化学反应的微环境,对纳米材料的形成[21-27]具有修饰作用,同时还可以通过形成复合物,成为合成纳米材料的模板.然而由于碳纳米管直径非常小,长度比较长,导致长径比十分大,极易成束并相互缠绕,在普通介质中难以分散.而发挥碳纳米管的优异性能,就要将其尽量均匀的分散.利用超声场的空化效应[28-30],可以加速碳纳米管在有机溶剂中的振动,使碳纳米管的管束分散开,同时可以对颗粒尺寸进行控制.目前制备氧化钨粉体的方法比较多,常用的制备方法有气相法、液相法和固相法等.采用液相法[31-34]制备氧化钨比较普遍,但是在液相法制备过程中,由于三氧化钨溶胶的稳定性差、黏度小,一般都会采用加入表面活性剂来改善其稳定性和黏度,但是最后所制得的氧化钨粉体中都含有较多的表面活性剂与吸附物,从而导致其光催化性能下降.
本文采用超声场辅助分散碳纳米管,以无水乙醇和水分别作为分散剂和溶剂,利用溶胶凝胶法,将钨酸沉积在碳纳米管管壁上,在高温区焙烧碳纳米管/钨酸前驱体,生成了平均粒径为70 nm的碳纳米管/氧化钨(WO2.8)纳米棒,纯度高,光催化性能优异,具有广泛的应用前景.
1 实验部分 1.1 催化剂的制备称取3 g钨酸钠溶于100 mL蒸馏水中,超声波震荡使其溶解,然后缓慢滴加15 mL的1.6 mol/L盐酸溶液,直至溶液pH值为3,搅拌3 h,得到钨酸溶液A.
称取20 mg碳纳米管溶于100 mL无水乙醇中,利用超声波分散24 h,得到分散均匀的碳纳米管溶液B.
将溶液A加到溶液B中,超声波分散24 h后进行真空抽滤,洗涤,100 ℃恒温干燥2 h,得到碳纳米管/钨酸前驱体C.
碳纳米管/钨酸前驱体C放入刚玉反应舟中,再将刚玉反应舟置于管式电阻炉中的卧式石英反应管中.打开电炉及温控仪,按照预先设计的升温方案,开始对刚玉反应舟加热,升温到800 ℃,保温时间3 h,卧式石英反应管中通入氮气和氢气,冷却至常温,取出,即得碳纳米管/氧化钨纳米棒.
图 1为实验所用的800 W循环水超声波清洗器装置.
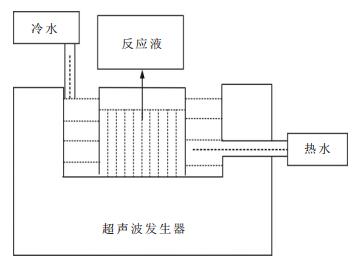 |
| 图 1 超声波装置 |
反应溶液置于超声波装置中进行超声震荡分散.主要利用超声波的空化效应,即利用超声能量对碳纳米管进行分散;利用机械搅动影响钨酸沉淀的形成过程;利用剪切破碎机理对反应物颗粒尺寸进行控制,降低颗粒的团聚程度.
1.2 催化剂的表征采用JEM-2010 F型高分辨率透射电子显微镜(HRTEM)直接观察纯化后的碳纳米管的形貌和纯化效果,以及碳纳米管/氧化钨棒复合颗粒的大小和形貌.
采用XL30扫描电子显微镜(荷兰飞利浦)观察碳纳米管/钨酸前驱体的分布情况,特征X射线能谱(EDS)分析了碳纳米管/氧化钨复合颗粒微区的化学成分.
采用UV-2550型(日本岛津)紫外可见分光光度计测量了所制备催化剂降解亚甲基蓝的紫外可见吸收光谱.
1.3 光催化活性测试光催化活性测试是利用日光直接照射含有催化剂的亚甲基蓝溶液的实验来完成的.光催化反应在光催化反应器中进行.光反应器中心光源为11 W的日光灯.染料亚甲基蓝溶液的初始浓度为1 mg/ mL,溶液体积为50 mL,催化剂的用量为30 mg.光催化反应开始前,将含光催化剂的染料悬浮液在暗处搅拌吸附30 min达到物理吸附和脱附平衡.打开光源,间隔一定时间取出2 mL样液,然后离心分离取上层清液,通过紫外分光光度计在染料的最大吸收波长下测定其吸光度A.以亚甲基蓝的脱色率表征催化剂的光催化性能.根据吸光度的变化求得亚甲基蓝的降解率,即降解率D=(A0-A)/A0×100 %(D为降解率,A0为光照前染料溶液的吸光度,A为光照后染料溶液的吸光度).
2 结果与讨论 2.1 前驱体的制备分析图 2为制备碳纳米管/钨酸前驱体的过程照片.
 |
| 图 2 碳纳米管/钨酸前驱体的制备 |
如图 2(a)所示,采用无水乙醇作为有机溶剂,将20 mg碳纳米管溶于100 mL无水乙醇中,利用超声波恒温水浴分散15 h,形成分散均匀的碳纳米管溶液.
由图 2(b)可知,乳白色絮状物为钨酸,且静置一段时间后,沉积于瓶底,呈棉花状,颗粒细而均匀分散,这说明钨酸不溶于水和无水乙醇.发生的反应公式如下:
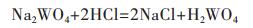
|
(1) |
由图 2(c)可知,将分散均匀的碳纳米管与钨酸混合,经恒温(室温)磁力搅拌5 h后,碳纳米管与钨酸充分混合.
图 3是碳纳米管/钨酸前驱体的SEM和TEM照片.
 |
| 图 3 碳纳米管/钨酸前驱体的SEM和TEM照片 |
由图 3得知,碳纳米管与钨酸结合在一起,钨酸较为均匀地负载在碳纳米管表面上.
2.2 样品的TEM照片图 4为纯化分散后的碳纳米管的TEM照片和碳纳米管/氧化钨复合物的TEM照片.
 |
| 图 4 典型样品的TEM照片 |
由图 4(a)得知,纯化分散后的碳纳米管细长而纯净,碳纳米管管壁上的杂质基本被除去,产品的纯度很高,且表面光洁,直径约为20~30 nm.
由图 4(b)看出,管状物为碳纳米管,棒状物为氧化钨,并且吸附在碳管外壁上,粒径约为70 nm.
2.3 样品的EDX谱图图 5为碳纳米管/氧化钨纳米棒的EDX谱图.
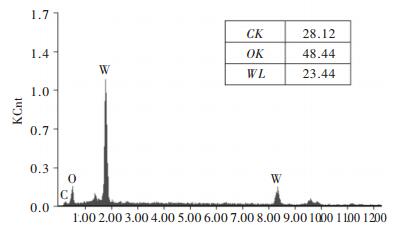 |
| 图 5 碳纳米管/氧化钨复合物的EDX谱图 |
由图 5可知,经过系统自带软件的分析,产物中只存在C、O和W 3种元素,未有其他杂质峰,且由检测得出W和O的原子比为5:14.碳纳米管具有较高的比表面积和不同层次的孔径结构,其内孔和外壁均具有很好的吸附性能,能够吸附溶液中的氧和有机物,促使其在WO2.8表面聚集,有助于提高催化剂对有机物的降解率.
2.4 催化剂的光催化性能测试样品的光催化活性通过在11W日光灯照射下降解亚甲基蓝模拟染料废水来测试.反应前进行暗处吸附30 min,待达到吸附平衡后,再打开日光光源照射溶液,每隔一定时间取3 mL反应液置于离心管中,离心分离取上层清液.催化剂降解亚甲基蓝溶液过程见图 6.
 |
| 图 6 催化剂降解亚甲基蓝溶液过程 |
图 7是亚甲基蓝反应溶液的紫外可见吸收光谱.
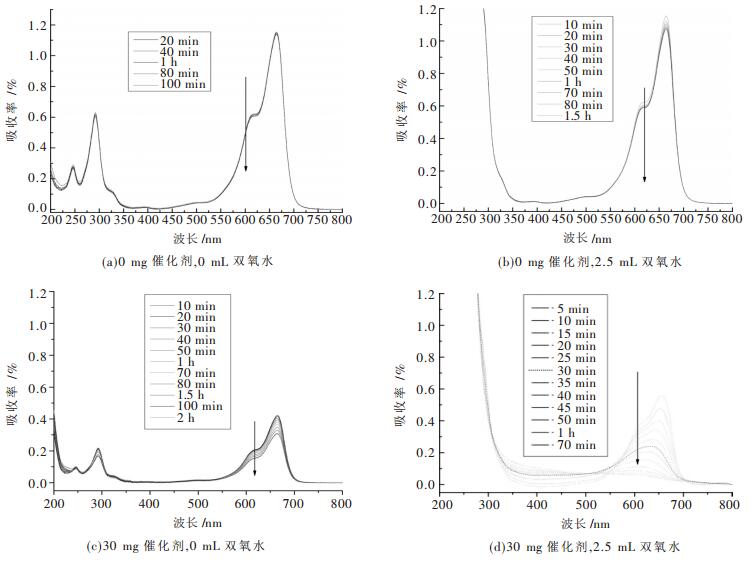 |
| 图 7 紫外可见吸收光谱 |
由图 7(a)可知,在日光照射均未加双氧水和催化剂情况下,随着光照时间的延长,吸光度基本不变,亚甲基蓝几乎无降解.这表明亚甲基蓝是一个稳定的染料分子,日光直接照射不能发生降解反应.
由图 7(b)可知,在日光照射下只加双氧水的情况下,亚甲基蓝几乎无降解.但是发现在双氧水中亚甲基蓝的吸收光谱的精细结构消失,成为一个宽带,这是由于外界因素如溶剂的改变会影响吸收光谱[35].
由图 7(c)可知,在日光照射下只加催化剂的情况下,亚甲基蓝降解率不高.
由图 7(d)可知,当加入30 mg催化剂和2.5 mL双氧水时,随着光照时间的延长,吸光值明显变化并减小,亚甲基蓝溶液的脱色率不断增大,当光照时间为50 min时,脱色率达到92.62 %.当光照时间为70 min时,脱色率达到95.3 %.
氧化钨(WO2.8)是n型半导体,其能带结构是由一个不连续的、充满电子的、低能价带(VB)和空的高能导带(CB)组成,它们之间被禁带隔开.当用能量等于或大于禁带宽度的光照射半导体时会产生光生电子和光生空穴,这些电子和空穴迁很快被半导体或杂质捕获,部分在皮秒级时间内复合,小部分移到催化剂表面与表面的羟基、水或氧分子等反应生成具有强氧化作用的前羟基自由基·OH,并进一步和亚甲基蓝发生反应,使其最终降解为二氧化碳和水.由实验可知,双氧水的加入可以协助催化剂降解亚甲基蓝溶液,这是因为,双氧水在光照作用下能使O-O键断裂生成自由基·OH.此外,催化剂中碳纳米管的空腔结构,可运输电子、储存电子,从而氧化钨(WO2.8)、双氧水(H2O2)和碳纳米管(CNTs)三者共存时可产生协同效应,双氧水和碳纳米管能俘获电子,有效降低催化剂表面电子-空穴对的重新复合,增强了体系的氧化能力.
2.5 催化剂的稳定性分析采用紫外-可见分光光度计在亚甲基蓝染料可见光区的最大吸收波长664 nm下测得吸光度A.根据D=(A0-A)/A0×100 %可以计算出反应液的降解率.
一般来说,催化剂对光具有一定的不稳定性,存在光腐蚀现象.为了较好地显示催化剂的稳定性,反复回收了催化剂,并将其与新制备的催化剂的光催化活性进行了比较研究,结果如表 1所示.
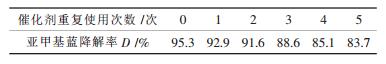
| 表1 碳纳米管/氧化钨催化剂稳定性研究 |
 |
| 点击放大 |
从表 1中可以看出,反复使用5次后的催化剂仍然具有较高的活性,降解时间为70 min时,亚甲基蓝降解率仍超过80 %.考虑到催化剂表面会发生吸附,则回收后的催化剂的光催化活性与新鲜的光催化剂相比,催化活性相差较小,即碳纳米管/氧化钨复合材料的光腐蚀现象比较轻.这可能是由于碳纳米管特殊的电子管腔结构,不仅可以运输电子,还可以储存电子,从而减小了氧化钨的光腐蚀.
3 结论(1)将碳纳米管/氧化钨前驱体在氮气和氢气气氛下,经800 ℃保温3 h,在碳纳米管管壁上生长出了氧化钨纳米棒.
(2)在11 W日光照射下,添加30 mg催化剂和2.5 mL双氧水可以使亚甲基蓝溶液的脱色率在70 min内达到95.3 %.
(3)当光照时间为70 min时, 反复使用5次后的催化剂仍然具有较高的活性.第1次回收的催化剂的降解率达到92.9 %,与新制备催化剂的降解率95.3 %相比,光催化活性略低于新制备催化剂,稳定性较好,可重复使用.
(4)利用碳纳米管的空腔结构,可运输电子、储存电子,有效阻止了光生电子一空穴的复合几率,从而提高了碳纳米管/氧化钨光催化剂的抗光腐蚀性.
| [1] | 柏双鹏, 崔鹏. 光催化氧化法降解水溶性染料罗丹明B的研究[J]. 当代化工, 2004, 33(4): 227–230. |
| [2] | 雷雪飞, 刘文占, 张洪林, 等. 纳米二氧化钛粉体光催化染料脱色的研究[J]. 南昌大学学报, 2006, 28(1): 12–14. |
| [3] | 景伟文, 刘义轩, 张欣茜. SiO2-TiO2复合催化剂降解水体中的邻苯二甲酸二甲酯[J]. 新疆农业大学学报, 2012, 35(10): 70–74. |
| [4] | 张宝亮, 张秋禹, 张和鹏, 等. ZnO@P (AA/MMA/GMA)@Fe3O4复合微球:制备及光催化性能[J]. 无机化学学报, 2012, 28(3): 503–508. |
| [5] | 王占领. SO42-/Fe2O3固体超强酸的制备及光催化降解甲基橙的研究[J]. 化学工程师, 2011, 11: 60–63. |
| [6] |
Shee Debaprasad, Deo Goutam, Hirt Andrew M. Characterization and reactivity of sol-gel synthesized TiO2-Al2O3 supported vanadium oxide catalysts[J].
JournalofCatalysis, 2010, 273: 221–228. |
| [7] |
Shen Yi, Huang Rong, Cao Yuanyuan, et al. Synthesis and photochromic properties of formaldehyde-induced MoO3 powder[J].
Materials Science and Engineering B, 2010, 172: 237–241. DOI: 10.1016/j.mseb.2010.05.023. |
| [8] | 宋继梅, 张小霞, 焦剑, 等. 三氧化钨纳米片的制备及其光催化性质研究[J]. 安徽大学学报:自然科学版, 2009, 33(3): 73–77. |
| [9] | 刘华俊. 镝掺杂纳米三氧化钨的制备及光催化活性研究[J]. 襄樊学院学报, 2007, 28(8): 31–34. |
| [10] | 解恒参, 朱亦仁. 三氧化钨的光催化氧化性能研究[J]. 工业用水与废水, 2004, 35(4): 45–48. |
| [11] | 刘华俊, 彭天右, 彭正合. Dy/WO3光催化降解罗丹明B的反应机理[J]. 武汉大学学报, 2007, 53(2): 127–132. |
| [12] | 杨海刚, 王聪明. 三氧化钨薄膜的微观结构与电致变色机制研究[J]. 功能材料, 2010(2): 181–184. |
| [13] | 蒋凯, 许亚杰, 牛新书. 纳米三氧化钨气敏材料的制备与表征[J]. 河南师范大学学报, 2003, 31(1): 58–60. |
| [14] | 魏少红, 石蔚云, 牛新书. 二氧化钛/氧化钨纳米粉体的制备及氨敏性能研究[J]. 电子元件与材料, 2003, 22(10): 26–28. |
| [15] | 成英之, 张渊明, 唐渝. 三氧化钨/二氧化钛薄膜型复合光催化剂的制备和性能[J]. 催化学报, 2001, 22(2): 203–205. |
| [16] | 李芳柏, 古国榜, 李新军, 等. 三氧化钨/二氧化钛纳米材料的制备及光催化性能[J]. 物理化学学报, 2000, 16(11): 997–1002. |
| [17] | 解恒参, 张驰, 苏苓. 光催化剂改性技术的研究进展[J]. 江苏化工, 2008, 36(5): 1–6. |
| [18] |
Yan Ai-hua, Xie Changsheng, Zeng Da-wen, et al. Synthesis, formation mechanism and sensing properties of WO3 hydrate nanowire netted-spheres[J].
Materials Research Bulletin, 2010, 45: 1541–1547. DOI: 10.1016/j.materresbull.2010.05.026. |
| [19] |
Deki Shigehito, Kotani Yuki, Mizuhata Minoru, et al. Synthesis of tungsten oxide thin film by liquid phase deposition[J].
Materials Chemistry and Physics, 2010, 123: 614–619. DOI: 10.1016/j.matchemphys.2010.05.024. |
| [20] | 高盐生, 董江庆, 徐晓燕. 纳米技术在生物传感器中的研究应用[J]. 江苏化工, 2008, 36(3): 4–6. |
| [21] | 张成国, 姜维峰, 赵斌. 碳纳米管负载二氧化镤纳米粒子的研究[J]. 江苏陶瓷, 2005, 38(6): 12–15. |
| [22] | 朱路平, 黄文娅, 马丽丽, 等. 多壁碳纳米管负载ZnO纳米复合材料的制备及其光催化性能研究[J]. 上海第二工业大学学报, 2009, 26(2): 87–93. |
| [23] | 侯珂珂, 崔平. 碳纳米管负载纳米金属氧化物的研究进展[J]. 安徽化工, 2007, 33(3): 7–10. |
| [24] | 吴玉程, 刘晓璐, 叶敏, 等. 碳纳米管负载纳米TiO2复合材料的制备及其性能[J]. 物理化学学报, 2008, 24(1): 97–102. |
| [25] | 于华荣, 成荣明, 徐学诚. 碳纳米管负载纳米Fe2O3的研究[J]. 无机化学学报, 2005, 21(11): 1649–1654. |
| [26] | 靳海波, 原伟伟, 郭志武. 负载氧化钴的碳纳米管催化剂催化氧化环己烷[J]. 石油学报, 2011, 27(1): 47–53. |
| [27] | 胡开文. 碳纳米管负载TiO2光催化剂制备与活性研究[J]. 湖北工业大学学报, 2009, 24(4): 22–24. |
| [28] |
WU Zi-Ping, XIA Bao-Yu, WANG Xiao-Xia, et al. Preparation of dispersible double-walled carbon nanotubes and application as catalyst support in fuel cells[J].
Journal of Power Sources, 2010, 195: 2143–2148. DOI: 10.1016/j.jpowsour.2009.10.013. |
| [29] | 赵海涛, 陈吉安, 范振民, 等. 铜基碳纳米管复合电镀辅助工艺的对比研究[J]. 电镀与环保, 2012, 1: 12–14. |
| [30] | 蔡万玲, 宿新泰, 王吉德. 表面活性剂辅助超声合成纳米氧化钨粉体[J]. 中国钨业, 2008, 23: 26–28. |
| [31] | 徐英明, 霍丽华, 赵辉, 等. 介稳态氧化钨超微粉体的水热合成与光致变色性质研究[J]. 无机化学学报, 2005, 21(4): 538–542. |
| [32] | 刁显珍, 侯长军. 微乳液法制备纳米三氧化钨粉体[J]. 传感技术学报, 2006, 19(5): 2362–2364. |
| [33] | 牛新书, 刘艳丽. 共沉淀法氧化锡-三氧化钨粉体的气敏性能研究[J]. 电子原件与材料, 2002(1): 10–12. |
| [34] | 苏连永, 陆祖宏. 电沉积三氧化钨薄膜电致变色及其光电化学性能[J]. 电子元件与材料, 1998(1): 17–21. |
| [35] | 周玉. 材料分析方法[M]. 北京: 机械工业出版社 , 2012. |
 2012, Vol. 3
2012, Vol. 3


