| 黄铁矿在拜耳法溶出过程中的反应行为研究 |
目前我国已探明高硫铝土矿(S>0.8 %)储量共计3.92亿t, 远景储量约10亿t.铝土矿硫含量过高时, 硫会在铝酸钠溶液中积累, 并对大部分生产工序(如溶出、沉降、蒸发等)产生不利影响, 甚至使整个生产过程无法进行.硫对拜耳法生产的危害主要表现在:使碱耗升高、产品质量变差、设备腐蚀加剧[1].因此, 高硫铝土矿至今尚未得到经济有效利用.研究解决高硫铝土矿生产氧化铝过程中带来的硫的问题, 扩大可利用铝土矿资源, 将大大缓解我国铝土矿供矿危机和矿石急剧贫化的趋势, 对我国氧化铝工业的可持续发展具有重大意义.
为减轻或消除硫对拜耳法生产的危害, 长期以来, 国内外研究工作者围绕高硫铝土矿脱硫及利用进行了大量研究, 并提出了许多方法.目前国内外脱硫方法主要有:火法脱硫、选矿法脱硫、添加脱硫剂湿法脱硫等.预焙烧脱硫[2]是针对我国高硫一水硬铝石型铝土矿的脱硫手段, 经预焙烧脱硫后, 高硫铝土矿中硫含量可降低到0.7 %以下, 达到氧化铝工业生产的要求, 但铝土矿经过焙烧处理后对氧化铝生产有不利影响, 而且要增设预处理工序, 增加加工费用和生产成本.前苏联进行了大量铝土矿浮选法脱硫工作[3], 乌拉尔铝厂将浮选作业在生产氧化铝的碱液中进行, 以降低浮选成本, 对北乌拉尔高硫铝土矿在洗液(Na2OT:43.4 g/L)中进行工业浮选试验, 可使硫的含量从2 %降低到0.4 %~0.5 %, 但该方法由于浮选要求的碱液浓度太低, 液固比过高, 工艺流程复杂而难于工业应用.向铝酸钠溶液中添加氧化钡或氢氧化钡, 脱硫率可达99 %, 但两者价格较为昂贵, 导致脱硫费用的增加.何润德等[4]提出并研究了添加铝酸钡除硫方法, 脱硫率达到了95 %, 但该方法需要增加一个合成铝酸钡的烧结工序, 同样增加了生产成本.石灰拜耳法通过添加石灰使溶液中的硫进入固相随赤泥排走[5], 但该工艺的缺点在于要求铝酸钠的浓度较低且会造成氧化铝的损失, 导致Al2O3溶出率降低和附液损失较大等.通过在拜耳循环碱液中添加氧化锌或高炉灰使硫生成ZnS析出, 可以将S2-完全脱除, 同时溶液中的铁也得以清除, 但缺点是含锌材料较贵.
由于高硫铝土矿中的硫主要以黄铁矿(约为90 %)的形式存在, 因此研究黄铁矿在溶出过程中的反应行为对我国氧化铝工业具有重要的理论和实际意义.首先对黄铁矿在铝酸钠溶液中发生的反应进行热力学分析, 并通过实验, 研究溶出过程中黄铁矿的反应规律及硫的存在形态.
1 热力学计算 1.1 黄铁矿在铝酸钠溶液中的主要反应在铝土矿溶出过程中, 黄铁矿与铝酸钠溶液可能发生的反应有式(1)~(3).
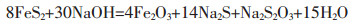
|
(1) |
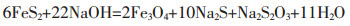
|
(2) |
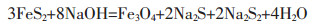
|
(3) |
进入到溶液中的含硫化物进一步发生氧化反应.在有空气存在的情况下, Na2S的氧化按反应式(4)进行:
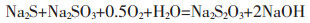
|
(4) |
同时还可能发生二硫化钠的分解反应, 如式(5)所示.
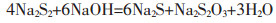
|
(5) |
随着温度升高, 硫代硫酸钠稳定性变小, 将在高压溶出过程中发生分解反应, 如式(6)~(7)所示.
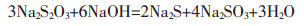
|
(6) |
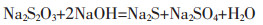
|
(7) |
对上述反应进行热力学分析, 反应吉布斯自由能计算采用公式(8)[6-8]:
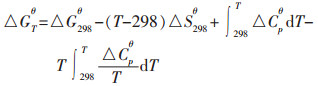
|
(8) |
参与反应的各物质热力学数据见热力学数据手册[9-10].确定有离子参与反应的△GTθ时, Cp0以在298 K和T温度之间的平均值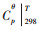
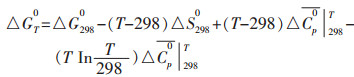
|
(9) |
其中离子形态的反应组分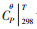
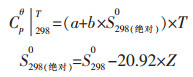
|
a, b是仅与离子类型有关的常数, 其值见文献[13], Z为离子的电荷数, 带相应的“+”, “-”.
由此可分别计算出反应式(1)~式(7)在373~573 K下的吉布斯自由能值ΔG, 并绘制各反应△GT0-T关系图如图 1.
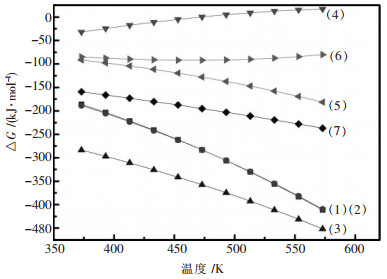 |
| 图 1 反应吉布斯自由能的变化与温度的关系 |
由图 1可见, 除反应(4)在温度高于473 K后吉布斯自由能大于零外, 其余反应在373~573 K范围内的△GT均为负值, 说明从热力学上讲这些反应都能够发生, 但反应吉布斯自由能随温度的变化趋势不同.反应(1)~(3), (5)以及(7)的△GT随温度的升高而减小, 表明升高温度会促进黄铁矿的分解, 并且反应进行的趋势很大.反应(6)的△GT随温度的升高先减小后增大, 但变化不大, 即使在温度为573 K时, 该反应的△GT也小于-80 kJ/mol, 说明该反应也很容易发生.由此可以看出, Na2S2在高压溶出过程中容易分解为Na2S和Na2S2O3; 而Na2S2O3在碱液中会被分解为Na2S、Na2SO3和Na2SO4, 随着温度的升高, 分解生成Na2SO4的趋势更大.从这也可以看出进入到溶液中的硫大部分将以S2-形式存在.
2 实验方法 2.1 仪器与原料群釜高压溶出设备(以熔盐为加热介质, 电加热, 中南大学机械厂); HDS3000测硫仪(长沙华德电子有限公司); Nicolet 6700傅里叶红外光谱(美国); 铝酸钠溶液采用工业氢氧化钠和工业氢氧化铝配制而成; 所用的黄铁矿原料为提纯黄铁矿样, 其中S含量为48 %.
2.2 实验方法在铝土矿溶出实际生产过程中, 铝土矿的配矿量大约为250 g/L, 而高硫铝土矿中含硫量为1 %~3 %.若按此比例在铝酸钠溶液中配入黄铁矿, 溶出过滤后得到的渣量很少, 这将使实验误差较大并难于分析.所以在实验研究中采用加入一定量基底的实验方法, 该基底不与铝酸钠溶液反应, 只起增大渣量的作用.实验采用Fe2O3为基底, 实验步骤如下:
称取25 g Fe2O3和不同配比的纯黄铁矿加入到高压钢弹中(容积为150 mL), 并移入100 mL配好的铝酸钠或氢氧化钠溶液, 放入2颗准20 mm和2颗准10 mm的钢球以加强搅拌, 密封拧紧钢弹盖后放入指定温度的熔盐中.溶出一定时间后, 取出高压钢弹冷却, 浆液进行抽滤, 将所得滤渣洗净、烘干、称重, 并分析滤渣中的硫含量.
2.3 渣中硫含量分析渣中硫含量采用测硫仪进行分析.分析时将待测渣于瓷舟中铺匀, 并加入适量助燃剂, 放入测硫仪中测量渣中硫含量, 并由此计算出黄铁矿的硫溶出率.
3 结果与讨论 3.1 溶出温度对硫溶出率的影响我国一水硬铝石型铝土矿拜耳法溶出温度一般在260~280 ℃, 为研究黄铁矿在拜耳法预热及溶出过程的反应行为, 在Na2Ok(指溶液中苛性Na2O, 以下标k表示)为260 g/L, 苛性分子比ak(指溶液中苛性Na2O与Al2O3的分子比)为3.0时, 研究180~280 ℃温度下硫的溶出率随时间的变化规律, 实验结果如图 2所示.
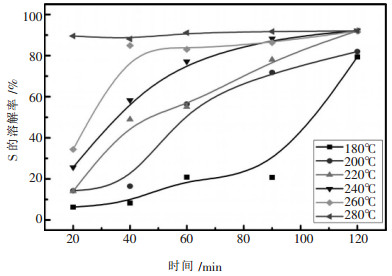 |
| 图 2 ak为3.0时不同溶出温度硫溶出率随时间的变化 |
由图 2可以看出, 相同反应时间下, 温度越高黄铁矿中硫的溶出率越大, 这与上述热力学计算结果相吻合.反应时间短时温度对硫溶出率的影响较大, 随着反应时间的延长, 不同温度下硫的溶出率的差值逐渐减小.当溶出温度为280 ℃时, 反应很快接近平衡, 反应20 min时, 硫的溶出率就达到89.52 %.
3.2 时间对硫溶出率的影响在拜耳法生产过程中, 为减轻含硅矿物对溶出工序的影响, 通常在高温溶出之前须将原矿浆在100~105 ℃下进行4~10 h的预脱硅.分别考察了原矿浆预脱硅和溶出过程中, 时间对硫溶出率的影响.在Na2Ok为232 g/L, ak为3.02, 温度为100 ℃时, 矿浆预脱硅过程黄铁矿中硫的溶出率随时间的变化规律如图 3所示.矿浆溶出过程硫的溶出率随时间的变化见图 4, 溶出条件为:Na2Ok为230 g/L, ak为3.15, 溶出温度260 ℃.
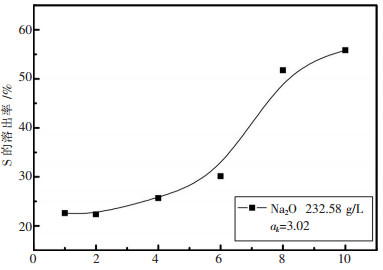 |
| 图 3 预脱硅时间对硫溶出率的影响 |
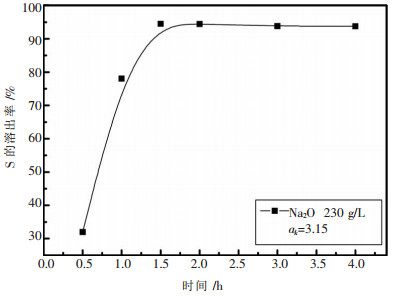 |
| 图 4 溶出时间对硫溶出率的影响 |
由图 3可以看出, 黄铁矿中的硫在矿浆预脱硅过程中即开始反应进入铝酸钠溶液.硫的溶出率随着预脱硅时间的延长而升高, 预脱硅8~10 h, 黄铁矿中约55 %的硫会反应进入到溶液.由此可以看出黄铁矿容易与碱溶液反应, 虽然预脱硅温度较低(约为100 ℃), 但在长时间(8~10 h)的预脱硅条件下, 黄铁矿中仍会有超过一半的硫反应进入溶液.
由图 4可以看出, 高温溶出过程中, 黄铁矿与铝酸钠溶液反应速度明显加快, 反应1 h硫的溶出率即达80 %, 反应1.5 h硫的溶出率超过90 %, 此后随着反应时间的延长, 硫的溶出率几乎不变.
通过上述实验可以看出, 在铝土矿高温溶出过程中, 绝大部分黄铁矿都将反应, 硫会进入铝酸钠溶液中, 并在溶液中积累, 对氧化铝生产造成危害.要减轻硫对氧化铝生产过程的危害, 只能对铝土矿进行选矿脱硫等预处理, 以避免黄铁矿随铝土矿进入溶出系统.
3.3 苛性碱浓度对硫溶出率的影响苛性碱浓度是铝酸钠溶液的一个重要参数, 为了确定不同苛性碱浓度的铝酸钠溶液对硫溶出率的影响, 实验配制了苛性分子比ak为3.0左右, Na2Ok为175~300 g/L的铝酸钠溶液, 在反应温度为260 ℃时, 不同苛性碱浓度下硫的溶出率与反应时间的关系如图 5所示.
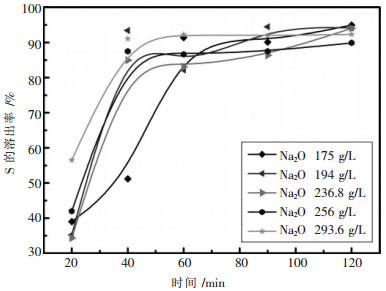 |
| 图 5 不同苛性碱浓度硫的溶出率与反应时间的关系 |
由图 5可以看出, 随着反应时间延长, 硫的溶出率快速升高, 当反应时间60 min后硫的溶出率基本不变, 说明黄铁矿在铝酸钠溶液中的反应较快, 反应主要集中在60 min内进行.反应前期溶液苛性碱浓度对黄铁矿的溶出影响较大, 当反应进行40 min时, 苛性碱浓度为175 g/L的溶液中硫的溶出率仅为51.19 %, 而苛性碱浓度大于175 g/L时, 硫的溶出率都超过80 %.随着反应时间的延长, 溶出液苛性碱浓度对硫溶出率的影响逐渐减小, 当反应进行到120 min时, 不同苛性碱浓度下硫的溶出率最大仅相差5 %.
3.4 高硫铝土矿溶出过程中硫的存在形态及反应机理研究对黄铁矿经高温溶出后的溶液进行过滤时发现, 当滤液温度较高(>85 ℃)时, 溶液透明并呈浅黄色, 随着静置时间的延长, 滤液温度降低, 溶液颜色逐渐加深, 并析出墨绿色物质.对放置不同时间的滤液上清液进行红外图谱分析, 结果如图 6所示.过滤析出的墨绿色物质, 并对该物质进行红外和XRD图谱分析, 结果如图 7、图 8所示.
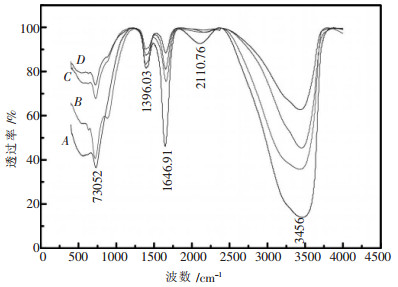 |
| A-滤液静置4 min; B-滤液静置10 min; C-滤液静置15 min; D-ak=3.0, Na2O=260 g/L的铝酸钠溶液 图 6 不同静置时间滤液红外图谱 |
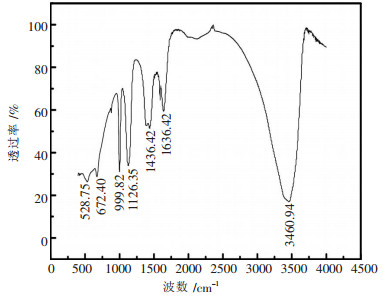 |
| 图 7 墨绿色析出物红外图谱 |
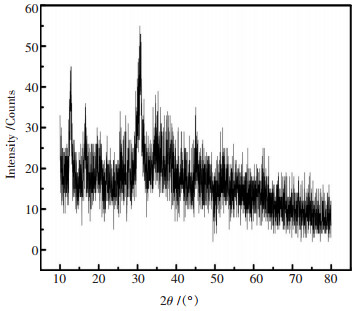 |
| 图 8 墨绿色析出物XRD图 |
从图 6可以看出, 滤液静置4 min时存在有2110.76 cm-1的峰, 该峰是S-O的吸收峰.当滤液静置10 min后, 该峰消失, 而且此时滤液红外图谱的特征峰和ak为3.0的纯铝酸钠溶液红外图谱的特征峰相同, 只是3456 cm-1和1646.91 cm-1处的峰强略有变化.说明在静置冷却过程中溶液中含硫的物质会沉淀析出.
从图 7、图 8可以看出, 墨绿色析出物为一种不定性物质, 该物质在 < 2000 cm-1的红外光谱曲线相对复杂.3460.94 cm-1处是结构水的吸收峰, 对应于-OH基团的反对称振动; 1636.42 cm-1处的吸收峰是水分子在区域内有角度的变形频率所引起的弯曲振动; 999.82 cm-1处是SO42-的吸收峰, 对应着-SO4-的伸缩振动; 528.75 cm-1, 672.40 cm-1为Fe-O-H弯曲振动峰; 1126.35 cm-1为Fe-S配位键的吸收峰; 1436.80 cm-1, 1588.52 cm-1为Fe-O吸收峰.由此可以推测出该墨绿色物质应该为氢氧基硫代铁酸钠.С.И.Кузнецов的研究也表明, 滤液在室温下静置30 d后, 将析出的沉淀与溶液分离, 沉淀中出现氢氧基硫代铁酸钠Na2[FeS2(OH)2]·2H2O [14], 该物质的生成可用反应式表示:
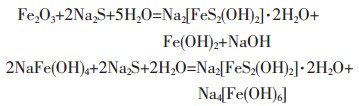
|
氢氧基硫代铁酸钠在溶液中的溶解度显著高于Fe(OH)2, Fe(OH)3, FeS, FeS2, Fe2S3的溶解度.温度、压力等因素对氢氧基硫代铁酸钠的溶液度影响很大, 在铝酸钠溶液冷却时, 氢氧基硫代铁酸钠的溶解度降低, 将沉淀析出并污染氢氧化铝产品.
4 结论(1)在373~573 K的温度范围内, 黄铁矿在苛性碱溶液中的分解反应吉布斯自由能均为负, 且随着温度的升高而减小, 说明以黄铁矿形式存在于铝土矿中的硫容易与碱液反应, 温度越高, 反应进行的趋势越大.
(2)黄铁矿在铝酸钠溶液中的反应较快, 反应主要集中在60 min内进行, 温度越高黄铁矿中硫的溶出率越大.反应时间短时, 温度、碱浓度对硫溶出率的影响较大, 随着反应时间的延长, 不同温度和碱浓度下硫溶出率的差值减小.
(3)在原矿浆预脱硅条件下(温度约为100 ℃, 时间8~10 h), 黄铁矿中会有超过一半的硫反应进入溶液; 在铝土矿高温溶出过程中, 绝大部分黄铁矿都将反应, 硫会进入铝酸钠溶液中.
(4)黄铁矿经高温溶出后的溶液在降温静置后会析出墨绿色物质, 该物质为氢氧基硫代铁酸钠, 是一种羟基铁硫聚合物.
| [1] |
杨重愚.
氧化铝生产工艺学[M]. 北京: 冶金工业出版社, 1982: 72.
|
| [2] |
吕国志, 张廷安, 鲍丽, 等. 高硫铝土矿的焙烧预处理[J].
过程工程学报, 2008, 8(5): 892–896.
|
| [3] |
欧阳坚, 卢寿慈. 国内外铝土矿选硫研究的现状[J].
矿产保护与利用, 1995(6): 25–28.
|
| [4] |
何润德, 田忠良. 论用铝酸钡脱除工业铝酸钠溶液中硫的经济合理性[J].
贵州工业大学学报:自然科学版, 2000, 29(6): 54–58.
|
| [5] |
刘连利, 翟玉春, 田彦. 水合硫铝酸钙的合成[J].
中国有色金属学报, 2003, 13(2): 506–510.
|
| [6] |
温元凯, 邵俊, 陈德伟. 含氧酸盐矿物生成自由能的计算[J].
地质科学, 1978(4): 348–357.
|
| [7] |
温元凯, 邵俊, 王三山. 含氧酸盐矿物生成热的简单计算[J].
金属学报, 1979, 15(3): 98–103.
|
| [8] |
傅崇说.
有色冶金原理[M]. 北京: 冶金工业出版社, 1984: 157-177.
|
| [9] |
姚允斌, 解涛, 高英敏.
物理化学手册[M]. 上海: 上海科学技术出版社, 1985: 838-912.
|
| [10] |
叶大伦, 胡建华.
实用无机物热力学数据手册[M]. 北京: 冶金工业出版社, 2008: 207-249.
|
| [11] |
Criss C M. The corresponding theory of ion entropy[J].
J.Amer.Chem.Soc, 1964(86): 53–85. |
| [12] |
Russell A S, Edwards J D, Taylor C S. Solubility and density of hydrated aluminas in NaOH solutions[J].
Journal of Metals, 1955, 203(7): 1123–1128. |
| [13] |
杨显万, 何蔼平.
高温水溶液热力学数据计算手册[M]. 北京: 科学出版社, 1983: 10-16.
|
| [14] |
黎志英. 贵州高硫铝土矿溶出性能研究[D]. 贵州: 贵州大学, 2006, 16-22.
|
 2011, Vol. 2
2011, Vol. 2


