| 由钨酸盐熔盐电解直接制备钨粉的可行性分析 |
钨作为一种熔点最高的稀有金属,是不可再生的重要的国家战略性储备资源,以其优异的性能被广泛运用于工业生产中.伴随着国民经济的日益发展,对钨粉的需求量越来越大[1].
钨粉是加工粉末冶金钨制品和钨合金的主要原料.目前从钨精矿到制取金属钨粉的工艺流程一般要经过:精矿分解制Na2WO4→APT的制备→煅烧→还原WO3制取金属钨粉[2],该流程存在工艺流程长等缺点.超细钨粉以其显著的特点成为多种重要功能材料和结构材料的重要原料,从而受到人们广泛的关注[3].超细钨粉的制备方法开始是将原有氢还原制备钨粉的方法加以改进,或采用新的还原方法.目前,有关超细钨粉的制备研究主要集中于自蔓延高温还原法、钨酸盐直接还原法、氧化钨还原法和卤化钨氢气还原法等.虽然现有的方法有各自的优点,但从设备的复杂程度和成本角度以及产品品质来看,在实际应用过程中还存在诸多问题,例如:卤化钨氢气还原法制备过程中会产生大量的有害气体(HC1或HF)既腐蚀生产设备,又污染环境.
熔盐电解冶金在制备难熔金属,如Ti、Zr、Mo、Ta、V、Nb等[4]有着独特的优势.与传统的氧化钨-氢原法相比,熔盐电解法不仅工艺简单、投资少、成本低,操作安全简便,而且通过预电解,可以除去电活性比钨小的杂质,电活性比钨大的杂质被留在电解质中,所以熔盐电解法可制取高纯钨粉[5].熔盐电解法制备金属钨也很早就得到了人们的重视.由于大部分钨精矿的组成形式为钨酸盐,若采用钨酸盐作为活性物直接电解制备钨粉,则能大幅缩短现有的工艺流程,降低生产成本,提高钨资源的利用率.本文结合已实施实验的结果和理论计算,提出由钨酸盐熔盐电解直接制备钨粉的理论依据和可行性.
1 熔盐电解法制备钨粉研究现状20世纪六七十年代,文献[6-7]报道了以磷酸钠-硼酸钠、氯化物-氟化物为电解质电解氧化钨制备钨粉的方法.以磷酸钠-硼酸钠为电解质电解按一定配比混合的Na4P2O7-Na2B4O7-WO3熔盐体系,在温度为1000 ℃,石墨为阴阳电极的条件下,对氧化钨进行电解制得钨粉,所制得的钨粉具有颗粒大,杂质含量高的特点,但至今未用于工业生产.以氟化物-氯化物体系电解制钨是以KAlF4-NaF-NaCl为电解质,在温度为1100 ℃,石墨作为阴阳电极的条件下,所制得的钨粉杂质含量高于10 %,钨粉粒度达到20 μm,但也未在生产加以应用.
冯乃祥等[8]采用NaCl-KCl-Na2WO4-WO3作为熔盐体系,在电解温度为720 ℃,阴极电流密度为250 mA/cm2的条件下,用熔盐电解法制得了平均粒度为1.2 μm的超细钨粉,这种钨粉呈非球形,长宽比为1.6,但至今未见其后续报道.
2 由钨酸盐熔盐电解直接制备钨粉可行性及相关试验依据 2.1 由钨酸盐熔盐电解直接制备钨粉的理论可行性理论上,用碱或碱土金属氯盐和氟盐体系组成的单元或多元熔体的槽电压窗口较宽,都可以起到支持电解质作用.但考虑高温下的氟盐对实验设备有腐蚀作用和对环境污染较重,碱或碱土金属氯盐作为电解质体系则较为理想,其中NaCl、CaCl2价格相对便宜,各项物理化学性质也符合电解要求,故优先选择熔点较低的NaCl-CaCl2体系作为熔盐电解质. 750 ℃时,NaCl和CaCl2理论分解电压分别为3.26 V和3.36 V.X.Y.Yan等[9]报道了在800 ℃附近,NaCl-CaCl2体系中NaCl的活度对Raoult定律的偏差值为负,而NaCl实际的分解电压要比理论计算值高,从而可以得出混合熔盐分解电压应大于3.26 V.
当采用NaCl-CaCl2-Na2WO4熔盐体系电解制备钨粉时,电解过程中可能会发生以下反应:
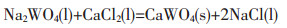
|
(1) |
根据参考文献[10]提供的数据分析发现,在实际电解温度下,式(1)的反应速度较快,因此电解过程中可能会发生前置反应,实际被电解物质主要为CaWO4.在电解进行的中途断电,电解槽冷却后取出的熔盐底部发现有大片白色固体物质,检测到该白色物质为CaWO4.CaWO4的熔点高达1580 ℃,电解过程中不会先熔化后离解形成Ca2+和WO42-.文献[10]提供的数据表明实际电解温度下反应CaO(s)+WO3(s)→ CaO·WO3(s)为自发过程,这表明CaO·WO3分子团可以自发存在,为便于理解,直观上可以将CaWO4等价为CaO·WO3分子团.
钨酸盐的化学分子式为:MexWOy (Me为金属单质),熔盐电解MexWOy制备钨粉,直观上可以理解为是对MexOy-3·WO3的电解.由此当MexOy-3与WO3的理论分解电压差值较大时,一定条件下可以让一方优先在阴极析出;差值较小时,可以同时析出Me与W.根据公式:
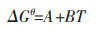
|
(2) |
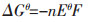
|
(3) |
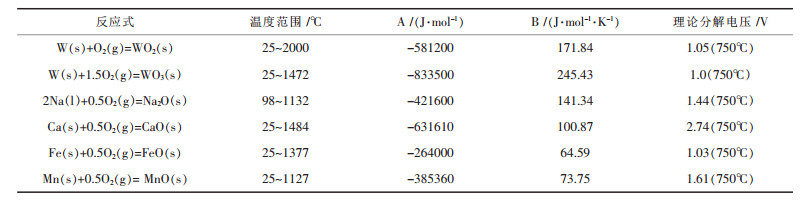
其中ΔGθ为吉布斯自由能,Eθ为理论分解电位,n为反应得失电子数,F 为法拉第常数,取96485 C/mol,A与B数值来源于文献[10],可以计算出相关的氧化物理论分解电压(见表 1).
| 表 1 相关氧化物的理论分解电压 |
 |
| 点击放大 |
2.2 由钨酸钠熔盐电解直接制备钨粉的相关试验依据
工业上由钨精矿开始到制得钨粉的流程中,首先一步就是钨精矿的分解得到Na2WO4. 表 2中列出了一些钨酸盐熔盐电解直接制备钨粉过程中可能存在的置换反应及相应的吉布斯自由能,其中的ΔGθ值根据式(2)及文献[10]的数据计算得来.表 1显示,Na2O的理论分解电压均比三氧化钨的大,理论上阴极析出物质为W,但由于存在极化效应等因素,WO3的实际分解电压要比理论计算值大,所以,当槽电压大于Na2O的理论分解电压时,钠也有可能被电解析出.由于钠是活泼性很强的金属,从表 2中反应式1的ΔGθ值计算结果来看,就算钠被析出,也会马上发生下面的置换反应:
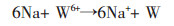
|
(4) |
| 表 2 相关置换反应及相应的吉布斯自由能 |
 |
| 点击放大 |
所以阴极最终析出产物是钨.
通过实验研究也发现,在一定的条件下,对NaCl-CaCl2-Na2WO4熔盐体系进行电解可以制备得到钨粉,钨粉纯度达到95 %,平均粒度为6 μm.
2.3 由钨酸钙熔盐电解直接制备钨粉的相关试验依据表 1显示,CaO的理论分解电压比WO3的要大很多,一定条件下,钨可优先于钙在阴极析出.当采用一定配比的NaCl-CaCl2-CaWO4作为熔盐电解体系,并在合适的电解条件下,也可以制得纯度为96 %,平均粒度为5 μm的钨粉.
2.4 由钨酸铁、钨酸锰熔盐电解直接制备钨粉的理论预期黑钨矿主要成分是(Fe、Mn)WO4. 表 1显示,铁与钨的氧化物理论分解电压较为接近,但由于表 2中反应式2的ΔGθ值小于零,电解过程中很可能会发生如下反应:
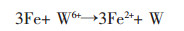
|
(5) |
但从ΔGθ值的大小来说,式(5)向右进行的趋势没有式(4)强烈;而如果阴极析出物为钨铁合金,由于合金的生成将削弱阴极极化作用,这更有利于钨铁合金在阴极的析出,所以理论上得出,熔盐电解钨酸铁阴极最终产物很可能是钨铁合金.由于锰的氧化物理论分解电压值比钨的要大许多,故钨将优先于锰在阴极析出,所以合适的电解条件下(如调节槽电压低于氧化锰理论分解电压),熔盐电解钨酸锰阴极产物是钨粉.
3 结论目前,熔盐电解法制备钨粉的相关研究还处于实验室阶段.由钨酸盐熔盐电解直接制备钨粉大幅的缩短了工业制备钨粉的工艺流程,在开发短流程、低成本制备钨粉的工艺途径中具有很强的竞争力.在理论上,熔盐电解法制备钨粉体系中,电解质的选择范围是很宽泛的,同时也有许多制备难熔金属的成功经验可以借鉴.实验上可以证明由钨酸钠、钨酸钙熔盐电解直接制备钨粉是可行的.但由钨酸铁和钨酸锰电解的过程预计工艺选择条件较为复杂,还没有取得实验支持,有待进一步研究.
| [1] |
殷俐娟. 我国钨资源现状与政策效应[J].
中国矿业, 2009, 18(11): 1–3.
DOI: 10.3969/j.issn.1004-4051.2009.11.001. |
| [2] |
莫似浩.
钨冶炼的原理和工艺[M]. 北京: 轻工业出版社, 1984: 154-158.
|
| [3] |
刘辉明, 范景莲, 田家敏, 等. 超细钨粉的研究与应用[J].
中国钨业, 2009, 24(1): 29–32.
|
| [4] |
陈延禧.
电解工程[M]. 天津: 天津科学技术出版社, 1993: 369-370.
|
| [5] |
高玉明. 熔盐电解法制取钨粉的试验与研究[D]. 沈阳: 东北大学, 1997.
|
| [6] |
彭少方.
钨冶金学[M]. 北京: 冶金工业出版社, 1981: 25-30.
|
| [7] |
叶帷洪, 王崇敬. 钨-资源、冶金、性质和应用[M]. 罗英, 阮允翔, 译. 北京: 冶金工业出版社, 1983: 1-20.
|
| [8] |
冯乃祥, 刘希诚, 孙阳. 用熔盐电解法制备超细钨粉[J].
材料研究学报, 2001, 15(4): 459–462.
|
| [9] |
Yan X Y, Fray D J. Production of Niobium Powder by Direct Electrochemical Reduction of Solid Nb2O5 in a Eutectic CaCl2-NaCl Melt[J].
Metallurgical and Materials Transactions B, 2002, 33: 685–692. DOI: 10.1007/s11663-002-0021-6. |
| [10] |
粱英教, 车荫昌.
无机物热力学数据手册[M]. 沈阳: 东北大学出版社, 1994: 45-55.
|
 2011, Vol. 2
2011, Vol. 2

