| 稀土发光性能研究及其应用 |
自1964年Y2O3:Eu被用于制造发光材料以来,稀土发光材料的研究得到了迅猛的发展,目前已经成为照明、显示、光电器件等领域中的支柱材料.在所有的稀土元素中,由于其离子结构具有特殊的4f电子组态能级,为多种能级跃迁创造了条件,使得含稀土的化合物具备许多独特的化学性质和物理性质,因而在光、电等领域得到广泛的应用.本文拟对稀土材料的发光性能以及应用作一简要综述.
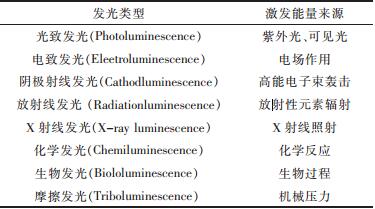
1 稀土的发光种类根据对发光材料的能量激发方式不同,稀土发光材料可分为光致发光材料、阴极射线发光材料、电致发光材料、高能量光子激发发光材料等.具体分类列举于表 1.不管哪种方式,一般都包括能量吸收、能量传递及光发射3个阶段.
| 表1 不同激发方式的发光种类 |
 |
| 点击放大 |
根据发光方式的不同,稀土发光又可分为非激活型发光和激活型发光两大类.非激活型发光是由发光材料基质的热歧化作用出现的结构缺陷,在晶格间产生空位和离子或原子,由这些晶格缺陷所引起的发光.由于此类发光不需要加入激活物质,因此非激活型发光又称为自激活发光.激活型发光则通过向基质晶格中掺入另一种元素的离子或原子时出现杂质缺陷,由这种缺陷引起的发光.其中掺入的激活物质称之为激活剂.常用作激活剂的稀土离子主要包括Sm3+、Eu3+、Eu2+、Tb3+、Dy3+等,其中又以Eu3+和Tb3+两种离子应用最为广泛.另外,Pr3+、Er3+、Yb3+除作为激活剂外,还被用于上转换材料的敏化剂.
此外,根据发光驰豫时间的长短,以持续时间10-8s为分界,可以把发光分为荧光和磷光两类.持续时间短于10-8s的发光称为荧光,长于10-8s的发光称为磷光.
2 稀土的发光原理通常意义上的发光都是指物质吸收外部能量后,经过一定的物理化学变化,最后又将部分能量以光的形式辐射出来.稀土材料发光一般指稀土固体发光材料受到紫外线、X射线、电子轰击等激发方式的作用时,产生辐射的一种物理过程.根据激发能量的来源不同,具体的原理略有区别.但无论何种发光形式,都包含激发、能量传递和发光3个过程.激发是指材料接受外部能量后,内部电子由基态跃迁至激发态的过程.能量传递分为辐射传递和无辐射传递两类.所谓辐射传递,是指当两种离子能量谱带相重合时,一个离子的辐射光能被另一个离子再吸收的过程.在发光过程中,当存在辐射传递时,由于能量的耗损而最终导致发射光向长波方向偏移.根据激发能量的不同,不同发光类型的发光原理大致可分为如下几种:
(1)光致发光(Photoluminescence):以外界光源作为激发能量的来源,主要通过紫外光、可见光或者红外光激发而产生的发光现象.光致发光是发光现象中研究最多、应用最广的发光类型.发光材料首先将吸收的能量传递给激活剂.激活剂电子受激发后从基态向不同能级之间发生跃迁再返回基态,多余的能量以光的形式发射,同时伴随有部分非发光跃迁,以热的形式发射.
在光致发光中,吸收光和发射光通常服从Stokes规则:即吸收光子的能量高于发射光子的能量.当激发波长大于发射波长,此类光致发光现象称为反Stokes效应,又被称为上转换发光现象.上转换发光机理是基于发光材料能够将两个或多个低能光子转换成一个高能光子,即在发光中心相继吸收两个或多个光子并经过无辐射驰豫达到发光能级后,再跃迁到基态放出一个可见光子.一般特指将红外光转换成可见光的材料,其特点是所吸收的光子能量低于所发射的光子能量.
(2)电致发光(Electroluminescence):以电能作为激发能量的来源.根据发光材料的不同,电致发光可以分为本征型电致发光和半导体型电致发光.本征型电致发光通过电场的加速作用使电子获得足够的能量,最终碰撞电离或激发发光中心而导致复合发光.半导体型电致发光则通过将电子(空穴)注入到p(n)型材料区后,电子以直接或间接的途径与多数载流子复合而产生发光现象.
(3)阴极射线发光(Cathodoluminescence):以高能电子束作为激发能量的来源.高能电子入射发光物质后,将能量传递给原子中原有电子使其获得很高的动能而成为高速的次级发射电子,次级发射电子最终将能量传递给发光物质而引起发光.
此外,还有由机械压力引起的摩擦发光(Triboluminescence),以及在生物过程中产生的能量被发光体所捕获而导致的生物发光(Biololumineseence)现象等.除以上类型的发光方式,还有组合型发光.以电致化学发光为例,电致化学发光是化学发光与电化学相结合的产物,指通过施加一定的电压引起电化学反应,在电极表面产生某种新物质,电生物质之间或电生物质与其他物质进一步反应,经过高能电子转移,使电子跃迁至激发态,再返回基态时的发光现象[1].早在20世纪20年代,Harvey小组便发现电解过程时可以产生发光现象[2].
3 稀土的发光应用由于转换率高、可发射光谱范围宽、物理化学性质稳定等优点,稀土发光材料得到了迅猛的发展,目前已经被广泛应用于荧光材料的合成、电子显示、照明、光电器件等领域.
(1)在显示照明中的应用.稀土发光材料具有发光效率高、承受紫外辐射性能好、热猝灭温度高等优点,可用于节能照明使用[3].通过将稀土与其他材料掺杂制备复合发光材料,可有效调整光色和提高色质,改善荧光强度和热稳定性[4].
在电子显示方面,利用稀土荧光响应时间快、光量子产率高、密度大等特点,可以将稀土荧光材料用于制备各类影视成像技术.随着现代科技的迅猛发展、稀土及其复合物制备方法的更新,稀土发光性能研究的深入,稀土发光材料己从简单的照明材料发展到今天的超薄电视、高负荷荧光灯、等离子体显示、精密分析探头等高科技领域的主导材料.
(2)在分析测试中的应用.利用稀土的荧光性能,可将稀土荧光材料应用于对特定物质的分析检测之中.如将铽与吡啶组成的荧光复合材料可用于混合稀土氧化物中铽的直接荧光光度测定[5].通过三乙胺三水杨酰胺(TSTA)对铕荧光材料的荧光增强现象,可通过三元体系建立测定铕的新方法并成功用于测定高纯钇中的铕[6].利用铽的敏化发光可同时测定饮料中的苯甲酸和糖精含量[7].
在生命分析检测领域,稀土元素作为放射性同位素和非同位素标记的荧光探针,在生物活性物质检测中同样发挥着至关重要的作用,特别是铽已被广泛应用于研究DNA与生物体内镁离子的作用及功能.镧系金属离子当中的铽[8]和铕[9]与核酸相互作用后,可促使金属离子产生特征荧光,由此可提供有关核酸结构及组成的信息.通过核酸三线态与镧系金属离子之间激发态能量匹配时发生的能量转移引起材料荧光强度的变化,据此可以建立测定DNA和RNA的方法[10].此外,通过不同的蛋白质对铽5D4→7F5电子跃迁荧光敏化程度的不同,可利用稀土荧光作为生物探针研究生物大分子与金属离子之间相互结合部位和结构类型[11].结合荧光免疫分析技术,利用稀土元素为标记物可以建立新型时间分辨荧光免疫分析法[12].首先将抗体和稀土离子相结合,通过稀土离子与敏化剂之间形成高效的荧光鳌合物,以此作为检测的依据.目前利用铕(Ⅲ),钐(Ⅲ)等稀土元素的荧光性能所制备的荧光配合物用于时间分辨荧光免疫分析,已经实现商品化生产[13].
(3)在其他领域中的应用.在选矿采矿方面,利用稀土荧光光谱的高灵敏度和高选择性,可以实现对矿物的发光分析,用以检测矿样中稀土含量.利用稀土及其配合物的光致发光性能可将稀土配合物溶于印刷油墨印制各种防伪商标等,还可与塑料混合制成各种显示材料.利用Gd3+的6P7/2→8S电子跃迁产生的310nm窄线光谱,可用于对饮用水的净化杀菌作用.
通过光诱导电子转移作用(PIET: Photoinduced Electron Transfer),可利用稀土的荧光性能制备荧光开关装置[14-15].荧光PIET开关通常由荧光团(fluor)、间质(spacer)及受体(receptor)三部分组成,三者间通过间质的连结作用而结合在一起.根据荧光能量的转移不同,可以将荧光开关分为“switch on”和“switch off”两大类.当受体同客体(如质子)络合后,可以引发或禁阻体系的PIET过程.如通过铕络合物在不同pH值条件下所表现出来不同的荧光强度,可以测量溶液的酸碱性[16].随后,Gunnlaugsson小组将三价铕与四酰氨-1, 10-邻菲罗啉形成配合物后,制备出第一个完全由pH控制的荧光开关装置[17-18].
在临床药物分析检测方面,稀土的荧光性能同样发挥着重要的作用.以近年来广泛应用于临床的新一代广谱抗菌药氟喹诺酮类药物为例,由于此类药物均含有α一酮酸,能与三价铽络合生成配合物并通过分子内能量转移而产生铽的特征荧光[19-21],从而实现对生物体液中此类药物的光化学敏化荧光法测定,检测限可低至10-9mol·L-1.
在航空航天领域,稀土材料由于其独特的耐高温、硬度高等性能正日益受到广泛关注.如镧与硼组成的化合物LaB6具有耐高温性能,可以用作航空飞机中的耐高温喷嘴材料[22].此外,由于LaB6还具有电阻恒定、抗热辐射性好、耐离子轰击性好等许多特殊性能,因此在真空或氮气氛围条件下用LaB6作阴极材料时,可为军工、航空航天等高科技领域提供纯度接近于100%的单一硼离子,形成强大而且稳定的离子源[23-25].
4 结束语凭借其丰富的光转换方式和能级跃迁组态,稀土发光材料在新光源、显像显示、分析检测和矿物探测等领域得到了广泛的应用.作为世界上稀土资源最丰富的国家,我国在稀土的研究与应用方面具有得天独厚的资源优势.现在已查明的世界稀土资源中,80%的稀土资源分布在我国,并且品种齐全.但是长期以来,我国稀土贸易都处于原料和粗产品的低端出口,而对一些精制产品及深加工产品却又依赖进口.因此,加大对稀土功能材料的开发和应用方面的研究,特别是结合物理、化学和材料学科等多个交叉学科,强化稀土深加工、研发新型稀土功能材料、研制新颖高级发光材料和发光器件及其应用将是今后我国稀土科研工作者的重点.
| [1] |
Miao W J. Electrogenerated Chemiluminescence and Its Biorelated Applications[J].
Chemical Reviews, 2008, 108(7): 2506–2553. DOI: 10.1021/cr068083a. |
| [2] |
Harvey N. Luminescence During Electrolysis[J].
Journal of Physical Chemistry, 1929, 33(10): 1456–1459. |
| [3] | 张中太, 张俊英. 无机光致发光材料及其应用[M]. 北京: 化学工业出版社, 2005. |
| [4] | 刘杰凤, 蒋维, 卓少钟, 等. 铕配合物-蒙脱土复合发光材料的合成与表征[J]. 安徽大学学报:自然科学版, 2008, 32(1): 65–69. |
| [5] | 慈云祥, 宁民柱, 阳芳英. 微量铽的萤光光度测定——铽与吡啶-2, 6-二羧酸螯合物的萤光[J]. 高等学校化学学报, 1983, 4(1): 115–118. |
| [6] |
Yang W, Mo Z L, Teng X L, et al. Determination of Trace Europium Based on New Ternary Fluorimetric Enhancement System of Europium (Ⅲ) with Thenoyltrifluoroacetone and Trisalicylicamido Triethylamine[J].
Analyst, 1998, 123(8): 1745–1748. DOI: 10.1039/a802278j. |
| [7] |
Aguilar-Caballos M P, Gomez-Hens A, Perez-Bendito D. Simultane Ous Determination of Benzoic Acid and Saccharin in Soft Drinks by Using Lanthanide-sensitized Luminescence[J].
Analyst, 1999, 124(7): 1079–1084. DOI: 10.1039/a902402f. |
| [8] |
Prat O, LoPez E, Mathis G. Europium(Ⅲ) Cryptate: A Fluorescent Label for the Detection of DNA Hybrids on Solid Support[J].
Analytical Biochemistry, 1991, 195(2): 283–289. DOI: 10.1016/0003-2697(91)90331-M. |
| [9] |
Karsten U, Wollenberger A. Improvements in the Ethidium Bromide Method for Direct Fluorometric Estimation of DNA and RNA in Cell and Tissue Homogenates[J].
Analytical Biochemistry, 1977, 77(2): 464–470. DOI: 10.1016/0003-2697(77)90259-7. |
| [10] |
Ci Y X, Li Y Z, Chang W B. Fluorescence Reaction of Terbium(Ⅲ) with Nucleic Acids in the Presence of Phenanthroline[J].
Analytica Chimica Acta, 1991, 248(2): 589–594. DOI: 10.1016/S0003-2670(00)84680-2. |
| [11] |
Brittain H G, Richardson F S, Martin R B. Terbium(Ⅲ) Emission as a Probe of Calcium(Ⅱ) Binding Sites in Proteins[J].
Journal of the Americal Chemistry Society, 1976, 98(25): 8255–8260. DOI: 10.1021/ja00441a060. |
| [12] |
Richardson F S. Terbium (Ⅲ) and Europium (Ⅲ) Ions as Lumines-cent Probes and Stains for Biomolecular Systems[J].
Chemical Re-views, 1982, 82(5): 541–552. DOI: 10.1021/cr00051a004. |
| [13] |
Diamandis E P, Christopoulos T K. Europium Chelate Labels in Time-resolved Fluorescence Immunoassays and DNA Hybridization Assays[J].
Analytical. Chemistry, 1990, 62(22): 1149A–1157A. DOI: 10.1021/ac00221a716. |
| [14] |
Czarnik A W. Chemical Communication in Water Using Fluorescent Chemosensors[J].
Accounts of Chemical Research, 1994, 27: 302–308. DOI: 10.1021/ar00046a003. |
| [15] |
Bissell R A, de Silva A P, Gunaratne H Q, et al. Molecular Fluores- cent Signalling with 'fluor-spacer-receptor' Systems: Approaches to Sensing and Switching Devices via Upramolecular Photophysics[J].
Chemical Society Reviews, 1992, 21: 187–195. DOI: 10.1039/CS9922100187. |
| [16] |
De Silva A P, Gunaratne H Q N, Rice T E. Proton-Controlled Switching of Luminescence in Lanthanide Complexes in Aqueous So- lution: pH Sensors Based on Long-Lived Emission[J].
Angewandte Chemie International Edition in English, 1996, 35: 2116–2118. DOI: 10.1002/(ISSN)1521-3773. |
| [17] |
Gunnlaugsson T, Dónaill D A M, Parker D. Lanthanide Macrocyclic Quinolyl Conjugates as Luminescent Molecular-Level Devices[J].
Journal of the American Chemical Society, 2001, 123(51): 12866–12876. DOI: 10.1021/ja004316i. |
| [18] |
Gunnlaugsson T, O'Brien J E, Mulready S. Glycine-Alanine Conju- gated Macrocyclic Lanthanide Ion Complexes as Artificial Ribonucle- ases[J].
Tetrahedron Letters, 2002, 43: 8493–8497. DOI: 10.1016/S0040-4039(02)02071-3. |
| [19] |
Zhang T L, Zhao H C, Jin L P. Photochemical Fluorescence Enhancement of the Terbium-lomefloxacin Complex and Its Application[J].
Talanta, 1999, 49: 77–82. DOI: 10.1016/S0039-9140(98)00364-6. |
| [20] |
Fasani E, Mella M, Caccia D, et al. The Photochemistry of Lome- floxacin, An Aromatic Carbene as the Key Intermediate in Photode- composition[J].
Chemical Communications, 1997, 14: 1329–1330. |
| [21] |
Zhang T L, Zhao H C, Jin L P, et al. Study of Photochemical Fluo- rescence Enhancement of the Terbium-lomefloxacin Complex[J].
Journal of Photochemistry and Photobiology A: Chemistry, 1999, 121: 37–41. DOI: 10.1016/S1010-6030(98)00450-X. |
| [22] |
Lafferty J M. Boride Cathodes[J].
Journal of Applied Physics, 1951, 22: 299–309. DOI: 10.1063/1.1699946. |
| [23] |
Hiebl K, Sienko M J. Chemical Control of Superconductivity in the Hexaborides[J].
Inorganic Chemistry, 1980, 19(7): 2179–2180. DOI: 10.1021/ic50209a070. |
| [24] |
Otani S, Nakagawa H, Nishi Y, et al. Floating Zone Growth and High Temperature Hardness of Rare-Earth Hexaboride Crystals: LaB6, CeB6, PrB6, NdB6, and SmB6[J].
Journal of Solid State Chemistry, 2000, 154: 238–241. DOI: 10.1006/jssc.2000.8842. |
| [25] |
Zhao X D, Liu X Y, Lin F, et al. A New Route for the Synthesis of Boron-rich Rare-earth Boride NdB6 Under High Pressure and High Temperature[J].
Journal of Alloys and Compounds, 1997, 249: 247–250. DOI: 10.1016/S0925-8388(96)02856-3. |
 2011, Vol. 2
2011, Vol. 2

