| 微波活化铜精矿加压浸出动力学 |
2. 北京矿冶研究总院, 北京 100070
2. Beijing General Research Institute of Mining and Metallurgy, Beijing 100070, China
加压浸出是一种清洁的湿法冶金新技术, 具有浸取高效﹑流程短﹑无污染等优点[1], 在复杂硫化铜矿浸出方面具有广阔的应用前景[2-4].但复杂硫化铜矿在硫酸浸出过程中易“钝化”[5], 受该问题局限, 复杂硫化铜矿加压浸出目前仅停留在实验室研究阶段.
为克服矿石浸出“钝化”问题, 可以采用微波预处理方法[6-9].当微波快速加热矿物时, 由于微波穿过金属矿物产生很大的热应力, 致使矿物边缘出现微小裂缝[10], 这有可能是使矿物活性增强的原因之一.另外, 在微波场中, 大多数硫化矿(如黄铁矿、黄铜矿等)都能吸收微波能[11].物质吸收微波后, 其晶体结构、表面性质等有可能发生显著改变[12], 如黄铁矿在一定条件下经微波处理后会转变成磁黄铁矿[13].实践证明, 经微波活化, 原本难以浸出的铜精矿在中等温度(453 K)条件下即可顺利浸出[14].
为进一步完善微波活化铜精矿加压浸出工艺, 加强浸出行为及浸出过程研究是非常必要的.本文即以微波活化铜精矿为研究对象, 探讨微波活化铜精矿在408~453 K温度范围内加压浸出动力学, 进而分析铜、锌浸出过程的动力学控制因素.
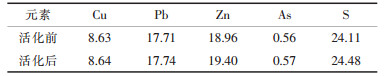
1 实验 1.1 原料与仪器实验所用铜精矿XRD谱图见图 1.由图 1可知, 铜精矿中主要的金属矿物有闪锌矿、黄铜矿、黝铜矿、黄铁矿、方铅矿.铜精矿粒度为-44 μm占99.7 %.铜精矿在微波功率82 W、每批处理量95 g条件下辐照时间120 s, 过程中未见铅、锌、硫、砷的挥发损失, 微波活化前后铜精矿主要元素成分见表 1.
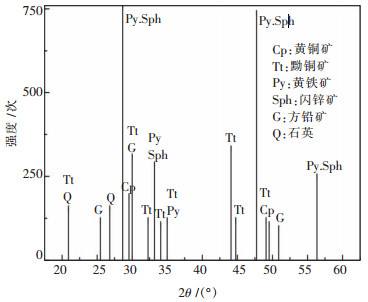 |
| 图 1 铜精矿XRD谱 |
| 表 1 微波活化前后铜精矿的主要元素成分 /% |
 |
| 点击放大 |
硫酸及其他化学试剂均为分析纯.微波活化铜精矿加压浸出过程中通入工业纯氧.
主要实验仪器:G70D20ASP-DF型微波炉(广东格兰仕微波炉电器有限公司), 额定微波频率2450 MHz, 额定输出功率700 W; CJF-T型高压釜(大连通达反应釜厂), 内容积1.0 L.
1.2 实验过程铜精矿经微波活化预处理后按一定液固比与浸出剂混合加入高压釜的钛胆中.高压釜加盖密封, 通过控制箱设定加热温度.升温至设定温度时, 向高压釜内通入工业纯氧并开始计时.浸出结束后通水冷却, 待釜内压力降为0后开启高压釜, 分别将浸出液和浸出渣送样分析.铜、锌浸出率计算均按渣计.
为保证各实验点间具有可比性, 控制每次实验时高压釜升温速率及降温速率相同.
为使浸出过程中, 反应物(即硫酸)浓度保持相对恒定, 在微波活化铜精矿加压浸出动力学实验中, 选取了相对偏高的初始硫酸浓度(1.23 mol/L)以及较大的液固比(mL/g)30/1.基于大量实验可知, 当搅拌转速达到500 r/min以上时, 可以保证1.0 L釜内气、液、固三相充分混合和氧的传质, 故在各次实验中控制搅拌转速恒定为500 r/min.本研究未考虑氧分压对微波活化铜精矿加压浸出动力学的影响, 各次实验氧分压恒定为0.6 MPa.
2 结果与讨论 2.1 铜的浸出速率在408~453 K温度范围内, 铜浸出率随浸出时间变化关系如图 2所示.图 2中直线为铜浸出率在一定浸出时间范围内的拟合直线.由图 2可见, 在铜浸出达到平衡之前, 铜浸出率与浸出时间之间呈良好的直线关系, 相关系数R≥0.99.进一步由图 2可知, 对于各浸出温度而言, 在浸出达到平衡之前, 铜浸出率随浸出时间延长而不断增大的规律是基本一致的.当浸出温度升高至453 K时, 铜浸出达到平衡的时间缩短至150 min.与未经微波活化预处理的铜精矿加压浸出行为[15]比较可知, 微波活化前后, 铜浸出行为规律基本一致.
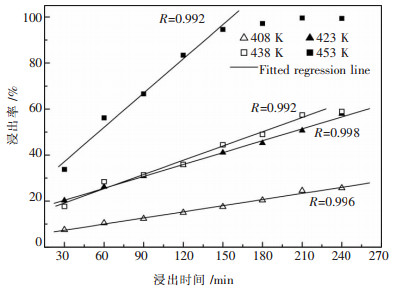 |
| 图 2 微波活化铜精矿铜浸出率与浸出时间的关系 |
铜精矿微波活化前后, 铜浸出率对应浸出时间的拟合直线方程见表 2.由表 2可见, 在408~438 K温度范围内, 微波活化前后, 铜浸出速率未见明显变化, 当温度升高至453 K时, 铜浸出速率较活化前略有增大.为保证铜的高效浸出, 微波活化铜精矿浸出温度宜选择453 K.
| 表 2 铜精矿铜浸出率与浸出时间对应的直线关系 |
 |
| 点击放大 |
2.2 锌的浸出速率
在408~453 K温度范围内, 锌浸出率随浸出时间变化关系如图 3所示.图 3中直线为锌浸出率在一定浸出时间范围内的拟合直线.由图 3可见, 在锌浸出达到平衡之前, 锌浸出率与浸出时间之间呈良好的直线关系, 相关系数R≥0.98.进一步由图 3可见, 锌浸出率随浸出时间变化的规律同铜浸出.当温度升高至453 K时, 锌浸出达到平衡的时间缩至120 min.相对于铜浸出而言, 锌浸出更早达到平衡.与铜浸出类似, 铜精矿微波活化前后锌浸出行为规律也基本一致.
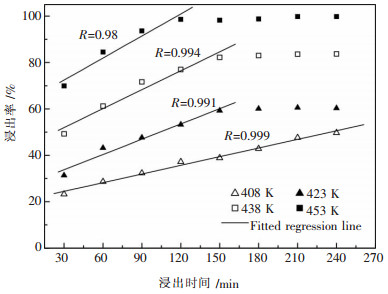 |
| 图 3 微波活化铜精矿锌浸出率与浸出时间的关系 |
铜精矿微波活化前后, 锌浸出率对应浸出时间的拟合直线方程见表 3.由表 3可见, 微波活化前后, 锌浸出速率随浸出温度的变化规律是相同的, 即在408~438 K温度范围内, 随浸出温度升高, 锌浸出速率不断增大; 当浸出温度进一步升高至453 K后, 锌浸出速率不再明显变化.当浸出温度低于423 K时, 锌浸出速率较活化前略有增大; 而当浸出温度高于438 K后, 虽然锌浸出率高于微波活化前, 但锌浸出过程反而略有放缓.
| 表 3 铜精矿锌浸出率与浸出时间对应的直线关系 |
 |
| 点击放大 |
进一步比较表 2、表 3结果可知, 在408~438 K温度范围内, 锌浸出速率始终高于铜浸出速率, 锌浸出优先于铜; 而当温度进一步升高至453 K后, 铜浸出得以明显促进, 铜浸出优先于锌.上述规律同精矿微波活化前.
2.3 浸出过程控制性步骤在铜精矿各金属硫化矿氧压酸浸过程中, 将有单质硫固体产物生成, 浸出总反应式如下:
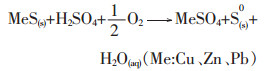
|
(1) |
因此, 反应式(1)可以用收缩核未反应模型来描述, 该模型同样适用于微波活化铜精矿.浸出控制步骤可分为液体边界层扩散控制、界面化学反应控制、固体产物层扩散控制[16].在加压浸出条件下, 因搅拌在气泡的作用下被强化, 所以浸出速率可不受液体边界层扩散控制.
经计算可知, 在408~453 K温度范围内, 对于微波活化铜精矿铜、锌浸出而言, 只有界面化学反应控制的动力学曲线才呈现良好的线性关系, 结果如图 4、图 5所示.1-(1-t)1/3~t之间拟合所得线性回归方程分别见表 4和表 5.
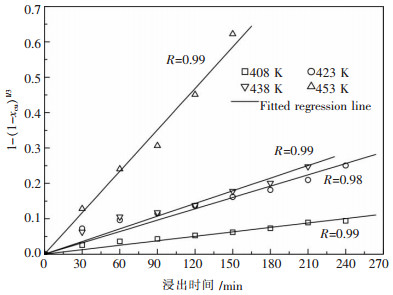 |
| 图 4 微波活化铜精矿铜浸出动力学曲线 |
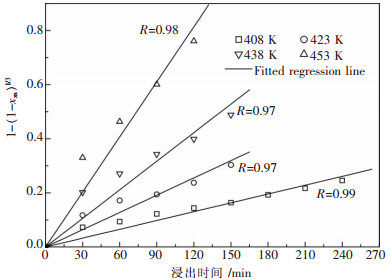 |
| 图 5 微波活化铜精矿锌浸出动力学曲线 |
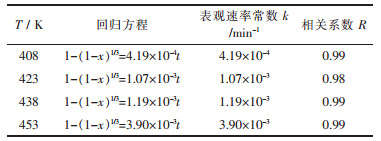
| 表 4 微波活化铜精矿铜浸出动力学方程 |
 |
| 点击放大 |
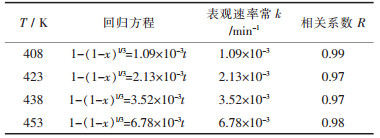
| 表 5 微波活化铜精矿锌浸出动力学方程 |
 |
| 点击放大 |
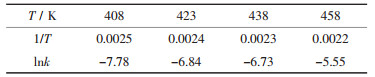
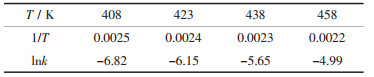
进一步由表 4、表 5所示的铜、锌浸出表观速率常数(k)求得对应不同浸出温度的lnk(如表 6、表 7所示).进一步以lnk对1/T作图, 如图 6、图 7所示, 无论对于铜还是锌浸出而言, lnk与1/T之间均呈良好的线性关系(相关系数R≥0.97).对于铜浸出而言, 所得直线斜率为-6798.88;对于锌浸出而言, 所得直线斜率为-5985.74.根据阿仑尼乌斯(Arrhenius)公式, 可求解浸出反应的活化能:
| 表 6 微波活化铜精矿铜浸出表观速率常数 |
 |
| 点击放大 |
| 表 7 微波活化铜精矿锌浸出表观速率常数 |
 |
| 点击放大 |
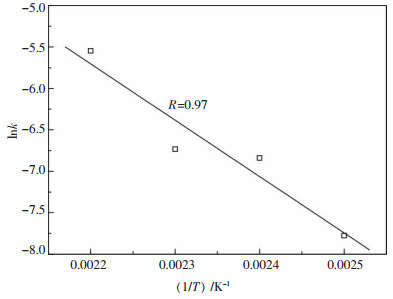 |
| 图 6 微波活化铜精矿铜浸出lnk-(1/T)图 |
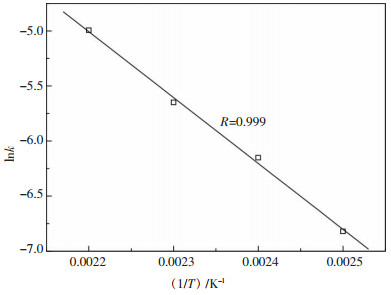 |
| 图 7 微波活化铜精矿锌浸出lnk-(1/T)图 |
对于铜浸出而言:
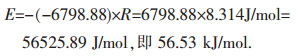
|
对于锌浸出而言:
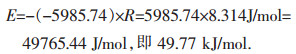
|
计算所得表观活化能均处于40~300 kJ/mol范围内, 由此可见, 微波活化铜精矿加压浸出过程的确受界面化学反应控制, 浸出控制步骤同微波活化前.铜、锌浸出反应表观活化能较微波活化前有明显降低, 这说明, 铜精矿经微波活化后铜、锌浸出过程得以促进.
3 结论(1) 在408~453 K范围内, 在铜、锌浸出达到平衡之前, 浸出率与浸出时间呈良好的线性关系.微波活化前后, 铜精矿铜、锌浸出行为规律基本一致.
(2) 在408~438 K温度范围内, 铜精矿微波活化前后, 铜浸出速率未见明显变化, 当温度升高至453 K后, 铜浸出速率较活化前略有增大.当温度低于423 K时, 锌浸出速率较活化前略有增大; 当温度高于438 K时, 锌浸出过程反而略有放缓.为保证铜的高效浸出, 微波活化铜精矿浸出温度宜选择453 K.
(3) 在408~438 K温度范围内, 锌浸出速率始终高于铜, 锌浸出优先于铜; 而当温度进一步升高至453 K后, 铜浸出优先于锌.上述规律同精矿微波活化前一致.
(4) 在408 ~453 K范围内, 微波活化铜精矿铜、锌浸出反应表观活化能分别为56.33 kJ/mol和49.77 kJ/mol, 铜、锌浸出过程受界面化学反应控制, 浸出控制步骤同微波活化前.经微波活化后铜精矿铜、锌浸出过程得以促进.
| [1] |
邱定蕃. 加压湿法冶金过程化学与工业实践[J].
矿冶, 1994, 3(4): 55–67.
|
| [2] |
Habashi F.Pressure Hydrometallurgy/Past, Present and Future[C]//Yang Xianwan.Proceedings of the Third International Conference on Hydrometallurgy'98.Kunming, China:International Academic Publishers, 1998:27-34.
http://www.academia.edu/22324769/Hydrometallurgy_in_the_Past_Decades._A_Personal_View |
| [3] |
王海北, 蒋开喜, 邱定蕃, 等. 国内外硫化铜矿湿法冶金发展现状[J].
有色金属, 2003, 55(4): 101–104.
|
| [4] |
郭亚惠. 铜湿法冶金现状及未来发展方向[J].
中国有色冶金, 2006(4): 1–13.
|
| [5] |
Hackl R P, Dreisinger D B, Peters E, et al. Passivation of Chalcopyrite during Oxidative Leaching in Sulfate Media[J].
Hydrometallurgy, 1995, 39(1-3): 25–48. DOI: 10.1016/0304-386X(95)00023-A. |
| [6] |
Jacobs I S, Zavitsnos P D. Microwave Handling of Mineral[J].
J ApplPhys, 1982, 53(3): 2730–2735. DOI: 10.1063/1.330949. |
| [7] |
张文朴. 微波在稀贵金属冶金中的应用研究进展[J].
稀有金属与硬质合金, 2008, 36(2): 49–53.
|
| [8] |
Hall S T, Finch J A. New Use of Microwave[J].
Miner Metall Process, 1984(11): 179–183. |
| [9] |
Standish N, Worner H. Microwave Handling of Iron Ore Powder[J].
Microwave Power and Electromagnetic Energy, 1990, 25(3): 177–180. DOI: 10.1080/08327823.1990.11688126. |
| [10] |
Haque K E. Microwave Energy for Mineral Treatment Process A Brief Review[J].
Int J Miner Process, 1999, 57(1): 1–24. DOI: 10.1016/S0301-7516(99)00009-5. |
| [11] |
Chen T T. The Relative Transparency of Minerals to Microwave Radiation[J].
Can Metall Q, 1984, 23(1): 349–351. |
| [12] |
段爱红. 晶体结构缺陷结构与物质吸收微波的能力[J].
云南师范大学学报, 1998, 18(3): 89–91.
|
| [13] |
崔礼生, 韩跃新. 微波技术在选矿中的应用[J].
金属矿山, 2006(4): 29–32.
|
| [14] |
徐志峰, 李强, 王成彦. 复杂硫化铜精矿微波活化预处理-加压浸出工艺[J].
过程工程学报, 2010, 10(2): 256–262.
|
| [15] |
徐志峰, 严康, 李强, 等. 复杂硫化铜精矿加压浸出动力学[J].
有色金属, 2010, 62(4): 76–81, 114.
|
| [16] |
华一新.
冶金过程动力学导论[M]. 北京: 冶金工业出版社, 2004-188.
|
 2011, Vol. 2
2011, Vol. 2
